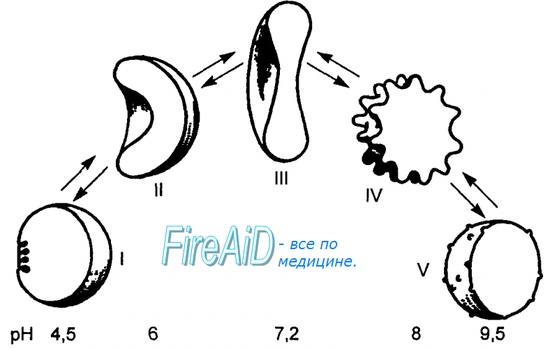
Аллостерические эффекты гемоглобина бора

Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 10 июля 2013; проверки требуют 29 правок.
Эффект Вериго — Бора (синонимы — эффект Вериго, эффект Бора) — зависимость степени диссоциации оксигемоглобина от величины парциального давления углекислоты в альвеолярном воздухе и крови, при снижении которого сродство кислорода к гемоглобину повышается, что затрудняет переход кислорода из капилляров в ткани. Эффект этот был открыт независимо друг от друга Б. Ф. Вериго в 1892 году[1] и датским физиологом К. Бором в 1904 году[2].
История открытия[править | править код]
Основу разработки проблемы гипоксии заложил русский учёный-физиолог И. М. Сеченов фундаментальными работами по физиологии дыхания и газообменной функции крови. Большое значение имеют также исследования русского физиолога Б. Ф. Вериго по физиологии газообмена в лёгких и тканях. Опираясь на идеи Сеченова о сложных формах взаимодействия между диоксидом углерода и кислородом в крови (Вериго работал в лабораториях Сеченова, И. Р. Тарханова и И. И. Мечникова), он впервые установил зависимость степени диссоциации оксигемоглобина от величины парциального давления углекислоты в крови.
Биохимический механизм[править | править код]
Эффект Вериго — Бора: влияние pH на кривую насыщения гемоглобина кислородом
В клетках периферических тканей органическое топливо окисляется в митохондриях с использованием кислорода (клеточное дыхание), доставляемого гемоглобином из лёгких; при этом в качестве продуктов образуются углекислый газ, вода и другие соединения. Образование углекислого газа в тканях одновременно приводит и к повышению концентрации ионов H+ (то есть к понижению pH), поскольку при гидратации CO2 образуется H2CO3 — слабая угольная кислота, диссоциирующая на ионы H+ и бикарбонат-ионы:
H2CO3 ⇄ H+ + HCO3-.
Гемоглобин переносит значительную долю (около 20 %) общего количества CO2 и ионов H+, образующихся в тканях и поступающих в лёгкие и почки, обеспечивающих выделение этих продуктов.
За много лет до открытия этого механизма было обнаружено, что на связывание кислорода гемоглобином очень сильное влияние оказывает pH и концентрация CO2: при присоединении CO2 и ионов H+ способность гемоглобина связывать O2 снижается. Действительно, в периферических тканях с относительно низким значением pH и высокой концентрацией CO2 сродство гемоглобина к кислороду падает. И наоборот, в лёгочных капиллярах выделение CO2 и сопутствующее ему повышение pH крови приводит к увеличению сродства гемоглобина к кислороду. Это влияние величины pH и концентрации CO2 на связывание и освобождение O2 гемоглобином и называют эффектом Вериго — Бора.
Реакция связывания кислорода гемоглобином в виде
Hb + O2 ⇄ HbO2
в действительности отражает неполную картину, поскольку не учитывает дополнительные лиганды H+ и CO2.
Чтобы объяснить влияние концентрации ионов H+ на связывание кислорода, следует записать эту реакцию в иной форме:
HHb+ + O2 ⇄ HbO2 + H+,
где HHb+ — протонированная форма гемоглобина. Из этого уравнения следует, что кривая насыщения гемоглобина кислородом зависит от концентрации ионов H+. Гемоглобин связывает и O2, и ионы H+, но между этими двумя процессами существует обратная зависимость. Если парциальное давление кислорода велико (что наблюдается, например, в лёгких), то гемоглобин связывает его, освобождая при этом ионы H+. При низком парциальном давлении кислорода (что имеет место в тканях) связываться с гемоглобином будут ионы H+.
Эффективность связывания гемоглобином углекислого газа (с образованием карбаминогемоглобина, чаще именуемого карбгемоглобином[3]) находится в обратной зависимости от связывания кислорода. В тканях часть избыточного CO2 связывается с гемоглобином, сродство последнего к O2 снижается, и происходит высвобождение кислорода. В лёгких же связывается избыток O2 воздуха, тем самым сродство гемоглобина к CO2 уменьшается, и CO2 выделяется в альвеолярный воздух, способствуя лёгкому закислению крови за счёт ионов H+, возникающих при диссоциации угольной кислоты (см. выше).
Описанные зависимости делают молекулу гемоглобина великолепно приспособленной к осуществлению совместного переноса эритроцитами кислорода, углекислого газа и ионов H+[4].
См. также[править | править код]
- Эффект Холдейна (открыт Джоном Скоттом Холдейном)
Примечания[править | править код]
- ↑ Verigo B. F. Zur Frage über die Wirkung des Sauerstoff auf die Kohlensäureausscheidung in den Lungen // Archiv für die gesammte Physiologie des Menschen und der Thiere : статья. — 1892. — № 51. — С. 321—361.
- ↑ Chr. Bohr, K. Hasselbalch, and August Krogh. Concerning a Biologically Important Relationship — The Influence of the Carbon Dioxide Content of Blood on its Oxygen Binding // Skand. Arch. Physiol. : статья. — 1904. — № 16. — С. 401—412.
- ↑ Карбгемоглобин // Биологический энциклопедический словарь (рус.).
- ↑ Ленинджер А. Основы биохимии: В 3-х томах. Том 1. — М.: Мир, 1985. — С. 208—210. — 367 с.
Литература[править | править код]
- Вериго эффект // Большой медицинский словарь (рус.). — 2000.
Источник
Оглавление темы “Вентиляция легких. Перфузия легких кровью.”: Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц. Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН. Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани. Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей. – Также рекомендуем “Углекислый газ. Транспорт углекислого газа.” |
Источник
Аллостерическая регуляция насыщения гемоглобина кислородом
Кривая диссоциации кислорода для гемоглобина
Механизм насыщения гемоглобина кислородом
Гемоглобин присоединяет О2 последовательно, по одной молекуле на каждый гем.
В апогемоглобине, благодаря координационной связи с белковой частью, атом железа выступает из плоскости гема в направлении гистидина F8.
Присоединение О2 к шестой координационной связи железа вызывает его перемещение в плоскость гема, за ним перемещаются гистидин F8 и полипептидная цепь, в состав которой он входит.
Происходит изменение конформации текущего протомера и связанных с ним оставшихся протомеров. При этом у протомеров возрастает сродство к кислороду, в результате каждый следующий кислород присоединяется к гемоглобину лучше предыдущего. Четвертая молекула кислорода присоединяется к гемоглобину в 300 раз легче, чем первая молекула. Обратный процесс аналогичен, чем больше О2 отдают протомеры, тем легче идет отщепление последующих молекул О2.
Кооперативность в работе протомеров гемоглобина формирует сигмовидный характер кривой насыщения его кислородом в зависимости от парциального давления кислорода.
S–образная кривая насыщения гемоглобина кислородом имеет важное биологическое значение.
Во-первых, пологий участок S–образной кривой (выше 60 мм.рт.ст.) обеспечивает максимальное насыщение гемоглобина кислородом в легких, даже если концентрация кислорода в альвеолярном воздухе заметно снижена. Например, в альвеолярной крови при РО2=95 мм.рт.ст. гемоглобин насыщается кислородом на 97%, а при РО2=60 мм.рт.ст. – на 90%.
Во-вторых, Крутой наклон среднего участка S–образной кривой (от 10 до 40 мм.рт.ст.) обеспечивает максимальный переход кислорода от гемоглобина к тканям.
В области венозного конца капилляра при РО2 = 40 мм.рт.ст. гемоглобин насыщен кислородом на 73%. При снижении РО2 на 5 мм.рт.ст. насыщение гемоглобина кислородом уменьшается на 7%.
Кроме РО2 на насыщение гемоглобина кислородом влияют и другие факторы, например, рН, температура, давление, концентрация 2,3-ДФГ, РСО2.
Увеличение температуры, присоединение к гемоглобину Н+, 2,3-ДФГ, СО2 уменьшает сродство гемоглобина к кислороду, при этом кривая диссоциации оксигемоглобина сдвигается вправо и гемоглобин легче отдает кислород тканям.
Влияние рН на характер кривой диссоциации оксигемоглобина называется эффектом Бора (по имени датского физиолога Христиана Бора, впервые открывшего этот эффект).
Гемоглобин в дезоксигенерированном состоянии имеет более высокое сродство к протонам, чем оксигемоглобин. Другими словами R – форма (оксигенерированная) является более сильной кислотой, чем Т-форма (дезоксигенерированная). Поэтому когда дезоксигемоглобин в легких присоединяет кислород, происходит переход в R – форму и разрыв некоторых связей, в результате чего и высвобождаются протоны, ответственные за эффект Бора. Наоборот, при высвобождении кислорода образуется Т-структура и разорванные связи между субъединицами должны быть восстановлены, и протоны вновь присоединяются к остаткам гистидина в b – цепях. Таким образом, протонирование гемоглобина снижает его сродство к О2 и увеличивает потребление О2 в ткани.
Эффект Бора имеет важное физиологическое значение. Образующийся в тканях СО2 должен транспортироваться в легкие. Он поступает в эритроциты по градиенту напряжения. В них фермент карбоангидраза превращает его в Н2СО3, который диссоциирует на бикарбонат, ион и протон. Последний сдвигает равновесие влево в уравнении (1).
Hb + 4 O2= Hb (О2)4 + (H+)n
Где n – величина порядка 2; число зависит от целого комплекса параметров, тем самым заставляя Hb О2 отдавать свой кислород.
НСО3- пассивно продвигается через ионный канал по градиенту концентрации в сыворотку.
Продвижение НСО3- не сопровождается перемещением Н+, поскольку нет канала, позволяющего ему пройти через мембрану эритроцитов. Для сохранения ионного равновесия при выходе НСО3- из клетки, Cl- перемещаются внутрь её через тот же ионный канал. Такое двойное перемещение известно как хлоридный сдвиг (сдвиг Хамбургера).
Растворенный НСО3- движется вместе с венозной кровью обратно в легкие. Здесь высвобождение протона из гемоглобина при оксигениции приводит к образованию НСО3- (по принципу Ле-Шателье).
НСО3-+ Н+= Н2СО3-,
что позволяет карбоангидразе образовать СО2.
Разрушение НСО3- в эритроците обуславливает вхождение в него НСО3- из сыворотки, так что в легких происходит обратный хлоридный сдвиг, приводящий к выведению СО2 с выдыхаемым воздухом.
Источник
Эффективность связывания кислорода с гемоглобином регулируется
Кооперативное взаимодействие
Взаимовлияние протомеров олигомерного белка друг на друга называется кооперативное взаимодействие.
В легких такое взаимодействие субъединиц гемоглобина повышает его сродство к кислороду и ускоряет присоединение кислорода в 300 раз. В тканях идет обратный процесс, сродство снижается и ускорение отдачи кислорода также 300-кратное.
Схема кооперативного взаимодействия субъединиц гемоглобина
Объясняется такой феномен тем, что в легких при присоединении первой молекулы кислорода к железу (за счет 6-й координационной связи) атом железа втягивается в плоскость гема, кислород остается вне плоскости. Это вызывает перемещение участка белковой цепи и изменение конформации первого протомера. Такой измененный протомер влияет на другие субъединицы и облегчает связывание кислорода со второй субъединицей. Это меняет конформацию второй субъединицы, облегчая присоединение последующих молекул кислорода и изменение других протомеров.
Изменение формы субъединиц гемоглобина
при присоединении и отщеплении кислорода
Дезоксиформа гемоглобина обозначается как Т-форма, напряженная (англ. tense), она обладает существенно более низким сродством к кислороду. Оксигенированная форма, или R-форма (англ. relaxed), обладает высоким сродством к кислороду.
Изменение рН среды
Влияние рН на сродство гемоглобина к кислороду носит название эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается.
При повышении концентрации протонов (закисление среды) в тканях возрастает освобождение кислорода из оксигемоглобина. В легких после удаления угольной кислоты (в виде СО2) из крови и одновременном увеличении концентрации кислорода высвобождаются ионы Н + из гемоглобина.
Реакция взаимодействия кислорода с гемоглобином упрощенно имеет вид:
Изменение сродства гемоглобина к кислороду в тканях и в легких при изменении концентрации ионов H + и О2 обусловлено конформационными перестройками глобиновой части молекулы. В тканях молекула О 2 отрывается от железа и ионы водорода присоединяются к остаткам гистидина (глобиновой части), образуя восстановленный гемоглобин (H-Hb) с низким сродством к кислороду. В легких поступающий в больших количествах кислород «вытесняет» ион водорода из связи с остатком гистидина гемоглобиновой молекулы.
Механизм эффекта Бора
Роль 2,3-дифосфоглицерата
2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного метаболита гликолиза, в реакциях, получивших название шунт Раппопорта.
Реакции шунта Раппопорта
2,3-Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с β-цепями, образуя поперечный солевой мостик между атомами кислорода 2,3-дифосфоглицерата и аминогруппами концевого валина обеих β-цепей, также аминогруппами радикалов лизина и гистидина.
Расположение 2,3-дифосфоглицерата в гемоглобине
Функция 2,3-дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду, что имеет особенное значение при подъеме на высоту и при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в 2 раза.
источник
Вопрос 8. Эффект Бора, аллостерическая регуляция насыщения гемоглобина кислородом
График зависимости насыщения миоглобина кислородом от парциального давления кислорода имеет вид гиперболы; для гемоглобина же это зависимость отражается S- образной кривой. Графики подтверждают функцию данных хромопротеинов. Функция миоглобина – присоединить кислород, доставляемый гемоглобином и его запасти. Миоглобин не может транспортировать кислород так как даже при парциальном давлении 20 мм.рт.ст., степень насыщения миоглобина кислородом будет около 85%. Однако при кислородном голодании, которым сопровождается тяжелая физическая работа, РО2 в мышечной ткани может понизиться и до 5 мм.рт.ст., при столь низком давлении миоглобин легко отдает связанный кислород, обеспечивая тем самым окислительный синтез АТФ в митохондриях мышечных клеток.
Кривая диссоциации оксигемоглобина имеет S- образную конфигурацию. Этот факт также связан с функцией гемоглобина и имеет биохимический смысл. В процессе поглощения кислорода в легких напряжение О2 в крови (РО2) приближается к таковому в альвеолах. У молодых людей РО2 артериальной крови составляет около 95 мм.рт.ст.. Насыщение гемоглобина при этом – 97%. С возрастом (или при заболеваниях легких) напряжение О2 в артериальной крови может значительно снижаться, однако, поскольку кривая диссоциации оксигемоглобина в правой её части почти горизонтальна, насыщение крови кислородом уменьшается не намного. При РО2 равное 60 мм.рт.ст. насыщение гемоглобина составляет 90%. Таким образом, горизонтальный участок кривой диссоциации предупреждает существенное снижение насыщения артериальной крови кислородом.
Крутой наклон среднего участка свидетельствует об очень благоприятных условиях для отдачи кислорода тканям. В состоянии покоя РО2 в области венозного конца капилляра равно приблизительно 40 мм.рт.ст., что соответствует примерно 73% насыщения. Если в результате увеличения потребления кислорода его напряжение в венозной крови падает лишь на 5 мм.рт.ст, то насыщение гемоглобина кислородом снижается не менее чем на 7%.
Олигомерные белки способны к аллостерической регуляции своих функций. Присоединение лигандов в участках, пространственно удаленных друг от друга (аллостерических), способно вызвать конформационные изменения во всем белке.
Результатом воздействия лигандов Н + , 2,3-ДФГ, СО2 является затруднение перехода из Т- состояния в R. Т-форма характеризуется меньшим сродством к кислороду и способна легко отдавать его тканям. Таким образом, при увеличение концентрации 2,3- ДФГ, уменьшение рН среды, а также при возрастании РСО2 и температуры кривая диссоциации оксигемоглобина сдвигается вправо.
Эффект Бора
Влияние рН на характер кривой диссоциации оксигемоглобина называется эффектом Бора (по имени датского физиолога Христиана Бора, впервые открывшего этот эффект).
Гемоглобин в дезоксигенерированном состоянии имеет более высокое сродство к протонам, чем оксигемоглобин. Другими словами R – форма (оксигенерированная) является более сильной кислотой, чем Т-форма (дезоксигенерированная). Поэтому когда дезоксигемоглобин в легких присоединяет кислород, происходит переход в R – форму и разрыв некоторых связей, в результате чего и высвобождаются протоны, ответственные за эффект Бора. Наоборот, при высвобождении кислорода образуется Т-структура и разорванные связи между субъединицами должны быть восстановлены, и протоны вновь присоединяются к остаткам гистидина в — цепях. Таким образом, протонирование гемоглобина снижает его сродство к О2 и увеличивает потребление О2 в ткани.
Эффект Бора имеет важное физиологическое значение. Образующийся в тканях СО2 должен транспортироваться в легкие. Он поступает в эритроциты по градиенту напряжения. В них фермент карбоангидраза превращает его в Н2СО3, который диссоциирует на бикарбонат, ион и протон. Последний сдвигает равновесие влево в уравнении (1).
Где n — величина порядка 2; число зависит от целого комплекса параметров, тем самым заставляя Hb О2 отдавать свой кислород.
НСО3 — пассивно продвигается через ионный канал по градиенту концентрации в сыворотку.
Продвижение НСО3 — не сопровождается перемещением Н + , поскольку нет канала, позволяющего ему пройти через мембрану эритроцитов. Для сохранения ионного равновесия при выходе НСО3 — из клетки, Cl — перемещаются внутрь её через тот же ионный канал. Такое двойное перемещение известно как хлоридный сдвиг (сдвиг Хамбургера).
Растворенный НСО3 — движется вместе с венозной кровью обратно в легкие. Здесь высвобождение протона из гемоглобина при оксигениции приводит к образованию НСО3 — (по принципу Ле-Шателье).
что позволяет карбоангидразе образовать СО2.
Разрушение НСО3 — в эритроците обуславливает вхождение в него НСО3 — из сыворотки, так что в легких происходит обратный хлоридный сдвиг, приводящий к выведению СО2 с выдыхаемым воздухом.
источник
Эффект Бора
Аллостерическая регуляция насыщения гемоглобина кислородом
Кривая диссоциации кислорода для гемоглобина
Механизм насыщения гемоглобина кислородом
Гемоглобин присоединяет О2 последовательно, по одной молекуле на каждый гем.
В апогемоглобине, благодаря координационной связи с белковой частью, атом железа выступает из плоскости гема в направлении гистидина F8.
Присоединение О2 к шестой координационной связи железа вызывает его перемещение в плоскость гема, за ним перемещаются гистидин F8 и полипептидная цепь, в состав которой он входит.
Происходит изменение конформации текущего протомера и связанных с ним оставшихся протомеров. При этом у протомеров возрастает сродство к кислороду, в результате каждый следующий кислород присоединяется к гемоглобину лучше предыдущего. Четвертая молекула кислорода присоединяется к гемоглобину в 300 раз легче, чем первая молекула. Обратный процесс аналогичен, чем больше О2 отдают протомеры, тем легче идет отщепление последующих молекул О2.
Кооперативность в работе протомеров гемоглобина формирует сигмовидный характер кривой насыщения его кислородом в зависимости от парциального давления кислорода.
S–образная кривая насыщения гемоглобина кислородом имеет важное биологическое значение.
Во-первых, пологий участок S–образной кривой (выше 60 мм.рт.ст.) обеспечивает максимальное насыщение гемоглобина кислородом в легких, даже если концентрация кислорода в альвеолярном воздухе заметно снижена. Например, в альвеолярной крови при РО2=95 мм.рт.ст. гемоглобин насыщается кислородом на 97%, а при РО2=60 мм.рт.ст. — на 90%.
Во-вторых, Крутой наклон среднего участка S–образной кривой (от 10 до 40 мм.рт.ст.) обеспечивает максимальный переход кислорода от гемоглобина к тканям.
В области венозного конца капилляра при РО2 = 40 мм.рт.ст. гемоглобин насыщен кислородом на 73%. При снижении РО2 на 5 мм.рт.ст. насыщение гемоглобина кислородом уменьшается на 7%.
Кроме РО2 на насыщение гемоглобина кислородом влияют и другие факторы, например, рН, температура, давление, концентрация 2,3-ДФГ, РСО2.
Увеличение температуры, присоединение к гемоглобину Н + , 2,3-ДФГ, СО2 уменьшает сродство гемоглобина к кислороду, при этом кривая диссоциации оксигемоглобина сдвигается вправо и гемоглобин легче отдает кислород тканям.
Влияние рН на характер кривой диссоциации оксигемоглобина называется эффектом Бора (по имени датского физиолога Христиана Бора, впервые открывшего этот эффект).
Гемоглобин в дезоксигенерированном состоянии имеет более высокое сродство к протонам, чем оксигемоглобин. Другими словами R – форма (оксигенерированная) является более сильной кислотой, чем Т-форма (дезоксигенерированная). Поэтому когда дезоксигемоглобин в легких присоединяет кислород, происходит переход в R – форму и разрыв некоторых связей, в результате чего и высвобождаются протоны, ответственные за эффект Бора. Наоборот, при высвобождении кислорода образуется Т-структура и разорванные связи между субъединицами должны быть восстановлены, и протоны вновь присоединяются к остаткам гистидина в b — цепях. Таким образом, протонирование гемоглобина снижает его сродство к О2 и увеличивает потребление О2 в ткани.
Эффект Бора имеет важное физиологическое значение. Образующийся в тканях СО2 должен транспортироваться в легкие. Он поступает в эритроциты по градиенту напряжения. В них фермент карбоангидраза превращает его в Н2СО3, который диссоциирует на бикарбонат, ион и протон. Последний сдвигает равновесие влево в уравнении (1).
Где n — величина порядка 2; число зависит от целого комплекса параметров, тем самым заставляя Hb О2 отдавать свой кислород.
НСО3- пассивно продвигается через ионный канал по градиенту концентрации в сыворотку.
Продвижение НСО3- не сопровождается перемещением Н+, поскольку нет канала, позволяющего ему пройти через мембрану эритроцитов. Для сохранения ионного равновесия при выходе НСО3- из клетки, Cl- перемещаются внутрь её через тот же ионный канал. Такое двойное перемещение известно как хлоридный сдвиг (сдвиг Хамбургера).
Растворенный НСО3- движется вместе с венозной кровью обратно в легкие. Здесь высвобождение протона из гемоглобина при оксигениции приводит к образованию НСО3- (по принципу Ле-Шателье).
что позволяет карбоангидразе образовать СО2.
Разрушение НСО3- в эритроците обуславливает вхождение в него НСО3- из сыворотки, так что в легких происходит обратный хлоридный сдвиг, приводящий к выведению СО2 с выдыхаемым воздухом.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Учись учиться, не учась! 10882 —
| 8142 — или читать все.
источник
Аллостерические эффекты гемоглобина бора
Источник