Анемии классификация патогенез лечение

Анемии. Классификация,этиология, патогенез, клиника, диагностика, лечение, профилактика.
Проф. Бабаджанова Ш.А.
Анемия- это патологическое состояние, характеризующееся снижением уровня гемоглобина и уменьшением количества эритроцитов в еденице объёма крови.

Классификация анемий:
1. Острая постгеморрагическая анемия
2. Анемии связанные с нарушением кровообразования
Железодефицитная анемия
Мегалобластные анемии (Витамин В 12 и фолиево-дефицитные анемии)
Гипопластические и апластические анемии
3. Гемолитические анемии
а) Врожденные гемолитические анемии
в) Приобретённые гемолитические анемии

Врождённые гемолитические анемии.
Врождённые гемолитические анемии.
Мембранопатии
-микросфероцитоз-болезнь Минковского-Шоффара
-овалоцитоз, акантоцитоз, стоматоцитоз
Ферментопатии
-недостаточность глюкозо-6-фосфатдегидрогенезы -Г6ФДГ
– недостаточность пируваткиназы;
Гемоглобинопатии:
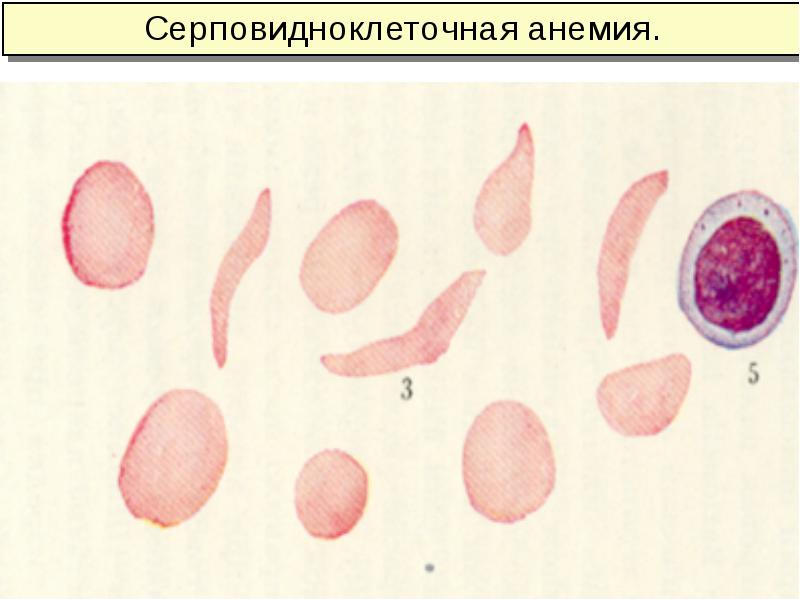
– серповидноклеточная анемия;
– альфа, бетта- талассемия.

Приобретённые гемолитические анемии:
Приобретённые гемолитические анемии:
Аутоиммунные гемолитические анемии;
Гемолитическая болезнь новорождённых;
Пароксизмальная ночная гемоглобинурия-болезнь Маркиафи-Микели;
Переливание групповой и резус несовместимой крови;
Гемолитические яды (свинец, тяжелые металлы, органические кислоты);
Укус ядовитых змей и насекомых.

Железодефицитная анемия (ЖДА)-патологическое состояние, характеризующееся нарушением синтеза гемоглобина в результате дефицита железа, развивающееся на фоне различных патологических (физиологических) процессов и проявляющееся признаками анемии и сидеропении.
Железодефицитная анемия (ЖДА)-патологическое состояние, характеризующееся нарушением синтеза гемоглобина в результате дефицита железа, развивающееся на фоне различных патологических (физиологических) процессов и проявляющееся признаками анемии и сидеропении.




Клиника ЖДА.
Анемия: слабость, быстрая утомляемость, головные боли, головокружения, мелькание мушек перед глазами, одышка, тахикардия, шум в ушах;
Сидеропения-симптомы тканевого дефицита железа:
Волосы секутся, выпадают и седеют
Сухость кожи и снижение её тургора
Койлонихии: искривление ногтей, повышенная ломкость ногтей, их выраженная поперечная исчерченность, воспаление околоногтевого валика, вогнутость, ложкообразные ногти
Наклонность к кариесу зубов
Рica chloratica- извращение вкуса и обоняния: тяга к мелу, зубному порошку, стирательной резинке, едят глину, землю, сырое мясо, тесто, привлекают запахи сырости, известки, керосина.

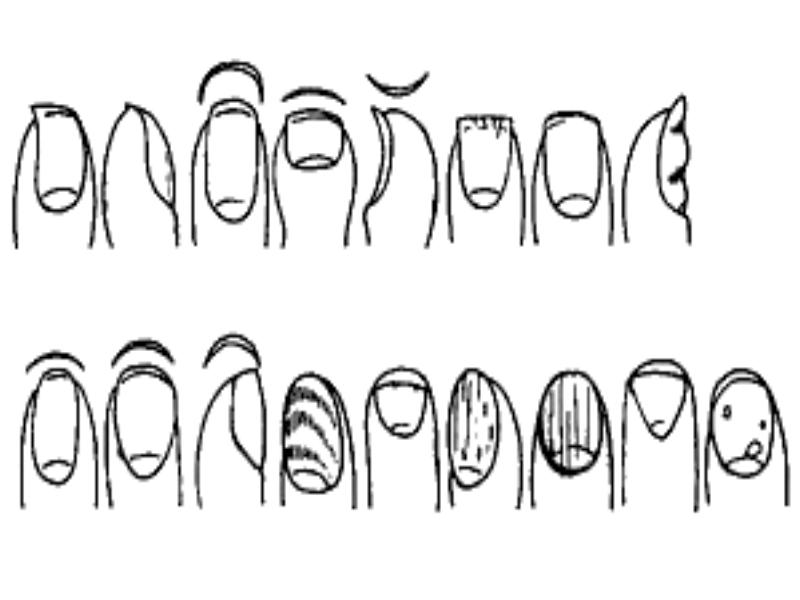
Объективно:
Кожа и слизистые оболочки бледные
Небольшое смещение границ относительной тупости влево
Мягкий систолический шум над верхушкой сердца
Лакированный язык: атрофия слизистой оболочки языка, заеды в углу рта, ангулярный стоматит
Затруднение глотания сухой пищи
Атрофия слизистой оболочки желудка с ахилией
Инфантильность, недоразвитие матки.

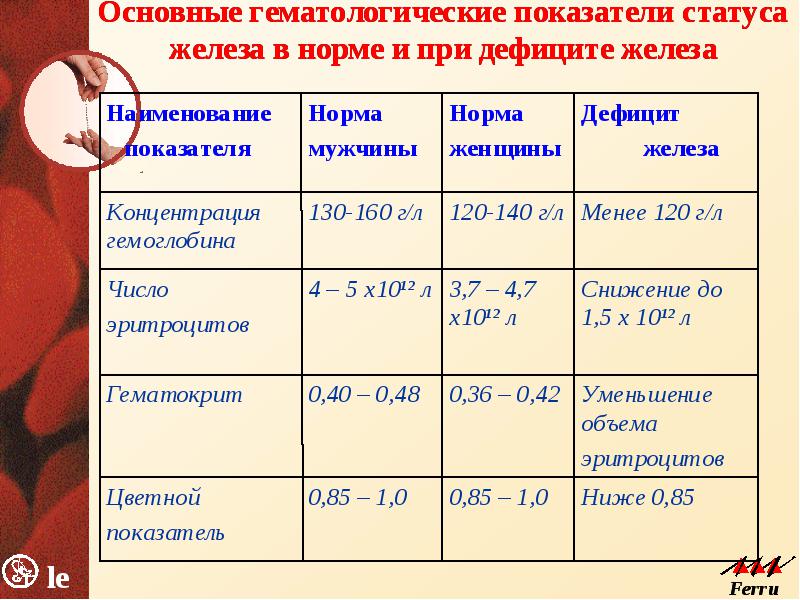
1. Нормальные эритроциты. 2. Железодефицитная анемия: гипохромия, анизоцитоз (микроциты), анулоциты, пойкилоцитоз, шизоцит.

Лечение ЖДА.
Устранить причину анемии
Организация адекватного питания (белки-140-150 г/сут, жиры-70-80 г/сут, витамин С)
1 степень анемии- препараты железа per os:
Мальтофер, феррум-лек, тардиферон
2 степень анемии- препараты железа в/м, в/в
Мальтофер, феррум-лек, венофер, космофер
3 степень анемии- препараты железа в/м, в/в,
Мальтофер, феррум-лек, венофер, космофер
Трансфузии эритроцитарной массы по жизненно-важным показаниям
При заболеваниях ЖКТ в I, II, III степенях
анемии препараты железа в/м, в/в.

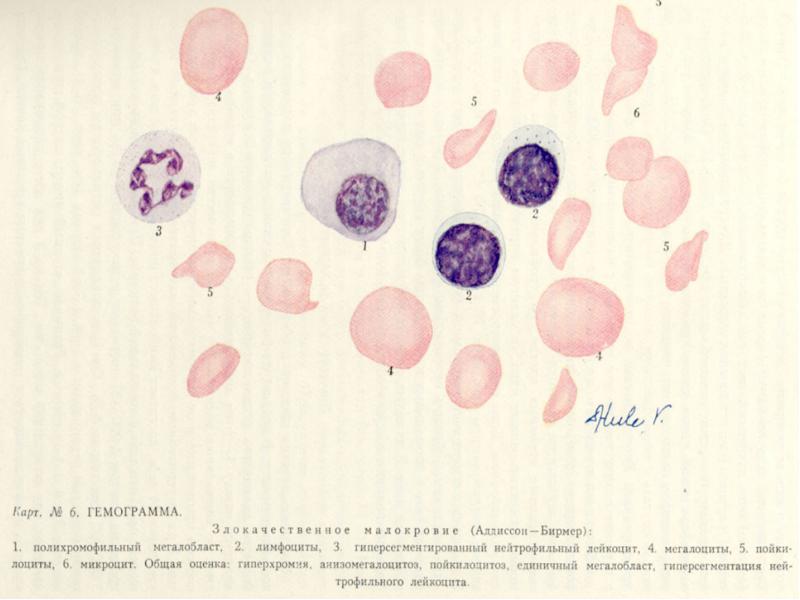
В 12 дефицитная анемия (пернициозная анемия, болезнь Адиссона-Бирмера)- анемия, развивающаяся вследствии недостаточности витамина В12.

Этиология.
Недостаточность внутреннего фактора Кастля- термолабильный гликопротеин, вырабатывающийся в фундальном отделе желудка париетальными клетками, который связывает витамин В 12. Образовавшийся комплекс в 100 раз быстрее всасывается в верхних отделах тонкой кишки
Алиментарный внешний фактор- витамин В 12, который в большом количестве содержится в мясных продуктах, яйце, сыре, в молочных продуктах, печени, почках.

Патогенез.
Витамин В12 участвует в образовании тимидина, что приводит к нарушениям образования ДНК и РНК. Ядерные изменения нарушают деление клетки, эритроциты не делятся, образуются огромные полиплоидные клетки- мегалобласты и мегалоциты
Витамин В12 участвует в образовании миелиновой оболочки нервных волокон, при этом развивается демиелинизация нервных волокон- развивается фуникулярный миелоз.

Клиника.
1. Анемия: слабость, быстрая утомляемость, головные боли, головокружения, мелькание мушек перед глазами, одышка, тахикардия, шум в ушах;
2. Фуникулярный миелоз: парестезия, нарушения чувствительности, боли, «чувство хождения по мягкой земле», ползание мурашек по теле, поясовидные боли, мышечная слабость, атрофия, иногда психические нарушения: бред, галлюцинации, эпилепсия;
3. Нарушения со стороны ЖКТ: Гюнтеровский глоссит: боли в языке, атрофия сосочков, воспаленный красный малиновый язык, атрофический гастрит, нарушение эвакуационной способности желудка.

Диагностика.
ОАК: снижение эритроцитов и гемоглобина
– возможны лейкопения, тромбоцитопения
-появление мегалоцитов, мегалобластов в крови
-анизоцитоз (макроцитоз, мегалоцитоз)
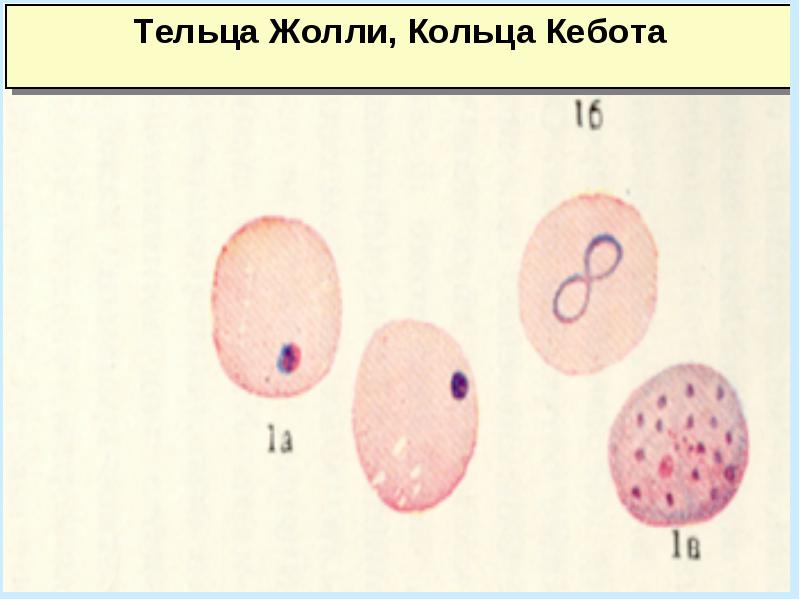
-появление колец Кебота, телец Жолли
-гиперхромия, повышение цветового показателя
появление полисегментоядерных нейтрофилов
биохимия: незначительное увеличение непрямого билирубина 28-47 мкмоль/л
Миелограмма: мегалобластное кроветворение
определение вит В12 радиоиммунным методом

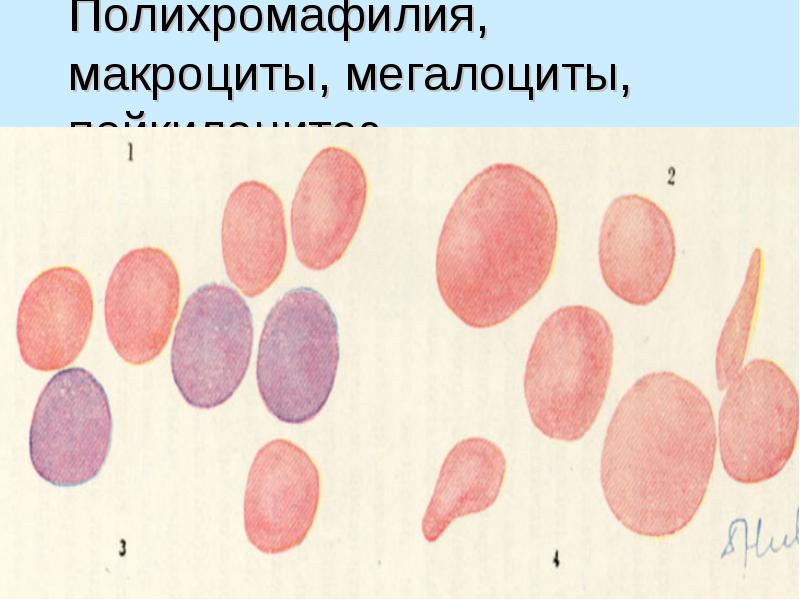
Полихромафилия, макроциты, мегалоциты, пойкилоцитоз.

Лечение.
Препараты витамина В12
-цианкоболамин 500 гамма в/м №10-15
при необходимости гемотрансфузии
при фуникулярном миелозе витамин В12 1000 гамма ежедневно

Под гипо-, апластической анемией понимают такое состояние, при котором резко угнетены 3 ростка кроветворения (эритро-, лейко-, тромбоцитопоэз), т.е. имеет место гипо-, аплазия костного мозга, следствием чего является развитие анемии, лейкопении, тромбоцитопении.
Под гипо-, апластической анемией понимают такое состояние, при котором резко угнетены 3 ростка кроветворения (эритро-, лейко-, тромбоцитопоэз), т.е. имеет место гипо-, аплазия костного мозга, следствием чего является развитие анемии, лейкопении, тромбоцитопении.
Впервые описана Эрлихом в 1888 г.

Этиопатогенез АА окончательно не выяснен.
Возможные причины АА:
Ионизирующая радиация;
Миелотоксичные яды (бензол и его производные, мышьяк и др.);
Лекарственные препараты (левомицетин, бутадион, сульфаниламиды, цитостатики);
Вирусная инфекция (гепатит, инфекционный мононуклеоз);
Идиопатическая форма 50-75 %.

Возможные механизмы развития заболевания:
Уменьшение количества стволовых клеток или их внутренний дефект;
Аутоиммунные реакции;
Анемия Фанкони- аутосомно-рециссивное заболевание с гиперчувствительностью к ДНК-повреждающим факторам
По клиническому течению различают:
Острое течение – 10-15%;
Подострое течение;
Хроническое течение.


Клинические признаки АА:
Анемия: слабость, быстрая утомляемость, головные боли, головокружения, мелькание мушек перед глазами, одышка, тахикардия, шум в ушах;
Геморрагии на коже и слизистых, крово-точивость дёсен, носовые, маточные кровотечения и др.;
Вторичные инфекции: гнойно-некроти-ческая ангина, пневмония, бронхит.

Диагноз АА считается достоверным при наличии двух из трёх критериев:
Нв менее 100 г/л или гематокрит менее 30%;
Лейкоциты менее 3,5х10*9/л с числом гранулоцитов менее 1,5х10*9/л;
Тромбоциты менее 50х10*9/л в сочетании с гипоклеточным костным мозгом при отсутствии признаков клонального гемопоэза в миелограмме.

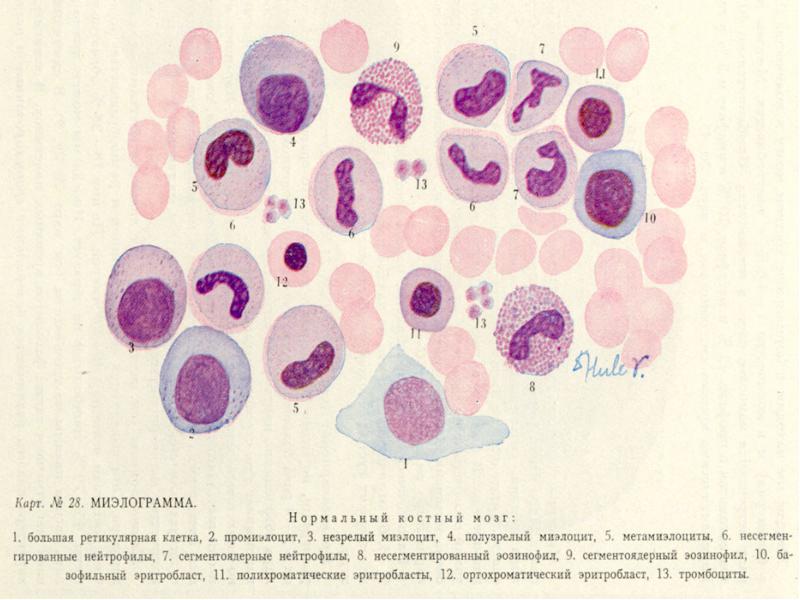
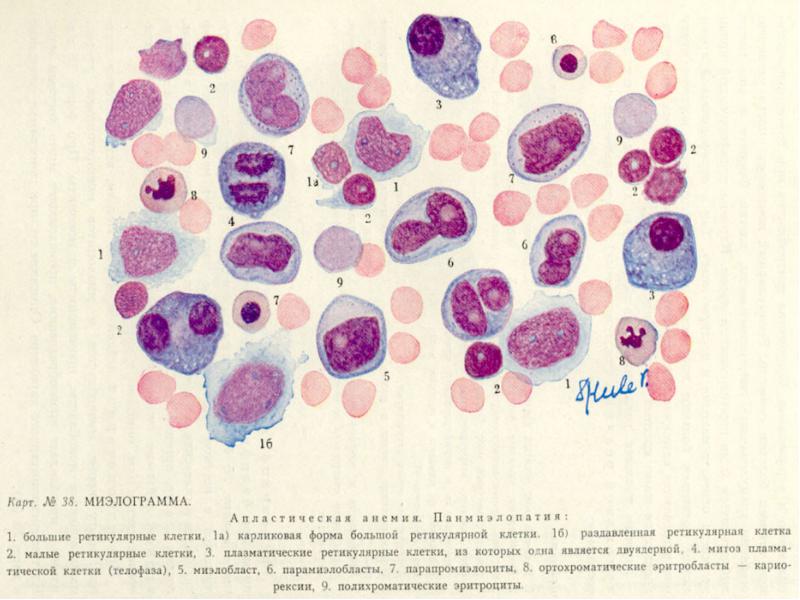
Трепанобиопсия:
Отмечается синдром островков: костный мозг расположен в виде островков, а основная часть костного мозга замещён жировой тканью.

Лечение АА:
Трансплантация костного мозга;
Глюкокортикоидные гормоны (преднизолон);
Спленэктомия;
Циклоспорин А;
Трансфузия эритроцитарной массы, тромбоцитарной и лейкоцитарной массы;
Анаболические гормоны (ретаболил, неробол)
Антилимфоцитарный глобулин;
Сосудоукрепляющие, гемостатические средства: вит С, дицинон, аминокапрон. к-та;
Антибиотики широкого спектра.

Гемолитические анемии составляют обширную группу анемических состояний различной этиологии, общим признаком которых является преобладание кроверазрушения над кровообразованием. Для гемолитической анемии свойственно укорочение жизни эритроцитов –гемолиз. Гемолиз может быть внутриклеточным или внутрисосудистым.
Гемолитические анемии составляют обширную группу анемических состояний различной этиологии, общим признаком которых является преобладание кроверазрушения над кровообразованием. Для гемолитической анемии свойственно укорочение жизни эритроцитов –гемолиз. Гемолиз может быть внутриклеточным или внутрисосудистым.

Этиопатогенез ГА.
Мембранопатии: имеется дефект структуры мембраны эритроцитов, вследствие чего увеличивается проницаемость мембраны эритроцитов. В эритроцит проникает большое количество натрия и воды, эритроцит набухает, теряет свою форму и приобретают форму сферы
Ферментопатии без провокации ничем не проявля-ются. Гемолитический криз возникает при приёме ЛС, обладающих высокой окислительной способностью (сульфаниламиды, нитрофураны, тубазид, ПАСК). Ферментная система не в состоянии нейтрализовать избыток образовавшихся комплексов, что приводит к окислению клетки и разрушению эритроцита
При талассемии один из цепей глобина продуцируется избыточно, что даёт мишеневидный вид и ведёт к повреждению мембраны и гемолизу.

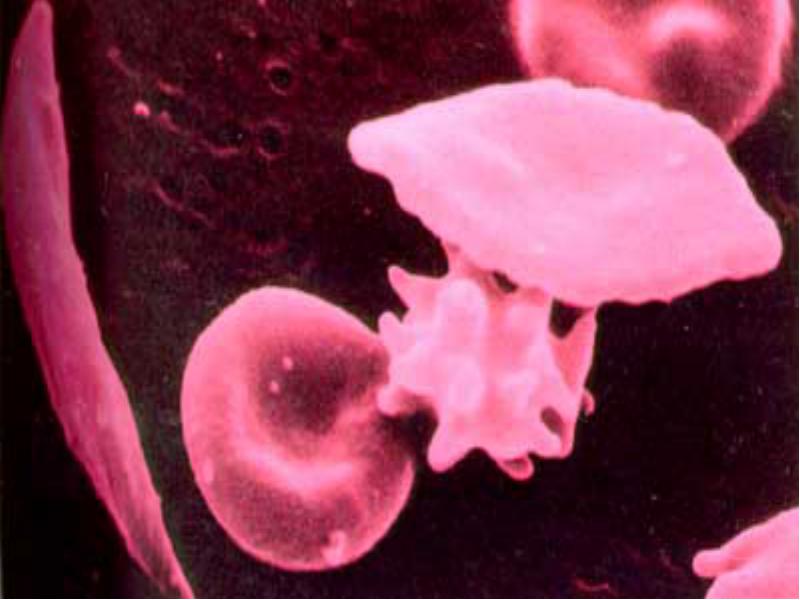
При серповидно-клеточной анемии в шестом положе-нии вместо глутаминовой кислоты располагается валин, следствием чего нарушается структура гемоглобина отдавшего кислород и превращается в гемоглобин S. Растворимость Нв S
При серповидно-клеточной анемии в шестом положе-нии вместо глутаминовой кислоты располагается валин, следствием чего нарушается структура гемоглобина отдавшего кислород и превращается в гемоглобин S. Растворимость Нв S
при отдаче кислорода уменьшается в 100 раз, что приводит к образованию геля и эритроциты принимают форму серпа. Деформированные эритроциты ригидные и их мембрана быстро повреждается
Развитие аутоиммунной гемолитической анемии обусловлено исходным нарушением иммунного статуса. При этих состояниях в организме больного синтезируются антитела против собственных неизменённых эритроцитов. Этот вид малокровия развивается при СКВ, РА, при хронической инфекции, лимфогранулематозе.

Гемолитическая болезнь новорожденных развивается при антигенной несовместимости матери и ребёнка. При резус несовместимости у ребёнка имеется антиген резуса (R+), а у матери этот антиген отсутствует (R-). Организм матери вырабатывает антитела против резус антигена и эти антитела разрушают эритроциты плода. При групповой несовместимости у матери I(0) группа, у плода II(А), III(В), IV(АВ) группы и организм матери вырабатывает антитела против А,В антигенов плода
Гемолитическая болезнь новорожденных развивается при антигенной несовместимости матери и ребёнка. При резус несовместимости у ребёнка имеется антиген резуса (R+), а у матери этот антиген отсутствует (R-). Организм матери вырабатывает антитела против резус антигена и эти антитела разрушают эритроциты плода. При групповой несовместимости у матери I(0) группа, у плода II(А), III(В), IV(АВ) группы и организм матери вырабатывает антитела против А,В антигенов плода
При пароксизмальной ночной гемоглобинурии эритроциты становятся чувствительными к изменению Рh среды. Гемолиз активизируется в ночные часы, при сдвиге Рh в кислую сторону
К гемолитическим ядам относится мышьяк, сапонины, свинец, фенилгидразин, змеиный яд и яд ядовитых насекомых, амилнитрит.

Клиника ГА:
Анемия: слабость, быстрая утомляемость, головные боли, головокружения, мелькание мушек перед глазами, одышка, тахикардия, шум в ушах;
Желтуха: желтушность кожи и слизистых, потемнение мочи, кала;
Гепатоспленомегалия: тяжесть или боли в левом и правом подреберье;
Интоксикация: тошнота, рвота, общая слабость,тахикардия, повышение температуры;
При врождённых гемолитических анемиях изменения в скелете: башенный череп, микрофтальмия, готическое нёбо, короткие пальцы;
При серповидно-клеточной анемии тромбоэмболии –инфаркты, инсульты при гипоксических состояниях;
Вторичный гемосидероз органов (лёгких, печени).

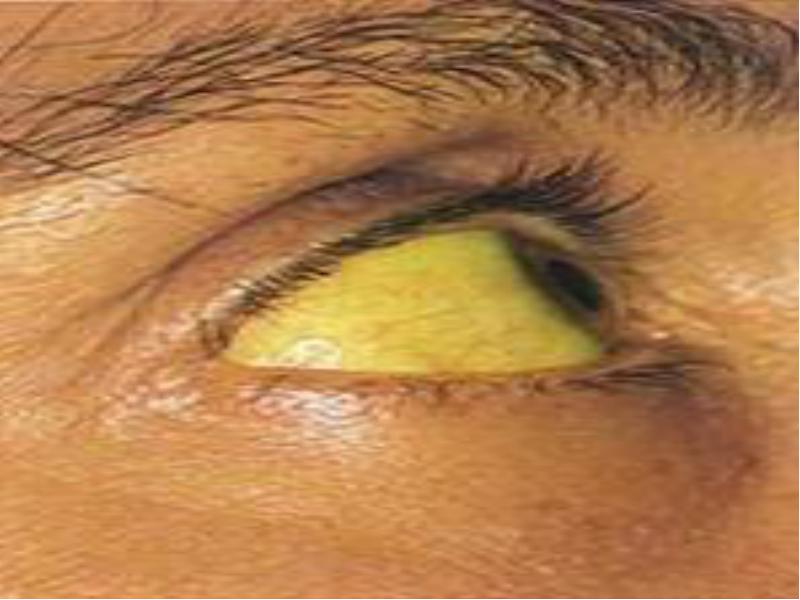
Диагностика ГА:
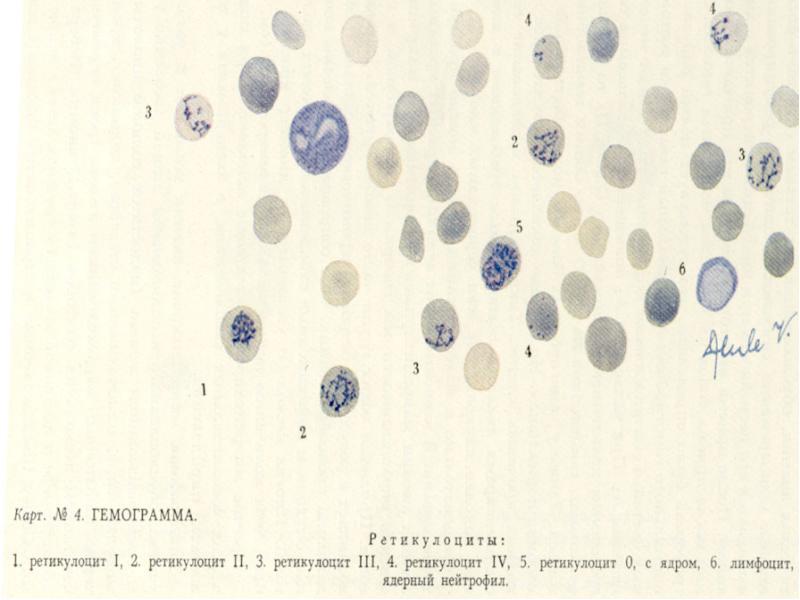
ОАК: снижение количества эритроцитов и гемоглобина, повышение ретикулоцитов, увеличение СОЭ.
при мембранопатиях микросфероцитоз, овалоцитоз, акантоцитоз, снижение осмотической резистентности
при аутоиммунных ГА СОЭ 60-80 мм/ч, поло-жительные серологические реакции Кумбса.
при серповидно-клеточной анемии серповидные клетки при пробе жгута на пальце, метабисульфатом
при талассемии мишеневидные клетки
Б/Х: увеличение непрямого билирубина, сывороточного железа
при ферментопатиях снижение активности ферментов.
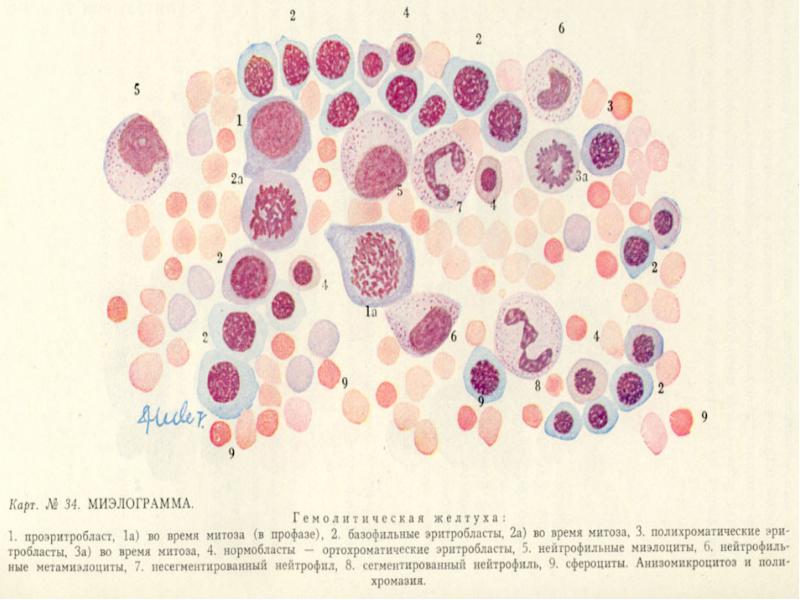
Миелограмма: гиперплазия красного ростка.
ОАМ: проба бензидина- гемоглобинурия, гемосидеринурия.

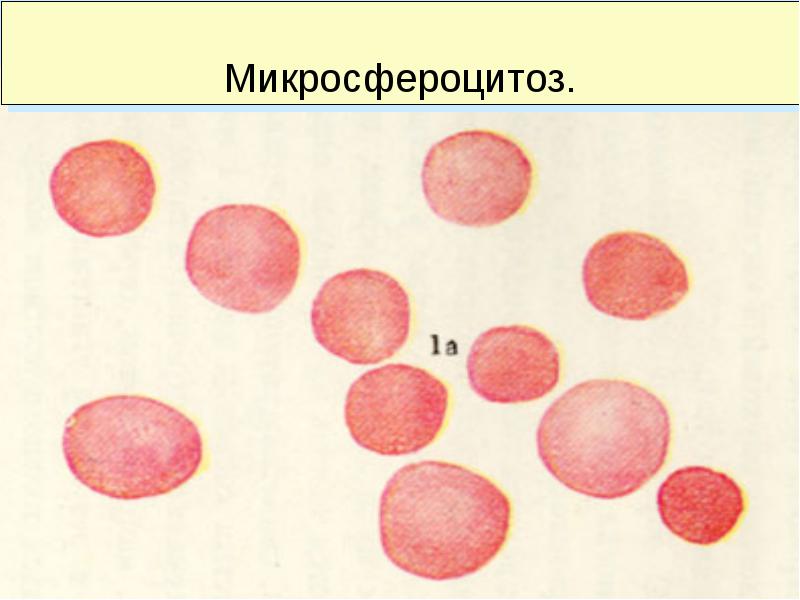

Лечение ГА.
При мембранопатиях спленэктомия;
При ферментопатиях отмена лекарств;
При серповидноклеточной анемии не выходить на горы, не плавать, не находиться на закрытых помещениях, оксигенотерапия.
При аутоиммунных гемолитических анемиях глюкокортикоиды (преднизолон).
При гемолитической болезни новорождённых заменное переливание крови
При укусе змей и насекомых введение специфических противоядных сывороток, при отравлении приём антидотов.
Дезинтоксикация: приём жидкостей, вливание NaCl 0,9%, глюкозы 5%, низкомолекулярного декстрана.
Эритроцитарная масса, оксигенотерапия
Трансплантация костного мозга.

Dostları ilə paylaş:
Железодефицитная анемия (ЖДА) – гипохромная микроцитарная анемия, развивающаяся вследствие абсолютного уменьшения запасов железа в организме.
Эпидемиология: ЖДА страдают около 200 млн. людей во всем мире; самая частая форма анемий (80%).
Этиология ЖДА:
1. Хронические периодические кровопотери (желудочно-кишечные кровотечения, маточные кровотечения, гематурия, кровоточащие опухоли, донорство и др.)
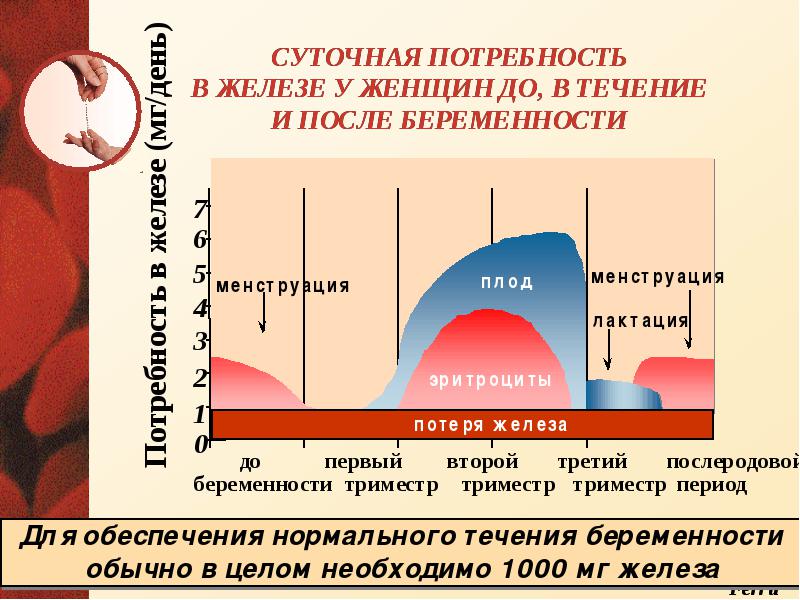
2. Повышенный расход железа (беременность, лактация, половое созревание, хронические инфекции)
3. Недостаточное поступление железа с пищей
4. Нарушение всасывания железа (синдром мальабсорбции, резекция желудка, высокая энтеропатия и др.)
5. Нарушение транспорта железа (наследственный недостаток трансферина, АТ к трансферрину)
6. Врожденный дефицит железа (нарушение реутилизации железа и т.д.)
Патогенез ЖДА:
В основе заболевания – дефицит железа, в котором выделяют 2 стадии:
а) латентный дефицит – уменьшаются запасы железа в печени, селезенке, костном мозге, при этом снижается уровень ферритина в крови, происходит компенсаторное усиление всасывания железа в кишечника и повышение уровня мукозного и плазменного трансферина; содержание сывороточного железа еще не снижено, анемии нет
б) собственно ЖДА – истощенные депо железа не способны обеспечить эритропоэтическую функцию костного мозга и, несмотря на сохраняющийся высокий уровень трансферина в крови, значительное содержается содержание сывороточного железа, синтез гемоглобина, развивается анемия и последующие тканевые нарушения.
При дефиците железа, помимо анемии, снижается активность железосодержащих и железозависимых ферментов в различных органах и тканях, уменьшается образование миоглобина ® дистрофические поражения эпителиальных тканей (кожи, слизистых ЖКТ, мочевыводящих путей и др.) и мышц (скелетный, миокарда).
Распределение железа в организме: 57-65% – гемоглобин; 27-30% – железо негемовых белков (ферритин, гемосидерин); 8-9% – миоглобин; до 0,5% – железо ферментов (цитохромов и пероксидаз); 0,1% – транспортное железо (с трансферрином).
Классификация ЖДА:
1) по этиологии:
а) хроническая постгеморрагическая ЖДА
б) ЖДА вследствие повышенного расхода железа
в) ЖДА вследстие недостаточного исходного уровня железа (у новорожденных и детей младшего возраста)
г) алиментарная ЖДА
д) ЖДА вследствие недостаточного всасывания в кишечнике
е) ЖДА вследствие нарушения транспорта железа
2) по стадии развития: латентная анемия и ЖДА с развернутой клинико-лабораторной картиной заболевания
3) по степени тяжести: легкая (Hb 90-120 г/л), средняя (Hb 70-90 г/л), тяжелая (Hb ниже 70 г/л).
Клиника ЖДА:
а) общеанемический синдром:
– общая слабость, повышенная утомляемость, снижение работоспособности, памяти, сонливость, головокружение, шум в ушах, мелькание мушек перед глазами, сердцебиение, одышка при физических нагрузках, склонность к ортостатическим обморокам
– бледность кожи и видимых слизистых оболочек (иногда с зеленоватым оттенком – «хлороз»)
– небольшая пастозность в области голеней, стоп, лица, утренние отеки – «мешки» над и под глазами
– синдром миокардиодистрофии (одышка, тахикардия, часто аритмия, умеренное расширение границ сердца влево, глухость тонов, систолический шум на верхушке)
б) сидеропеничекий синдром (синдром гипосидероза):
– извращение вкуса – непреодолимое желание употреблять в пищу что-либо необычное и малосъедобное (мел, зубной порошок, уголь, глину, сырое тесто, фарш, крупу); чаще встречается у детей и подростков
– пристрастие к острой, соленой, кислой, пряной пище
– извращение обоняния – пристрастие к запахам, которые большинством окружающих воспринимаются как неприятные (бензин, керосин, ацетон, запах лаков, красок, гуталина, нафталина и др.)
– выраженная мышечная слабость и утомляемость, атрофия мышц и снижение мышечной силы; императивные позывы на мочеиспускание, невозможность удержать мочу при смехе, кашле, чихании, возможно даже ночное недержание мочи (слабость сфиктера мочевого пузыря)
– дистрофические изменения кожи и ее придатков (сухость, шелушение, склонность к быстрому образованию на коже трещин; тусклость, ломкость, выпадение, раннее поседение волос; истончение, ломкость, поперечная исчерченность, тусклость ногтей; симптом койлонихии – ложкообразная вогнутость ногтей)
– дистрофические изменения слизистых: ангулярный стоматит – трещины, «заеды» в углах рта; глоссит – ощущение боли и распирания в области языка, покраснение его кончика, в дальнейшем атрофия сосочков («лакированный» язык); склонность к пародонтозу и кариесу; атрофические изменения ЖКТ (сухость слизистой пищевода и затруднения, а иногда боли при глотании пищи, особенно сухой – сидеропеническая дисфагия или симптом Пламмера-Винсона; атрофический гастрит и энтерит)
– снижение репаративных процессов в коже и слизистых
– симптом «синих склер» Ослера – синеватая окраска или выраженная голубизна склер (из-за нарушения гидроксилирования пролина и лизина при дефиците железа склера истончается и через нее просвечивается сосудистая оболочка глаза)
– «сидеропенический субфебрилитет» – длительное повышение температуры до субфебрильных величин
– выраженная предрасположенность к ОРВИ, хронизации инфекций (из-за нарушения фагоцитоза)
Диагностика ЖДА:
а) ОАК: снижение содержания гемоглобина и (в меньшей степени) эритроцитов; микроцитоз; ЦП < 0,8 (= 3*Hb / 3 первые цифры числа эритроцитов); нормальные лейкоциты и тромбоциты
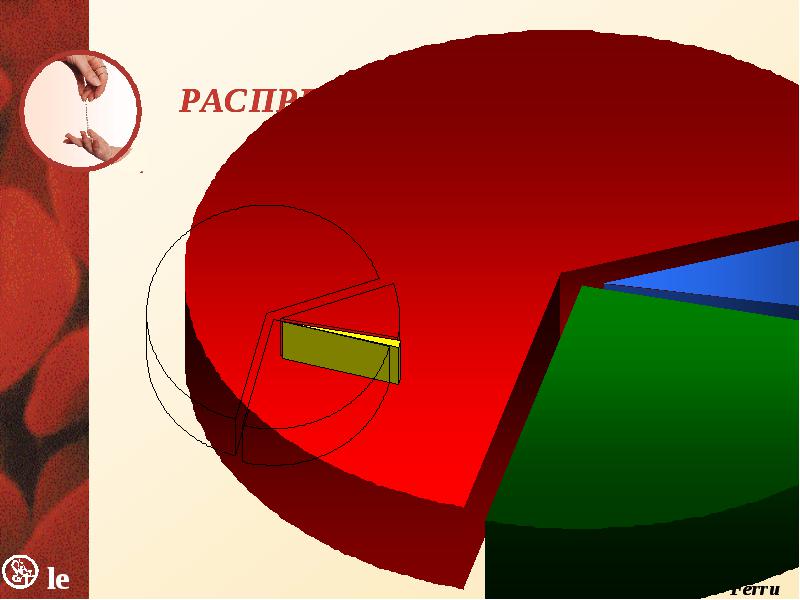
б) БАК: тесты феррокинетики:
1) сывороточное железо (СЖ): женщины – норма 11,5-30,4 мкмоль/л, при дефиците железа < 11,5 мкмоль/л; мужчины – норма 13,0-31,4 мкмоль/л, при дефиците железа < 11,5 мкмоль/л
2) общая железосвязывающая способность сыворотки (ОЖСС): женщины – норма 44,8-70,0 мкмоль/л, при дефиците железа > 70,0 мкмоль/л; мужчины – норма 44,8-70,0 мкмоль/л, при дефиците железа > 70,0 мкмоль/л
3) процент насыщения трансферрина железом (%НТЖ): женщины – норма 25-40%, при дефиците железа < 25%, мужчины – норма 25-50%, при дефиците железа < 25%
4) сывороточный ферритин: женщины – норма 10-100 нг/мл, при дефиците железа < 10 нг/л; мужчины – норма 30-200 нг/мл, при дефиците железа < 30 нг/мл
Принципы рациональной терапии ЖДА:
1. Основа лечения – препараты солевого железа per os; ЖДА невозможно купировать только диетой, богатой железом, т.к. из пищи в тонкой кишке всасывается 2-2,5 мг железа в сутки, а из препаратов – в 10-15 раз больше.
NB! Перед применением препаратов железа следует исключить сидероахрестическую (железонасыщенную) анемию, при которой дефицита железа нет, но оно не используется; образуются гипохромные эритроциты, а железо захватывается клетками макрофагальной системы и откладывается в органах и тканях, вызывая их гемосидероз. Назначение препаратов железа при данной анемии только ухудшит состояние больного!
2. Этапность лечения – 2 этапа (3-5 мес.):
1) купирование анемии (от начала терапии до нормального уровня Hb – обычно 4-6 недель)
2) «терапия насыщения» – восполнение депо железа в организме (8-12 недель – по 30-60 мг ЭЖ/сут).
3. Правильный расчет лечебной и профилактической дозы по элементарному железу (ЭЖ): лечебная доза рассчитывается по содержанию элементарного железа в препарате и для взрослого весом 70-80 кг составляет 100-200 мг ЭЖ
Основные препараты железа для перорального приема: «Ферроплекс»: 1 таблетка = 10 мг ЭЖ, «Ферроцерон»: 1 таблетка = 40 мг ЭЖ, «Феррокальм»: 1 таблетка = 44 мг ЭЖ; пролонгированные формы (1-2 раза/сут): Ферро-градумет»: 1 таблетка = 105 мг ЭЖ; «Мультирет»: 1 таблетка = 105 мг ЭЖ; «Тардиферон»: 1 таблетка = 80 мг ЭЖ; «Сорбифер»: 1 таблетка = 100 мг ЭЖ.
4. Лечение сочетают с одновременным применением аскорбиновой кислоты (0,3-0,5 г на прием), которая в 2-3 раза повышает всасывание железа в кишечнике; целесообразны также антиоксиданты и витамин В6.
5. Оптимально принимать препарат железа за 30 мин до еды, при плохой переносимости – через 1 час после еды, не разжевывая, запивая водой, можно фруктовыми соками без мякоти, но не молоком (кальций молока тормозит всасывание железа); для детей можно использовать сиропы – «Ферринсол», «Гемофер», «Интрофер».
6. Парентерально препараты железа используются по показаниям: синдром мальабсорбции; резекция желудка; резекция верхнего отдела тонкой кишки («Феррум-лек», «Эктофер», «Фербитол»).
7. При уровне гемоглобина < 70 г/л показано переливание эритроцитарной массы.
8. Критерии излеченности:
а) повышение уровня ретикулоцитов на 5-7 день от начала ферротерапии
б) повышение уровня гемоглобина с 3 (и раньше) недели лечения и восстановление его к 6-ой
в) нормализация показателей СФ, СЖ, ОЖСС, %НТЖ по окончании курса лечения
9. Профилактический курс ферротерапии – приём препарата по 30-40 мг ЭЖ/сутки в течение 4-6 недель (тардиферон по 1 таблетке в 2 дня и др.)
