Анемии лейкоз у детей
ЛЕКЦИЯ № 15. Анемии и лейкозы у детей
1. Анемия
Анемия (малокровие) – это полиэтиологическое заболевание, характеризующееся понижением содержанием гемоглобина, часто в сочетании с уменьшением количества эритроцитов.
Клиника. Заболевание проявляется изменением внешних признаков (бледностью кожных покровов, слизистых, склер), слабостью, головокружением, одышкой, тахикардией, нарушением памяти, появлением нарушений со стороны мышечной системы (слабости, снижения тургора тканей), отклонениями в центральной нервной системе (вялостью, апатией, легкой возбудимостью), функциональными нарушениями со стороны сердечно-сосудистой системы (расширением границ, появлением систолического шума), развитием гепатомегалии и спленомегалии, уменьшением в крови общего количества гемоглобина, эритроцитов, их осмотической стойкости.
Классификация анемий. Первичные (наследственные) и вторичные (приобретенные).
По причине:
1) дефицитные анемии, железодефицитные, витаминодефицитные, протеинодефицитные;
2) гипо– и апластические анемии: врожденная анемия Фанкони, анемия Даймонда – Блекфена, приобретенные анемии;
3) гемолитические анемии: сфероцитарная, серповидно-клеточная, аутоиммунная.
По тяжести:
1) легкая анемия – гемоглобин в пределах 90 – 110 г/л, число эритроцитов снижается до 3 млн;
2) анемия средней тяжести – гемоглобин 70 – 80 г/л, число эритроцитов снижается до 2,5 млн;
3) тяжелая анемия – гемоглобин ниже 70 г/л, число эритроцитов ниже 2,5 млн.
По цветовому показателю:
1) нормохромные;
2) гиперхромные;
3) гипохромные.
Железодефицитные анемии характеризуются снижением содержания гемоглобина из-за дефицита железа, связаны с нарушением синтеза порфиринов, талассемии, содержания эритроцитов в результате его нарушения при поступлении, усвоении или патологических потерь.
Этиология. Антенатальные причины:
1) нарушение маточно-плацентарного кровообращения, плацентарная недостаточность (токсикозы, угроза прерывания и перенашивания беременности, гипоксемический синдром, обострение соматических и острых инфекционных заболеваний);
2) фетоматеринские и фетоплацентарные кровотечения;
3) внутриутробная мелена;
4) недоношенность, многоплодие;
5) глубокий и длительный дефицит железа в организме беременной.
Интернатальные причины:
1) фетоплацентарная трансфузия;
2) преждевременная или поздняя перевязка пуповины;
3) интернатальные кровотечения из-за травматических акушерских пособий и (или) аномалий развития плаценты и сосудов пуповины.
Постнатальные:
1) недостаточное поступление железа с пищей (раннее искусственное вскармливание, использование неадаптированных молочных смесей, вскармливание коровьим или козьим молоком, несбалансированная диета, лишенная достаточного содержания мясных продуктов);
2) повышение потребности в железе у детей с ускоренными темпами роста (недоношенные, дети с большой массой тела при рождении, дети с лимфатическим типом конституции, дети пре– и пубертатного периода);
3) повышенная потеря железа из-за кровотечений различной этиологии, нарушения кишечного всасывания (наследственные и приобретенные синдромы мальабсорбции, хронические заболевания кишечника, гемморагические маточные кровотечения у девочек в период становления менструального цикла в пубертате), нарушение обмена железа в организме из-за гормональных нарушений (пре– и пубертатный гормональный дисбаланс), нарушения транспорта железа из-за снижения активности или содержания трансферрина в организме.
Клиника. В анамнезе – недостаточное, неправильное питание, вялость, повышенная утомляемость, сухость, шероховатость кожных покровов, ломкость ногтей, искривление и поперечная исчерченность ногтей, выпадение волос, извращения вкуса и обоняния, астеновегетативные нарушения, нарушения процессов кишечного всасывания, сердцебиение, одышка при физической нагрузке. По содежанию гемоглобина и эритроцитов анемии делятся на легкие (гемоглобин в пределах 90 – 109 г/л, эритроцитов менее 4 – 3,5 x 1012), анемии средней тяжести (гемоглобин в пределах 89 – 70 г/л, эритроцитов менее 3,5 x 1012), тяжелые анемии (гемоглобин менее 70 г/л, эритроциты менее 2,5 x 1012).
Диагностика – на основании клинических и лабораторных данных. в анализе крови – уменьшение эритроцитов, гемоглобина, концентрации сывороточного железа, уменьшение элементов крови, анизоцитоз, пойкилоцитоз. Цветовой показатель обычно низкий (иногда ниже 0,5); выраженная гипохромия эритроцитов, их анизоцитов, пойкилоцитоз; СОЭ обычно незначительно увеличена. Важнейший показатель болезни – снижение уровня железа в сыворотке (норма – 13 – 28 ммоль/л для мужчин; 11 – 26 ммоль/л для женщин). Низкий уровень сывороточного железа и ферритина, а также повышение уровня общей железосвязывающей способности сыворотки.
Лечение напрвлено на устранение дефицита железа и восстановление необходимого его запаса в организме. Терапию необходимо начать с устранения причин ее вызывающих и организации правильного, сбалансированного питания (в рацион должны включаться продукты, богатые витаминами и железом, особенно мясные). Лечение парентерально вводимыми препаратами железа менее эффективно, чем прием его в виде таблеток внутрь.
Для внутримышечного введения применяют жектофер, фербитол, Феррум Лек и др. Последний препарат выпускают и для внутривенного введения. Показанием к парентеральному введению железа при железодефицитной анемии служат тяжелые энтериты, состояния после обширных резекций тонкой кишки (но не резекций желудка). Дозы назначают из расчета 1,5 мг железа на 1 кг массы тела в сутки. Жектофер вводят в/м по 2 мл в день больному с массой тела 60 кг. Переливание крови при содержании гемоглобина ниже 60 г/л. Прием препаратов железа усиливает костномозговую продукцию эритроцитов и сопровождается подъемом уровня ретикулоцитов в крови через 8 – 12 дней после начала терапии (факт, имеющий дифференциально-диагностическое значение).
Прогноз благоприятный. Диспансерное наблюдение в течение 12 месяцев.
Анемии, связанные с дефицитом витамина В12независимо от причин этого дефицита характеризуются появлением в костном мозге мегалобластов, внутрикостномозговым разрушением эритроцитов, тромбоцитопенией и нейтропенией, атрофическими изменениями слизистой оболочки желудочно-кишечного тракта и изменениями нервной системы.
Этиология. Недостаточность витаминов редко бывает экзогенной (чаще эндогенной) природы, связанной с повышенным потреблением (при гельминотозах) и нарушением их всасывания различной природы (при заболеваниях желудка, синдроме мальабсорбции).
Патогенез. Дефицит витамина В12 чаще связан с нарушением выработки гликопротеина, соединяющегося с пищевым витамином В12 и обеспечивающего его всасывание (внутренний фактор). Нередко первые признаки заболевания появляются после перенесенного энтерита, гепатита. В первом случае это связано с нарушением всасывания витамина В12 в тонкой кишке, во втором – с расходованием его запасов в печени, являющейся основным депо витамина В12. Развитие В12-дефицитной анемии после тотальной гастрэктомии (когда полностью ликвидируется секреция внутреннего фактора) происходит через 5 – 8 лет и более после операции. В течение этого срока больные живут запасами витамина в печени при минимальном пополнении его за счет незначительного всасывания в тонкой кишке, не соединенного с внутренним фактором витамина. Редкой формой В12-дефицитной анемии является нарушение ассимиляции витамина при инвазии широким лентецом, когда паразит поглощает большое количество витамина В12. Причинами нарушенного всасывания витамина В12 при поражении кишечника могут быть тяжелый хронический энтерит, дивертикулез тонкой кишки, терминальный илеит, возникновение слепой петли тонкой кишки после операции на ней.
Клиника дефицита витамина В12 характеризуется поражением кроветворной ткани, пищеварительной и нервной систем. Появляются слабость, утомляемость, сердцебиения при физической нагрузке. Желудочная секреция угнетена, возможна стойкая ахлоргидрия. Нередко наблюдаются признаки глоссита – полированный язык, ощущение жжения в нем. Кожные покровы слегка желтушны, в сыворотке крови увеличен уровень непрямого билирубина (за счет повышенной гибели гемоглобинодержащих мегалобластов костного мозга). Определяется небольшое увеличение селезенки, реже печени.
Диагностика – на основании клинических и лабораторных данных. В анализе крови – гиперхромная анемия, лейкопения, тромбоцитопения, резко выраженный анизоцитоз эритроцитов наряду с очень крупными (более 12 мкм в диаметре) клетками – мегапоцитами, резчайший пойкилоцитоз, повышенное насыщение эритроцитов гемоглобином – гиперхромия, появление полисегментированных нейтрофилов, гиперхромный, реже нормохромный характер анемии, тромбоцитопения, лейкопения. Исследование костного мозга обнаруживает резкое увеличение в нем числа элементов эритроидного ряда с преобладанием мегалобластов. Клетки красного ряда, очень напоминающие мегалобласты, могут встречаться при остром эритромиелозе, который, как и В12-дефицитная анемия, сопровождается небольшой желтушностью, часто сочетается с лейко– и тромбоцитопенией. Однако при этом лейкозе нет столь выраженного анизо– и пойкилоцитоза, как при В12-дефицитной анемии, а главное – в костном мозге наряду с мегалобластоподобным и клетками встречаются в большом количестве миелобласты или недифференцируемые бласты. В сомнительных случаях следует после пункции костного мозга начать терапию витамином В12, которая при В12-дефицитной анемии через 8 – 10 дней приведет к резкому возрастанию в крови процента ретикулоцитов (рецикулоцитарный криз), подъему уровня гемоглобина, исчезновению в крови выраженного анизоцитоза, а в костном мозге – мегалобластов.
Лечение. Цианкобаламин (витамин В12) вводят ежедневно п/к в дозе 200 – 500 мгк 1 раз в день в течение 4 – 6 недель. После нормализации кроветворения и состава крови, наступающей через 1,5 – 2 месяца, витамин вводят 1 раз в неделю в течение 2 – 3 месяцев, затем в течение полугода 2 раза в месяц (в тех же дозах, что и в начале курса). В дальнейшем больных следует поставить на диспансерный учет; профилактически им вводят витамин В12 1 – 2 раза в год короткими курсами по 5 – 6 инъекций. Эта рекомендация может быть изменена в зависимости от динамики показателей крови, состояния кишечника, функции печени.
Фолиево-дефицитная анемия – мегалобластная анемия, сходная с проявлениями с В12-дефицитной анемии; развивается при дефиците фолиевой кислоты. Нарушение всасывания фолиевой кислоты наблюдается у беременных, страдающих гемолитической анемией, у недоношенных детей, при вскармливании их козьим молоком, у лиц, перенесших резекцию тонкой кишки, при целиакии, а также при длительном приеме противосудорожных препаратов типа фенобарбитала, дифенина.
Клиника аналогична, как при дефиците витамина В12.
Диагностика – на основании клинических и лабораторных данных. В анализе крови – снижение уровня фолиевой кислоты в эритроцитах и сыворотке крови.
Профилактика. Назначение фолиевой кислоты лицам, перенесшим ее дефицит, беременным, болеющим гемолитической анемией.
Гипо– и апластические анемии. В основе этого заболевания лежит уменьшение продукции клеток костного мозга.
Гемолитические анемии развиваются вследствие разрушения эритроцитов, характеризуются увеличением в крови содержания продуктов распада эритроцитов – билирубина или свободного гемоглобина или появлением гемосидерина в моче. Важный признак – значительное нарастание в крови ретикулоцитов за счет повышения продукции клеток красной крови. Костный мозг при гемолитических анемиях характеризуется значительным увеличением числа клеток красного ряда.
Анемия постгеморрагическая острая – малокровие вследствие острой кровопотери в течение короткого срока.
Этиология. Причиной кровопотери могут быть травмы, хирургическое вмешательство, кровотечение при язве желудка или двенадцатиперстной кишки, из расширенных вен пищевода, при нарушении гемостаза, внематочной беременности, заболеваниях легких и т. п.
Патогенез складывается из явлений острой сосудистой недостаточности, обусловленной острым опустошением сосудистого русла, потерей плазмы; при массивной кровопотере наступает и гипоксия из-за потери эритроцитов, когда эта потеря уже не может быть компенсирована ускорением циркуляции за счет учащения сердечных сокращений.
Клиника. Сосудистые нарушения (сердцебиение, одышка, падение артериального и венозного давления, бледность кожных покровов и слизистых оболочек).
Лечение начинают с остановки кровотечения.
Наследственные анемии, связанные с нарушением синтеза порфиринов (сидероахрестические анемии), характеризуются гипохромией эритроцитов, повышением уровня сывороточного железа, отложением железа с картиной гемосидероза органов.
Патогенез связан с нарушением синтеза протопорфирина, что ведет к нарушению связывания железа и накоплению его в организме при резко нарушенном образовании гемоглобина.
Клиника. Жалобы отсутствуют или отмечают небольшую слабость, утомляемость. Чаще страдают мужчины. Болезнь наследуется по рецессивному типу, наследование сцеплено с Х-хромосомой. В начале болезни отмечается небольшое увеличение селезенки, в дальнейшем в связи с повышенным отложением железа в органах развивается гемосидероз печени (печень увеличивается и становится плотной), поджелудочной железы (появляется картина сахарного диабета). Накопление железа в сердечной мышце приводит к тяжелой недостаточности кровообращения, гемосидероз яичек сопровождается развитием евнухоидизма. Иногда кожа приобретает серый оттенок.
Диагностика – на основании клинических и лабораторных данных. В анализе крови – выраженная гипохромия эритроцитов (цветовой показатель 0,4 – 0,6), уровень гемоглобина снижен, в меньшей степени изменено число эритроцитов, повышен уровень сывороточного железа. Морфологически отмечают анизоцитоз, пойкилоцитоз, иногда небольшое количество мишеневидных форм. Содержание ретикулоцитов обычно нормальное.
Лечение. Назначают пиридоксин (витамин В6) по 1 мл 5%-ного раствора в/м 2 раза в день. При эффективной терапии через 1,5 недели резко возрастает содержание ретикулоцитов, а затем повышается и уровень гемоглобина.
Мегалобластные анемии – группа анемий, общим признаком которых служит обнаружение в костном мозге своеобразных эритрокариоцитов со структурными ядрами, сохраняющими эти черты на поздних стадиях дифференцировки (результат нарушения синтеза ДНК и РНК в клетках, называемых мегалобластами), в большинстве случаев мегалобластная анемия характеризуется цветовым показателем выше единицы. Поскольку синтез нуклеиновых кислот касается всех костномозговых клеток, частыми признаками болезни являются уменьшение числа тромбоцитов, лейкоцитов, увеличение числа сегментов в гранулоцитах.
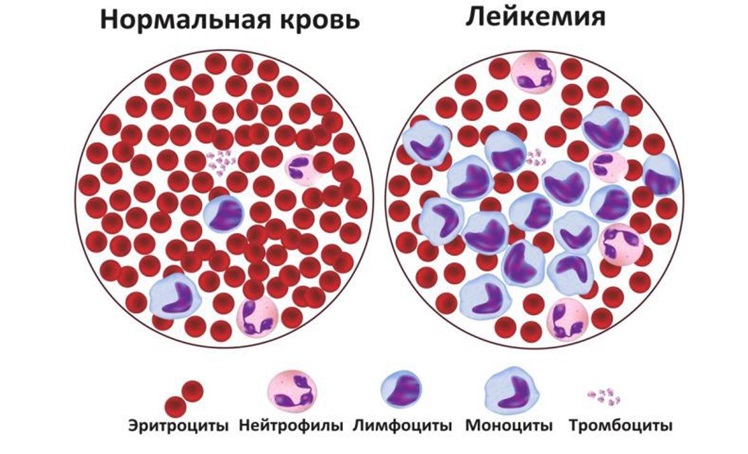
2. Лейкозы
Лейкозы – это общее название злокачественных опухолей возникающих из кроветворных клеток и поражающих костный мозг. Заболеваемость колеблется от 1 до 5 на 1 000 000 детского населения с пиком в возрасте от 2 до 4 лет. Хронический миелолейкоз – это опухоль, возникающая из дифференцирующихся клеток – предшественников миелопоэза.
Этиология. Не установлена, но наиболее распространенная теория – вирусно-генетическая. Роль факторов, ослабляющих реактивность организма: иммунодефицитные состояния, хромосомные аномалии, врожденная и гипопластическая анемия Фанкони, ионизирующее излучение, акселерация с лимфатизмом.
Патогенез. Лейкозные клетки являются потомством одной мутировавшей костномозговой кроветворной клетки, утратившей способность к созреванию, но сохраняющей способность к размножению.
Опухолевая прогрессия при лейкозах: угнетение нормальных ростов кроветворения, изменение морфологии пораженной кроветворной клетки и исходящего из ее клона опухолевых клеток, метастазирующих и растущих вне органов кроветворения; выделение лейкозными клетками веществ, угнетающих нормальное кроветворение; самоподдерживаемость лейкемического клона и динамичность его свойств в процессе лечения с приобретением большой агрессивности и устойчивости к действию цитостатиков.
Классификация: острые лейкозы (могут быть лимфобластными и миелобластными) и хронические лейкозы.
Клиника. Основные синдромы – это анемический, интоксикационный, геморрагический, пролиферативный, костно-суставной, поражение внутренних органов, нервной системы, инфекционные осложнения.
Диагностика – на основании клинических и лабораторных данных, анализа периферической крови, миелограммы, цитохимического исследования бластов крови и костного мозга.
Дифференциальный диагноз проводят с инфекционным мононуклеозом, инфекционным лимфоцитозом, лейкемоидными реакциями при инфекционных заболеваниях, лекарственной болезни и отравлениях.
Лечение препаратами, обладающими иммунодепрессивным и цитостатическим эффектами по периодам индукции, консолидации, реиндукции. Симптоматическая терапия, лечение инфекционных осложнений.
Лейкозы относятся к большой группе злокачественных новообразований системы крови под названием «гемобластозы». Лейкоз (от греческого слова «leukos» — белый) — злокачественная опухоль, возникающая из ранних незрелых кроветворных клеток костного мозга и метастазирующая из костного мозга в кровь, лимфатические узлы, печень, селезенку, головной мозг, спинной мозг и другие органы и ткани.

Все лейкозы можно разделить на острые лимфобластые, острые миелоидные лейкозы (ОМЛ) и хронический миелолейкоз.
Острый лимфобластный лейкоз
Более 80% всех лейкозов у детей составляет острый лимфобластный лейкоз (ОЛЛ). Причиной его развития является химерный ген TEL/AML, формирование которого происходит внутриутробно, возможно, в результате спонтанных ошибок в процессе репликации и репарации ДНК. Накопление генетических аномалий в опухолевом клоне ведет к блоку нормальной клеточной дифференцировки и нарушениям в процессе пролиферации и апоптоза.
В соответствии с франко-американо-британской (FAB) классификацией выделяют три морфологических варианта: L1, L2, L3.
Клинические симптомы ОЛЛ обусловлены степенью инфильтрации костного мозга лимфобластами, а также наличием экстрамедуллярного распространения процесса. Нередко отмечаются общие симптомы опухолевой интоксикации, а именно, повышение температуры тела, снижение аппетита, слабость, вялость. В течение процесса выделяют несколько периодов: начальный, развернутый, период ремиссии.
Развернутый период характеризуется бурным началом, многообразием клинических симптомов. К симптомам общей интоксикации присоединяются костные боли вследствие лейкозной инфильтрацией костной ткани (чаще поражаются диафизы длинных трубчатых костей), артралгии, вызванные лейкемической инфильтрацией суставов. Кожные покровы и слизистые становятся бледными. К сожалению, нередко на них появляются кровоизлияния, обусловленные геморрагическим синдромом, а также кровотечения (носовые, желудочно-кишечные, почечные). Увеличение периферических лимфатических узлов (шейно-надключичных, подмышечных, паховых) является одним из основных симптомов заболевания. Практически у всех пациентов отмечается обусловленное пролиферацией лейкозных клеток увеличение печени и селезенки. В некоторых случаях у пациентов поражение кожи и слизистых оболочек проявляется в виде лейкемидов, некроза, гингивита и стоматита.
Таким образом, можно выделить несколько симптомокомплексов, характерных для ОЛЛ:
- гиперпластический – лимфоаденопатия, боли в костях, тяжесть и боли в левом и правом подреберьях, гепатоспленомегалия;
- анемический – головокружение, мерцание мушек перед глазами, одышка при физической нагрузке, сердцебиение, шум в голове и ушах;
- геморрагический – кожные геморрагии, кровоточивость десен, носовые кровотечения;
- интоксикационный – повышение температуры тела, слабость, отсутствие аппетита, оссалгии;
- синдром инфекционных осложнений – присоединение тяжелых пневмоний.
При диагностике оцениваются морфологические особенности бластов костного мозга и периферической крови. Помимо обнаружения опухолевых клеток лимфоидной линии кроветворения при окраске по Романовскому – Гимзе, проводятся следующие методы исследования:
- цитохимические – позволяют отнести бласты к лимфоидному или миелоидному ростку (тест на миелопероксидазу, фосфолипиды, гликоген), отдельным клеточным линиям;
- иммунофенотипические – определяют иммунные маркеры клеток (CD);
- цитогенетические – определяют аномалии кариотипа и хромосомные аберрации (делеции, транслокации, инверсии и др.);
- молекулярно-биологические – позволяют установить количество клеток с определенной аберрацией во всей массе костного мозга.
Для подтверждения диагноза ОЛЛ необходимо комплексное обследование, в котором ведущая роль отводится морфологическому методу.
В настоящее время используются программы лечения BFM (БФМ: Берлин-Франкфурт-Мюнстер) и МВ (МБ: Москва-Берлин).
Все лечение можно разделить на базисное и сопроводительное. Базисная терапия представляет собой системную и локальную химиотерапию и, при необходимости, лучевую терапию. Сопроводительное лечение обязательно назначается для профилактики инфекционных осложнений и коррекции постцитостатических реакций. Выделяют следующие этапы в лечении злокачественных процессов: индукция ремиссии, консолидация ремиссии (как правило, несколько фаз), поддерживающее лечение.
Острый миелоидный лейкоз
Острый миелоидный лейкоз составляет 15% всех острых лейкозов у детей. Существующая FAB-классификация (Франко-Американо-Британская) позволяет разделить ОМЛ на следующие варианты:
- M0 (минимально дифференцированный ОМЛ), который характеризуется бластными клетками средних размеров с округлым ядром, отсутствием зернистости и палочек Ауэра в цитоплазме;
- М1 (ОМЛ без созревания), при котором менее 90% неэритроидных клеток представлены бластными клетками с преобладающей мезогенераций с округлыми ядрами и высоким ядерно-цитоплазматическим отношением;
- М2 (ОМЛ с созреванием), характеризующийся бластными клетками средних размеров с высоким и умеренным ядерно-цитоплазматическим отношением (20 – 90% всех неэритроидных клеток), в их цитоплазме выражено наличие азурофильной зернистости и палочек Ауэра;
- М2 баз (базально-клеточный), бластные клетки характеризуются наличием базофильной зернистости, составляет не более 0,5% острых нелимфобластных лейкозов;
- М3 (промиелоцитарный) вариант характеризуется бластными клетками крупных размеров с ядрами неправильной формы, отмечается крупная зернистость и палочки Ауэра в цитоплазме;
- М3v (гипогранулярный) с отсутствием зернистости;
- М4 (миеломонобластный): бластные клетки с ядрами округлой и неправильной формы, низким и умеренным ядерно-цитоплазматическим отношением, некоторые бластные клетки могут содержать зернистость, палочки Ауэра;
- М5а (монобластный без созревания), при котором монобласты составляют свыше 80% моноцитоидных клеток, бластные клетки крупных размеров с ядрами бобовидной или лопастной формы, в части из них просматривается зернистость, палочки Ауэра при этом не выявляются;
- М5b (монобластный с созреванием): монобласты составляют менее 80% моноцитоидных клеток, крупные с ядрами моноцитоидной формы, цитоплазмой без зернистости, палочки Ауэра не выявляются;
- М6 (эритромиелоз): более 50% бластом в костном мозге представлены эритробластами;
- М7 (мегакариобластный) лейкоз, при котором бластные клетки полиморфны, с отростчатой базофильной цитоплазмой, какие-либо специфические морфоцитохимические признаки отсутствуют.
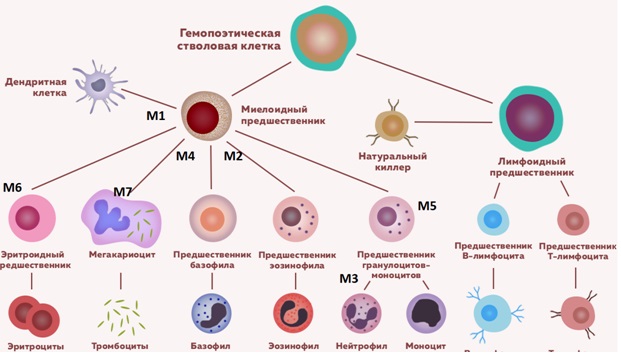
Схема гемопоэза с клетками предшественниками острого миелоидного лейкоза
Клиническая картина ОМЛ также складывается из анемического, геморрагического и токсического синдромов, которые являются следствием снижения продукции эритроцитов, тромбоцитов и гранулоцитов.
У 50% пациентов отмечается увеличение размеров печени (гепатомегалия) и селезенки (спленомегалия) вследствие инфильтрации органов опухолевыми клетками.
Внекостномозговые проявления заболевания связаны с лейкозной инфильтрацией центральной нервной системы и метастатическим поражением оболочек и вещества головного и спинного мозга (нейролейкемия). В этих ситуациях отмечается постоянная головная боль, возможна рвота, вялость, выявляется отек дисков зрительных нервов, могут быть нистагм, косоглазие, другие признаки поражения черепно-мозговых нервов, выявляются ригидность затылочных мышц, симптом Кернига.
Решающую роль в диагностике также имеет цитохимическое, иммунофенотипическое и морфологическое исследование бластов в костном мозге и периферической крови.
Ремиссию заболевания можно достичь посредством проведения высокодозной полихимиотерапии с последующей трансплантацией гемопоэтических стволовых клеток от HLA-геноидентичного родственного или альтернативного (неродственного, гаплоидентичного) донора у пациентов группы высокого риска рецидива. Благодаря адаптивным протоколам удается достичь ремиссии у 90% детей.
Хронические миелолейкоз
Хронический лейкоз – это вариант гемобластоза, субстратом которого являются созревающие клетки. У детей встречается только хронический миелолейкоз, который характеризуется пролиферацией гранулоцитарного ростка, гиперплазией миелоидной ткани, миелоидной метаплазией кроветворных органов, ассоциированной с хромосомной транслокацией t(9;22)(q34;q11), в результате которой образуется химерный онкоген BCR-ABL.
В течение хронического миелолейкоза выделяют три фазы:
- Хроническая фаза: выраженные симптомы отсутствуют.
- Фаза акселерации: повышение уровня лейкоцитов (>50 х 109/л), бластов в периферической крови и костном мозге (> 10%); анемия и тромбоцитопения; персистирующий тромбоцитоз (> 1000 х 109/л).
- Острая (бластная) фаза: миелобласты >30% в крови или в костном мозге; лимфобласты >30% в крови или в костном мозге; наличие бластных клеток в ликворе.
В дебюте заболевание трудно диагностировать, поскольку основные симптомы обусловлены общим опухолевым симптомокомплексом и носят преходящий характер. Наиболее частые симптомы, присоединяющиеся позднее – гепатомегалия и спленомегалия. Нарастающая интоксикация приводит к появлению слабости, утомляемости, повышению температуры тела, болям в костях.
В периферической крови отмечается гиперлейкоцитоз (до 200 – 300 х 109/л и более) с увеличением содержания гранулоцитов до 95% и преобладанием незрелых клеток гранулоцитарного ряда: промиелоцитов, миелоцитов, метамиелоцитов, миелобластов, базофилов (до 10%) и эозинофилов (до 5%). Характерна анемия и повышение СОЭ. Уровень тромбоцитов преимущественно в норме, однако может отмечаться гипертромбоцитоз (до 600 х 109/л и более).
В пунктате костного мозга отмечается увеличение числа миелокариоцитов за счет пролиферирующего пула клеток гранулоцитарного ряда с увеличением базофилов и эозинофилов. Позднее отмечается угнетение эритронормобластического и мегакариоцитарного ростков кроветворения.
Основным средством терапии и стандартом лечения хронического миелолейкоза в настоящее время является применение ингибиторов тирозинкиназы (ИТК). Данные препараты имеют механизм таргетного (целенаправленного) воздействия на BCR-ABL-положительные опухолевые клетки и должны назначаться всем пациентам после подтверждения диагноза. Для оценки эффективности и переносимости терапии ИТК рекомендуется регулярный мониторинг гематологических, цитогенетических и молекулярно-генетических и других показателей у пациента.
Список литературы
- Кузник Б. И. Клиническая гематология детского возраста: учеб. пособие / Б. И. Кузник, О. Г. Максимова. — М.: Вузовская книга, 2010. — 496 с.
- Румянцев А. Г. Практическое руководство по детским болезням. Т. 4. Гематология/онкология детского возраста / А. Г. Румянцев, Е. В. Самочатова. — М. : Медпрактика-М, 2004. — 792 c.
- Румянцев А.Г. Эволюция лечения острого лимфобластного лейкоза у детей. Педиатрия, 2016; 95(4): 11-22.
- Möricke A., Zimmermann M., Reiter A., et al. Long-term results of five consecutive trials in childhood acute lymphoblastic leukemia performed by the ALL-BFM study group from 1981 to 2000. Leukemia. 2010 Feb;24(2):265-84. doi: 10.1038/leu.2009.257.
- Creutzig U, van den Heuvel-Eibrink MM, Gibson B, et al. AML Committee of the International BFM Study Group. Diagnosis and management of acute myeloid leukemia in children and adolescents: recommendations from an international expert panel. Blood. 2012 Oct 18;120(16):3187-205. doi: 10.1182/blood-2012-03-362608.
- de la Fuente J, Baruchel A, Biondi A, de Bont E, Dresse MF, Suttorp M, Millot F; International BFM Group (iBFM) Study Group Chronic Myeloid Leukaemia Committee. Managing children with chronic myeloid leukaemia (CML): recommendations for the management of CML in children and young people up to the age of 18 years. Br J Haematol. 2014 Oct;167(1):33-47. doi: 10.1111/bjh.12977.
