Анемия аддисона бирмера гематологические показатели
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 21 января 2019;
проверки требуют 6 правок.
Перницио́зная анеми́я (от лат. perniciosus — гибельный, опасный) или B12-дефицитная анемия или мегалобластная анемия или болезнь Аддисона — Бирмера или (устаревшее название) злока́чественное малокро́вие — заболевание, обусловленное нарушением кроветворения из-за недостатка в организме витамина B12. Особенно чувствительны к дефициту этого витамина костный мозг и ткани нервной системы.
Основные сведения[править | править код]
Это синдром, связанный с недостатком B12 и фолиевой кислоты в организме. Характеризуется наличием в костном мозге большого количества крупных незрелых предшественников эритроцитов (мегалобластов).
Витамин B12всасывается в основном в нижней части подвздошной кишки. Анемия может быть вызвана недостаточным потреблением витамина B12 в пищу, недостаточной выработкой внутреннего фактора Касла в париетальных клетках желудка, патологическими процессами в подвздошной кишке с нарушением всасывания или конкуренцией за витамин B12 со стороны ленточных червей или бактерий.
При дефиците витамина B12 на фоне анемической клинической картины (или без неё) могут возникнуть и неврологические расстройства из-за связанного с дефицитом витамина B12 нарушения синтеза жирных кислот. Может наблюдаться демиелинизация и необратимая гибель нервных клеток. Симптомами такой патологии являются онемение или покалывание конечностей и атаксия.
Проявления[править | править код]
- Ярко-красный, а затем «лакированный» язык.
- Желудочная ахилия.
- Малокровие с наличием патологических эритроцитов.
- Поражение нервной системы.
- Желтоватый цвет кожи.
- Образование в костном мозге аномальных крупных клеток вместо эритроцитов (переход на мегалобластический тип кроветворения).
Причины[править | править код]
- Недостаток витамина B12 в питании или нарушение его всасывания
- Расстройство кишечника
- Долгое использование медицинских препаратов, приводящих к уменьшению кислотности в желудке
- Гастрэктомия
- Аутоиммунное поражение внутреннего фактора Касла или париетальных клеток.
- Заражение ленточными червями (лентец широкий)
- Токсическое воздействие на стенку желудка
- Рак желудка
- Наследственный дефект, передается аутосомно-рецессивно
Осложнения[править | править код]
В отсутствие лечения развиваются анемия и дегенерация нервов, так как костный мозг и ткани нервной системы особенно чувствительны к дефициту витамина B12.
Историческая справка[править | править код]
В 1855 году английский врач Томас Аддисон, а затем в 1872 году более подробно немецкий врач Антон Бирмер описали болезнь, которую назвали злокачественной (пернициозной) анемией. Вскоре французский врач Арман Труссо предложил называть эти болезни аддисоновой анемией и болезнью Аддисона.
В 1926 году Дж. Уипл, Дж. Майнот и У. Мерфи сообщили, что пернициозная анемия лечится введением в рацион питания сырой печени и что в основе заболевания лежит врожденная неспособность желудка секретировать вещество, необходимое для всасывания витамина B12 в кишечнике. За это открытие они в 1934 году получили Нобелевскую премию.
См. также[править | править код]
- Внутренний фактор
- https://en.wikipedia.org/wiki/Vitamin_B12_deficiency
Примечания[править | править код]
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
Ссылки[править | править код]
- Анемия
- Наше здоровье
- [da-med.ru/diseases/cat-60/d-125/ Da-med.ru ::: B12-дефицитная анемия (Пернициозная анемия)]
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист. Эти сайты могут нарушать авторские права, быть признаны неавторитетными источниками или по другим причинам быть запрещены в Википедии. Редакторам следует заменить такие ссылки ссылками на соответствующие правилам сайты или библиографическими ссылками на печатные источники либо удалить их (возможно, вместе с подтверждаемым ими содержимым). Список проблемных доменов |
Лабораторная диагностика болезни Аддисона-Бирмера (злокачественной анемии) – анализы
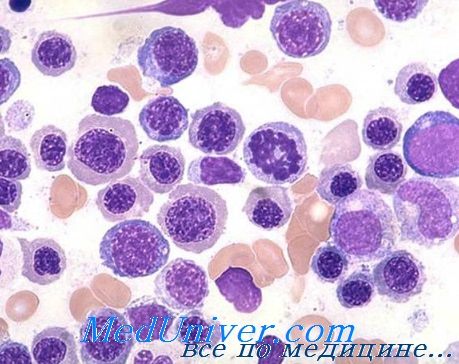
В периферической крови макроцитоз наиболее показательный элемент. Большинство эритроцитов крупных размеров (до 12 u и более), немного овальной формы, хорошо загруженные гемоглобином (без светлой центральной зоны); тем не менее существуют эритроциты и меньших размеров (менее 5 u), некоторые из них нерегулярной формы (пойкилоциты); также встречаются точечнобазофильные эритроциты, кольца Cabot.
Наличие анизоцитоза отмечает широкая кривая Price-Jones, верхушка которой сдвинута вправо; в принципе DEM (СДЭ) укладывается в пределы от 8 до 9 u, а иногда и более.
Соответственно повышаются показатели VEM (СОЭ) (95—110 u3, иногда более 140 u3) и НЕМ (33—38 пг, в отдельных случаях 50 пг.) В связи с макроцитозом число эритроцитов меньше соответственных показателей гемоглобина и гематокрита, при этом больные переносят относительно хорошо анемию, показатель которой равняется 1,5 мл Э/мм3. Число ретикулоцитов меньше нормы. Важным но не постоянным признаком для постановки диагноза составляет наличие в крови единичных мегалобластов.
Лейкоцитная картина характеризуется, вообще, умеренной лейкопенией (от 3000 до 5000 на мм3), сокращением численности гранулоцитов, которые крупные и проявляют тенденцию к гиперсегментированию (одновременно появляются молодые элементы — метамиэлоциты и миэлоциты). Численность тромбоцитов умеренно уменьшается (редко менее 50 тыс.), при этом отмечается анизоцитоз, в отдельных случаях с некоторым функциональным дефицитом.
В костном мозге обнаруживается (выраженная) гиперплазия предшественников эритроцитов и мегалобластические изменения во всех костномозговых рядах, морфологический характер, генез и последствия которых уже рассматривались при описании мегалобластоза. В некоторых тяжелых случаях обнаруживается наличие эктопических очагов кроветворения в печени и селезенке.
Среди прочих биологических постоянных бирмеровской болезни следует отметить: гипербилирубинемию (в основном костномозговой природы) — с увеличенным выделением с фекалиями билирубиновых телец (до 800 мг в сутки); рост показателя сывороточных ферментов — таких как лактикодегидрогеназа (изофермент эритроидной природы), малико-6-фосфоглюконат и 2-гидроксибутиратдегидрогеназа (за счет неэффективности эритропоэза и повышения их активности в мегалобластах); некоторые сдвиги в белковом обмене (увеличивается выделение с мочой аминокислот, растет РОЭ, уменьшается гаптоглобин (в связи с расплавлением крови), также в жировом обмене (при этом уменьшаются альфа- и растут бета-липопротеиды, сокращается поглощение кишечником жирных кислот); нарушение гемостаза (в принципе легкое, за счет тромбоцитопении и понижения активности протромбина).

Что касается обмена железа нередко обнаруживается наличие завышенного количества железа в крови с общей невысокой способностью связывания, одновременно понижение поглощения железа кишечником.
В процессе диагностирования представляют значение определения метаболизма витамина В12.
В сыворотке уровень витамина В12 (определяемый микробиологическом путем или способом радиоактивных изотопов) в отдельных случаях значительно меньше критического — 100 пг/мл.
Поглощаемость кишечником витамина В12 определяется реакцией Шиллинга, которая, судя по леченным нами больным, предоставляет существенную информацию. Эта реакция заключается в назначении внурть небольшого количества радиоактивного витамина (0,5 uCi), а спустя 2 ч с помощью внутримышечного инъецирования еще 1000 мкг витамина В12 (чтобы воспрепятствовать связыванию поглощаемого 60СоВ12 и одновременно способствовать его удалению). В подобных условиях за сутки у человека в норме выделяются с мочой 10% введенной в организм радиоактивности, в то время как у страдающих бирмеровской болезнью — менее 2%.
Однако заключение, по которому неполноценность поглощения обусловлена отсутствием внутреннего фактора требует подтверждения повторным испытанием (спустя 2 недели) при одновременном введении ВФ для поправки результата (при бирмеровской болезни). К ведущим факторам погрешности относятся почечная и сердечная недостаточность, инфекционные заболевания и пр.
На практике лишь в редких случаях оказывается необходимым определение активности внутреннего фактора в желудочном соке или исследование в сыворотке антител против внутреннего фактора (серологическим методом или путем радиоактивных изтотопов).
Косвенным методом выявления недостатка В12 является определение выделения с мочой метилмалоновой кислоты (норма 1—7 мг в сутки); при бирмеровской болезни этот показатель растет до нескольких десятков или даже сотен мг/сутки (в частности при формах болезни с невропатией).
Реакция на суппрессию включения дезоксиуридина (дУ), при дефиците В12 или фолиевой кислоты, основывается на факте включения меченного тимидина в эритробласты (или стимулированные лимфоциты), преимущественно по сравнению с дезоксиуридином (которого метилирование не преобразовывает в тимидин); откорригировать это положение возможно добавлением недостающего витамина (Killman).
В текущей клинической практике диагноз болезни Бирмера можно заподозрить по данным анамнеза и клинического обследования. Выявление признаков мегалобластической анемии и неподдающейся гистамину ахилии желудка по существу обеспечивают диагностирование, при этом подтверждение правильности определения дает наступление межприступного периода после назначения специфической терапии.
Реакция Шиллинга применяется для подтверждения отсутствия внутреннего фактора, в частности у леченных лиц или в случаях неполной симптоматологии. Определение витамина в крови (равно как и выделения АММ) можно применять лишь в сложных случаях (например при подозрительной нервной симптоматологии, без анемии), при этом сыворотку отбирать до начала лечения и сохранить в замороженном состоянии.
Дифференциальная диагностика рассматривается в общих сведениях о мегалобластической анемии.
– Также рекомендуем “Лечение болезни Аддисона-Бирмера (злокачественной анемии)”
Оглавление темы “Анемии”:
- Лечение апластической анемии – пересадка костного мозга
- Эритробластопении – причины, клиника, диагностика, лечение
- Остеопетроз (мраморная болезнь, болезнь Альберса-Шенберга) – клиника, диагностика, лечение
- Мегалобастическая анемия – морфология, причины
- Обмен витамина В12 в норме и его источники. Значение цианокобаламина
- Классификация недостатка витамина В12 – причины дефицита цианокобаламина
- Болезнь Бирмера (Аддисона-Бирмера, злокачественная анемия) – история изучения, причины
- Клиника болезни Аддисона-Бирмера (злокачественной анемии) – признаки
- Лабораторная диагностика болезни Аддисона-Бирмера (злокачественной анемии) – анализы
- Лечение болезни Аддисона-Бирмера (злокачественной анемии)
Существует несколько видов патологий, связанных с нехваткой микроэлементов в организме. Одна из них — анемия Аддисона Бирмера. Это злокачественное течение болезни, выражающееся анемия в дефиците витамина В12 и фолиевой кислоты. Заболевание, встречающееся в 30 – 50 случаях на 10000 населения, больше подвержены этому недугу женщины, причем, в возрасте старше 50 лет риск развития болезни возрастает (возможно это связано с менопаузой).
Классификация
Впервые анемия Аддисона Бирмера развивается при дефиците витамина B12, она была описана в 1855 году Аддисоном, позднее подтвердилась Бирмером, который изучил болезнь и дал подробное клиническое описание. Впоследствии, это состояние получило название по именам своих исследователей. Долгое время считалась заболеванием неизлечимым, протекающим тяжело и неудержимо. В настоящее время достаточно ясен патогенез заболевания, но этиология в большей мере остается лишь предположением.
Анемия Аддисона — Бирмера характеризуется наличием специфической триады нарушений в организме:
- Тяжелое течение гастрита по атрофическому типу. Происходит постепенное снижение функции железистого эпителия, слизистая инфильтрируется, замещается несвойственными данному органу клетками, выработка ферментов в крови резко сокращается или прекращается вовсе.
- Невозможность усвояемости витамина В12 и фолиевой кислоты. Оба компонента необходимы для построения клеток, с их помощью синтезируется ДНК и правильно формируется ядро клетки. При недостатке и того, и другого страдают, прежде всего, гемопоэз и нервная ткань.
- Развитие мегалобластного кроветворения. Это образование множества незрелых гранулоцитов крови, не способных нормально выполнять свои функции. В этом течение анемии Аддисона-Бирмера схоже со злокачественными болезнями крови.
Причины
Основным фактором, ведущим к развитию заболевания, причины анемии Аддисона Бирмера является атрофия слизистой оболочки желудка, в результате прекращается секреция (выработка) пепсиногена. А роль пепсиногена в организме такова, что он обеспечивает транспорт и всасывание цианкобаламина. Однако далеко не всегда атрофический гастрит ведет к развитию мегабластной анемии. Вероятно, для развития болезни должны совпасть несколько факторов.
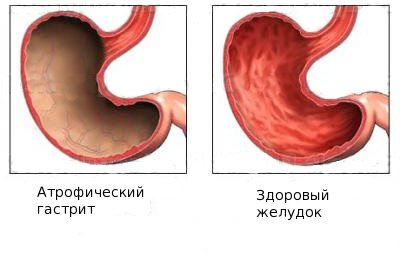 Атрофия слизистой желудка
Атрофия слизистой желудка
Усвоение В12 и фолиевой кислоты может нарушиться из-за обширного воспаления слизистой желудка и подвздошного отела кишечника или поражения их злокачественными опухолями.
Пернициозная анемия в, немалой степени, является аутоиммунным заболеванием, так в сыворотке крови пациентов в 70 -75% случаев выявлены антитела к внутренним клеткам желудка. При проведении опытов над крысами, выяснилось, что подобные клетки ведут к атрофии желудочной железистой ткани. Подобные антитела присутствуют и в желудочном секрете. Аутоиммунный ответ с высокой долей вероятности можно считать наследственным фактором, так как некоторое количество антител против париетальных клеток желудка, а так же клеток эндокринной системы обнаруживаются у здоровых родственников.
Дополнительным, но не менее важным фактором является наследственная склонность к заболеваниям поджелудочной железы.
Образ жизни, ведущий к сбоям в иммунной системе, например, экспериментирование с жесткими принципами диеты, резкий переход на вегетарианство, неконтролируемый прием медицинских препаратов, нарушение дозировок в приеме лекарств. Что важно, в послевоенные голодные годы заболеваемость пернициозной анемией не возрастала, а значит, недоедание количественное и качественное можно отнести лишь к сопутствующим причинам.
Поражение кишечника некоторыми паразитическими микроорганизмами и чрезмерное развитие патологической кишечной микрофлоры.
Существуют разрозненные факты по описанию случаев заболеваемости мегалобластной анемией. Например: в северных районах это патология встречается чаще; есть указания на увеличение заболеваемости у людей, чья работа связана со свинцом и возможностью медленного отравления окисью углерода; после операции по удалению желудка, когда происходит тотальная ликвидация секреторной функции, анемия способна развиться спустя 5-7 лет; есть сведения о развитии мегабластной анемии, как результате токсического отравления при хроническом алкоголизме.
Симптомы
Симптомы анемии Аддисона-Бирмера выглядит следующими образом, нарушается свертываемость крови, образуются эритроцитарные клетки аномальных размеров, с разросшейся цитоплазмой, а их ядра, содержат мелкие включения.
Из-за критической нехватки витамина В12 возникает дефект в метаболизме фолиевой кислоты, участвующей в синтезе ДНК. Как результат, нарушается деление клеток и понижается уровень эритроцитов на периферии. Таки же количественные и качественные деформации происходят и с тромбоцитами. Костный мозг изменяет окраску, приобретает насыщенный алый цвет, в нем преобладают мегабластные незрелые клетки, которые по типу развития напоминают злокачественное течение заболеваний крови.
Витамин В12 используется организмом не только для гемопоэза, но и для обеспечения нормальной работы нервной системы. При его недостатке наблюдается дистрофия в нервных окончаниях позвоночного столба.
Со стороны пищеварительной системы выявляется атрофия слизистой оболочки неба, глотки, пищевода, желудка и кишечника. Возможно образование полипов, небольшое увеличение печени. Клиника течения болезни анемии Аддисона-Бирмера проявляется постепенно: периодически возникает сильная слабость, хроническая усталость, усиливаются приступы головокружения, возникает шум в ушах.
Возникающие симптомы анемии Аддисона Бирмера можно разделить на проявления:
- со стороны нервной системы: нарушается регуляция движений, появляется парестезия; возникают боли в межреберье; иногда наблюдается поражение зрительного и слухового нерва; нарушение памяти.
- со стороны пищеварительного тракта: глоссит, характеризующийся синдромом «лакированного языка» и болезненные ощущения в языке; тошнота, тяжесть в области эпигастрия, формирование отвращения к пище, ухудшение вкусовых ощущений; увеличение печени, реже – селезенки, появление желтушности склер, слизистых оболочек;
- внешние проявления: холодные руки и ноги, бледная с желтоватым оттенком кожа, формируется характерный синдром анемии Аддисона-Бирмера – лицо восковой куклы; одутловатость лица, значительные отеки; вялость, сонливость.
- со стороны сердца: появление симптомов одышки, болей, дистрофических изменений в миокарде.
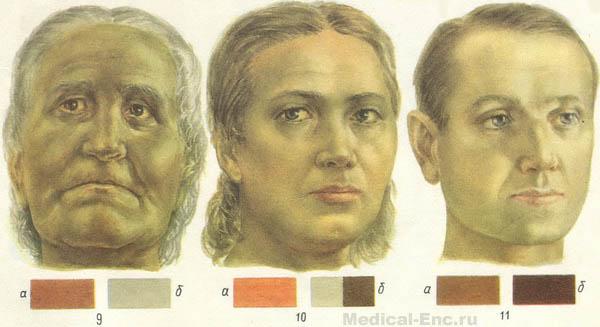 Лицо восковой куклы
Лицо восковой куклы
Диагностика
Диагностика анемии складывается из нескольких этапов.
Визуальный осмотр выявляет: бледные кожные покровы, желтушный оттенок склер, пигментные пятна на лице, руках и теле. Характерную картину дает осмотр ротовой полости, на начальной стадии заболевания язык болезненный, покрыт мелкими трещинками. В разгар болезни, язык приобретает алый цвет и отечность, выглядит, словно покрытый лаком. При проведении пальпации обнаруживается небольшое увеличение печени и выступление ее за край ребра. Селезенка увеличивается в размерах у небольшого количества пациентов. Проведение неврологических проб выявляет изменение чувствительности в конечностях.
При диагностике анемии Аддисона-Бирмера анализ крови играет ключевую роль. Проводится тщательное исследование периферической крови, где выявляется значительное повышение эритроцитарного объема крови, при этом количество ретикулоцитов резко снижено. Обнаруживается наличие гиперхромных эритроцитов. Главным признаком мегабластной анемии можно считать наличие гиперсегментарных нейтрофилов (имеющих пять и более сегментов в ядре). У человека относительно здорового таких клеток встречается в пределах 2%, у страдающих злокачественной анемией, количество гиперсегментарных нейтрофилов поднимается выше 5%.
Не менее важным является исследование костного мозга при анемии. В нем обнаруживается мегалобластный рост клеток – это остановившиеся в своем развитии клетки, предшествующие эритрацитам. Они аномально увеличены в размерах, деформированы, с заметной разницей в уровне развития ядра и цитоплазмы. Вообще, непродуктивный эритропоэз – характерная черта мегабластной анемии. Подавляющее число незрелых и деформированных клеток эритроцитов (мегабластов) разрушаются еще в костном мозге, не выходя в кровоток. При прогрессировании заболевания, количество ретикулоцитов продолжает падать, понижается количество тромбоцитов, при этом происходит их деформация.
Инструментальная диагностика включает в себя: исследование желудочного сока, где, как правило, выясняется снижение кислотности или полное ее отсутствие. Зато присутствует значительное количество слизи, схоже по составу с кишечной. Проводится эндоскопическое исследование, где явно наблюдается обширная атрофия слизистой оболочки желудка, часто называемая «перламутровыми бляшками», потеря секреторных клеток. К сожалению, даже в период ремиссии синтез пепсиногена не восстанавливается.
 Исследование желудочного сока
Исследование желудочного сока
Часто проводят гистологическое исследование тканей, так как одной из причин, способных вызвать анемию Аддисона Бирмера, являются злокачественные новообразования.
Таким больным требуется дополнительная консультация узких специалистов: невролога, эндокринолога, кардиолога, иммунолога.
Обязательным методом диагностики является проведение пробы Шиллинга. Этот метод нацелен на разграничение фолиево-дефицитной анемии от В12-дефицитной анемии для того, чтобы выявить первопричину, и наметить правильное лечение. Для этого измеряют их концентрацию в сыворотке крови. Норма фолиевой кислоты – 5-20нг/мл, норма В12 – 150-900нг/мл. Показатели ниже этих рамок свидетельствуют о наличии дефицита этих компонентов в организме. Чтобы провести пробу, больному вводят витамин В12 внутримышечно, через достаточное время определяют его концентрацию в моче, малое количество при В12-дефицитной анемии, максимальное – при фолиево-дефицитной.
Дефицит фолиевой кислоты в организме встречается чаще в молодом возрасте и не имеет сопутствующими факторами атрофию секреторной функции желудка и наличие неврологических симптомов. Она благоприятно реагирует на введение фолиевой кислоты перорально и лучше поддается лечению. При обследовании пациентов с В12-дефицитной анемией важно установить первопричину заболевания.
Лечение
Лечение анемии Аддисона Бирмера имеет свои особенности. Выбор лекарственного препарата зависит от причины заболевания. Фолиево-дефицитная анемия возникает из-за нарушения ее всасывания в кишечнике. Частой причиной этого вида анемии является хронический алкоголизм, причем особенно опасен он в период беременности.
Недостаток фолиевой кислоты более благоприятен для организма в плане лечения, так как при нем не страдает секреторная функция желудка, и введение перорально терапевтических доз препарата дает быстрый эффект.
Фолиевая кислота выпускается как отдельный препарат в форме таблеток или раствора для инъекций, так и в составе комплексных витаминов. Побочные эффекты при приеме фолиевой кислоты при лечении анемии возникают редко, но возможны аллергические реакции на внутримышечное введение препарата.
 Препараты фолиевой кислоты с витаминами
Препараты фолиевой кислоты с витаминами
В случае с дефицитом витамина В12 в организме, применение таблетированных форм не обоснованно, так как наличие атрофического гастрита сводит подобное лечение к нулю. В лечении этого вида анемии применяются внутримышечные или подкожные инъекции цианокобаламина. Внутривенное введение препарата опасно. Цианокобаламин – это жидкость розоватого цвета, в ампулах по 1мл, иногда его применение может вызвать аллергическую сыпь. Лекарство вводят ежедневно в дозе до 500мгк, в течение 6 недель, дополнительно вводят фолиевую кислоту в дозе до 100мгк.
При легкой или средней степени тяжести анемии, лечение, возможно, отложить до окончания полной диагностики и выявления причин дефицита. При выраженных неврологических нарушениях и значительных изменениях картины крови лечение начинают немедленно.
Часто, внешние признаки анемии Аддисона-Бирмера исчезают уже в первые дни лечения. Стихают боли в языке и ротовой полости, появляется аппетит, проходит слабость, восстанавливается зрение и слух. Через несколько суток восстанавливается ретикулоцитоз, количество мегабластов в костном мозге резко сокращается. Восстановление кроветворения происходит обычно через 1 -2 месяца. Тяжелые неврологические нарушения могут сохранять свою симптоматику в течение нескольких месяцев, а могут полностью и не исчезнуть вовсе.
При тяжелой атрофии слизистой желудка и при В12-дефицитной анемии препараты, содержащие витамин В12 приходится принимать всю жизнь. Пациент должен знать, что отказ от поддерживающей терапии влечет за собой рецидив мегалобластной анемии. Как правило, переболевшие анемией Аддисона-Бирмера ставятся на диспансерный учет и находятся под регулярным наблюдением. Поддерживающие дозы вводятся короткими курсами по назначению врача и под постоянным контролем картины крови.
Препараты для профилактики
В целях профилактики анемии фолиевую кислоту назначают лишь определенным группам граждан. Например, беременным женщинам для предотвращения патологий спинного мозга у плода, кормящим мама, для правильного развития ребенка. Пожилым людям при некоторых формах анемии, а так же пациентам, находящимся в коматозном состоянии. Во всех остальных случаях, достаточно того количества, которое поступает с пищей в обычном рационе.
Витамин В12 в целях профилактики назначают лишь при возможном его дефиците, например, при строгом вегетарианстве или тотальном удалении желудка. Цианокобаламин имеет широкую репутацию общеукрепляющего препарата, что совершенно не доказано, но его часто назначают при общем истощении, утомляемости и повышенной усталости как тонизирующее средство. Учитывая необходимость витаминов группы В в регуляции работы нервной системы, возможно применение цианокоболамина для лечения воспаления тройничного нерва и прочих нейропатиях.
Лечение анемии Аддисона Бирмера любыми витаминными препаратами должно быть строго нацеленным. И только если есть подозрение на дефицит нескольких витаминных компонентов, можно принимать поливитаминные комплексы.
