Анемия и беременность журнал

Введение
Анемия – патологическое состояние, характеризующееся уменьшением концентрации гемоглобина и, в подавляющем большинстве случаев, числа эритроцитов в единице объема крови. Частота анемии у беременных колеблется от 15 до 30% и, по данным Минздрава России, за последние 10 лет увеличилась в 6,3 раза, причем наиболее распространенной является железодефицитная анемия (ЖДА), на ее долю приходится около 90% от всех анемий [1]. Синдром ЖДА характеризуется ослаблением эритропоэза из-за дефицита железа вследствие несоответствия между поступлением и расходом (потреблением, потерей) железа, снижением наполнения гемоглобина железом с последующим уменьшением содержания гемоглобина в эритроците [2].
В соответствии с МКБ 10-го пересмотра учитывают следующие формы анемий, связанных с дефицитом железа:
D50 – железодефицитная анемия (асидеротическая, сидеропеническая, гипохромная);
D50.0 – железодефицитная анемия, связанная с хронической кровопотерей (хроническая постгеморрагическая анемия);
D50.1 – сидеропеническая дисфагия (синдромы Келли – Паттерсона и Пламмера – Винсона);
D50.8 – другие железодефицитные анемии;
D50.9 – железодефицитная анемия неуточненная.
ЖДА – нарушение, при котором снижается содержание железа в сыворотке крови, в костном мозге и депо, что приводит к нарушению образования гемоглобина, эритроцитов, возникновению анемий и трофических расстройств в тканях.
ЖДА занимают одно из ведущих мест в структуре экстрагенитальной заболеваемости беременных, т. к. во время беременности потребность в железе резко увеличивается вследствие высокой потребности в нем плаценты и плода, и возникает дисбаланс поступления и потребности необходимого микроэлемента. Согласно современным данным, дефицит железа в конце гестационного процесса развивается у всех без исключения беременных [2].
В организме человека содержится около 4 г железа: основная часть его (75%) входит в состав гемоглобина, меньшая часть входит в состав миоглобина (3,5%) и тканевых ферментов (0,5%), а также депонируется в печени и селезенке в виде ферритина и гемосидерина. Часть ферритина присутствует в плазме, а его концентрация служит индикатором запасов железа в организме [3].
Во время беременности потребность в железе неуклонно увеличивается (I триместр – на 1 мг/сут, II триместр – на 2 мг/сут, III триместр – на 3–5 мг/сут). Для выработки дополнительного железа используется 300–540 мг этого элемента. У большинства женщин к 28–30-недельному сроку физиологически протекающей беременности развивается анемия, связанная с неравномерным увеличением объема циркулирующей плазмы крови и объема эритроцитов. В результате показатель гематокрита снижается с 0,4 до 0,32, количество эритроцитов уменьшается с 4 до 3,5×1012/л, концентрация гемоглобина также снижается со 140 до 110 г/л (от I до III триместра). Подобные изменения картины красной крови, как правило, не отражаются на состоянии и самочувствии беременной. Истинная анемия беременных сопровождается типичной клинической картиной и оказывает влияние на течение беременности и родов. По сравнению с анемией, развившейся до беременности, анемия беременных протекает тяжелее, поскольку представляет собой осложнение, подобное гестозу. При наличии у женщины анемии, возникшей до наступления беременности, организм, как правило, успевает адаптироваться [3]. Суммарная потеря железа к окончанию беременности составляет примерно 1000–1200 мг. Процесс всасывания железа на протяжении беременности усиливается и составляет в I триместре 0,6–0,8 мг/сут, во II триместре – 2,8–3,0 мг/сут, в III триместре – до 3,5–4,0 мг/сут [4, 5]. Однако это не компенсирует повышенный расход элемента во время беременности. Более того, уровень депонированного железа у 100% беременных к концу гестационного периода снижается. Для восстановления запасов железа, потраченного в период беременности, родов и лактации, требуется не менее 2–3-х лет [6].
Биологическая значимость железа определяется его участием в тканевом дыхании. При дефиците железа у беременных возникает прогрессирующая гемическая гипоксия с последующим развитием вторичных метаболических расстройств. Поскольку при беременности потребление кислорода увеличивается на 15–33%, это усугубляет развитие гипоксии [4, 7].
ЖДА характеризуется нарушениями белкового обмена с возникновением дефицита белков в организме, что приводит к развитию отеков у беременной. При ЖДА развиваются дистрофические процессы в матке и плаценте, которые ведут к нарушению функции и формированию плацентарной недостаточности, у 10–15% отмечаются гипотония и слабость родовой деятельности. При этом развивающийся плод не получает в достаточном количестве полагающиеся ему питательные вещества и кислород, вследствие чего возникает задержка роста плода. Основными осложнениями беременности при ЖДА являются: угроза прерывания беременности (20–42%); гестоз (40%); артериальная гипотония (40%); преждевременная отслойка плаценты (25–35%); задержка роста плода (25%); преждевременные роды (11–42%). Роды часто осложняются кровотечениями. В послеродовом периоде могут возникать различные воспалительные осложнения (12%) [3, 5]. Даже при скрытом дефиците железа у 59% женщин отмечено неблагоприятное течение беременности в виде угрозы ее прерывания и гестоза [2, 5].
Одним из основных критериев ЖДА служит уровень гемоглобина, экспертами ВОЗ принята классификация анемии у беременных по концентрации гемоглобина (Hb) в крови:
• анемия легкой степени тяжести – концентрация Hb в крови от 90 до 110 г/л;
• умеренно выраженная анемия – концентрация Hb в крови от 89 до 70 г/л;
• тяжелая анемия – концентрация Hb в крови < 70 г/л.
Также к диагностическим критериям ЖДА относятся: цветовой показатель – < 0,85, микро- и анизоцитоз; средний диаметр эритроцитов – < 6,5 мкм; общая железосвязывающая способность сыворотки – > 64,4 мкмоль/л; сывороточное железо – < 12,6 мкмоль/л и уровень сывороточного ферритина (в норме 32–35 мкг/л), который служит индикатором дефицита железа в организме (≤ 12 мкг/л).
Для лечения ЖДА необходимы сбалансированная диета и назначение железосодержащих препаратов.
Cогласно Национальным рекомендациям «Клинические рекомендации (протоколы лечения) – железодефицитная анемия» (2015 г.), терапия железодефицитных состояний требует комплексного подхода, который включает коррекцию питания, применение лекарственных средств, строго соответствующих определенному патогенетическому варианту анемии, использование преимущественно препаратов орального применения, адекватно высокие суточные дозы одного препарата с хорошей переносимостью. Возможно назначение трансфузии эритроцитов по жизненным показаниям. Оценивают эффект лечения по клинико-лабораторным признакам, в т. ч. по ретикулоцитарному кризу [8].
В первую половину беременности рекомендуется суточный рацион, состоящий из 110 г белков, 80 г жиров и 350–400 г углеводов. Общая энергетическая ценность суточного рациона должна составлять 2600–2800 ккал. Во вторую половину беременности количество белков должно быть увеличено до 125 г, жиров – до 70–90 г, углеводов – до 400–420 г, калорийность питания составляет в этом случае 2900–3050 ккал. Таким образом, в физиологических условиях коррекция рациона может обеспечивать потребности организма в железе и предупреждать развитие железодефицитных состояний.
Однако, учитывая тот факт, что из пищи всасывается 2,5 мг железа в сутки, а из лекарственных препаратов – в 15–20 раз больше, необходима дотация железа лекарственными препаратами.
Рекомендуется назначение препаратов, содержащих Fe2+, FeSO4, из-за их лучшей абсорбции. Суточная доза для профилактики анемии и лечения легкой формы заболевания – 50–60 мг Fe2+, а для лечения выраженной анемии – 100–120 мг Fe2+. Железа сульфат назначают внутрь по 320 мг (соответствует 100 мг Fe2+) 2 р./сут строго за 1 ч до или через 2 ч после еды, т. к. на абсорбцию влияют различные ингредиенты пищи.
Наиболее предпочтительным является прием препаратов железа внутрь, а не в виде инъекций, т. к. в последнем случае чаще могут возникать различные побочные эффекты: запор, вздутие живота, понос, изжога, боли в желудке, тошнота, темный стул.
Причинами неэффективной терапии препаратами железа могут быть:
1) отсутствие ЖДА;
2) недостаточная доза лекарства;
3) недостаточная длительность лечения;
4) нарушение всасывания в кишечнике;
5) одновременный прием препаратов, уменьшающих всасывание железа;
6) имеющаяся незначительная кровопотеря (геморрой и пр.).
Из лекарственной формы всасывается не более 10–12% содержащегося в ней железа. При тяжелой степени дефицита железа показатель всасываемости железа может возрастать до 3-х раз. Повышению биодоступности железа способствуют присутствие аскорбиновой и янтарной кислот, фруктозы, цистеина и других акселераторов, а также использование в ряде препаратов специальных матриц, замедляющих высвобождение железа в кишечнике [3, 4].
Расчет суточного количества препарата (СКП) для пероральных препаратов железа выполняют по следующей формуле:
СКП = НСД/СЖП
где НСД – необходимая суточная доза двухвалентного или трехвалентного (не элементарного) железа (у взрослых – 200 мг/сут, у детей – 30–100 мг/сут);
СЖП – содержание двухвалентного или трехвалентного (не элементарного) железа в единице препарата (таблетке, капсуле, капле раствора, миллилитре сиропа или раствора) [5].
Расчет ориентировочной курсовой дозы препарата железа, назначаемого парентерально, может быть произведен по формуле с учетом массы тела больного и уровня гемоглобина, отражающего степень дефицита железа:
А=М(Hb1–Hb2) × 0,24+D,
где A – количество железа в мг;
M – масса тела в кг;
Hb1 – нормативная величина гемоглобина для массы тела < 35 кг – 130 г/л, > 35 кг – 150 г/л;
Hb2 – уровень гемоглобина у пациента в г/л;
D – расчетная величина депо железа для массы тела < 35 кг – 15 мг/кг, для массы тела > 35 кг – 500 мг.
Оптимальная суточная доза для препаратов железа при лечении ЖДА должна соответствовать необходимой суточной дозе и рассчитываться по приведенным формулам. Применение меньших доз препаратов не дает адекватного клинического эффекта. При латентном дефиците железа или для насыщения депо после окончания курса терапии применяются половинные относительно лечебных дозы препаратов [9].
Из железосодержащих препаратов особого внимания заслуживают многокомпонентные оральные препараты. Предпочтение данных препаратов обусловлено отсутствием или низкой частотой побочных эффектов, а главное, быстрым увеличением уровня гемоглобина и нормализацией показателей ферростатуса. Положительный эффект объясняется дополнительными компонентами в составе этих препаратов. Оптимальный препарат должен состоять из сульфата железа в достаточном количестве, аскорбиновой кислоты, превышающей в 2–5 раз количество железа в препарате, больших доз фолиевой кислоты и цианокобаламина. Эти компоненты принимают активное участие в процессах метаболизма железа в организме, обеспечивая лучшую абсорбцию этого микроэлемента из ЖКТ.
На сегодняшний день представлен большой выбор ферропрепаратов, различающихся по составу. Препаратом, наиболее удовлетворяющим всем основным требованиям, является Сорбифер.
Форма выпуска препарата в оболочке предотвращает образование желтой каймы на зубах при длительном приеме. Препарат содержит 320 мг сульфата железа (что соответствует100 мг двухвалентного железа) и 60 мг аскорбиновой кислоты (для улучшения всасывания и усвоения микроэлемента). Мы использовали схему приема препарата – 1 таблетка 2 р./сут. Основными достоинствами препарата являются наименьшая частота побочных эффектов, быстрое купирование объективных и субъективных клинических признаков ЖДА, хорошая переносимость [9, 10]. Эти качества наиболее важны при выборе метода лечения ЖДА у беременных. Дополнительные компоненты препарата обеспечивают лучшую абсорбцию железа и профилактику поливитаминной недостаточности у женщин во время беременности. Результаты исследований доказывают, что Сорбифер оказывает положительное влияние на общее состояние беременной.
Основные схемы лечения препаратом Сорбифер с приемом внутрь после еды: при анемии легкой формы – по 1 таблетке 2 р./сут в течение 3–4-х нед.; при среднетяжелом течении – по 1 таблетке 3 р./сут в течение 8–12 нед., при тяжелой форме – по 2 таблетки 3 р./сут в течение 16 нед. и более. Оценка первых результатов лечения (по уровню гемоглобина) проводится уже через 2 нед. от начала терапии [10].
Таким образом, в настоящее время комбинированный препарат Сорбифер можно считать препаратом выбора при лечении беременных с ЖДА.
Цель исследования: оценка эффективности применения препарата Сорбифер в коррекции ЖДА во время беременности.
Материал и методы
Для реализации поставленной цели были проведены клинико-лабораторное обследование и лечение 33 беременных во II триместре гестации (13–20 нед.) с ЖДА в сочетании с угрозой прерывания различного генеза.
Возраст беременных варьировал от 16 до 39 лет (средний возраст – 27,5±5,6 года).
Результаты анализа свидетельствуют, что характерными для обследованных пациенток явились следующие особенности: высокая частота инфекционных заболеваний, наличие сопутствующей экстрагенитальной патологии, особенно со стороны желудочно-кишечного тракта, хронические очаги инфекции, осложненное течение предыдущих беременностей. ЖДА при предыдущей беременности имела место у 14 (42%) женщин. В обследованной группе первобеременных было 5 (15,1%), первородящих – 9 (27,2%). Из 28 (84%) повторно беременных лишь у 11 (33%) женщин предыдущие беременности закончились срочными родами; у 5 (15,1%) пациенток в анамнезе были самопроизвольные выкидыши и у 3-х женщин (9%) – неразвивающаяся беременность.
Все пациентки предъявляли жалобы на общую слабость, утомляемость, нарушение сна и тянущие боли в низу живота.
Для подтверждения диагноза ЖДА проводилось исследование показателей периферической крови: уровня гемоглобина (Hb), эритроцитов, цветового показателя. Для оценки запасов железа использовано также определение уровня сывороточного железа (Fe) и ферритина (SF). О тяжести течения ЖДА судили по уровню гемоглобина. У 20 беременных имела место легкая степень анемии (снижение уровня гемоглобина от 90 до 110 г/л) и у 13 – средняя степень (снижение уровня гемоглобина от 70 до 89 г/л).
Все беременные, помимо терапии, направленной на пролонгирование беременности (спазмолитики, антиоксиданты, гормоны по показаниям), для лечения анемии получали препарат Сорбифер, который назначали внутрь после еды 3 р./сут в течение 3–4-х нед. при ЖДА легкой степени и в течение 8–10 нед. при ЖДА средней степени тяжести.
До назначения Сорбифера лечение другими железосодержащими препаратами не проводилось. У каждой беременной до и после приема препарата Сорбифер определяли гематологические и феррокинетические параметры.
Результаты и обсуждение
Результаты изучения показателей до и после лечения препаратом представлены в таблице 1.
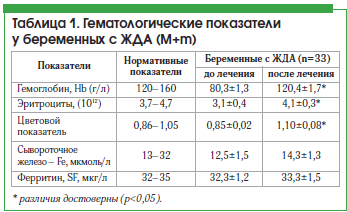
Как видно из приведенных данных, у пациенток после лечения препаратом Сорбифер наблюдались достоверное (р<0,05) увеличение содержания гемоглобина, цветового показателя и уровня эритроцитов, а также увеличение уровня сывороточного железа, хотя разница показателей до и после лечения была недостоверной, что, возможно, связано с наличием легкой степени тяжести ЖДА у большинства пациенток (рис. 1). Нами не выявлено снижение уровня ферритина. Однако, согласно имеющимся данным, содержание сывороточного железа не всегда отражает показатели запасов железа, т. к. оно зависит от скорости высвобождения ферритина из тканей и плазмы [6].
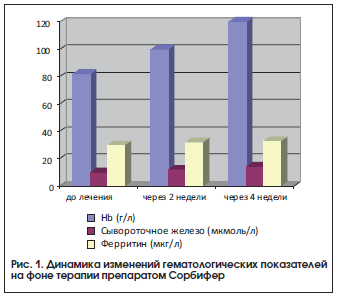
За время наблюдения состояние беременных значительно улучшилось: купировались признаки угрозы прерывания беременности, исчезли жалобы на слабость, утомляемость, нарушение сна. Необходимо также отметить, что за время лечения препаратом Сорбифер побочных эффектов, таких как аллергические реакции, желудочно-кишечные расстройства и др., не наблюдалось.
Таким образом, включение препарата Сорбифер в лечение беременных с ЖДА способствует нормализации показателей периферической крови, улучшению состояния пациенток, а также пролонгированию беременности, что является одним из факторов профилактики невынашивания беременности.
Источник

Для цитирования. Логутова Л.С. Анемия у беременных: вопросы этиологии, диагностики и лечения // РМЖ. 2016. No 5. С. 290–293.
Структура заболеваемости беременных женщин практически не меняется на протяжении десятков лет. Самое распространенное гематологическое заболевание в период гестации — это анемия [3].
Анемия — клинико-гематологический синдром, обусловленный снижением концентрации гемоглобина и, в большинстве случаев, эритроцитов в единице объема крови и их морфологическими изменениями.
Диагностика истинной анемии у беременных представляет определенные трудности. Это обусловлено тем, что во время беременности увеличиваются объем циркулирующей крови и его составляющих, объем плазмы и объем эритроцитов, причем объем плазмы возрастает в большей степени (почти в 2 раза). Происходит разведение эритроцитов в большом количестве жидкости, относительное уменьшение их числа при абсолютном увеличении объема плазмы. Это состояние называется гидремией и не является анемией, хотя наблюдается закономерное снижение показателей красной крови, но при этом отсутствуют морфологические изменения эритроцитов.
Допустимым пределом физиологической гемодилюции при беременности считается снижение показателя гематокрита до 0,32, гемоглобина – до 100 г/л, эритроцитов – до 3,5×1012/л. Дальнейшее снижение показателей красной крови следует расценивать как истинную анемию.
Компенсаторное значение гемодилюции беременных состоит в том, что облегчается обмен питательных веществ и газов через плаценту, а при кровопотере истинная потеря эритроцитов уменьшается примерно на 20%.
Клиническая гидремия беременных протекает бессимптомно и лечения не требует. С окончанием беременности быстро (в течение 1–2 нед.) восстанавливается нормальная картина крови.
Различают анемии, диагностируемые во время беременности, и догестационные.
Некоторые клиницисты склонны подразделять анемию на «анемию беременных» и «анемию у беременных», подразумевая в первом случае заболевание, развивающееся во время беременности, а во втором – малокровие, существовавшее еще до гестационного процесса.
По литературным данным, во второй половине гестации анемия диагностируется почти в 40 раз чаще, чем в первые недели, что, несомненно, связано с нарушением гемопоэза из-за изменений, вызванных беременностью [3].
При беременности развитие анемии связано с гормональными изменениями, развитием ранних токсикозов, препятствующих всасыванию в желудочно-кишечном тракте элементов железа, магния, фосфора, необходимых для кроветворения. Одной из основных причин является прогрессирующий дефицит железа, связанный с его утилизацией на нужды фетоплацентарного комплекса (ФПК), для увеличения массы циркулирующих эритроцитов. Анемию беременных также связывают с нарушением перекисного окисления липидов (ПОЛ) [1, 2].
У 9 из 10 пациенток во время беременности диагностируется железодефицитная анемия (ЖДА). Частота ЖДА во время беременности, по разным данным, колеблется от 21 до 80% (если судить по уровню гемоглобина) и от 49 до 99% (по уровню сывороточного железа). ЖДА – заболевание, на первый взгляд, безобидное, но ведущее к многочисленным осложнениям для матери, новорожденного и здоровья в течение всей последующей жизни ребенка. Проблема ЖДА у женщин в период гестации остается актуальной, поскольку осложняет течение беременности, родов и послеродовый период [2].
ЖДА – патологическое состояние, характеризующееся нарушением синтеза гемоглобина в результате дефицита железа, развивающееся на фоне различных патологических или физиологических (беременность) процессов. По данным ВОЗ, частота ЖДА среди беременных колеблется от 14% в странах Европы до 70% в Юго-Восточной Азии. В странах с высоким уровнем жизни населения ЖДА диагностируется у 18–25% беременных женщин, в развивающихся странах частота железодефицита при беременности может достигать 80%. Частота данного осложнения беременности в России стабильно на протяжении 15 лет составляет 30–40% [6].
Следует отметить, что у 20–25% женщин выявляется латентный дефицит железа. Так, дефицит железа в III триместре беременности обнаруживается почти у 90% женщин и сохраняется после родов и лактации у 55% из них [1, 4, 9].
Во время беременности железо усиленно расходуется вследствие интенсификации обмена веществ: в I триместре потребность в железе не превышает потребности до беременности и составляет 0,6–0,8 мг/сут; во II триместре – увеличивается до 2–4 мг/сут; в III триместре – до 10–12 мг/сут [7].
К концу беременности неизбежно наступает обеднение железом организма матери в связи с депонированием его в ФПК (около 450 мг), с увеличением объема циркулирующей крови, на что затрачивается около 500 мг, в послеродовом периоде – в связи с физиологической кровопотерей в 3-м периоде родов (100–150 мг) и лактацией (400 мг). Суммарная потеря железа к окончанию беременности и лактации составляет 1200–1400 мг [5].
Для своевременной диагностики и лечения ЖДА необходимо учитывать риск развития этого осложнения у различных групп беременных:
– перенесенные заболевания (частые инфекции): острый пиелонефрит, дизентерия, вирусный гепатит;
– экстрагенитальная фоновая патология (хронический тонзиллит, хронический пиелонефрит, ревматизм, пороки сердца, сахарный диабет, гастрит);
– меноррагии;
– частые беременности;
– наступление беременности при лактации;
– беременность в подростковом периоде;
– анемия при прошлых беременностях;
– вегетарианская диета;
– уровень Hb в I триместре беременности <120 г/л;
– осложнения беременности (ранний токсикоз, вирусные заболевания, угроза прерывания);
– многоплодная беременность.
Выявлено, что при ЖДА отмечается усиление процессов ПОЛ без активации антиоксидантной системы защиты, что приводит к повреждению мембранных структур клеток ФПК.
При дефиците железа у беременных возникает прогрессирующая гемическая гипоксия с последующим развитием вторичных метаболических расстройств. Поскольку при беременности потребление кислорода увеличивается на 15–33%, это усугубляет развитие гипоксии. У беременных с тяжелой степенью ЖДА развивается не только тканевая и гемическая гипоксия, но и циркуляторная, обусловленная развитием дистрофических изменений гипокинетического типа кровообращения.
Анемия осложняет течение беременности и родов. Истинные анемии беременных могут сопровождаться нарушением коагуляционных свойств крови, что является причиной массивных кровопотерь; оказывают неблагоприятное влияние на развитие сократительной деятельности матки; возможны длительные затяжные или быстрые и стремительные роды.
Беременные с ЖДА нуждаются в медикаментозном лечении и диетическом питании. Но невозможно купировать ЖДА лишь диетой, состоящей из богатых железом продуктов, без препаратов железа (ПЖ). Из лекарственных препаратов в организме может усвоиться в 15–20 раз больше железа, чем из пищи.
В настоящее время в распоряжении врача имеется большой арсенал лекарственных ПЖ, характеризующихся различным составом и свойствами, количеством содержащегося в них железа, наличием дополнительных компонентов (аскорбиновая и янтарная кислоты, витамины, фруктоза и др.), влияющих на фармакокинетику препарата, лекарственной формой, переносимостью, стоимостью. В клинической практике ПЖ применяются внутрь или парентерально.
В комплексной терапии ЖДА при беременности целесообразно применять антиоксиданты (витамин Е в дозе от 100 до 300 мг/сут). Для улучшения белкового метаболизма рекомендуется подключить так называемую белково-синтетическую терапию (оротат калия, витамин В6).
Лечение ЖДА у беременных при ее верификации должно проводиться до конца беременности. Это имеет принципиально важное значение и для коррекции анемии у беременной, и, главным образом, для профилактики дефицита железа у плода. Кроме того, по рекомендации ВОЗ, все беременные на протяжении II—III триместров беременности и в первые 6 мес. лактации должны получать ПЖ в профилактической дозе [8].
Контроль показателей красной крови необходимо проводить на фоне лечения каждые 10 дней. Неэффективность лечения ЖДА может быть обусловлена неадекватностью назначаемой терапии.
Несмотря на многообразие ПЖ, до настоящего времени продолжается дискуссия о преимуществах и недостатках двухвалентного железа, оценивается переносимость ПЖ пациентами, а также отслеживаются их возможные побочные действия.
Идеальный железосодержащий препарат должен обладать минимальным количеством побочных эффектов, иметь простую схему применения, наилучшее соотношение эффективности и цены, оптимальное содержание железа, желательно наличие компонентов, усиливающих всасывание и стимулирующих гемопоэз.
Применение комбинаций ПЖ с витамином В12 и фолиевой кислотой не всегда является оправданным, т. к. фолиеводефицитная анемия у беременных возникает крайне редко и имеет специфические клинико-лабораторные признаки.
Более целесообразным считается применять ПЖ, содержащие аскорбиновую кислоту. Одним из таких препаратов является Сорбифер Дурулес, выпускаемый фармацевтическим заводом «Эгис» (Венгрия). В препарате содержится оптимальное количество микроэлемента: в 1 таблетке – 320 мг сульфата железа (соответствует 100 мг железа II) и 60 мг аскорбиновой кислоты, улучшающей всасывание, усвоение железа и оказывающей антиоксидантное действие.
Нами проведен анализ результатов применения во время беременности препарата Сорбифер Дурулес с лечебной и профилактической целью в некоторых районах Московской области (гг. Балашиха, Домодедово, Видное, Люберцы, Мытищи). По результатам анализа количество анемий у беременных в этих районах колеблется от 27,8 до 48,3%. Всего было обследовано 125 беременных, которые с лечебной (82 (65,6%) и профилактической целью (43 (34,4%)) получали Сорбифер Дурулес. С лечебной целью назначали по 1 таблетке 2 р./сут, для профилактики – по 1 таблетке 1 р./сут. Длительность применения и дозу препарата определяли индивидуально на основании динамической оценки результатов гематологических показателей красной крови. Распределение обследованных пациенток в зависимости от цели приема препарата представлено в таблице 1.
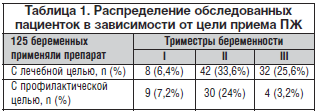
Как показано в таблице, чаще всего ЖДА выявлялась во II и III триместрах беременности. В связи с этим и профилактику ЖДА чаще всего начинали проводить со II триместра гестации. Важнейшими и наиболее доступными показателями красной крови при ЖДА являются пониженный уровень гемоглобина, низкий цветовой показатель, снижение количества эритроцитов. Эти показатели и использовались нами для оценки степени тяжести, адекватности лечения и эффективности профилактики ЖДА.
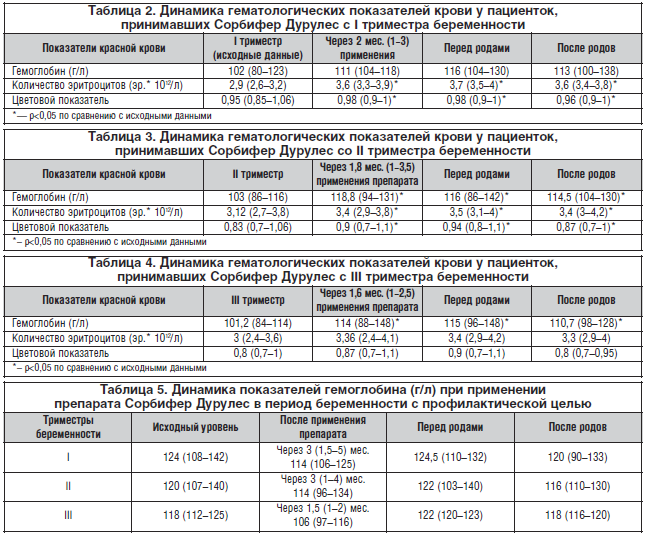
Результаты применения препарата Сорбифер Дурулес с I триместра беременности для лечения ЖДА представлены в таблице 2 (med (g1-g2)).
Из приведенных в таблице 2 данных следует, что применение препарата Сорбифер Дурулес в течение 2 мес. для лечения анемии с I триместра беременности привело к повышению гемоглобина в среднем на 10 единиц. Этот показатель сохраняется стабильным на протяжении всего периода гестации и в послеродовом периоде. Показатели количества эритроцитов и цветовой показатель после лечения на протяжении оставшегося периода беременности и в послеродовом периоде достоверно выше, чем исходные данные.
Динамика показателей гемоглобина, количества эритроцитов и цветового показателя у беременных с ЖДА, выявленной во II триместре гестации, до лечения и на его фоне представлена в таблице 3 (med ( g1-g2)).
При анализе полученных данных (табл. 3) видно, что на фоне проводимой терапии, продолжительность которой в среднем составила 1,8 мес., показатель гемоглобина стал достоверно выше аналогичного показателя до лечения и оставался в пределах нормативных значений до родов и в послеродовом периоде. Такая же тенденция наблюдалась и в динамике показателей количества эритроцитов и цветового показателя.
При выявлении ЖДА у беременных в III триместре беременности лечение проводилось в среднем 1,6 мес. и, как правило, продолжалось в послеродовом периоде. Динамика показателей красной крови при лечении анемии с III триместра беременности представлена в таблице 4 (med ( g1-g2)).
Таким образом, из анализа полученных результатов видно, что уровень гемоглобина после лечения препаратом Сорбифер Дурулес становился достоверно выше по сравнению с исходным, выявленным в III триместре беременности, и оставался таковым до родов.
Главная задача акушера в такой важный период для жизни женщины, как беременность, – не лечить осложнения, а предупредить их развитие. В нашем исследовании скрининговый анализ гемоглобина у беременных позволил осуществить профилактику ЖДА в период гестации.
Динамика показателей гемоглобина при применении препарата Сорбифер Дурулес в период беременности с профилактической целью представлена в таблице 5 (med (g1-g2)).
Данные, приведенные в таблице 5, подтверждают результаты других исследователей о том, что во II триместре беременности происходит наибольшее снижение показателей красной крови, а также тот факт, что повышение этих показателей происходит не быстро, а на фоне длительного применения (в нашем исследовании – в среднем 1,5–3 мес.) ПЖ (в частности, эффективного препарата Сорбифер Дурулес).
Представленные в настоящем исследовании данные свидетельствуют о высокой клинической эффективности железосодержащего препарата Сорбифер Дурулес, что позволяет рекомендовать его для лечения ЖДА, а также профилактики ее развития. Каких-либо побочных отрицательных эффектов, потребовавших отмены препарата, отмечено не было.
Источник
