Анемия и тромбоз артерий
Железодефицитная анемия,
тромбоз, инсульт
Нарушение мозгового кровообращения может случиться в любом возрасте, хотя большинство инсультов происходит после 65 лет, но примерно одна четверть приходится на молодых людей. Причины инсультов в этой группе: кардиоэмболия, гематологические нарушения, злоупотребление наркотиками или алкоголем, травмы и операции, оральные контрацептивы и беременность, послеродовое состояние и мигрени. Вторичный тромбоцитоз, вызванный железодефицитной анемией (ЖДА) – редкая, но известная причина инсульта. В настоящей статье описана страдающая железо-дефицитной анемией с динамическим нарушением мозгового кровообращения, обусловленным тромбозом внутренней сонной артерии.
Описание случая
Женщина 41 года поступила в больницу с жалобами на минутные приступы преходящего онемения и слабость в конечностях, в день госпитализации отмечено два подобных эпизода. За день до госпитализации перенесла серию аналогичных приступов. В анамнезе анемия и метроррагия, женщина не принимала каких-либо лекарственных препаратов. У пациентки не отмечалось факторов риска развития сердечно-сосудистых заболеваний, за исключением курения. Семейный анамнез неврологическими и гематологическими патологиями не отягощен.
Направлена обследоваться в неврологическую амбулаторию. Общий осмотр, осмотр невролога, исследование глазного дна не выявили патологических изменений. Лабораторные данные указали на наличие железодефицитной анемии. Уровень гемоглобина 7,5 г/Дл (13-17), среднее гематокритное число 58 фл (80-92), среднее содержание гемоглобина в эритроците 16,75пг (27-31), тромбоцитов 450 тыс/мл (130-400). Уровень сывороточного железа 12 мг/дл (135-526), уровень ферритина 12 нг/мл (7-26). Липидный профиль нормальный: ЛПНП 106 мг/дл (60-130), ЛПВП 64 мг/дл (30-80). Остальные показатели крови, включая лейкоцитарную формулу, биохимию, уровни мочевины и креатинина были в пределах нормальных значений.
На ЭКГ и рентгенографии органов грудной клетки паталогических изменений не обнаружено. Анализы на тромбофилию отрицательны, также как и на антифосфолипидные антитела (антикардиолипины IgG и IgM), не обнаружено волчаночного антикоагулянта. С-реактивный белок, белки S, антитромбин III, фибриноген, витамин В12, уровни фолатов, гомоцистеина, протромбина в пределах нормы. Не обнаружено варианта G20210 гена протромбина и лейденовской мутации V фактора. Не найдены антинуклеарные, анти-ДНК и антитела к цитоплазме нейтрофилов. Трансторакальное ЭХО-КГ не выявило дефектов перегородок и источников тромбоэмболии.
МР-ангиография шейной области зарегистрировала ослабление сигнала в районе бифуркации левой внутренней сонной артерии, классифицированное как имеющее отношение к тромбу, выявленному при УЗИ. В правой сонной и обеих позвоночных артериях отклонений при МР-ангиографии не обнаружено.
Дефицит железа был объяснён меноррагией. Назначены пероральные препараты-заместители железа и гепарин, позже заменённый варфарином. Повторный осмотр через месяц показал рассасывание тромботической массы, а на доплеровском УЗИ – нормальная структура левой внутренней сонной артерии.
Обсуждение
ЖДА ассоциирована с отёком диска зрительного нерва, идиопатической внутричерепной гипертензией, тромбозом синусов твёрдой мозговой оболочки и ишемическим инсультом. Не до конца изучены механизмы, приводящие к анемии и нарушению кровообращения, считается, что в развитии инсульта, обусловленного дефицитом железа, может играть роль несколько механизмов. Дефицит железа всегда приводит к тромбоцитозу.
Микроцитоз ведёт к сокращению способности эритроцитов к деформации и может спровоцировать состояние гиперкоагуляции. Количество тромбоцитов и состояние эритроцитов при ЖДА могут содействовать формированию тромба, особенно при сопутствующей атеросклеротической болезни. Анемия также может усугубить гипоксию мозга в участках сниженной перфузии, вызывая так называемые «анемические инфаркты».
Факторы риска для формирования тромба сонной артерии при отсутствии атеросклероза точно не определены, хотя известно о каротидных тромбах, ассоциированных с железодефицитной анемией.
Гиперкоагуляция при ЖДА может провоцироваться изменением характера сосудистого кровотока, обусловленным ограничением деформации микроцитов. Для компенсации недостатка кислорода при анемии требуется увеличение объёма кровотока. Таким образом, увеличение кровотока может повлечь повреждение эпителия, приводящее к агрегации тромбоцитов и заканчивающееся свертыванием крови с формированием тромба.
Присутствие флотирующегося тромба у пациента с клинической и МРТ-картиной инсульта, представляет значительную терапевтическую дилемму и требует немедленного лечения, в том числе антикоагулянтами. Немедленное их применение при симптоматике внутрисосудистого тромбоза сонной артерии позволяет снизить частоту ишемических эпизодов, и при планировании реваскуляризации артерии, позволяет отложить вмешательство.
При микроцитарной анемии необходимо оценить уровень железа в крови, так как его дефицит может быть следствием острого желудочно-кишечного кровотечения, спровоцированного противотромбоцитарной или антикоагулянтной терапией. Железодефицитное состояние следует немедленно купировать у пациентов с прочими серьёзными рисками развития тромбозов.
Введение
Нарушение мозгового кровообращения может случиться в любом возрасте, хотя большинство инсультов происходит после 65 лет, но примерно одна четверть приходится на молодых людей. Причины инсультов в этой группе: кардиоэмболия, гематологические нарушения, злоупотребление наркотиками или алкоголем, травмы и операции, оральные контрацептивы и беременность, послеродовое состояние и мигрени. Вторичный тромбоцитоз, вызванный железодефицитной анемией (ЖДА) – редкая, но известная причина инсульта. В настоящей статье описана страдающая железо-дефицитной анемией с динамическим нарушением мозгового кровообращения, обусловленным тромбозом внутренней сонной артерии.
Описание случая
Женщина 41 года поступила в больницу с жалобами на минутные приступы преходящего онемения и слабость в конечностях, в день госпитализации отмечено два подобных эпизода. За день до госпитализации перенесла серию аналогичных приступов. В анамнезе анемия и метроррагия, женщина не принимала каких-либо лекарственных препаратов. У пациентки не отмечалось факторов риска развития сердечно-сосудистых заболеваний, за исключением курения. Семейный анамнез неврологическими и гематологическими патологиями не отягощен.
Направлена обследоваться в неврологическую амбулаторию. Общий осмотр, осмотр невролога, исследование глазного дна не выявили патологических изменений. Лабораторные данные указали на наличие железодефицитной анемии. Уровень гемоглобина 7,5 г/Дл (13-17), среднее гематокритное число 58 фл (80-92), среднее содержание гемоглобина в эритроците 16,75пг (27-31), тромбоцитов 450 тыс/мл (130-400). Уровень сывороточного железа 12 мг/дл (135-526), уровень ферритина 12 нг/мл (7-26). Липидный профиль нормальный: ЛПНП 106 мг/дл (60-130), ЛПВП 64 мг/дл (30-80). Остальные показатели крови, включая лейкоцитарную формулу, биохимию, уровни мочевины и креатинина были в пределах нормальных значений.
На ЭКГ и рентгенографии органов грудной клетки паталогических изменений не обнаружено. Анализы на тромбофилию отрицательны, также как и на антифосфолипидные антитела (антикардиолипины IgG и IgM), не обнаружено волчаночного антикоагулянта. С-реактивный белок, белки S, антитромбин III, фибриноген, витамин В12, уровни фолатов, гомоцистеина, протромбина в пределах нормы. Не обнаружено варианта G20210 гена протромбина и лейденовской мутации V фактора. Не найдены антинуклеарные, анти-ДНК и антитела к цитоплазме нейтрофилов. Трансторакальное ЭХО-КГ не выявило дефектов перегородок и источников тромбоэмболии.
На МРТ головного мозга картина подострого инфаркта левой теменно-затылочной доли, в правой лобной доли также видны симметричные очаги (рис. 1).
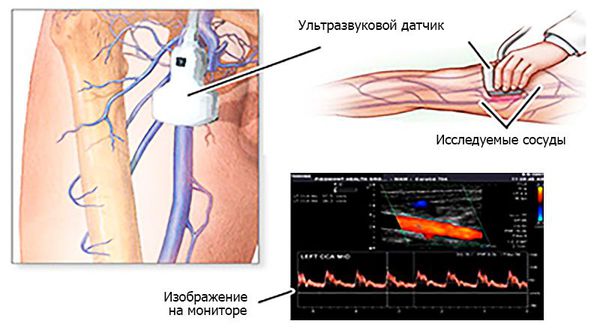
На доплеровском УЗИ сонной артерии в области бифуркации левой внутренней сонной артерии определяется тромботическая масса (рис. 2). В правой внутренней сонной артерии аномалий не найдено.
МР-ангиография шейной области зарегистрировала ослабление сигнала в районе бифуркации левой внутренней сонной артерии, классифицированное как имеющее отношение к тромбу, выявленному при УЗИ. В правой сонной и обеих позвоночных артериях отклонений при МР-ангиографии не обнаружено.
Дефицит железа был объяснён меноррагией. Назначены пероральные препараты-заместители железа и гепарин, позже заменённый варфарином. Повторный осмотр через месяц показал рассасывание тромботической массы, а на доплеровском УЗИ – нормальная структура левой внутренней сонной артерии.
Обсуждение
ЖДА ассоциирована с отёком диска зрительного нерва, идиопатической внутричерепной гипертензией, тромбозом синусов твёрдой мозговой оболочки и ишемическим инсультом. Не до конца изучены механизмы, приводящие к анемии и нарушению кровообращения, считается, что в развитии инсульта, обусловленного дефицитом железа, может играть роль несколько механизмов. Дефицит железа всегда приводит к тромбоцитозу. Микроцитоз ведёт к сокращению способности эритроцитов к деформации и может спровоцировать состояние гиперкоагуляции. Количество тромбоцитов и состояние эритроцитов при ЖДА могут содействовать формированию тромба, особенно при сопутствующей атеросклеротической болезни. Анемия также может усугубить гипоксию мозга в участках сниженной перфузии, вызывая так называемые «анемические инфаркты».
Факторы риска для формирования тромба сонной артерии при отсутствии атеросклероза точно не определены, хотя известно о каротидных тромбах, ассоциированных с железодефицитной анемией.
Гиперкоагуляция при ЖДА может провоцироваться изменением характера сосудистого кровотока, обусловленным ограничением деформации микроцитов. Для компенсации недостатка кислорода при анемии требуется увеличение объёма кровотока. Таким образом, увеличение кровотока может повлечь повреждение эпителия, приводящее к агрегации тромбоцитов и заканчивающееся свертыванием крови с формированием тромба. Присутствие флотирующегося тромба у пациента с клинической и МРТ-картиной инсульта, представляет значительную терапевтическую дилемму и требует немедленного лечения, в том числе антикоагулянтами. Немедленное их применение при симптоматике внутрисосудистого тромбоза сонной артерии позволяет снизить частоту ишемических эпизодов, и при планировании реваскуляризации артерии, позволяет отложить вмешательство.
При микроцитарной анемии необходимо оценить уровень железа в крови, так как его дефицит может быть следствием острого желудочно-кишечного кровотечения, спровоцированного противотромбоцитарной или антикоагулянтной терапией. Железодефицитное состояние следует немедленно купировать у пациентов с прочими серьёзными рисками развития тромбозов.
/
Рис. 1 МРТ головного мозга, демонстрирующая подострые ишемические поражения в левой лобной доле и симметричные пораженные участки в теменных долях.
Рис. 2 УЗИ с тромбом в просвете левой сонной артерии
Iron-Deficiency Anemia Leading to Transient Ischemic Attacks due to Intraluminal Carotid Artery Thrombus/H. Z. Batur Caglayan, B. Nazliel, C. Irkec, A. Dumlu, A. Filiz, and M. Panpalli Ates /www.hindawi.com/crim/neurological.medicine/2013/813415
Перевод Синицыной Елены
Дата публикации 7 мая 2020Обновлено 7 мая 2020
Определение болезни. Причины заболевания
Тромбоз артерии — внезапное острое прекращение артериального кровотока, вызванное перекрытием тромбом кровеносного сосуда. Тромб (с др.-греч. — ком, сгусток) — прижизненный сгусток крови, образующийся при заболеваниях или травмах. В норме в кровеносной системе тромбы не содержатся. Их появление в сосуде угрожает жизни пациента.
Артерии — кровеносные сосуды, по которым обогащённая кислородом кровь направляется от сердца к конечностям, органам и тканям. Артериальные тромбозы приводят к резкому прекращению или ухудшению артериального кровотока в конечности или органе с потенциальной угрозой их жизнеспособности [1].
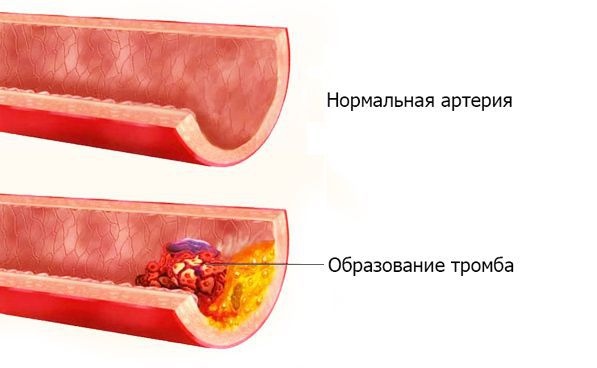
Артериальные тромбозы в 40 % случаев становятся причиной острой ишемии конечности (недостаточности кровоснабжения), а в 37 % — эмболии [2][3]. Эмболия (с греч. — вторжение) — отрыв тромба от места его первоначального образования, либо перенос патологического субстрата с током крови по сосудистому руслу c последующей закупоркой артериального сосуда. Патологическим субстратом могут служить твёрдые, жидкие или газообразные образования: капли жира, пузырьки газа или воздуха, массы из “лопнувшей” холестериновой бляшки, гной и т. д.
Артериальные тромбозы и эмболии нельзя считать самостоятельными заболеваниями. Они всегда возникают как следствие других патологических состояний.
Причины возникновения тромба в просвете сосуда описаны немецким учёным Рудольфом Вирховым. Они объединены в известную триаду:
- Повреждение сосудистой стенки.
- Замедление кровотока.
- Нарушение состава крови.
Тромб образуется под воздействием всех трёх факторов с доминированием одного из них.
Повреждения сосудистой стенки вызывают:
- травмы — механические, термические, электрические и т. д.;
- воспалительные заболевания артерий — артерииты, облитерирующий атеросклероз с развитием атеротромбоза;
- тяжёлые инфекционные заболевания — сыпной тиф, грипп, сепсис.
Замедление кровотока возникает в следующих случаях:
- экстравазальные компрессии — сдавление сосуда извне опухолью, излившейся кровью, добавочным шейным ребром, костным фрагментом при переломе, механическим давлением при катастрофах и т. д.;
- аневризмы (расширения сосудов);
- артериальные спазмы;
- острая недостаточность кровообращения;
- длительное обездвиживание конечностей;
- онкологические заболевания.
К нарушению состава крови приводят патологии [11]:
- заболевания крови — лейкоз, эритроцитоз, полицитемия;
- значительное обезвоживание организма;
- наследственная или приобретённая тромбофилия (патологическое тромбообразование);
- системный атеросклероз;
- сахарный диабет;
- гипертоническая болезнь;
- злокачественные новообразования;
- эндотоксинемия (накопление в крови и тканях токсичных продуктов распада и жизнедеятельности бактерий);
- шоковые состояния;
- приём лекарственных препаратов — глюкокортикостероидов, эстрогенов и гестагенов (заместительная гормональная терапия и комбинированные оральные контрацептивы), гемостатиков, антифибринолитических средств.
Эмболии могут быть вызваны как заболеваниями сердца, так и другими причинами.
Кардиальные причины эмболии:
- ишемическая болезнь сердца;
- инфаркт миокарда;
- постинфарктный кардиосклероз;
- постинфарктные аневризмы левого желудочка;
- ревматические пороки сердца;
- септические бактериальные эндокардиты;
- опухоли сердца (миксомы).
В этих случаях тромб образуется в полостях сердца. Затем под влиянием гипертонического криза, смены сердечного ритма и других причин происходит его дефрагментация. Тромб устремляется с потоком крови, перекрывает участок артериального русла меньшего диаметра или развилку в области деления сосуда.
Внекардиальные причины:
- аневризма аорты;
- изъязвленные артериальные бляшки;
- пневмония;
- опухоль лёгких.
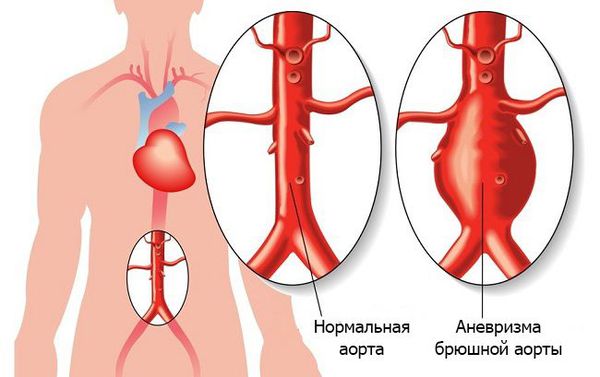
В редких случаях возможны парадоксальные эмболии — миграция тромба из венозной системы через правые отделы сердца в левые. Это возникает при врождённом пороке сердца и эмболии инородными предметами (например пулей или дробью) [4].
Частота острой ишемии конечностей составляет один случай на 6000 человек ежегодно [12]. С возрастом заболеваемость резко повышается. В подавляющем большинстве случаев патологией страдают люди старше 60 лет [8]. Ишемия, возникшая как осложнение тромбоза, чаще поражает мужчин, чем женщин.
Курение, малоактивный образ жизни и неправильное питание ведут к развитию атеросклероза, гипертонической болезни и сахарного диабета. Одновременно с этим повышается и риск развития артериальных тромбозов.
К индивидуальному риску сосудистой патологии относят:
- возраст моложе 50 лет при наличии сахарного диабета и одного из факторов риска атеросклероза: курение, дислипидемия (нарушение соотношения липидов в сыворотке крови), гипертензия, гипергомоцистеинемия (повышение уровня аминокислоты гомоцистеина в крови);
- возраст 50—69 лет и наличие сахарного диабета или курения;
- возраст 70 лет и старше [8].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы тромбоза артерии
Патологические симптомы при артериальном тромбозе или эмболии вызваны прекращением кровоснабжения органа или конечности. Их выраженность зависит от уровня поражения сосуда и степени ишемии.
Как правило, заболевание развивается достаточно остро, на фоне “полного благополучия”. При тромбозах клиническая картина более смазана по сравнению с эмболиями, т. к. при последних закупорка просвета артерии наступает внезапно.
Основные клинические симптомы:
- боль;
- бледность;
- парестезии (жжение, онемение, покалывание, “ползание мурашек”);
- паралич;
- отсутствие пульса в определённых местах конечности;
- снижение температуры кожи на несколько градусов.
Для удобства применяют симптомокомплекс “5 П” (в англоязычном варианте – 5 Р):
- появление болей (Pain) в поражённой конечности;
- отсутствие пульсации (Pulselessness) артерий;
- побледнение и похолодание (Pallor) кожных покровов;
- парестезия (Paresthesia) ;
- парез или паралич (Paralysis) с уменьшением активных движений вплоть до их полного отсутствия [5].
Заболевание в первую очередь проявляется болью в поражённой конечности. Следом возникает чувство онемения, похолодания, парестезии в виде покалываний, жжения, “ползания мурашек”. Затем — нарушения как поверхностной, так и глубокой чувствительности вплоть до полного её отсутствия. Побледнение кожи сочетается со снижением температуры поражённой конечности, особенно отстоящих её отделов. При выраженной ишемии вскоре присоединяются нарушения двигательных функций в виде пареза со снижением мышечной силы и до полной обездвиженности конечности. Если кровоток не восстанавливается, появляется болезненность и отёчность поражённых тканей конечности. На финальных этапах наступает контрактура, при которой невозможны даже пассивные движения в конечности, а в дальнейшем — некроз.
Симптомы не оторвавшегося тромба точно такие же, но наступают не так резко, как при эмболиях.
Патогенез тромбоза артерии
Первичными нарушениями, ведущими к образованию тромба является триада Вирхова. В процессе образования и тромба участвуют три компонента:
- сосудистая стенка (эндотелий);
- тромбоциты;
- каскад коагуляции.
Разрушение тромбоцитов сопровождается высвобождением фермента тромбопластина. Под действием тромбопластина неактивный фермент плазмы крови протромбин, образующийся в печени, переходит в активную форму — тромбин. Тромбин действует на растворимый белок плазмы — фибриноген. Фибриноген превращается в нерастворимый волокнистый белок фибрин. Нити фибрина захватывают форменные элементы крови и образуется плотный субстрат — тромб.
Мигрировавший эмбол, как правило, достигает места деления артерии. В ряде случаев при хорошо развитой сети обходных коллатералей (ветвей сосудов) закупорка артерии не приводит к существенным изменениям. В других случаях даже небольшого размера эмбол может значительно ухудшить кровообращение в конечности, особенно при изначальном выраженном поражении артериального русла.
К нарушениям гемодинамики начинают присоединяться микроциркуляторные нарушения. В дальнейшем происходят функциональные изменения нервно-мышечного аппарата и структурные и метаболические нарушениями в тканях. Наступает острое голодание ишемизированных тканей. Развивается отёк мышц со сдавлением тканей, находящихся в фасциальном футляре, что усугубляет нарушение тканевого кровотока [1].
Классификация и стадии развития тромбоза артерии
Классификация основана на прогрессировании острой артериальной непроходимости. В нашей стране наиболее часто применяется клиническая классификация острой артериальной непроходимости, разработанная В.С. Савельевым. Она состоит из 4-х степеней:
- 0 степень — жалобы появляются в ответ на нагрузку;
- IА — парестезии, онемение и похолодание в покое;
- IБ — боли в покое;
- IIА — парез конечности (ослабление мышечной силы);
- IIБ — плегия конечности (отсутствие мышечной силы);
- IIIА — субфасциальный отёк мышц;
- IIIБ — частичная мышечная контрактура (ограничение пассивных движений в суставе);
- IIIВ — тотальная мышечная контрактура;
- IV — гангрена конечности.
Классификация Савельева не всегда отражает выраженность ишемии при артериальных тромбозах. Клинически более востребована классификация, созданная И. И. Затевахиным. Она позволяет определять тактику лечения вне зависимости от причины ишемии и состоит из 3-х степеней:
- I степень ишемии — онемение, боли и/или парестезии в покое либо при малейшей физической нагрузке. Угрозы для конечности в ближайшее время нет.
- II степень ишемии — двигательные расстройства. Развитие болезни неминуемо ведёт к гангрене конечности:
– ишемия IIА степени — парез конечности, активные и пассивные движения сохранены, но мышечная сила ослаблена;
– ишемия IIБ степени — паралич конечности, пассивные движения возможны, активные отсутствуют, подвижность суставов сохранена;
– ишемия IIВ степени — присоединяется отёк мышц.
- III степень ишемии — финальная стадия ишемических повреждений тканей конечностей и мышц с развитием мышечных контрактур на разном уровне. Поражения носят необратимый характер:
– ишемия IIIА степени — ограниченные дистальные контрактуры;
– ишемия IIIБ степени — полная контрактура конечности.
Таким образом, I степень поражения не угрожает жизнеспособности конечности. II степень — угрожает потерей конечности, III — необратимая стадия [2].
По расположению в сосуде различают тромбы:
- пристеночный — ток крови сохранён;
- выстилающий (облитерирующий) — для тока крови остаётся лишь малый просвет;
- центральный, расположенный в центре сосуда — фиксирован к стенке тяжами, кровоток ограничен;
- закупоривающий (обтурирующий) — закрывает просвет сосуда полностью.
По форме:
- шаровидные тромбы в аневризмах или полостях сердца;
- мелкие тромбы, напоминающие бисер, часто встречаются на створках клапанов;
- продолговатые.
По механизму образования и строению выделяют следующие виды тромбов:
- Белый — состоит из тромбоцитов, лейкоцитов и фибрина с незначительным количеством эритроцитов. Образуется постепенно, чаще в артериальном русле, где скорость кровотока высока.
- Красный — формируется из тромбоцитов, фибрина и большого количества эритроцитов, которые попадают в сети фибрина, как в ловушку. Красные тромбы обычно возникают в венозной системе, где медленный кровоток способствует захвату красных клеток крови.
- Гиалиновый — возникает в сосудах микроциркуляторного русла. Состоит из тромбоцитов, гемолизированных эритроцитов и выпавших в осадок белков плазмы. Белковые соединения тромба напоминают гиалиновую массу (плотное образование, похожее на хрящевую ткань).
- Смешанный — встречается чаще всего, имеет слоистое строение. Слоистые тромбы образуются, как правило, в венах, в полости аневризмы аорты и сердца.
Осложнения тромбоза артерии
Осложнения зависят от того, как долго длилась ишемия конечности до момента оказания медицинской помощи. Также на возникновение осложнений влияет снижение компенсаторных свойств организма. При несвоевременном лечении конечность теряет функциональную активность, может возникнуть тромбоэмболия венозного русла, а также за несколько дней развиться гангрена, которая приведёт к летальному исходу [10].
Во время операции по удалению тромба возможны следующие осложнения:
- отрыв атеросклеротической бляшки;
- распространение тромба из одной ветви в другую;
- перфорация артериального русла, поражённого атеросклеротическим процессом.
После запуска кровотока в ишемизированную конечность в 15 % случаев возникают метаболические осложнения в виде миопатического (снижение силы мышц) и нефротического (воспаление почек с отёками и появлением белка в моче) синдромов. Они могут привести к потере конечности и летальному исходу [6].
Редким осложнением артериального тромба служит его гнойное расплавление при инфицировании. Это осложнение проявляется местной (покраснение, отёк, болезненность) и общей (повышение температуры, септическое состояние) симптоматикой.
Диагностика тромбоза артерии
Диагностика включает клинические и инструментальные методы.
Клинические методы диагностики:
- оценка кожной температуры, поверхностной чувствительности и венозного рисунка;
- определение артериальной пульсации конечности в сравнении с оценкой пульсации второй конечности;
- измерение артериального давления;
- выслушивание шумов над зоной деления аорты и бедренных артерий;
- выявление резкой болезненности при пальпации мышечных тканей;
- оценка амплитуды движений в суставах.
К инструментальной диагностике относят ультразвуковые и лучевые методы обследования.
Ультразвуковая допплерография позволяет выявить наличие либо отсутствие допплеровских сигналов от артериального сосуда. С помощью ультразвукового дуплексного ангиосканирования можно определить характер, степень и протяжённость тромба.

Если предыдущие исследования недостаточно определяют локализацию, степень, протяжённость и анатомо-топографические особенности поражения и не позволяют выбрать оптимальную тактику оперативного лечения, применяют высокоточные лучевые методы диагностики. К ним относятся:
- рентгеноконтрастная ангиография;
- мультиспиральная компьютерная томография;
- магнитно-резонансная ангиография.
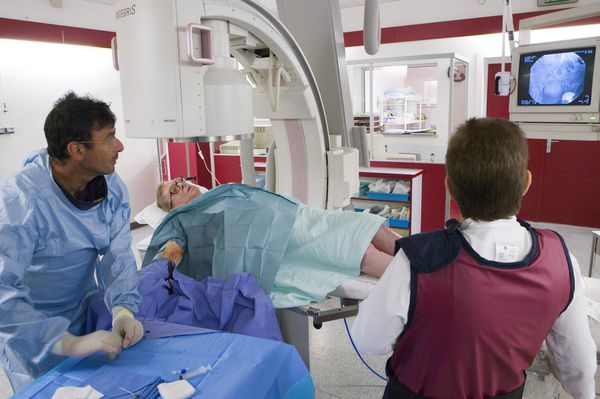
С помощью этих исследований уточняют характер анатомо-топографических особенностей поражения и выбирают тактику оперативного лечения [1]. Все эти исследования позволяют определить протяжённость и локализацию тромба.
Лечение тромбоза артерии
Лечебные мероприятия зависят от степени ишемического поражения конечности. В настоящее время препаратов с доказанной эффективностью лечения острой ишемии не существует. Консервативная терапия возможна при I степени острой ишемии в качестве пробного метода лечения. Также она показана всем пациентам при подготовке к операции и послеоперационном ведении [7][8].
Цели консервативной терапии:
- профилактика нарастания и распространения тромба;
- растворение тромба;
- улучшение кровообращения в поражённой конечности;
- восстановление функции поражённых органов.
Для терапии применяют:
- антикоагулянты;
- активаторы фибринолиза;
- анальгетики и спазмолитики;
- раствор натрия гидрокарбоната.
Тромболитическую терапию с введением препаратов фибринолизина, стрептокиназы, урокиназы и стрептодеказы назначают на начальных этапах заболевания для растворения тромба. В качестве самостоятельного лечения применение препаратов ограничено. Их эффективность повышается в сочетании с баллонной ангиопластикой и катетерной аспирационной тромбэктомией.
Консервативная терапия является профилактикой прогрессирования ишемических явлений. При отсутствии эффекта от медикаментозного лечения назначают операцию, которая также предотвращает развитие ишемии.
Хирургическое лечение включает:
- тромбэмболэктомию;
- реконструктивные операции;
- фасциотомию;
- ампутацию конечностей.
Тромбэмболэктомией называют удаление патологических тромбоэмболических масс из просвета поражённого сосуда. При прямой тромбэмболэктомии удаление масс проводят через хирургический доступ артерии непосредственно над ними. Непрямая тромбэмболэктомия подразумевает удаление патологического субстрата вне артериального доступа специальным баллонным катетером Фогарти. Этот катетер вводят в артерию через её разрез и продвигают дальше патологических масс. После чего раздувают баллон, которым перекрывают просвет сосуда и путём обратной тракции катетера извлекают его вместе с этими массами.
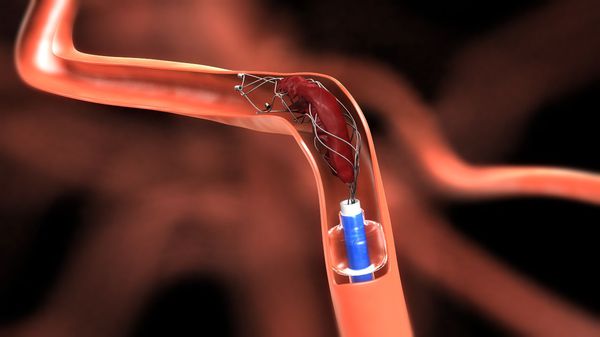
В ряде случаев проводят хирургическое устранение причины эмболии — резекцию добавочного шейного ребра и аневризмы, митральную комиссуротомию и т. д.
Необходимость реконструктивных операций возникает примерно в 10 % при выраженных атеросклеротических и атеротромботических процессах, когда результаты тромбэмболэктомии не могут обеспечить полноценное поступление крови в поражённую конечность. К реконструктивным операциям относят различные виды шунтирований, например бедренно-подколенное или бедренно-берцовые шунтирования.
При ишемии IIВ степени операцию необходимо завершить рассечением поверхностных фасций (фасциотомия) для предотвращения некроза мышц вследствие их отёка. Всего в данной операции нуждается от 5 до 25 % пациентов с острой артериальной непроходимостью.
При необратимых процессах, произошедших в тканях конечности, проводят её ампутацию на различных уровнях [8].
Прогноз. Профилактика
Острую ишемию конечностей ежегодно выявляют у 14 пациентов на 100 тыс. населения. Её распространённость достигает 16 % среди всех сосудистых заболеваний.
Прогноз в отношении сохранения нижних конечностей зависит от локализации и характера поражения артерий, степени и остроты ишемии конечности, возможностей восстановления артериального кровообращения.
Тромб, как правило, отрывается при высоком давлении, резких движениях, низкой фиксированности к сосудистой стенке, его “хрупкости”. Полностью тромб заполнит просвет или нет, зависит от системы коагуляции (свёртываемости крови). Станет ли тромб причиной ишемии, обусловлено его размером и сосудом, в котором он находится, а также степенью компенсации.
Прогноз для жизни зависит как от тяжести ишемии конечности, так и от сопутствующих патологий.
Естественное течение заболевания без специализированного лечения ведёт к усугублению клинической симптоматики с возможной потерей конечности либо летальным исходом. Гангрена конечности развивается у 5—24 % пациентов с эмболиями и у 28—42 % с тромбозами. Инвалидизация наступает в 15—25 % случаев. Летальность среди неоперированных больных составляет от 15 до 38 % [4].
Профилактические мероприятия сводятся к предупреждению развития заболеваний, которые служат причиной артериальных тромбозов и эмболий и борьбе с факторами риска атеротромбоза.
К факторам риска относятся:
- малоподвижный образ жизни;
- артериальная гипертония;
- сахарный диабет;
- ожирение;
- курение;
- гиперхолестеринемия.
Для профилактики тромбозов европейское общество кардиологов предлагает стратегию “0-3-5-140-5-3-0”:
- 0 – избегать курения табака;
- 3 – ежедневно заниматься физкультурой в течение 30 минут или ходить 3 км;
- 5 – ежедневно употреблять 5 фруктов и овощей;
- 140 – артериальное давление не выше 140/90 мм рт. ст.;
- 5 – показатель общего холестерина менее 5 ммоль/л;
- 3 – уровень холестерина низкой плотности менее 3 ммоль/л;
- 0 – индекс массы тела менее 25 кг/м2[9].

