Анемия плода по доплеру
Анемия у плода. Эхографические признаки анемии у плодаРезультатом изоиммунизации эритроцитов является прогрессирующее снижение их количества, что приводит к развитию анемии у плода. Внутриутробные внутрисосудистые гемотрансфузии, выполняемые при кордоцентезе, являются стандартным методом лечения анемии у плода. Эти процедуры сопровождаются быстрым введением большого количества крови в его кровеносное русло. Использование допплер-эхокардиографии позволило изучить особенности гемодинамических изменений, возникающих у плода при анемии, а также ответную реакцию на ее быструю коррекцию путем переливания крови. При анемии минутные объемы левого и правого желудочковых выбросов бывают достоверно выше, чем при нормальном состоянии, и между тяжестью анемии и сердечным выбросом имеется достоверная взаимосвязь. Вследствие высокого объема крови максимальные скорости в выносящих трактах повышаются. Кроме того, повышается отношение Е/А для обоих атриовентрикулярных клапанов. Венозный кровоток подвергается аналогичным изменениям: повышается маскимальная скорость в венозном протоке и исчезает пульсация КСК.
Хотя механизмы, отвечающие за увеличения сердечного выброса, остаются еще не выяснены, к этому могут иметь отношение два основных фактора: первый заключается в снижении вязкости крови, что ведет к увеличению венозного возврата и преднагрузки, а второй связан с периферической вазодилатацией, вызванной падением содержания кислорода в крови, что ведет к уменьшением постнагрузки. Роль первого механизма подтверждается высокими значениями отношения Е/А, которые отмечаются при наличии анемии у плода. В настоящее время нет данных о перераспределении сердечного кровотока, которое наблюдается при гипоксии у плодов с задержкой внутриутробного развития (эффект защиты головного мозга), поскольку отношение ПЖВ/ЛЖВ у плодов с анемией остается в переделах нормы. Это согласуется с нормальными значениями ПИ в периферических сосудах при внутриутробной анеми. Полученные данные позволяют предположить, что при изоиммунизации эритроцитов изменения функции сердца у плода связаны главным образом со снижением вязкости крови, что приводит к появлению гипердинамического типа кровообращения. После внутриутробной внутрисосудистой гемотрансфузии наблюдается временное достоверное падение объемов минутного правого и левого желудочкового выброса, сопровождающееся повышением отношения Е/А. Последние изменения, вероятно, вызваны повышением преднагрузки, возникающей вследствие относительно большого объема перелитой крови, попавшей в кровяное русло. Снижение сердечного выброса теоретически может быть следствием изменения четырех различных факторов (ЧСС, преднагрузки, сократительной функции миокарда или постнагрузки). Первый фактор можно исключить, поскольку минутный объем сердца снижается при отсутствии каких-либо достоверных изменений ЧСС у плода. Преднагрузка должна была бы снижаться, для того чтобы подтвердить свое влияние на снижение сердечного выброса, но высокие значения отношения Е/А свидетельствуют об увеличении, а не уменьшении преднагрузки. Аналогично представляется маловероятным, что ухудшение сократительной активности миокарда может играть роль с точки зрения влияния на КСК в аорте и легочном стволе. Таким образом, повышение сердечной постнагрузки оказывается наилучшим объяснением уменьшения сердечного выброса сразу после переливания крови плоду. Заслуживает внимания тот факт, что снижение сердечного выброса у плода человека происходит пропорционально увеличению объема крови в фетоплацентарном русле. Более того, в течение 2 ч после гемотрансфузии все эхокардиографические параметры возвращаются практически к нормальному уровню, свидетельствуя о быстром восстановлении функции сердца плода. – Также рекомендуем “Диссоциированное развитие близнецов. Осложнения развития близнецов из двойни” Оглавление темы “Допплерография плода. Исследование плаценты плода”: |
Источник
Алгоритм оценки анемии у плода. Кровоток в средней мозговой артерии при анемии у плода
Для эффективного использования алгоритма особое значение имеет соблюдение следующих условий.
1. Плод должен находиться в группе риска по развитию анемии.
2. Исследование должен проводить опытный специалист.
3. Сразу после определения позиции плода в полости матки необходимо получить максимально увеличенное изображение области расположения СМА.
4. Максимальная скорость кровотока должна определяться при угле между ультразвуковым лучом и направлением кровотока, близким к 0°. Должна учитываться максимальная из зарегистрированных скоростей кровотока.
5. Контрольный объем импульсно-волнового допплера устанавливается максимально близко к месту отхождения СМА от внутренней сонной артерии.
6. Все измерения должны быть выполнены не менее 3-5 раз.
Мультицентровые исследования позволили установить, что в 70% случаев проведение инвазивных процедур (амниоцентеза и кордоцентеза), используемых для оценки состояния плодов из группы риска по развитию анемии вследствие иммуноконфликтной беременности, не имело необходимости . Чувствительность теста, основанного на выявлении увеличения максимальной скорости кровотока в СМА, для прогнозирования анемии средней или тяжелой степени составила 100% как при наличии, так и при отсутствии водянки плода (95% доверительный интервал, 86-100%) с ложноположительным результатом на уровне 12%. Предварительные проспективные исследования подтвердили эти результаты.

Аналогичные данные были получены при изучении кровотока в селезеночной артерии. Однако в целях диагностики мы выбрали для использования среднюю мозговую артерию, так как при ее исследование легко получить угол 0° между направлением ультразвукового луча и ходом сосуда, а получаемые значения высоко воспроизводимы.
Приведем описание двух клинических наблюдений.
Первая пациентка (26 лет, беременностей 2, роды 1) была обследована в сроке 32 нед. Беременность осложнилась антенатальной гибелью одного плода из двойни. Проводилось наблюдение для оценки роста и состояния оставшегося живого плода. Кровоток в артерии пуповины был в пределах нормы. Максимальная скорость кровотока в СМА была выше нормативных значений (116 см/с). У пациентки имелась резус-отрицательная кровь, и она получала иммуноглобулин антирезус (RhoGAM).
Через несколько дней у плода был диагностирован асцит. При рождении его гематокрит составлял 12%. Был установлен диагноз резус-иммунизации. Новорожденному произведено заменное переливание крови, после чего его состояние нормализовлось. У второй пациентки до 36 нед беременность протекала без осложнений, когда она поступила в клинику с жалобами на снижение двигательной активности плода. При нестрессовом тесте отмечалась синусоидальный тип кривой КТГ. Данные фетометрии при ультразвуковом исследовании были нормальными, также как и значения ПИ в артерии пуповины. Максимальная скорость кровотока в СМА составляла 111 см/с. Было выполнено родоразрешение путем операции кесарева сечения. Родилась девочка, гематокит крови которой составил 7%. Был установлен диагноз трансплацентарного материнско-плодового кровотечения. После рождения состояние новорожденной нормализовалось.
– Также рекомендуем “Допплерометрия при многоплодной беременности. Кровоток в артериях пуповины при двойне”
Оглавление темы “Допплерометрия при ЗВРП. Оценка кровотока при гемолитической болезни у плода”:
1. Тактика ведения плодов с задержкой внутриутробного развития. Пример задержки внутриутробного развития (ЗВРП)
2. Повторяющийся синдром ЗВРП. Примеры повторяющихся форм ЗВРП
3. Наблюдение задержки внутриутробного развития плода. Причины ЗВРП
4. Оценка кровотока у плода при ЗВРП. Оценка кровотока в нисходящей аорте
5. Кровоток в ветвях аорты при ЗВРП. Венозная гемодинамика у плода в норме
6. Венозная гемодинамика при ЗВРП. Атриовентрикулярные клапаны при ЗВРП
7. Показатели ускорения кровотока при ЗВРП. Допплерография сердечного выброса у плода
8. Допплерометрия при гемолитической болезни плода. Оценка гематокрита плода
9. Алгоритм оценки анемии у плода. Кровоток в средней мозговой артерии при анемии у плода
10. Допплерометрия при многоплодной беременности. Кровоток в артериях пуповины при двойне
Источник
Девочки, всем привет!!!
В общем, может кто-то об этом не знает, но существует конфликт по группе крови, не только по резус фактору. Даже если оба родителя положительные, то это не гарантия что не возникнет конфликта между матерью и ребенком. В общем собрала информацию, а то некоторые гинекологи в обычных ЖК и не слышали о таком, только о резус-факторе слышали, сама столкнулась с таким врачом, в итоге я ей объясняла)))). Слава Богу я у нее на учете не стою, это мы так разговорились, она знакомая моей мамы. Ну думаю, раз врач о таком не знает, то и мы девочки других профессий тем более можем об этом и не знать!!!
Конфликт по группе крови: причины и опасность для плода
О том, что существует противоречие резус-факторов отца и матери, которое может негативно сказаться на плоде и на самом течении беременности, хорошо знают все будущие матери. Но для многих шоком оказываются сведения о том, что существует риск возникновения в беременности конфликта по группе крови. Это происходит в тех случаях, когда будущий ребенок унаследует кровь от своего отца, плохо сочетающуюся с группой крови матери.
В организме матери начинают вырабатываться антитела к крови плода, то есть имеется угроза, что материнское тело может отторгнуть беременность, а плод рискует пострадать, получив гемолитическую болезнь новорожденных.
Конфликт по группам крови может возникнуть, если группа крови женщины отличается от группы крови будущего малыша,
Например:
-если у матери I или III группа крови, а у плода II,
-если у матери I или II группа крови, а у плода III,
-если у плода IV группа крови, а у матери – любая другая.
Наиболее тяжелые последствия несовместимости по группам крови возникают, если у матери I группа крови, а у плода II или III.
При нормальном течении беременности конфликт по группам крови не возникнет, благодаря особому строению плаценты. Плацента состоит из двух частей: материнской и плодовой, разделенных плацентарным барьером. Питательные вещества и кислород поступают из крови матери в материнскую часть плаценты, затем передаются через барьер в плодовую часть и к плоду. Благодаря плацентарному барьеру кровь матери и плода не смешивается.
Но если произойдет даже небольшая отслойка плаценты, клетки крови матери и плода могут смешаться. Также они могут смешаться во время родов, если нарушится целостность сосудов плаценты. Вследствие такого смешивания у матери образуются антитела к чужеродным клеткам крови, которые проникают к плоду и приводят к распаду его клеток крови. В процессе распада образуются токсические вещества, которые могут повреждать печень, почки, головной мозг. У плода и новорожденного может развиться гемолитическая болезнь, симптомами которой являются отеки, желтуха, анемия. Также у ребенка может наблюдаться увеличение печени и селезенки.
Чтобы предотвратить развитие конфликта по группам крови, в женской консультации выявляют беременных женщин из группы риска:
-у которых в анамнезе есть переливание крови;
-выкидыши;
-дети, рожденные с гемолитической болезнью или с отставанием в психическом развитии.
-выкидыши;
-дети, рожденные с гемолитической болезнью или с отставанием в психическом развитии.
Так как профилактики гемолитической болезни плода и новорожденного в случае конфликта по группам крови не существует, то женщины из группы риска регулярно сдают анализы крови на наличие антител к клеткам крови и в случае необходимости направляются в специализированный стационар. Необходимо также отметить, что конфликт по группам крови встречается реже и приводит к меньшим негативным последствиям, чем резус-конфликт, при котором женщина с отрицательным резусом вынашивает резус-положительного ребенка.
Конфликт, обусловленный несовместимостью по группе крови, встречается чаще, но при АВО-конфликте большие проблемы развиваются реже, чем при несовместимости по резус-фактору. Предсказать вероятность возникновения патологического процесса можно, зная резус-принадлежность и группу крови отца и матери. Если у папы и мамы резус-отрицательная кровь, то и все дети этой пары будут резус-отрицательными. При наличии у отца резус-положительной крови а у матери резус-отрицательной вероятная резус-принадлежность плода рассчитывается как 50% на 50 %.
ПОЧЕМУ ОПАСЕН КОНФЛИКТ ПО ГРУППЕ КРОВИ ПРИ БЕРЕМЕННОСТИ?
Опасен конфликт по группе крови при беременности для ребенка, а не для мамы. В организм малыша проникают антитела к А- и В- антигенам, далее они вступают во взаимодействие с эритроцитами плода, вследствие этого наступает гемолиз (разрушение эритроцитов крови) и анемия (снижение гемоглобина в крови). Затем образуется непрямой токсичный билирубин, он растворяется в клетках головного мозга малыша, печени и селезенки. Поэтому крайне тяжелой степенью ГБН (гемолитическая болезнь новорожденного) есть водянка ребенка, он будто весь налит водой. Но тяжелые случаи ГБН при несовместимости группы крови матери и ребенка встречаются очень редко.Отличительной особенностью изосерологического конфликта по системе АВО отличается позднее проявление гемолитической болезни новорожденного, это может произойти через несколько дней после родов, кожа малыша становится желтой, так называемая желтуха новорожденных.В современных медицинских центрах роженице при большом титре антител в крови, когда ребенок рождается с ГБН, не разрешают некоторое время прикладывать малыша к груди, а могут и совсем запретить грудное вскармливание. Дело в том, что в молозиве также содержатся антитела, и атака детского организма продолжается.
Женщинам с возможным конфликтом по группе крови при беременности важно быть очень осторожной с инвазивными процедурами (амниоцентез, кордоцентез). Когда прокалывают материнский живот с целью забора амниотической жидкости или анализа крови плода, то после этих манипуляций повышается уровень антител.
Иммунологическая несовместимость чаще бывает, когда у женщины первая группы крови 0(I), а у мужчины другая группа, но конфликтуют чаще, когда плод наследовал вторую А(II) группу крови. В таком случае у женщины берется анализ крови на определение антител к эритроцитам по системе ABO.
Интересно знать, что несовместимость по крови и по резус-фактору одновременно гораздо лучше, чем по отдельности. Это объясняется тем, что две несовместимости «конкурируют» между собой.
Всем Удачи девочки!!! И здоровых малышей крепышей!!!
Источник

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
По данным ISUOG, в последние десятилетия отмечено увеличение более чем на 70% случаев рождения двоен [1]. Это связано с широким внедрением вспомогательных репродуктивных технологий, отсроченным поздним зачатием, использованием противозачаточных препаратов.
По типу хориальности различают дихориальные и монохориальные двойни, причем 2/3 из них составляют дихориальные двойни.
Каждый плод из дихориальной двойни имеет собственную плаценту, свое отдельное сосудистое русло, и каждый развивается по своему сценарию, общим для них является состояние матери, которое, естественно, отражается на состоянии плодов.
Монохориальные двойни имеют одну общую плаценту. Практически в 100% случаев в общей плаценте имеются многочисленные сосудистые анастомозы, связывающие напрямую системы кровообращения обоих плодов. Плацентарные анастомозы бывают артерио -артериальные (АА), вено-венозные (ВВ) и артериовенозные (АВ) [2]. Все эти анастомозы могут располагаться и на поверхности плаценты, и в глубине. И если АА- и ВВ-анастомозы в большинстве случаев скомпенсированы, то АВ-анастомозы, где кровь из артерий одного плода дренируется напрямую в вены другого плода, являются причиной многочисленных осложнений.
Фето-фетальные трансфузионные синдромы
По статистике, течение беременности при монохориальных двойнях осложняется в 10–15% случаев фето-фетальными трансфузионными синдромами (ФФТС) разной степени тяжести [3–5], причем клинические проявления ФФТС зависят от наличия именно АВ-анастомозов, их количества и размеров. Классический ФФТС диагностируется обычно на сроках от 16 до 26 нед и характеризуется наличием маловодия, максимальный вертикальный карман (МВК) менее 2 см у плода-донора, и многоводием, МВК более 8 см у плода-реципиента. Практически одновременно с этим первым признаком ФФТС при ультразвуковом исследовании (УЗИ) выявляется второй признак: у плода-донора мочевой пузырь или не визуализируется, или бывает значимо маленьким, а у реципиента – переполнен, или значимо большой. Эта самая частая форма ФФТС в настоящее время называется синдромом олигурии-полиурии (TOPS), связана с наличием крупных АВ-анастомозов на поверхности плаценты, приводящих к гиперволемии плода-реципиента и гиповолемии плода-донора. При своевременной ультразвуковой диагностике эта форма поддается антенатальной коррекции фетоскопической лазерной коагуляцией АВ-анастомозов.
При наличии глубоких АВ-анастомозов малого диаметра (до 1 мм) и в отсутствие компенсирующих АА-анастомозов в 3–5% случаев у монохориальной двойни может развиваться еще одна форма ФФТС – синдром анемии-полицитемии (TAPS), когда по мельчайшим анастомозам происходит хроническое медленное кровотечение от донора к реципиенту [6]. При УЗИ количество околоплодных вод может быть приблизительно одинаково нормальным, и заподозрить TAPS можно, если обратить внимание на разницу в толщине и эхогенности территорий плацент донора и реципиента. При измерении пиковой систолической скорости (ПСС) в средней мозговой артерии (СМА) каждого плода подтверждается, что у плода с признаками анемии с ПСС выше 1,5 МоМ территория плаценты утолщена, эхогенность ее повышена, а у реципиента с признаками полицитемии с ПСС ниже 1,0 МоМ территория плаценты обычной толщины и низкой эхогенности. В случае ФФТС в виде TAPS в отличие от TOPS существующие методы пренатального лечения не так эффективны, так как мелкие глубокие АВ-анастомозы практически не видны при фетоскопии. Некоторые специалисты проводят полную лазерную дихорионизацию плаценты по сосудистому руслу с предварительной амниоинфузией. Методом выбора является внутриутробная гемотрансфузия плоду-донору, однако она эффективна только в отсутствие значимо крупных анастомозов, усугубляющих полицитемию плода-реципиента. Таким образом, эффективность однократной гемотрансфузии плоду-донору имеет и лечебное, и диагностическое значение. В противном случае некоторые специалисты проводят обменные гемотрансфузии с возмещением реципиенту объема изъятой крови физиологическим раствором [7]. Так как в большинстве случаев TAPS возникает после 26 нед, все мероприятия направлены на продление беременности с целью достижения периода жизнеспособности плодов.
Синдром селективной задержки внутриутробного роста
Синдром селективной задержки внутриутробного роста (сЗВУР) выражается в отставании в росте одного из плодов и характеризуется дискордантностью фетометрических показателей двух плодов более чем на 25% и высчитывается по формуле:
(Масса тела большего плода – Масса тела меньшего плода) / Масса тела большего плода × 100 ≥ 25%.
Селективная ЗВУР не считается уникальным осложнением монохориальной двойни и не относится к ФФТС. У дихориальной двойни также может возникать дискордантность в росте и развитии одного из плодов, причиной может быть хромосомная аномалия одного из плодов дихориальной двойни, например трисомия 18, или триплоидия, оболочечное прикрепление пуповины, пороки развития плода типа скелетных дисплазий и т.д. Причиной может быть и истинная плацентарная недостаточность одной из плацент, когда недоразвиты ворсины, сосуды ворсин и соответственно сосудистое русло плаценты. Терминальная плацентарная недостаточность может привести к гибели меньшего плода, однако отсутствие каких-либо общих сосудов между плацентами позволяет оставшемуся плоду развиваться без осложнений до доношенного срока.
При синдроме сЗВУР у монохориальной двойни при идентичном генном и хромосомном наборе может быть катастрофическая разница по площади принадлежащих плодам плацентарных территорий с аномальным развитием ворсин и сосудистого русла плацентарной ткани у плода с сЗВУР (рис. 1).
При терминальной плацентарной недостаточности происходит гибель меньшего плода, которая в большинстве случаев влечет за собой гибель нормального плода. Объясняется это наличием сосудистых анастомозов (АА и ВВ) в одной общей плаценте, но в отличие от ФФТС плацентарные анастомозы здесь играют положительную роль, долгое время компенсируя и поддерживая жизнь плода с маленькой плацентарной территорией (рис. 2).
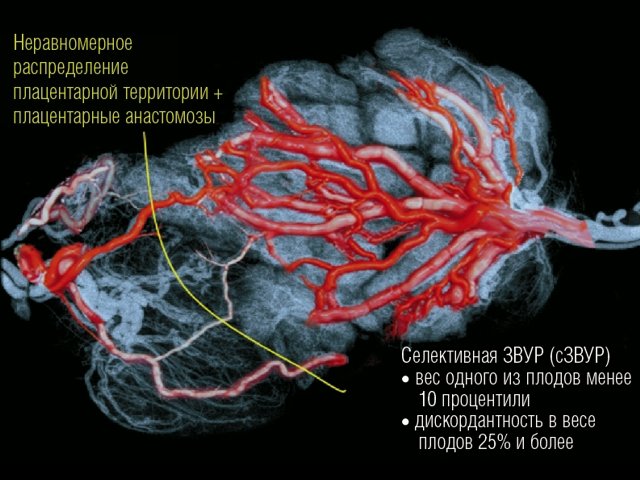
Рис. 1. Распределение сосудов в плаценте монохориальной двойни при селективной ЗВУР.
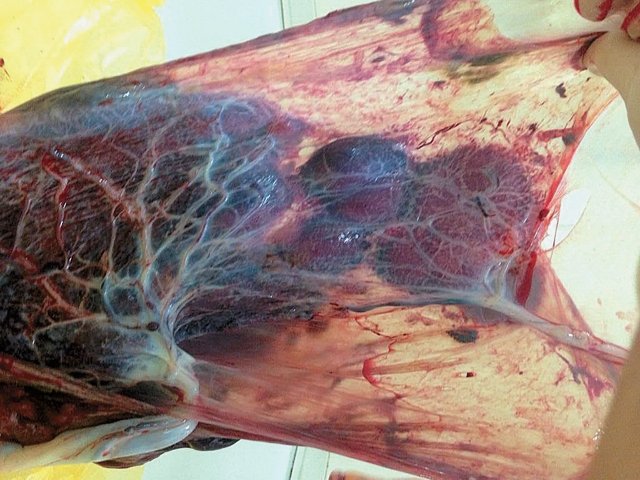
Рис. 2. Фото типичной плаценты при селективной ЗВУР монохориальной двойни.
Как только плод погибает, давление падает, и по этим же анастомозам происходит острое кровотечение из сосудистого русла живого плода в сосудистое русло мертвого. Живой плод в большинстве случаев погибает от кровопотери или становится в будущем инвалидом из-за обширных кровоизлияний в мозг на фоне анемии, тромбоцитопении и гипоксии.
Прогноз при монохориальной беременности с сЗВУР оценивается по состоянию диастолического кровотока в артериях пуповины меньшего плода [8]. При положительном диастолическом кровотоке беременность пролонгируют до 35 нед (тип I, исход предсказуем), при отсутствии конечного диастолического кровотока (ОКДС) в артериях пуповины, при нормальном кровотоке в венозном протоке беременность пролонгируют до 29 нед в зависимости от состояния кровотока в венозном протоке (тип II, исход предсказуем), при интермиттирующем диастолическом кровотоке в артериях пуповины, когда наблюдаются фазы с положительным и реверсным диастолическим кровотоком (тип III, исход непредсказуем), пролонгируют беременность до 32 нед, то есть до периода жизнеспособности (рис. 3).
Синдром сЗВУР, по данным различных авторов, встречается в 5–25% случаев и в большинстве наблюдений развивается по вышеописанному сценарию. Однако нет правил без исключения. Мы представляем наблюдение монохориальной диамниотической двойни, которое по всем диагностическим критериям соответствовало синдрому сЗВУР, а закончилось острым развитием синдрома анемии-полицитемии (TAPS).
Клиническое наблюдение
Первобеременная К., 27 лет, поступила в гинекологическое отделение РКБ 30 декабря 2019 г. с диагнозом: беременность 18 нед, монохориальная диамниотическая двойня. Подозрение на ФФТС.
При УЗИ определяется монохориальная диамниотическая двойня с дискордантностью в массе тела плодов 38%, околоплодные воды в норме, МВК первого плода 6 см, а МВК второго – 4 см. Кровоток в артериях пуповины обоих плодов в норме, пульсативные индексы соответственно 1 и 1,6, диастолический кровоток положительный, оболочечное прикрепление пуповины у меньшего плода. Полученные данные соответствуют синдрому сЗВУР I типа, диагноз ФФТС исключается. В соответствии с протоколом ведения беременности при монохориальных двойнях рекомендуется УЗ-контроль через 2 нед.
УЗ-контроль от 09. 01. 2020: ФПК у обоих плодов в норме, диастолический кровоток положительный, воды в норме.
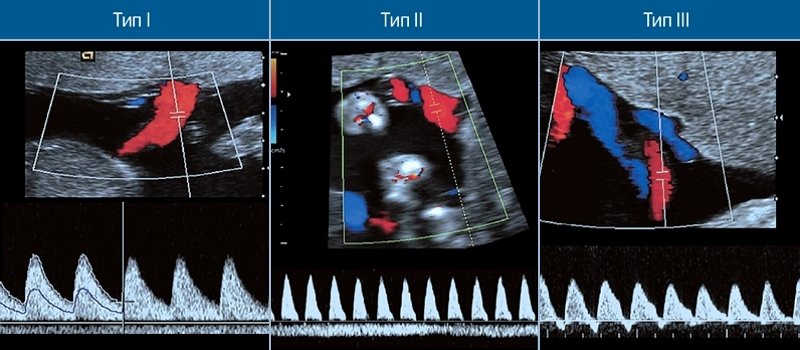
Рис. 3. Кривые скоростей кровотока в артериях пуповины при I, II и III типах селективной ЗВУР монохориальной диамниотической двойни.
УЗ-контроль от 21.01.2020: беременность 21 нед, монохориальная диамниотическая двойня, дискордантность в массе тела 30% (430 и 301 г соответственно), воды в норме, в артериях пуповины плода с сЗВУР обнаружено отсутствие диастолического кровотока (ОКДС). Таким образом, диагноз сЗВУР I типа трансформировался в сЗВУР II типа. Однако кровоток в венозном протоке у обоих плодов оставался в норме, ПИ – 0,78, воды в норме.
УЗ-контроль от 04.02.2020: беременность 23 нед, монохориальная диамниотическая двойня, сЗВУР II типа, дискордантность в массе тела 30% (627 и 437 г соответственно), кровоток в венозном протоке и воды в пределах нормы у обоих плодов. Рекомендован контроль через 1 нед по стандарту наблюдения за двойней с сЗВУР II типа с целью наблюдения за меньшим плодом, пролонгируя беременность до жизнеспособного срока.
При контрольном УЗИ (18.02.2020) монохориальной двойни на сроке беременности 25 нед, осложненной сЗВУР, были выявлены признаки синдрома анемии-полицитемии (TAPS). Признаки полицитемии: гипоэхогенная тонкая территория плаценты (рис. 4), ПСС в СМА – 30см/с – 0,8 МоМ, признаки перегрузки правых отделов сердца: асцит (рис. 5), гидроторакс, кардиомегалия, трикуспидальная регургитация, реверсный кровоток в венозном протоке (рис. 6), отек мягких тканей были у меньшего плода, а у плода с нормальной массой тела выявлены признаки тяжелой анемии: ПСС в СМА – 61 см/с – 1,8 МоМ, расчетный гемоглобин 15 г/л, плацентарная территория утолщена с повышенной эхогенностью
(рис. 4). Воды у этого плода тоже были в норме.
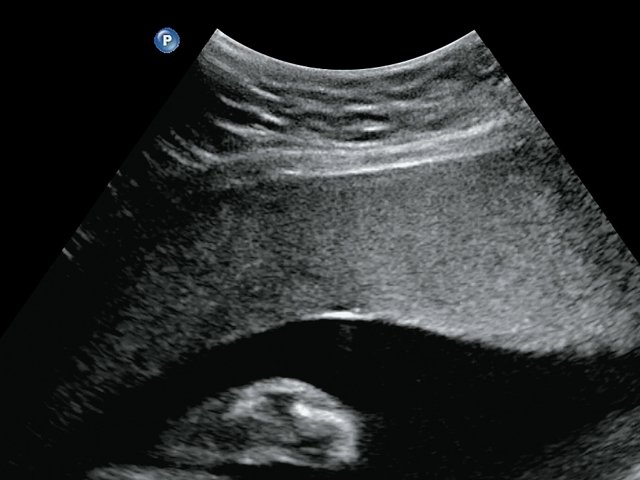
Рис. 4. Гипоэхогенная тонкая территория плаценты у плода с полицитемией, плацентарная территория утолщена с повышенной эхогенностью у плода с анемией.
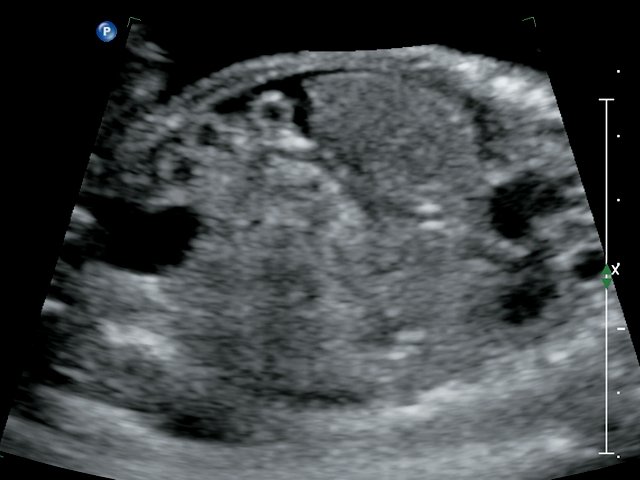
Рис. 5. Эхограмма асцита у плода с полицитемией.
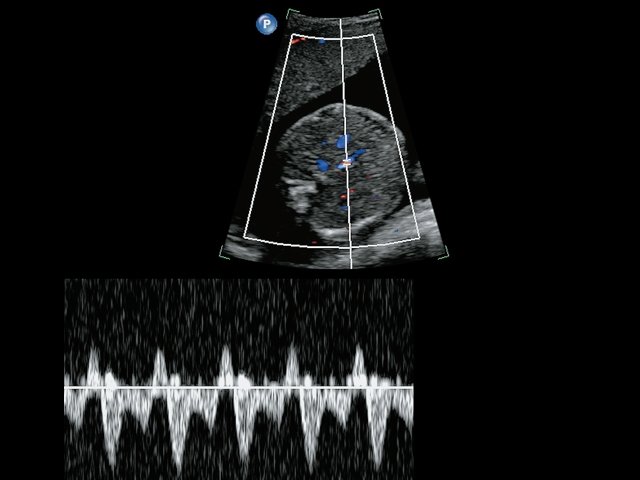
Рис. 6. Эхограмма реверсного кровотока в венозном протоке у плода с полицитемией.
Таким образом, было диагностировано острое развитие синдрома анемии-полицитемии у монохориальной диамниотической двойни, осложненной селективной ЗВУР II типа с дискордантностью в массе тела плодов 30%. Пациентка была срочно госпитализирована в Перинатальный центр. В связи с терминальным состоянием меньшего плода и экстремально ранним сроком беременности (25 нед) была принята выжидательная тактика в надежде сохранить больший плод после гибели меньшего, начата подготовка эритромассы для гемотрансфузии плоду с анемией на утро следующего дня.
Однако на следующий день до начала трансфузии при контрольном УЗИ была диагностирована гибель обоих плодов.
После родов при осмотре плодов (рис. 7) и плаценты (рис. 8) были подтверждены диагнозы селективной ЗВУР (sIUGR) и синдрома анемии-полицитемии (TAPS). У маленького плода темно-бордовый цвет кожи, корень пуповины расположен по краю плаценты, пуповина темная, отечная, плацентарная территория темная, маленькая, на ней видны только два поверхностных сосуда и один анастомоз. Плацентарная территория большего плода нормальных размеров, очень светлой окраски, на ней видны множество крупных сосудов белого цвета, корень пуповины расположен центрально, кожа плода светлая.
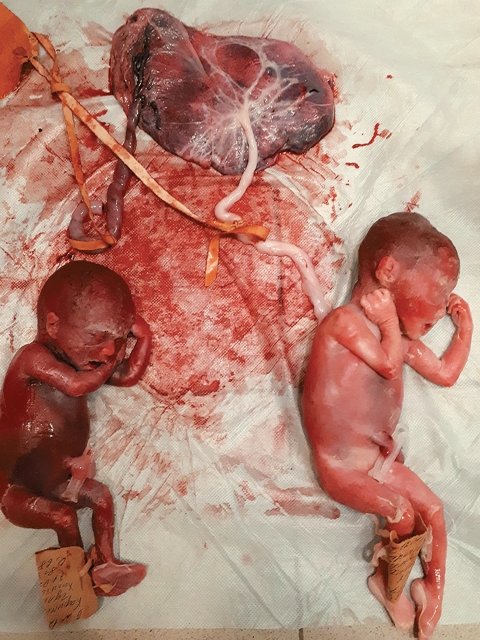
Рис. 7. Фото плодов после родоразрешения.
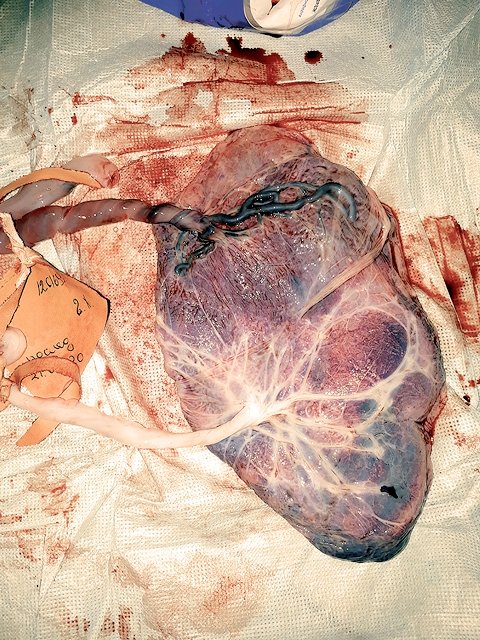
Рис. 8. Фото плаценты.
В доступной англоязычной и русскоязычной литературе мы не обнаружили сообщений о подобном случае. Синдром анемии-полицитемии (TAPS) относится к ФФТС с хроническим сбросом через мелкие глубокие АВ-анастомозы, характеризует его хроническую, медленно текущую форму. В свою очередь синдром сЗВУР не связан с ФФТС, имеющиеся при этом характерные для любой монохориальной двойни АА- и ВВ-анастомозы играют положительную роль, обеспечивая жизнь и рост плода с сЗВУР, компенсируя тяжелую первичную недостаточность плацентарной территории этого плода.
В нашем наблюдении произошла декомпенсация АА- и ВВ-анастомозов, затем начались расширение мелких АВ-анастомозов в общей плаценте, массивный сброс крови от плода с нормальной массой тела плоду с сЗВУР с последующей гибелью плода с анемией от острой кровопотери и плода с полицитемией от терминальной сердечной недостаточности в условиях хронической фето-плацентарной недостаточности.
Наше наблюдение показывает безграничность вариантов осложнений монохориальной двойни, переход одного синдрома в другой и высокую вероятность антенатальной гибели обоих плодов даже при самом строгом стандартизированном наблюдении за такой беременностью и готовности оказать помощь.
Литература
- Martin J.A., Hamilton B.E., Sutton P.D. et al. Births: final data for 2006. Natl Vital Stat Rep. 2009; 57: 1–102.
- Lewi L., Deprest J., Hecher K. The vascular anastomoses in monochorionic twin pregnancies and their clinical consequences. Am J Obstet Gynecol. 2013; 208 (1): 19–30.
- Lewi L., Guccardo L., Van Mieghem T. et al. Monochorionic diamniotic twin pregnancies, natural history and risk stratification. Fetal Diagn Ther. 2010; 27: 121–133.
- Huber A., Diehl W., Zikulnig L. et al. Perinatal outcome in monochorionic twin pregnancies complicated by amniotic fluid discordance without severe twin – twin transfusion syndrome. Ultrasound Obstet Gynecol. 2006; 27: 48–52.
- Van Mieghem T., Eixarch E., Gucciardo L. et al. Outcome prediction in monochorionic diamniotic twin pregnancies with moderately discordant amniotic fluid. Ultrasound Obstet Gynecol. 2011; 37: 15–21.
- Tollenaar L., Slaghekke F., Middeldorp J. et al. Twin anemia polycythemia sequence: current views on pathogenesis, diagnostic criteria, perinatal management, and outcome. Twin Res Hum Genet. 2016; 19 (3): 222–233.
- Михайлов А.В., Романовский А.Н., Шлыкова А.В., Кузнецов А.А. Специфические осложнения монохориального многоплодия – фетофетальный трансфузионный синдром и синдром анемии-полицитемии. Акушерство и гинекология Санкт-Петербурга. 2017; 2: 18–23.
- Gratacos E., Lewi L., Munoz B. et al. A classification system for selective intrauterine growth restriction in monochorionic pregnancies according to umbilical artery Doppler flow in the smaller twin. Ultrasound Obstet Gynecol. 2007; 30: 28–34.

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Источник