Анемия после резекции тонкой кишки
После частичного (резекция) и полного (гастрэктомия) удаления желудка у многих онкологических пациентов развивается анемия — состояние, при котором в крови снижается содержание эритроцитов и гемоглобина, органы и ткани перестают получать нужное количество кислорода. После операций по удалению желудка это происходит из-за нарушения усвоения трех веществ, необходимых для кроветворения: железа, витамина B12 (цианкобаламина) и фолиевой кислоты (иногда ее называют витамином B9).
По некоторым данным, анемия возникает у 50% пациентов, перенесших гастрэктомию. Симптомы зависят от того, насколько сильно снижен уровень эритроцитов и гемоглобина. Такие пациенты испытывают постоянную слабость, упадок сил, плохо переносят физические нагрузки, становятся бледными, у них снижается концентрация внимания. В более серьезных случаях даже при небольших физических нагрузках возникает одышка, учащенное сердцебиение, беспокоят головные боли, шум в ушах, нарушается сон, аппетит. Тяжелая анемия грозит развитием сердечной недостаточности.
Железодефицитная анемия
Железо — важный компонент гемоглобина, белка, который находится в эритроцитах и переносит кислород.
Главная причина железодефицитной анемии после удаления желудка — нарушение пищеварения:
- Железо во многих продуктах (в основном растительного происхождения) содержится в трудноусвояемой негемовой форме (Fe3+). В кислой среде желудка оно превращается в легкоусвояемую гемовую форму (Fe2+) и затем всасывается в двенадцатиперстной кишке и верхней части тощей кишки. После удаления желудка нарушается превращение негемового железа в гемовое и его всасывание.
- После некоторых операций, например, реконструкции желудка по Ру, двенадцатиперстная кишка выключается из работы, и в ней не происходит всасывания железа.
Риск зависит от объема и вида хирургического вмешательства: после гастрэктомии он выше, чем после субтотальной резекции (удаления большей части органа). Нарушение всасывания железа может усугубляться такими факторами, как снижение аппетита, недостаточное питание, кровопотеря в области швов на желудке и кишечнике, побочные эффекты химиопрепаратов.
Обычно поначалу дефицит железа протекает латентно — без выраженных симптомов. Через 1–3 года появляются ярко выраженные проявления железодефицитной анемии.
Как выявить железодефицитную анемию после удаления желудка? Нужно провести анализ крови. Определяют такие показатели, как уровень гемоглобина, ферритина, трансферина, сывороточного железа, процент насыщения трансферина, латентная железосвязывающая способность сыворотки, количество эритроцитов, гематокрит (соотношение объемов клеток и плазмы крови), MCH (среднее содержание гемоглобина в одном эритроците), MCV (средний объем эритроцита).
Как повысить содержание гемоглобина и эритроцитов в крови? В тяжелых случаях (уровень гемоглобина менее 70 г/л) может быть показано переливание эритроцитарной массы. Для профилактики и коррекции железодефицитной анемии врач может назначить пероральные (для приема путем проглатывания) препараты железа: сульфат, глюконат. Если пациент не может принимать железо в пероральных формах из-за побочных реакций, или если оно не всасывается в кишечнике, назначают внутривенные инъекции. Среди продуктов питания легкоусвояемым гемовым железом богаты мясо, птица, рыба, морепродукты. Витамин C улучшает усвоение железа.
Дефицит витамина B12
Витамин B12 (цианкобаламин) необходим для созревания красных кровяных клеток — эритроцитов. Он не синтезируется в организме человека и должен постоянно поступать с пищей.
Витамин B12 всасывается в нижнем отделе тонкой кишки. Но для того чтобы перейти в усвояемую форму, прежде он должен связаться с белком под названием внутренний фактор Касла, который вырабатывается клетками слизистой оболочки дна и тела желудка. После гастрэктомии фактор Касла перестает вырабатываться, и усвоение витамина B12 нарушается. Развивается пернициозная анемия.
Возможные проявления дефицита витамина B12: похудение, потеря вкуса, тошнота, диарея или запоры, жжение, увеличение языка, ярко-красный цвет языка, «лакированный язык», небольшая желтушность кожи, витилиго (обесцвеченные пятна на коже), раннее поседение волос.
Кроме того, дефицит витамина может приводить к гибели нервных клеток и неврологическим расстройствам: онемение, покалывание в руках и ногах, нарушение согласованности работы разных групп мышц.
Симптомы дефицита витамина B12 могут появиться уже через год после операции. Они возникают не сразу, потому что в печени хранится довольно большой запас витамина.
Как выявить B12-дефицитную анемию? В анализе крови обнаруживают увеличенный MCV (средний объем эритроцитов), нормальный MCH (среднее содержание гемоглобина в одном эритроците), анизоцитоз (изменение размеров эритроцитов), пойкилоцитоз (изменение формы эритроцитов), уменьшение количества ретикулоцитов (молодых форм эритроцитов), обнаруживают мегалоциты (большие клетки овальной формы), лейкопению (уменьшение количества лейкоцитов). В биохимическом анализе крови можно обнаружить сниженное содержание витамина B12, но это не очень надежное исследование.
Как обеспечить организм витамином B12? Классически после удаления желудка пациентам рекомендуется вводить витамин B12 в виде внутримышечных инъекций. Однако, исследования показывают, что пероральный (путем проглатывания) прием препаратов B12 тоже помогает, потому что в этом случае начинает работать другой путь усвоения, не зависящий от внутреннего фактора Касла. Также могут применяться подкожные инъекции. Витамином B12 богаты такие продукты, как молоко, красное мясо, рыба, ракообразные, говяжья печень.
Дефицит фолиевой кислоты
Фолиевая кислота также важна для нормального кроветворения, и она работает в связке с витамином B12, так как активируется им. Для того чтобы обнаружить дефицит этого соединения, нужно определить уровень фолиевой кислоты в эритроцитах (RBC).
Для профилактики и борьбы с дефицитом фолиевой кислоты применяют соответствующие препараты. Она также содержится в таких продуктах, как цитрусовые, свекла, брокколи, листовые овощи, бобовые, спаржа, яйца.
Список литературы:
- https://www.ncbi.nlm.nih.gov/
- https://my.clevelandclinic.org/
- https://www.nostomachforcancer.org/
- https://www.nostomachforcancer.org/
- https://postnauka.ru/faq/69736
- https://cyberleninka.ru/
- https://cyberleninka.ru/
- https://www.invitro.ru/
- https://www.gemotest.ru/
- https://t-pacient.ru/articles/387/
- https://empendium.com/
- https://www.rlsnet.ru/
- https://www.rlsnet.ru/
- https://www.rlsnet.ru/
- https://empendium.com/
Источник
Специалистам / Практика / Практика (статья)
Статья |
17-09-2014, 22:10
|
 АнемияВ практике гастроэнтеролога анемический синдром встречается достаточно часто. При этом основными видами анемий у пациентов с патологией органов пищеварения являются железодефицитная и В12-фолиеводефицитная анемии. В патогенезе анемий при заболеваниях желудочно-кишечного тракта ведущими механизмами выступают хроническая кровопотеря и нарушение всасывания гемопоэтических факторов.
АнемияВ практике гастроэнтеролога анемический синдром встречается достаточно часто. При этом основными видами анемий у пациентов с патологией органов пищеварения являются железодефицитная и В12-фолиеводефицитная анемии. В патогенезе анемий при заболеваниях желудочно-кишечного тракта ведущими механизмами выступают хроническая кровопотеря и нарушение всасывания гемопоэтических факторов.
Железодефицитная анемия – наиболее частая форма анемий в гастроэнтерологии, и причиной ее развития являются кровотечения, нарушения всасывания железа, диетические ограничения. Ряд хронических заболеваний пищеварительной системы сопровождается развитием анемии различной степени тяжести. Анемия может являться первым признаком основного заболевания, в частности, опухолевого процесса пищевого канала, а также быть причиной снижения качества жизни пациентов.
Выделяют три глобальные причины развития дефицита железа в организме:
- Недостаточное поступление с пищей или повышенная потребность.
- Нарушение всасывания железа в кишечнике.
- Хронические потери крови.
Заболевания желудочно-кишечного тракта являются одной из основных причин развития железодефицитной анемии, что обусловлено нарушением всасывания железа в кишечнике или его потерями вследствие эрозивно-язвенных, опухолевых или аутоиммунных воспалительных поражений слизистой оболочки кишечника.
Перечень заболеваний пищеварительного тракта, сопровождающихся развитием анемии, достаточно широк. Причиной железодефицитных состояний часто выступают болезни верхних отделов желудочно-кишечного тракта и толстой кишки.
Одной из важных причин развития железодефицитной анемии является нарушение процессов всасывания железа в двенадцатиперстной кишке и проксимальном отделе тощей кишки. Различные заболевания тонкой кишки, сопровождающиеся синдромом мальабсорбции (энтерит, амилоидоз, целиакея, идеопатическая стеаторея), а также оперативные вмешательства на желудке и тонкой кишке (состояние после тотальной гастроэктомии, субтотальной резекции желудка, ваготомии с гастроэктомией, резекция тонкой кишки) приводят к развитию дефицита железа.
Накапливаются данные о потенциальной связи инфекции H. pylory с железодефицитной анемией, которая может быть следствием скрытых кровотечений при эрозивном гастрите и язвенной болезни, нарушение всасывания железа при хеликобактерном атрофическом пангастрите, а также снижения содержания аскорбиновой кислоты в желудке и конкурентного захвата и утилизации железа самой бактерией. Таким образом, эрадикация H. pylory может стать еще одним подходом к лечению железодефицитной анемии в отсутствии других явных ее причин.
Этиологическим фактором анемии может стать прием нестероидных противовоспалительных препаратов (НПВП). Врачам хорошо известна возможность как массивных, так и скрытых кровотечений из эрозий и язв желудка и двенадцатиперстной кишки при НПВП-гастропатии. Однако, железодефицитная анемия может быть следствием НПВП-энтеропатии, другими клиническими проявлениями которой могут служить гипоальбуминемия, мальабсорбция и наличие измененной крови в кале.
Причиной нарушения всасывания гемопоэтических факторов являются и заболевания тонкой кишки. К ним можно отнести целиакию (половина пациентов с неясной этиологией железодефицитной анемии, резистентной к терапии препаратами железа), резекцию участка тонкой кишки, синдром избыточного бактериального роста в тонкой кишке, диабетическую энетропатию, амилоидоз, склеродермию, болезнь Уиппла, туберкулез, лимфому тонкой кишки, тропическое спру, паразитарные заболевания (лямблиоз) и гельминтозы (дифиллоботриоз).
Воспалительные заболевания кишечника, прежде всего, неспецифический язвенный колит и болезнь Крона, часто сопровождаются развитием анемии. Ведущими механизмами при этом выступают кровопотеря у пациентов с язвенным колитом и болезнью Крона, а также мальабсорбция при вовлечении в процесс тощей и подвздошной кишки при болезни Крона.
Ведущей причиной анемии при патологии нижних отделов желудочно-кишечного тракта, особенно у пациентов старше 50 лет, служит колоректальный рак. Хроническая кровопотеря наблюдается при полипах толстой кишки, дивертикулезе, ишемическом колите, геморрое и анальных трещинах.
Анемический синдром часто делает необходимым тщательное обследование желудочно-кишечного тракта. Для уточнения вида анемии проводят исследования общего и биохимического анализа крови.
Среди причин железодефицитной анемии (почти 30-50% всех случаев) прежде всего рассматривают острые или хронические кровопотери из желудочно-кишечного тракта.
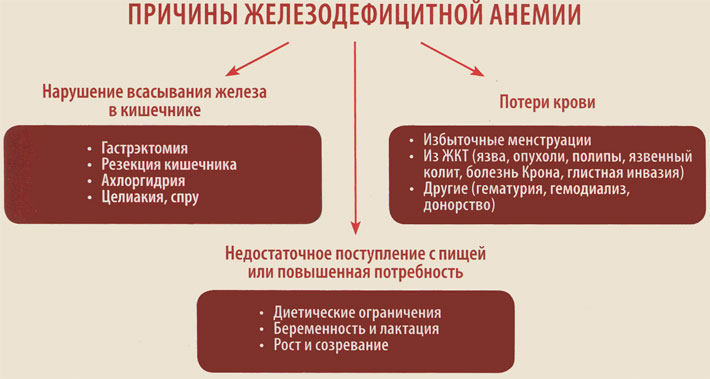
Причины железодефицитной анемии
Как показали результаты открытого мультицентрового исследования, проведенного в Украине в 2008 году и базировавшиеся на анализе 1299 историй болезней больных железодефицитной анемией, основной причиной развития были эрозивно-язвенные поражения пищевого канала (44,58%) и заболевания, сопровождающиеся синдромом мальабсорбции. Циррозы печени являлись причиной железодефицитной анемии в 10,39% случаев, воспалительные заболевания кишечника – 4,54% больных.
Диагностируется железодефицитная анемия у больных с гастроэнтерологическими заболеваниями по совокупности анамнестических данных (указания на оперативные вмешательства на желудке или кишечнике, прием нестероидных или гормональных противовоспалительных препаратов, антикоагулянтов и антиагрегантов, язвенный анамнез, наличие хронических заболеваний печени и воспалительных заболеваний кишечника и т.д.), клинических проявлений (наличие специфического сидеропенического синдрома, проявляющегося сухостью и истончением кожи, ангулярный хейлит, дисфагия, ломкость ногтей, их поперечная исчерченность, вогнутость ногтевой пластинки, извращение вкуса и обоняния, симптом «голубых склер», мышечная слабость) и лабораторных показателей.
Диагностика анемии основывается, главным образом, на данных лабораторных исследований, в первую очередь – на результатах клинического исследования крови с определением концентрации гемоглобина.
Верхние отделы желудочно-кишечного тракта | Нижние отделы желудочно-кишечного такта | Весь желудочно-кишечный тракт |
– Язва желудка | – Аденома толстой кишки | – Болезнь Крона |
Согласно рекомендациям ВОЗ, критерием анемии является снижение концентрации гемоглобина до уровня 120 г/л для женщин (во время беременности – менее 110 г/л), для мужчин – менее 130 г/л. По степени тяжести различают анемию легкую (уровень гемоглобина крови 90-110 г/л), средней тяжести (гемоглобин – 70-89 г/л) и тяжелую (гемоглобин менее 70 г/л).
В лабораторной диагностике железодефицитной анемии основное практическое значение имеют три показателя: сывороточные концентрации железа, ферритина и общая железосвязывающая способность сыворотки (ОЖСС). ОЖСС – это общее количество железа, которое может связаться с трансферином. В норме сывороточная концентрация железа составляет 12-30 мкМоль/л (50-150мкг%), а ОЖСС – 30-85 мкМоль/л (300-360 мкг%).
Важное значение в лечении железодефицитной анемии имеет место устранение причин ее развития (оперативное лечение опухоли желудка, кишечника, лечение энтерита, коррекция алиментарной недостаточности и др.), а также возмещение дефицита железа в крови и тканях и достижение полной клинико-гематологической ремиссии. В ряде случаев радикальное устранение причины железодефицитной анемии невозможно, и тогда основное значение приобретает патогенетическая терапия железосодержащими лекарственными препаратами.
В качестве заместительной терапии при железодефицитной анемии используют препараты железа.
Терапия железодефицитной анемии при заболеваниях желудочно-кишечного тракта проводится преимущественно препаратами железа для перорального приема, за исключением случаев тяжелой мальабсорбции и состояний после резекции тонкой кишки.
Рекомендуемая ВОЗ оптимальная доза составляет 120 мг элементарного железа в сутки. Более высокие дозы не увеличивают эффективность, однако могут вызвать диспепсические явления вследствие раздражения желудочно-кишечного тракта. Лечение препаратами железа должно быть длительным.
Суточная доза для профилактики анемии и лечения легкой формы заболевания составляет 50-60 мг Fe2+, а для лечения выраженной анемии – 100-120 мг Fe2+.
При выборе препаратов железа необходимо учитывать и их состав.
В настоящее время существуют препараты двухвалентного и трехвалентного железа. По мнению специалистов, наибольшей биодоступностью обладает двухвалентная форма железа, именно поэтому старт терапии начинают с препаратов этой группы. Согласно проведенным клиническим исследованиям, терапия препаратами двухвалентного железа позволяет за более короткий временной интервал нормализовать показатели красной крови.
Таким образом, анемический синдром достаточно часто является «маской» многих распространенных и тяжелых заболеваний желудочно-кишечного тракта. Ключевыми моментами диагностики являются определение вида и причины развития анемии, а залогом успешного лечения служат своевременная терапия основного заболевания и правильная патогенетическая терапия с восполнением дефицита железа.
Источник
Обширные резекции тонкой кишки. Энтеральная недостаточность
Многочисленными исследованиями, проведенными в условиях эксперимента на животных, а также у человека было показано, что в результате резекции тонкой кишки в оставшихся отделах кишечника происходят процессы адаптации, которые осуществляются как на уровне структурных изменений, так и с участием функции тонкой кишки.
К структурным изменениям относятся: увеличение диаметра кишки, высота ворсинок, глубина крипт, клеточная пролиферация, ускорение ритма обновления кишечного эпителия.
Функциональная адаптация сводится к повышению транспорта воды, электролитов и различных нутриентов тонкой кишки, повышению активности интестинальных энзимов на единицу поверхности тонкой кишки, другими сдвигами в метаболических процессах в этом органе. При умеренных объемах резекции эти адаптивные изменения компенсируют убыль всасывающей поверхности.
При массивной резекции компенсаторные механизмы оказываются недостаточными. Возникновение энтеральной недостаточности зависит от следующих факторов:
– протяженности и локализации резекции;
– сохранения илеоцекальной заслонки;
– степени адаптивных изменений оставшейся тонкой кишки;
– состояния печени и поджелудочной железы.
Массивная резекция тонкой кишки вызывает энтеральную недостаточность в связи со значительной убылью всасывающей поверхности кишки. Определенную роль играет также снижение стимуляции функций поджелудочной железы секретином и панкреозимином/холецистокинином, синтез которых в кишечнике благодаря резекции значительно снижается.

При резекции дистальных отделов подвздошной кишки с удалением илеоцекального сфинктера кишечная флора легко проникает из толстой кишки в тонкую, развивается кишечный дисбактериоз. У больных, перенесших резекцию подвздошной кишки, наблюдается повышение фекальной экскреции желчных кислот, снижается их общий пул, что свидетельствует о нарушении кишечно-печеночной циркуляции желчных кислот, малабсорбции холатов, возрастает их деконъюгация в кишечнике. Нарушения всасывания желчных кислот отмечаются и у илеостомированных больных. Деконъюгация желчных кислот происходит с участием кишечных бактерий, в связи с чем дисбактериоз служит одним из ведущих факторов, вызывающих нарушения метаболизма холатов.
Развитию энтеральной недостаточности после резекции тонкой кишки способствует ускорение транзита содержимого по сохранившимся отделам кишки. Наиболее это выражено после резекции подвздошной кишки. Так, после удаления 1,8—2,4 метров терминальной части этого отдела кишечника барий достигает толстой кишки примерно в два раза скорее, чем в норме (Booth).
После массивной резекции тонкой кишки развивается ферментативная недостаточность за счет изменения активности и количества энтеральных пищеварительных энзимов.
Первый ее тип (проксимальный резекционный синдром) может развиться после резекции проксимального отдела кишки (Беюл и др.). В то же время чаще всего при удалении не более 50% тощей кишки выраженных клинических проявлений малабсорбции не возникает.
Некоторые авторы полагают, что при данном объеме резекции нарушения всасывания жиров, стеаторея в большей мере обусловлены выпадением функции мицеллообразования в связи с расстройствами метаболизма желчных кислот, чем выключением всасывающей и ферментпродуцирующей поверхности кишки (Wester и соавт.). Деконъюгированные жирные кислоты, попадая в толстую кишку, стимулируют процессы кишечной секреции. Стеаторея вызывает потерю организмом ионов кальция, экскреция которого взаимосвязана с обменом жиров. Нарушения транспорта кальция влияют и на дефицит витамина D. Наряду с ионами кальция теряются ионы магния и цинка, которые также образуют мыла с невсосавшимися жирами. У больных с резекцией подвздошной кишки нередко наблюдается и оксалатурия, создающая условия для образования оксалатных камней.
При состояниях после резекции тонкой кишки, наряду с нарушениями функций гепатобилиарной системы и поджелудочной железы, отмечается желудочная гиперсекреция. Продукция гастрина повышена (Williams и соавт.). Вопрос о состоянии процессов всасывания углеводов после обширных резекций тонкой кишки до настоящего момента не решен, данные противоречивы.
Клинически резецированная тонкая кишка, как правило, проявляется поносами. Может наблюдаться типичная «желчная диарея», стул 6—8 раз в сутки, водянистый, пенистый, со значительным содержанием натрия и других электролитов.
При резекции проксимальных отделов тонкой кишки стул реже, может быть более обильным, глинистым («жирная диарея»).
У больных, перенесших массивную резекцию, наблюдаются различные обменные нарушения, вызванные дефицитом тех или других нутриентов.
Для резекции терминальных отделов подвздошной кишки характерна В12-дефицитная анемия нетяжелой степени, которая легко корригируется назначением витамина В12.
Характерна кишечная транслокация микрофлоры. Состав микрофлоры дистального отдела подвздошной кишки существенно отличается от обычно выше локализующихся биотипов. При этом возрастает как общее число бактерий, так и их распределение (внутрипросветная микрофлора превалирует над пристеночной), причем важной экологической особенностью является приблизительно равное количество аэробных и анаэробных бактерий.
– Также рекомендуем “Обширные резекции толстой кишки. Последствия”
Оглавление темы “Питание после операции на желудке, кишечнике”:
- Питание после гастрэктомии. Поддержка при постгастррезекционной дистрофии
- Оценка пациентов с постгастррезекционной дистрофией. Классификация трофологической недостаточнoсти
- Питание при постгастррезекционной дистрофии. Смеси Нутрихим
- Факторы риска синдрома короткой кишки. Причины
- Обширные резекции тонкой кишки. Энтеральная недостаточность
- Обширные резекции толстой кишки. Последствия
- Лечение синдрома короткой кишки. Принципы
- Печень пожилых при хирургическом эндотоксикозе. Функции
- Послеоперационная печеночная недостаточность у пожилых. Факторы риска
- Классификация печеночной недостаточности. Стадии
Источник
