Анемия постгеморрагическая принципы лечения
Постгеморрагическая анемия – комплекс клинических и гематологических изменений, возникающий вследствие острой или хронической кровопотери. Постгеморрагическая анемия характеризуется бледностью, одышкой, потемнением в глазах, головокружением, гипотермией, артериальной гипотонией; в тяжелых случаях – заторможенностью, нитевидным пульсом, шоком, потерей сознания. Постгеморрагическую анемию диагностируют по данным клинической картины и общего анализа крови; для установления источника кровотечения проводятся инструментальные исследования. При развитии данного состояния необходимо устранение источника кровопотери, проведение трансфузионной и симптоматической терапии.
Общие сведения
Постгеморрагическая анемия – гипогемоглобинемия, развивающаяся вследствие геморрагического синдрома и сопровождающаяся ощутимым снижением объема циркулирующей крови (ОЦК). Постгеморрагическая анемия протекает с эритропенией, но часто без уменьшения концентрации гемоглобина (Hb). В норме уровень общего Hb и объем циркулирующих эритроцитов крови составляет соответственно: у мужчин – не ниже 130 г/л и 29-30 мл/кг веса, у женщин – не ниже 120 г/л и 22-23 мл/кг. Постгеморрагическая анемия может осложнять течение самых различных патологический состояний в хирургии, гематологии, гинекологии, гастроэнтерологии, кардиологии и др. Постгеморрагическая анемия может носить острый или хронический характер. Хроническая форма является вариантом железодефицитной анемии, так как механизм развития и симптомы патологии обусловлены усиливающимся дефицитом железа.
Постгеморрагическая анемия
Причины постгеморрагической анемии
Непосредственной причиной постгеморрагической анемии выступает острая или хроническая потеря крови, возникшая вследствие наружного или внутреннего кровотечения. Острая постгеморрагическая анемия возникает при быстрых, массивных кровопотерях, вызванных обычно механическим повреждением стенок крупных кровеносных сосудов или полостей сердца при различных травмах и хирургических операциях, разрывом стенок сердечных камер в зоне инфаркта, разрывом аневризмы аорты и ветвей легочной артерии, разрывом селезенки, разрывом фаллопиевой трубы при внематочной беременности.
Острая постгеморрагическая анемия характерна для обильных маточных кровотечений (менорагий, метрорагий), может сопровождать течение язвы желудка и 12-перстной кишки. У новорожденных постгеморрагическая анемия может быть вызвана плацентарным кровотечением, родовой травмой.
Хроническая постгеморрагическая анемия обусловлена продолжительными, часто возникающими потерями небольших объемов крови при желудочно-кишечных, геморроидальных, почечных, носовых кровотечениях, нарушениях механизмов свертывания крови (ДВС-синдроме, гемофилии). Опухолевые процессы (рак желудка, рак толстой кишки), протекающие с разрушением тканей и органов, проводят к развитию внутреннего кровотечения и постгеморрагической анемии. Гипогемоглобинемия может быть связана с повышением проницаемости стенок капилляров при лейкозах, лучевой болезни, инфекционно-септических процессах, недостаточности витамина C.
Патогенез постгеморрагической анемии
Основными факторами развития постгеморрагической анемии выступают явления сосудистой недостаточности, гиповолемия с уменьшением общего объема плазмы и циркулирующих форменных элементов, в частности, эритроцитов, осуществляющих транспорт кислорода. Этот процесс сопровождается снижением артериального давления, кровенаполнения внутренних органов и тканей, гипоксемией, гипоксией и ишемией, развитием шока.
Степень выраженности защитно-приспособительных реакций организма определяется объемом, скоростью и источником кровотечения. В раннюю рефлекторно-сосудистую фазу компенсации кровопотери (первые сутки) благодаря возбуждению симпатико-адреналовой системы наблюдается вазоконстрикция и усиление сопротивления периферических сосудов, стабилизация гемодинамики за счет централизации кровообращения с первоочередным кровоснабжением головного мозга и сердца, уменьшение возврата крови к сердцу и сердечного выброса. Концентрация эритроцитов, Hb и гематокрит пока близки к норме («скрытая» анемия).
Вторая гидремическая фаза компенсации (2-3 сутки) сопровождается аутогемодилюцией – поступлением в кровеносное русло тканевой жидкости и восполнением объема плазмы. Усиление секреции катехоламинов и альдостерона надпочечниками, вазопрессина – гипоталамусом способствует стабильности уровня электролитов в плазме крови. Происходит прогрессирующее снижение показателей эритроцитов и Hb (общего и в единице объема), гематокрита; значение цветового показателя в норме (постгеморрагическая нормохромная анемия).
В третью, костномозговую фазу компенсации (4-5 сутки) из-за недостатка железа анемия становится гипохромной, усиливается образование эритропоэтина почками с активацией ретикулоэндотелиальной системы, эритропоэза костного мозга, очагов экстрамедуллярного кроветворения. В красном костном мозге наблюдается гиперплазия эритроидного ростка и увеличение общего числа нормоцитов, в периферической крови – значительное повышение количества молодых форм эритроцитов (ретикулоцитов) и лейкоцитов. Уровни Hb, эритроцитов и гематокрит понижены. Нормализация уровня эритроцитов и Hb при отсутствии дальнейшей кровопотери происходит через 2-3 недели. При массивной или длительной кровопотере постгеморрагическая анемия приобретает гипорегенеративный характер, при истощении адаптационных систем организма развивается шок.
Симптомы постгеморрагической анемии
Клинические признаки постгеморрагической анемии однотипны вне зависимости от причины кровопотери, определяются ее объемом и длительностью.
В первые сутки после острой кровопотери у пациентов отмечается резкая слабость, бледный оттенок кожи и слизистых, одышка, потемнение и мелькание мушек в глазах, головокружение, шум в ушах, пересыхание во рту, снижение температуры тела (особенно, конечностей), холодный пот. Пульс становится частым и слабым, появляется артериальная гипотония. Следствием геморрагического синдрома является малокровие внутренних органов, жировая дистрофия миокарда, печени, ЦНС и других органов. Дети, особенно новорожденные и 1-го года жизни, кровопотерю переносят намного тяжелее, чем взрослые пациенты.
Постгеморрагическая анемия при массивной и быстрой кровопотере сопровождается геморрагическим коллапсом, резким падением артериального давления, нитевидным аритмичным пульсом, адинамией и заторможенностью, учащенным поверхностным дыханием с возможным развитием рвоты, судорог, потерей сознания. Если давление падает до критического уровня, вызывая острое нарушение кровоснабжения и гипоксию органов и систем, смерть наступает от паралича дыхательного центра и остановки сердца.
Медленно развивающаяся постгеморрагическая анемия характеризуется менее выраженными проявлениями, так как успевает частично компенсироваться за счет адаптационных механизмов.

Постгеморрагическая анемия
Диагностика постгеморрагической анемии
Диагностика постгеморрагической анемии проводится по данным клинической картины, лабораторных и инструментальных исследований (общего и биохимического анализов крови и мочи, ЭКГ, УЗ-диагностики, пункции костного мозга, трепанобиопсии). При осмотре пациента с острой постгеморрагической анемией обращает внимание гипотония, частое дыхание, слабый аритмичный пульс, тахикардия, приглушенность сердечных тонов, небольшой систолический шум на верхушке сердца.
В крови – абсолютное снижение эритроцитарной массы; при продолжающейся кровопотере наблюдается прогрессирующее равномерное падение содержания Hb и эритроцитов. При умеренной кровопотере гематологические признаки постгеморрагической анемии обнаруживается только на 2-4 сутки. Обязателен контроль диуреза, уровня тромбоцитов, электролитов и азотистых продуктов в крови, АД и ОЦК.
При острой постгеморрагической анемии нет необходимости в исследовании костного мозга, его проводят при трудно диагностируемых кровопотерях. В образцах костномозговой пункции признаками анемии являются повышение активности красного костного мозга, в препаратах трепанобиопсии – замещение жировой ткани костного мозга красным кроветворным мозгом.
При диагностике внутренних кровотечений показателен синдром острого малокровия и лабораторные данные. В селезенке, печени, лимфоузлах выявляются очаги экстрамедуллярного кроветворения, указывающие на повышенную нагрузку на гемопоэтическую систему; в крови – транзиторное понижение уровня железа, небольшое увеличение АлТ.
Для выявления и устранения источника кровопотери больные нуждаются в консультациях гематолога, хирурга, гинеколога, гастроэнтеролога и других специалистов; проведении УЗИ органов брюшной полости и малого таза, ФГДС и пр. ЭКГ при постгеморрагической анемии может демонстрировать снижение амплитуды Т-зубца в стандартном и грудном отведении.
Лечение и прогноз постгеморрагической анемии
Первостепенным в лечении постгеморрагической анемии является установление источника кровотечения и его немедленная ликвидация за счет перевязки и ушивания сосудов, резекции и ушивания поврежденных органов и тканей, повышения свертываемости крови и т. д.
Для восстановления ОЦК и снижения степени гемодинамических нарушений по наблюдением трансфузиолога проводится неотложное переливание консервированной крови, кровезаменителей, плазмы и плазмозаменителей. При незначительном, но продолжительном кровотечении трансфузия цельной крови или плазмы показана в небольших гемостатических дозах. При значительной потере ОЦК трансфузии должны выполняться в дозах, превышающих кровопотерю на 20-30%. Тяжелая постгеморрагическая анемия лечится переливаниями больших доз крови («трансплантация крови»). В период коллапса гемотрансфузии дополняют гипертоническими кровозамещающими растворами.
После восстановления ОЦК проводится коррекция качественного состава крови – восполнение ее компонентов: эритроцитов, лейкоцитов, тромбоцитов. При большой одномоментной кровопотере и остановившемся кровотечении необходимы массивные дозы эритроцитарной массы (> 500 мл). Об эффективности гемотрансфузий судят по повышению АД, гематологическим сдвигам.
Также необходимо введение белковых и электролитных растворов (альбумина, физ. раствора, глюкозы), восстанавливающих водно-солевой баланс. В лечении постгеморрагической анемии используются препараты железа, витамины группы B. Назначается симптоматическая терапия, направленная на нормализацию функциональных нарушений со стороны сердечно-сосудистой и дыхательной систем, печени, почек и др.
Прогноз постгеморрагической анемии зависит от длительности и объема кровотечения. Резкая потеря 1/4 ОЦК приводит к острой анемии и состоянию гиповолемического шока, а потеря 1/2 ОЦК является несовместимой с жизнью. Постгеморрагическая анемия при медленной потере даже значительных объемов крови не столь опасна, поскольку может компенсироваться.
Острая постгеморрагическая анемия – клиника, диагностика, лечение
Острая постгеморрагическая анемия развивается после резкой и разовой потери крови за счет внешнего или внутреннего кровоизлияния.
При небольших, повторяющихся в течение длительного периода времени геморрагиях, развивающаяся анемия представляется как результат деплеции тканевого железа.
В большинстве случаев место кровоизлияния нетрудно установить. Частные, связанные с этим проблемы возникают при внутреннем кровоизлиянии. В таких случаях следует не забывать, что наиболее частые острые геморрагии отмечаются у мужчин в желудочно-кишечном тракте, в то время как у женщин — в половых органах.
Большое практическое значение представляет также уточнение причины явления — местного ли она характера или составляет проявление кровоточивости.
Клинические признаки острой постгеморрагической анемии
Обнаруживаемые у больного признаки зависят от величины и скорости кровотечения, его локализации, общего состояния больного (состояния сердечно-сосудистой системы, наличия сопутствующих заболеваний и пр.), прошедшего от кровоизлияния времени.
Исходные клинические проявления относятся за счет быстрого развития гиповолемии. Их интенсивность пропорциональна объему потерянной крови. На следующем за восстановлением объема сосудистой крови этапе развиваются собственно признаки анемии.
Количество потерянной крови не получает точной оценки по цифровым показателям гемоглобина или гематокрита, в связи с компенсаторными колебаниями общего объема сосудистой крови. Клиницисту предстоит решить эту проблему по интенсивности функциональных признаков.
Толкование признаков, связанных с наличием гиповолемии необходимо связать с сопутствующими патологическими условиями и возрастом больного.
После восстановления объема сосудистой крови (самопроизвольно или в результате проведения терапевтических мероприятий) на первый план выступают признаки, связанные с деплецией, находящихся в сосудистой крови эритроцитов. К таковым относятся бледность, общая слабость, одышка при физической нагрузке, сердцебиение, головокружения, анемические шумы.
Выраженность этих признаков зависит от степени анемии, состояния работы сердечно-сосудистой системы и приспособления организма больного к созданным недостатком кислорода условиям.
Признаки, связанные с быстрым сокращением объема сосудистой крови у молодого здорового
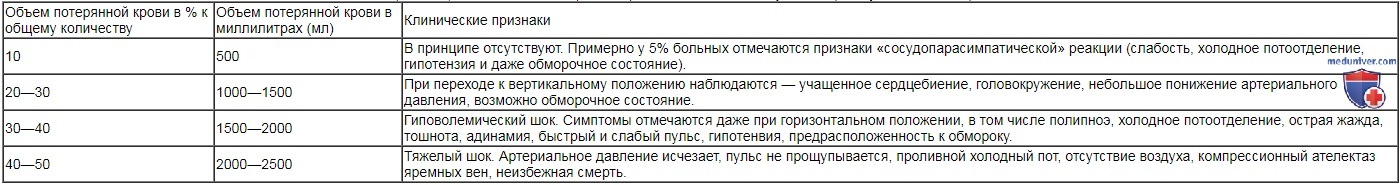
| Объем потерянной крови в % к общему количеству | Объем потерянной крови в миллилитрах (мл) | Клинические признаки |
| 10 | 500 | В принципе отсутствуют. Примерно у 5% больных отмечаются признаки «сосудопарасимпатической» реакции (слабость, холодное потоотделение, гипотензия и даже обморочное состояние). |
| 20—30 | 1000—1500 | При переходе к вертикальному положению наблюдаются — учащенное сердцебиение, головокружение, небольшое понижение артериального давления, возможно обморочное состояние. |
| 30—40 | 1500—2000 | Гиповолемический шок. Симптомы отмечаются даже при горизонтальном положении, в том числе полипноэ, холодное потоотделение, острая жажда, тошнота, адинамия, быстрый и слабый пульс, гипотенвия, предрасположенность к обмороку. |
| 40—50 | 2000—2500 | Тяжелый шок. Артериальное давление исчезает, пульс не прощупывается, проливной холодный пот, отсутствие воздуха, компрессионный ателектаз яремных вен, неизбежная смерть. |

Лабораторные признаки острой постгеморрагической анемии
Тромбоцитоз (значения которого достигают 1 млн/мм3) развивается в течение первого часа от начала геморрагии (Hillman). Спустя 2—6 часов отмечается лейкоцитоз (10—30 тыс. на мм3) за счет мобилизации запасов зрелых гранулоцитов (Wintrobe и сотр.). Через 3—5 день после кровоизлияния развивается ретикулоцитоз, максимальные значения которого (10—15%) достигаются за 6—11 дней (Hillman). Гематокрит медленно понижается в ближайшие после прекращения геморрагии 2—3 дня.
У человека в норме, до кровоизлияния, красные кровяные клетки нормоцитные и нормохромные. После развития ретикулоцитоза наблюдается макроцитоз и полихроматофилия.
В формах, сопровождающихся острой анемией, выявляется наличие эритробластов. Обнаружение гипохромии наиболее часто свидетельствует о предшествующем геморрагическому явлению железодефиците. Формула белой крови отражает сдвиг влево.
В костном мозге определяется развитие гиперплазии эритробластов спустя 3—5 дней от геморрагии.
При внутриполостных кровоизлияниях развивается гипербилирубинемия за счет рассасывания разлитой крови. Кровоизлияние в кишечник может сопровождаться повышением показателя азотемии (Попеску,
Патофизиология острой постгеморрагической анемии
Резкое понижение объема сосудистой крови и давления в ней кислорода приводят в действие компенсационные механизмы. Потеря сосудистой крови до 20—30% возмещается, по началу, сужением глубоких и кожных вен, в дальнейшем — сердцебиением и перераспределением крови спланхнических зон в направлении сердечной мышцы и мозга. Когда же объем потерянной крови превышает 40%, отмечается провал артериального давления.
На весьма ранних сроках присоединяется компенсирующее разжижение крови за счет подвоза воды и белков из внесосудистого пространства. Тканевая недостаточность кислорода, в развитии которой участвуют все отмеченные факторы, способствует выделению сосудоактивных веществ и кислых метаболитов, ускоряющих развитие коллапса (Киотан и Кристя).
Линейному сокращению гематокрита соответствует логарифмический рост синтеза эритропоэтина (Адамсон). Эффекты влияния эритропоэтина следующие:
а) ускорение выделения кислорода из эритроцитов;
б) ранний диабез ретикулоцитов;
в) рост костномозгового эритропоэза.
Реакция костного мозга зависит от интенсивности анемии, структурной целостности костного мозга, запаса железа и катализаторов.
Течение острой постгеморрагической анемии
Нормальный костный мозг может восстановить объем красных кровяных клеток примерно за 33 дня (Wintrobe и сотр.). Спустя 10—14 дней от прекращения геморрагии признаки активного восстановления эритроцитов исчезают. Лейкоцитоз нормализуется за 3—4 дня. Дальнейшие наличие гипертромбоцитоза и/или ретикулоцптоза подсказывает мысль о продолжающемся кровоизлиянии. В одинаковой мере сохраняющийся лейкоцитоз свидетельствует о непрекратившейся геморрагии, в частности в той или иной полости организма, или о развитии инфекции.
Диагностирование острой постгеморрагической анемии
В принципе определение механизма развития геморрагии не ставит каких-либо проблем. Лишь появившуюся после внутриполостной геморрагии с дальнейшей желтухой и лихорадкой анемию можно принять за анемию, развившуюся за счет резкого расплавления крови. Вопрос решает определение места кровоизлияния.
Терапия острой постгеморрагической анемии
Проводимое лечение задается целью качественного и количественного восстановления сосудистой крови. В порядке их значения проводятся следующие мероприятия:
а) восстановление объема сосудистой крови;
б) пресечение кровотечения;
в) восстановление массы эритроцитов.
Вместе с тем подбор терапевтического подхода делается в соответствии с количеством потерянной крови, по приведенным ниже критериям. Количество жидкостей, необходимых восстановлению объема сосудистой крови, оценивается из расчета общего количества последней по следующим данным Кривда и Манолеску:
| У мужчин (к % веса тела) | У женщин (к % веса тела) | |
| С развитой мускулатурой… | 7,5% | 7,0% |
| В норме… | 7,0% | 6,5% |
| Худых… | 6,5% | 6,0% |
| Ожирелых… | 6,0% | 5,5% |
Для восстановления общего количества сосудистой крови применяются следующие средства: расствор декстрана, раствор белковой плазмы, кристаллоидный раствор, цельная кровь. Капельное вливание декстрана и крови составляет наиболее полезный способ восстановления массы сосудистой крови. Кровь показана лишь в случае потери более 20% кровяной массы. Назначение сосудопрессорных средств в принципе противопоказано.
Реакция на проводимое лечение оценивается по окраске и температуре покровов, наполнению вен (в основном яремных), исчезновению явлений аноксии, росту артериального давления.
В принципе, после преодоления исходного критического периода лечение анемии сводится к гигиено-диетическим мероприятиям. При нормальном костном мозге и адекватном количестве железа, восстановление всегда может быть самопроизвольным.
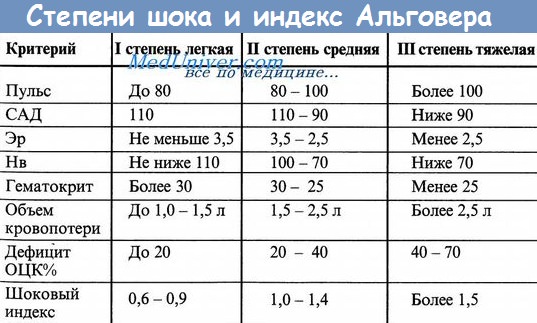
Учебное видео – шоковый индекс Альговера, степени кровопотери и анемии
– Также рекомендуем “Апластическая анемия (миелоидная аплазия) – история изучения, классификация”
Оглавление темы “Апластическая анемия”:
- Острая постгеморрагическая анемия – клиника, диагностика, лечение
- Апластическая анемия (миелоидная аплазия) – история изучения, классификация
- Причины апластической анемии – конституционная апластическая анемия Фанкони
- Химическая и лекарственная апластическая анемия – лекарства поражающие костный мозг
- Радиационная апластическая анемия – влияние ионизирующего облучения на организм
- Инфекционная апластическая анемия – инфекции поражающие костный мозг
- Механизмы развития апластической анемии – патогенез
- Клиника апластической анемии – признаки
- Лабораторная диагностика апластической анемии – анализы
- Течение апластической анемии – осложнения
