Анемия у беременных патогенез
Анемия при беременности — это уменьшение уровня гемоглобина, возникшее в период гестации и связанное с ней патогенетически. Проявляется слабостью, быстрой утомляемостью, головокружениями, извращением вкуса и обонятельных предпочтений, кардиальными болями, мышечной слабостью, парестезиями, поражением слизистых, изменением кожи, ногтей, волос. Диагностируется с помощью общеклинического анализа крови и лабораторного исследования метаболизма железа. Для лечения применяют железосодержащие препараты, фолиевую кислоту, цианокобаламин, по показаниям проводят комплексную противогипоксическую терапию.
Общие сведения
Существование физиологических предпосылок для возникновения гестационной анемии (гидремии) делает это заболевание одним из наиболее распространенных видов патологии при беременности. Манифестные формы болезни с клинически выраженной симптоматикой в экономически развитых государствах встречаются у 16-21% пациенток, в развивающихся странах их распространенность достигает 80%. При этом скрытый (латентный) дефицит железа с учетом полноценности рациона к концу беременности наблюдается у 50-100% женщин. Преобладающая форма анемии гестационного периода — железодефицитная, диагностируемая в 75-95% случаев. Актуальность своевременного выявления патологии связана с высокой вероятностью осложненного течения беременности и возникновения гипоксических состояний на фоне физиологического повышения потребности в кислороде на 15-33%.

Анемия при беременности
Причины анемии при беременности
Недостаточное содержание гемоглобина и эритроцитов в крови беременной женщины обусловлено как факторами, непосредственно связанными с гестацией, так и предшествующими заболеваниями. По наблюдениям специалистов в сфере акушерства, у большинства пациенток гестационная гидремия имеет такие легко объяснимые физиологические причины, как:
- Повышенная потребность в железе. Начиная со II триместра беременности, для адекватного обслуживания фетоплацентарного комплекса требуется больше железа. Этот микроэлемент ускоренно потребляется растущим плодом, поступает в плаценту, используется для увеличения общего числа эритроцитов, циркулирующих в крови женщины. К началу III триместра суточная потребность беременной в железе составляет минимум 4-6 мг, а на 32-34 неделях его требуется не менее 10 мг/сут.
- Физиологическая гемодилюция. При беременности объем циркулирующей плазмы возрастает на 40-50%, а объем эритроцитарной массы лишь на 20-35%. Это обусловлено повышенной потребностью организма в железе и пластических веществах, при недостаточном поступлении которых темпы эритропоэза не соответствуют скорости нарастания ОЦК. Согласно рекомендациям ВОЗ, допустимый уровень гемоглобина у беременных снижен до 110,0 г/л, а гематокрит — до 33%.
Фактором, усугубляющим анемию в послеродовом периоде, становится физиологическая потеря до 150 мл крови в родах, в каждых 2,0-2,5 мл которой содержится до 1 мг железа. Специалисты также выделяют ряд патологических причин, вызывающих заболевание. Уменьшение объема эритроцитов (микроцитарный вариант анемии) с соответствующим падением уровня гемоглобина наблюдается при отравлении производственными ядами (например, свинцом), многих хронических болезнях (ревматизме, сахарном диабете, язвенной болезни, гастрите, хронических инфекционных процессах), сидеробластной анемии, талассемии. Данное состояние также возникает при железодефиците, обусловленном недостаточностью в рационе мяса и потреблением продуктов, содержащих негемовые формы микроэлемента (растительная пища, молоко и молокопродукты).
Нормоцитарная анемия со сниженным содержанием нормальных эритроцитов чаще отмечается при кровопотерях вследствие патологии плаценты, хронической почечной недостаточности, гипотиреозе, гипопитуитаризме, аутоиммунной гемолитической форме заболевания, угнетении эритропоэза в костном мозге. Макроцитарный тип анемии с увеличением объема эритроцитов характерен для дефицита фолиевой кислоты и витамина В12, острого миелодиспластического синдрома, печеночной патологии (гепатиты, цирроз), алкогольной зависимости, ретикулоцитоза. Дополнительными факторами риска являются низкий материальный уровень жизни беременной, частые роды, многоплодная беременность, долгое вскармливание грудью с коротким межродовым промежутком, осложненное течение настоящей беременности (выраженный ранний токсикоз с многократной рвотой, гестозы).
Патогенез
Механизм формирования анемии при беременности обычно связан с нарушением баланса между поступлением железа в организм, особенно в сочетании с дефицитом белка, фолиевой кислоты, витамина В12, и их высоким расходом в пластических целях. Дополнительным звеном патогенеза является угнетение эритропоэза за счет повышения концентрация эстрадиола и накопления метаболитов, токсически воздействующих на костный мозг. Ситуация усугубляется иммунологическими изменениями, связанными с постоянной стимуляцией организма матери антигенами плода, что повышает противотканевую сенсибилизацию. Результатами патофизиологических процессов становятся тканевая, гемическая и циркуляторная гипоксия с нарушениями метаболизма и дальнейшим накоплением вредных продуктов обмена.
Классификация
Оптимальными критериями систематизации форм анемии беременных являются концентрация гемоглобина в крови и элемент или вещество, дефицит которого привел к возникновению заболевания. Такой подход к классификации позволяет более точно прогнозировать вероятные осложнения и подбирать схему ведения беременности. Современные акушеры-гинекологи выделяют следующие формы гестационной анемии:
- По степени тяжести: согласно классификации ВОЗ с учетом уровня гемоглобина заболевание бывает легким (90-109 г/л), умеренно выраженным (70-89 г/л), тяжелым (менее 70 г/л).
- По типу дефицита: наиболее распространенной является железодефицитная анемия (в структуре заболеваемости занимает около 95%), реже встречаются фолиеводефицитная и В12-дефицитная формы болезни.
Симптомы анемии при беременности
Легкая степень обычно протекает латентно. При понижении концентрации железа менее 90 г/л становятся заметными признаки гемической гипоксии (собственно анемического синдрома) и железодефицита в тканях (сидеропенического синдрома). О возможном развитии кислородного голодания свидетельствуют общая слабость, головокружения, шум в ушах, дискомфорт и боль в прекардиальной области, жалобы на учащение сердцебиения, одышка при физнагрузках. Слизистые оболочки и кожа выглядят бледными. Женщина становится раздражительной, нервозной, невнимательной, у нее снижается память, ухудшается аппетит.
Тканевый железодефицит проявляется быстрой утомляемостью, извращенным вкусом (желанием есть штукатурку, мел, глину, песок, фарш, сырое мясо), утолщением и ломкостью ногтевых пластин, сухостью и выпадением волос, мышечной слабостью, недержанием мочи вследствие ослабления сфинктерного аппарата. У части пациенток поражаются эпителиальные оболочки: возникают трещины («заеды») в уголках рта, воспаляется слизистая ротовой полости, появляются жалобы на зуд, жжение в области вульвы. При умеренно выраженных и тяжелых анемиях нередко наблюдается незначительная желтизна ладоней и носогубного треугольника, связанная с нарушенным метаболизмом каротина при железодефиците, и «синева» склер, вызванная дистрофическими процессами.
Осложнения
Вероятность осложнений беременности напрямую зависит от выраженности нарушений и времени возникновения заболевания. Особенно неблагоприятна анемия, развившаяся до зачатия. В таких случаях возможны первичная плацентарная недостаточность, гипоплазия плодных оболочек, низкое расположение плаценты и ее предлежание, ранний выкидыш, неразвивающаяся беременность. При появлении анемического симптомокомплекса во II-III триместрах повышается риск гестозов, поздних выкидышей и преждевременных родов, преждевременной отслойки нормально расположенной плаценты.
При тяжелом течении заболевания возникает миокардиодистрофия, ухудшается сократительная способность сердечной мышцы. Как следствие, гемическая и тканевая гипоксии усугубляются циркуляторной, в результате страдают паренхиматозные органы беременной, наблюдается декомпенсация их функции. В родах у 10-15% рожениц выявляется слабость родовых сил, часто наблюдаются обильные кровотечения гипотонического типа. После родов у 10-12% родильниц и у 35-37% новорожденных развиваются различные гнойно-септические процессы. У 4 кормящих матерей из 10 отмечается гипогалактия.
Наличие у беременной анемии представляет непосредственную угрозу для ребенка. Перинатальная заболеваемость при такой патологии может возрастать до 100%, а смертность — до 14-15%. Вследствие фетоплацентарной недостаточности в 63% случаев отмечается гипоксия плода, в 40% — гипоксическая травма мозга, в 32% — задержка развития. Почти треть новорожденных рождаются в асфиксии. Дефицит витамина В12, фолиевой кислоты вызывает аномалии развития позвоночника и нервной системы (spina bifida и др.). У детей, матери которых при беременности страдали выраженной или тяжелой анемией, хуже устанавливается функция внешнего дыхания. В постнатальном периоде они чаще отстают в росте и массе тела, более склонны к возникновению инфекционных заболеваний.
Диагностика
Ключевыми задачами диагностического поиска при подозрении на анемию при беременности считаются оценка степени тяжести расстройства и своевременное выявление осложнений. Поскольку в большинстве случаев анемия является железодефицитной, для постановки диагноза наиболее информативны лабораторные методы определения уровня железа и гемоглобина:
- Общий анализ крови. Содержание гемоглобина составляет менее 110 г/л. Цветовой показатель снижен до 0,85. Количество эритроцитов ниже 3,5х1012 клеток/л. Отмечаются признаки микроцитоза (уменьшения диаметра эритроцитов менее 6,5 мкм). В морфологической картине эритроцитов возможны пойкилоцитоз, анизоцитоз.
- Исследование обмена железа. Уровень сывороточного железа составляет менее 12 мкмоль/л. Общая железосвязывающая способность сыворотки (ОЖСС) повышена до 85 мкмоль/л и более. Снижены концентрация ферритина (менее 15 мкг/л) и насыщение железом трансферрина (менее 16%). Увеличена латентная железосвязывающая способность крови (ЛЖСС).
Для исключения В12-дефицитного и фолиеводефицитного вариантов анемии, возникшей при беременности, определяют сывороточный уровень цианокобаламина и фолиевой кислоты. С учетом возможных осложнений со стороны плода рекомендована оценка его состояния в динамике с проведением фетометрии, кардиотокографии, фонокардиографии. Дифференциальная диагностика осуществляется между разными формами заболевания, гемоглобинопатиями, синдромом анемизации, вызванным осложнениями беременности, и экстрагенитальной патологией.
Лечение анемии при беременности
Основными задачами терапии у беременных со сниженным гемоглобином являются коррекция железодефицита, устранение проявлений гипоксии, стабилизация гемодинамики и метаболизма. При умеренно выраженном и тяжелом течении анемии особое внимание уделяется поддержке адекватного функционирования фетоплацентарного комплекса. Схема лечения включает лекарственные средства, позволяющие:
- Восстановить содержание гемоглобина. При железодефицитной анемии рекомендован пероральный прием оптимально высоких доз железа в удобной для усвоения двухвалентной форме. Предпочтительно использование препаратов-депо с медленным высвобождением элемента. Парентеральная коррекция анемии проводится при непереносимости двухвалентного железа, принимаемого внутрь, нарушении его всасывания слизистой ЖКТ, обострившейся язвенной болезни желудка или двенадцатиперстной кишки. Для более эффективного усвоения микроэлемента назначают аскорбиновую кислоту. Эксперты ВОЗ рекомендуют дополнять прием железосодержащих препаратов фолиевой кислотой, предупреждающей развитие фолиеводефицитной анемии. Дефицит цианокобаламина является основанием для парентерального введения витамина В12.
- Устранить последствия гипоксии. Чтобы обеспечить адекватное снабжение плода кислородом и питательными веществами, комплексно воздействуют на разные элементы системы маточно-плацентарного кровотока. Для усиления притока крови к плаценте применяют токолитики, расслабляющие маточную стенку. Микроциркуляцию можно улучшить при помощи ангиопротекторов и препаратов, оказывающих влияние на реологию крови. Назначение мембраностабилизаторов, антикосидантов, актовегина позволяет повысить устойчивость плода к гипоксии. Антигипоксическую терапию обычно применяют при II-III степенях анемии, осложнившейся фетоплацентарной недостаточностью. При необходимости используют препараты для коррекции метаболического ацидоза и улучшения сердечной деятельности беременной.
Противоанемическая терапия обычно является длительной, позволяет полностью нормализовать показатели красной крови только на 5-8 неделях лечения. Для повышения эффективности лекарственных средств обязательна коррекция диеты. Рекомендуется дополнить рацион продуктами, богатыми железом: говядиной, телятиной, нежирной ветчиной, свиной, говяжьей, куриной печенью, рыбой. Следует уменьшить количество пищи, ухудшающей всасывание железа: хлебных злаков, отрубей, сои, кукурузы, чая, кофе, молока, карбонатной, гидрокарбонатной, фосфатной минеральной воды. С осторожностью назначают альмагель, тетрациклины, соли магния и кальция, способные усугубить анемию.
Прогноз и профилактика
Анемия легкой степени, диагностируемая у большинства беременных женщин со сниженным уровнем гемоглобина, не представляет угрозы жизни матери и плода. Своевременная коррекция умеренной и тяжелой форм заболевания позволяет существенно улучшить показатели крови, предупредить развитие осложнений. Для предупреждения перинатальных и материнских осложнений рекомендованы сбалансированное питание, раннее назначение препаратов железа пациенткам с меноррагиями в анамнезе, коротким интервалом между родами, длительной лактацией после предыдущих родов, многоплодием. Женщинам с анемией следует уделять повышенное внимание в период родов для быстрого выявления и коррекции возможных нарушений родовой деятельности, послеродовых кровотечений.
Источник

Для цитирования. Логутова Л.С. Анемия у беременных: вопросы этиологии, диагностики и лечения // РМЖ. 2016. No 5. С. 290–293.
Структура заболеваемости беременных женщин практически не меняется на протяжении десятков лет. Самое распространенное гематологическое заболевание в период гестации — это анемия [3].
Анемия — клинико-гематологический синдром, обусловленный снижением концентрации гемоглобина и, в большинстве случаев, эритроцитов в единице объема крови и их морфологическими изменениями.
Диагностика истинной анемии у беременных представляет определенные трудности. Это обусловлено тем, что во время беременности увеличиваются объем циркулирующей крови и его составляющих, объем плазмы и объем эритроцитов, причем объем плазмы возрастает в большей степени (почти в 2 раза). Происходит разведение эритроцитов в большом количестве жидкости, относительное уменьшение их числа при абсолютном увеличении объема плазмы. Это состояние называется гидремией и не является анемией, хотя наблюдается закономерное снижение показателей красной крови, но при этом отсутствуют морфологические изменения эритроцитов.
Допустимым пределом физиологической гемодилюции при беременности считается снижение показателя гематокрита до 0,32, гемоглобина – до 100 г/л, эритроцитов – до 3,5×1012/л. Дальнейшее снижение показателей красной крови следует расценивать как истинную анемию.
Компенсаторное значение гемодилюции беременных состоит в том, что облегчается обмен питательных веществ и газов через плаценту, а при кровопотере истинная потеря эритроцитов уменьшается примерно на 20%.
Клиническая гидремия беременных протекает бессимптомно и лечения не требует. С окончанием беременности быстро (в течение 1–2 нед.) восстанавливается нормальная картина крови.
Различают анемии, диагностируемые во время беременности, и догестационные.
Некоторые клиницисты склонны подразделять анемию на «анемию беременных» и «анемию у беременных», подразумевая в первом случае заболевание, развивающееся во время беременности, а во втором – малокровие, существовавшее еще до гестационного процесса.
По литературным данным, во второй половине гестации анемия диагностируется почти в 40 раз чаще, чем в первые недели, что, несомненно, связано с нарушением гемопоэза из-за изменений, вызванных беременностью [3].
При беременности развитие анемии связано с гормональными изменениями, развитием ранних токсикозов, препятствующих всасыванию в желудочно-кишечном тракте элементов железа, магния, фосфора, необходимых для кроветворения. Одной из основных причин является прогрессирующий дефицит железа, связанный с его утилизацией на нужды фетоплацентарного комплекса (ФПК), для увеличения массы циркулирующих эритроцитов. Анемию беременных также связывают с нарушением перекисного окисления липидов (ПОЛ) [1, 2].
У 9 из 10 пациенток во время беременности диагностируется железодефицитная анемия (ЖДА). Частота ЖДА во время беременности, по разным данным, колеблется от 21 до 80% (если судить по уровню гемоглобина) и от 49 до 99% (по уровню сывороточного железа). ЖДА – заболевание, на первый взгляд, безобидное, но ведущее к многочисленным осложнениям для матери, новорожденного и здоровья в течение всей последующей жизни ребенка. Проблема ЖДА у женщин в период гестации остается актуальной, поскольку осложняет течение беременности, родов и послеродовый период [2].
ЖДА – патологическое состояние, характеризующееся нарушением синтеза гемоглобина в результате дефицита железа, развивающееся на фоне различных патологических или физиологических (беременность) процессов. По данным ВОЗ, частота ЖДА среди беременных колеблется от 14% в странах Европы до 70% в Юго-Восточной Азии. В странах с высоким уровнем жизни населения ЖДА диагностируется у 18–25% беременных женщин, в развивающихся странах частота железодефицита при беременности может достигать 80%. Частота данного осложнения беременности в России стабильно на протяжении 15 лет составляет 30–40% [6].
Следует отметить, что у 20–25% женщин выявляется латентный дефицит железа. Так, дефицит железа в III триместре беременности обнаруживается почти у 90% женщин и сохраняется после родов и лактации у 55% из них [1, 4, 9].
Во время беременности железо усиленно расходуется вследствие интенсификации обмена веществ: в I триместре потребность в железе не превышает потребности до беременности и составляет 0,6–0,8 мг/сут; во II триместре – увеличивается до 2–4 мг/сут; в III триместре – до 10–12 мг/сут [7].
К концу беременности неизбежно наступает обеднение железом организма матери в связи с депонированием его в ФПК (около 450 мг), с увеличением объема циркулирующей крови, на что затрачивается около 500 мг, в послеродовом периоде – в связи с физиологической кровопотерей в 3-м периоде родов (100–150 мг) и лактацией (400 мг). Суммарная потеря железа к окончанию беременности и лактации составляет 1200–1400 мг [5].
Для своевременной диагностики и лечения ЖДА необходимо учитывать риск развития этого осложнения у различных групп беременных:
– перенесенные заболевания (частые инфекции): острый пиелонефрит, дизентерия, вирусный гепатит;
– экстрагенитальная фоновая патология (хронический тонзиллит, хронический пиелонефрит, ревматизм, пороки сердца, сахарный диабет, гастрит);
– меноррагии;
– частые беременности;
– наступление беременности при лактации;
– беременность в подростковом периоде;
– анемия при прошлых беременностях;
– вегетарианская диета;
– уровень Hb в I триместре беременности <120 г/л;
– осложнения беременности (ранний токсикоз, вирусные заболевания, угроза прерывания);
– многоплодная беременность.
Выявлено, что при ЖДА отмечается усиление процессов ПОЛ без активации антиоксидантной системы защиты, что приводит к повреждению мембранных структур клеток ФПК.
При дефиците железа у беременных возникает прогрессирующая гемическая гипоксия с последующим развитием вторичных метаболических расстройств. Поскольку при беременности потребление кислорода увеличивается на 15–33%, это усугубляет развитие гипоксии. У беременных с тяжелой степенью ЖДА развивается не только тканевая и гемическая гипоксия, но и циркуляторная, обусловленная развитием дистрофических изменений гипокинетического типа кровообращения.
Анемия осложняет течение беременности и родов. Истинные анемии беременных могут сопровождаться нарушением коагуляционных свойств крови, что является причиной массивных кровопотерь; оказывают неблагоприятное влияние на развитие сократительной деятельности матки; возможны длительные затяжные или быстрые и стремительные роды.
Беременные с ЖДА нуждаются в медикаментозном лечении и диетическом питании. Но невозможно купировать ЖДА лишь диетой, состоящей из богатых железом продуктов, без препаратов железа (ПЖ). Из лекарственных препаратов в организме может усвоиться в 15–20 раз больше железа, чем из пищи.
В настоящее время в распоряжении врача имеется большой арсенал лекарственных ПЖ, характеризующихся различным составом и свойствами, количеством содержащегося в них железа, наличием дополнительных компонентов (аскорбиновая и янтарная кислоты, витамины, фруктоза и др.), влияющих на фармакокинетику препарата, лекарственной формой, переносимостью, стоимостью. В клинической практике ПЖ применяются внутрь или парентерально.
В комплексной терапии ЖДА при беременности целесообразно применять антиоксиданты (витамин Е в дозе от 100 до 300 мг/сут). Для улучшения белкового метаболизма рекомендуется подключить так называемую белково-синтетическую терапию (оротат калия, витамин В6).
Лечение ЖДА у беременных при ее верификации должно проводиться до конца беременности. Это имеет принципиально важное значение и для коррекции анемии у беременной, и, главным образом, для профилактики дефицита железа у плода. Кроме того, по рекомендации ВОЗ, все беременные на протяжении II—III триместров беременности и в первые 6 мес. лактации должны получать ПЖ в профилактической дозе [8].
Контроль показателей красной крови необходимо проводить на фоне лечения каждые 10 дней. Неэффективность лечения ЖДА может быть обусловлена неадекватностью назначаемой терапии.
Несмотря на многообразие ПЖ, до настоящего времени продолжается дискуссия о преимуществах и недостатках двухвалентного железа, оценивается переносимость ПЖ пациентами, а также отслеживаются их возможные побочные действия.
Идеальный железосодержащий препарат должен обладать минимальным количеством побочных эффектов, иметь простую схему применения, наилучшее соотношение эффективности и цены, оптимальное содержание железа, желательно наличие компонентов, усиливающих всасывание и стимулирующих гемопоэз.
Применение комбинаций ПЖ с витамином В12 и фолиевой кислотой не всегда является оправданным, т. к. фолиеводефицитная анемия у беременных возникает крайне редко и имеет специфические клинико-лабораторные признаки.
Более целесообразным считается применять ПЖ, содержащие аскорбиновую кислоту. Одним из таких препаратов является Сорбифер Дурулес, выпускаемый фармацевтическим заводом «Эгис» (Венгрия). В препарате содержится оптимальное количество микроэлемента: в 1 таблетке – 320 мг сульфата железа (соответствует 100 мг железа II) и 60 мг аскорбиновой кислоты, улучшающей всасывание, усвоение железа и оказывающей антиоксидантное действие.
Нами проведен анализ результатов применения во время беременности препарата Сорбифер Дурулес с лечебной и профилактической целью в некоторых районах Московской области (гг. Балашиха, Домодедово, Видное, Люберцы, Мытищи). По результатам анализа количество анемий у беременных в этих районах колеблется от 27,8 до 48,3%. Всего было обследовано 125 беременных, которые с лечебной (82 (65,6%) и профилактической целью (43 (34,4%)) получали Сорбифер Дурулес. С лечебной целью назначали по 1 таблетке 2 р./сут, для профилактики – по 1 таблетке 1 р./сут. Длительность применения и дозу препарата определяли индивидуально на основании динамической оценки результатов гематологических показателей красной крови. Распределение обследованных пациенток в зависимости от цели приема препарата представлено в таблице 1.
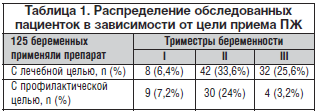
Как показано в таблице, чаще всего ЖДА выявлялась во II и III триместрах беременности. В связи с этим и профилактику ЖДА чаще всего начинали проводить со II триместра гестации. Важнейшими и наиболее доступными показателями красной крови при ЖДА являются пониженный уровень гемоглобина, низкий цветовой показатель, снижение количества эритроцитов. Эти показатели и использовались нами для оценки степени тяжести, адекватности лечения и эффективности профилактики ЖДА.
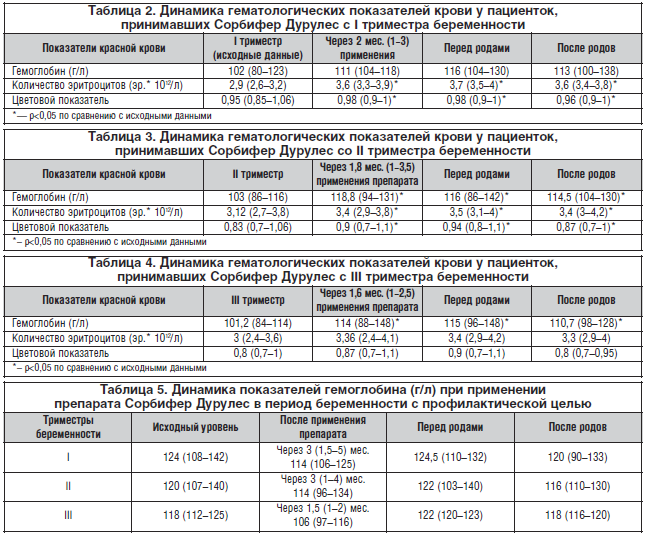
Результаты применения препарата Сорбифер Дурулес с I триместра беременности для лечения ЖДА представлены в таблице 2 (med (g1-g2)).
Из приведенных в таблице 2 данных следует, что применение препарата Сорбифер Дурулес в течение 2 мес. для лечения анемии с I триместра беременности привело к повышению гемоглобина в среднем на 10 единиц. Этот показатель сохраняется стабильным на протяжении всего периода гестации и в послеродовом периоде. Показатели количества эритроцитов и цветовой показатель после лечения на протяжении оставшегося периода беременности и в послеродовом периоде достоверно выше, чем исходные данные.
Динамика показателей гемоглобина, количества эритроцитов и цветового показателя у беременных с ЖДА, выявленной во II триместре гестации, до лечения и на его фоне представлена в таблице 3 (med ( g1-g2)).
При анализе полученных данных (табл. 3) видно, что на фоне проводимой терапии, продолжительность которой в среднем составила 1,8 мес., показатель гемоглобина стал достоверно выше аналогичного показателя до лечения и оставался в пределах нормативных значений до родов и в послеродовом периоде. Такая же тенденция наблюдалась и в динамике показателей количества эритроцитов и цветового показателя.
При выявлении ЖДА у беременных в III триместре беременности лечение проводилось в среднем 1,6 мес. и, как правило, продолжалось в послеродовом периоде. Динамика показателей красной крови при лечении анемии с III триместра беременности представлена в таблице 4 (med ( g1-g2)).
Таким образом, из анализа полученных результатов видно, что уровень гемоглобина после лечения препаратом Сорбифер Дурулес становился достоверно выше по сравнению с исходным, выявленным в III триместре беременности, и оставался таковым до родов.
Главная задача акушера в такой важный период для жизни женщины, как беременность, – не лечить осложнения, а предупредить их развитие. В нашем исследовании скрининговый анализ гемоглобина у беременных позволил осуществить профилактику ЖДА в период гестации.
Динамика показателей гемоглобина при применении препарата Сорбифер Дурулес в период беременности с профилактической целью представлена в таблице 5 (med (g1-g2)).
Данные, приведенные в таблице 5, подтверждают результаты других исследователей о том, что во II триместре беременности происходит наибольшее снижение показателей красной крови, а также тот факт, что повышение этих показателей происходит не быстро, а на фоне длительного применения (в нашем исследовании – в среднем 1,5–3 мес.) ПЖ (в частности, эффективного препарата Сорбифер Дурулес).

Представленные в настоящем исследовании данные свидетельствуют о высокой клинической эффективности железосодержащего препарата Сорбифер Дурулес, что позволяет рекомендовать его для лечения ЖДА, а также профилактики ее развития. Каких-либо побочных отрицательных эффектов, потребовавших отмены препарата, отмечено не было.
Источник
