Анемия вследствие кровопотери этиология патогенез
Различают острую и хроническую
постгеморрагическую анемии.
Острая постгеморрагическая анемия
Возникает в результате острой массивной
потери крови в объеме от 5 мл/кг массы
тела и выше (травма, хирургическое
вмешательство, желудочные, маточные,
кишечные кровотечения, разрыв фаллопиевых
труб, нарушение гемостаза и др.). Сразу
после потери крови вследствие уменьшения
ее массы появляется общеанемические
признаки — тахикардия, одышка, бледность
кожных покровов и слизистых оболочек,
падение АД. Содержание эритроцитов и
гемоглобина снижается равномерно
(нормоцитемическая гиповолемия),
развивается нормохромная анемия.
Изменения периферической крови носят
стадийный характер. На 2–3-е сутки после
кровотечения в кровь поступает тканевая
жидкость, масса ее восстанавливается
(гидремическая фаза), а количество
эритроцитов и гемоглобина снижается,
падает гематокрит, но в связи с выходом
эритроцитов из депо цветовой показатель
сохраняется в норме (нормохромная
анемия), развивается лейкопения (утрата
лейкоцитов во время кровотечения,
гемодиллюция), тромбоцитопения (утрата
тромбоцитов при потере крови, потребление
при образовании тромба). Наблюдается
умеренный анизоцитоз и пойкилоцитоз
эритроцитов. Возникшая гипоксия ведет
к повышению уровня эритропоэтина и на
4–5-е сутки после кровотечения активируется
функция костного мозга (костномозговая
фаза компенсации) появляются регенеративные
формы эритроцитов — полихроматофилы,
единичные нормобласты (полихроматофильные,
оксифильные), ретикулоцитоз. Анемия
приобретает гипохромный характер, т.
к. ускоренная регенерация опережает
созревание эритроцитов из-за возникшего
дефицита железа. Развивается нейтрофильный
лейкоцитоз со сдвигом влево по
регенеративному типу.
Данные нарушения обусловлены уменьшением
объема циркулирующей крови и гипоксией.
В ответ на кровопотерю включаются
механизмы компенсации, направленные
на восстановление утерянного объема
крови и на борьбу с анемическим состоянием
(гипоксией).
Хроническая постгеморрагическая анемия
Развивается в результате длительно
повторяющихся небольших кровотечений.
Является вариантом железодефицитных
анемий, патогенез и проявления обусловлены
нарастающим дефицитом железа.
Железодефицитная анемия
Железо — один из важнейших микроэлементов,
входящих в состав организма человека.
Взрослому человеку требуется 15–18 мг/сут
железа, из которых всасывается 2–2,5 мг.
При этом биодоступность содержащегося
в пище гемового железа существенно
выше, чем негемового. Основные депо
железа: печень (гепатоциты и макрофаги),
костный мозг, селезёнка, мышцы. Если
метаболизм железа нормален, 30–40 %
нормобластов костного мозга содержат
гранулы ферритина (сидеробласты).
Отсутствие сидеробластов характерно
для железодефицита. Избыток гранул в
сидеробласте служит признаком переполнения
организма железом (гемосидероз) или
неспособности утилизировать его
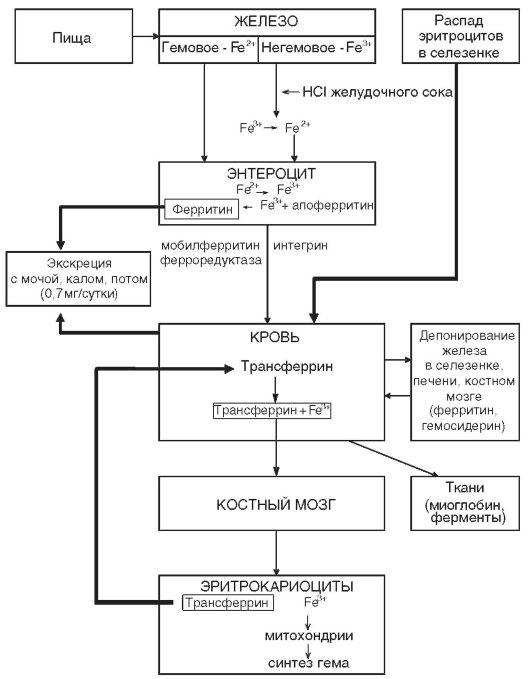
(сидеробластная анемия). На рис. 2
представлена схема метаболизма железа.
Дефицит железа в организме существует
в двух формах, представляющих собой две
последовательные стадии одного процесса:
латентный (тканевый) дефицит железа
(ЛДЖ) и собственно железодефицитная
анемия (ЖДА).
ЖДА составляет около 80–90 % всех случаев
анемий и является одной из самых
распространенных ее форм. Женщины
страдают данным заболеванием чаще, чем
мужчины, поскольку запасы железа у
последних значительно превышают (на
100–200 %) таковые у женщин. Явный и скрытый
дефицит железа отмечается почти у 60 %
женщин земного шара. Железодефицитные
анемии встречаются во всех возрастных
группах. Различают «истинные» ЖДА —
при абсолютном дефиците железа и «ложные»
— при нарушении включения железа в
гемм, в отсутствие первичного истинного
железодефицита.

Рисунок 2 – Схема метаболизма
железа в организме
Этиология
По патогенетическому принципу с учетом
основных этиологических причин
железодефицитные анемии делят на пять
основных подгрупп (Л.И. Идельсон): 1)
связанные с повышенной потерей железа;
2) связанные с недостаточным исходным
уровнем железа; 3) связанные с повышенным
расходованием железа; 4) связанные с
нарушением всасывания железа и
недостаточным поступлением его с пищей
(алиментарные); 5) связанные с нарушением
транспорта железа.
Таблица 3.Причины и механизмы
развития железодефицитных состояний
Группы | Характеристика | Патогенез |
Особенные периоды | Дети недоношенные Дети первых лет | Недостаточный |
Интенсивный рост Беременность Лактация | Повышенное | |
Патологические | Хроническая При При Из Из При Припатологии | Повышенная потеря |
Патологические | Патология ЖКТ: Резекция желудка Гипосекреция Хронический Дисбактериозы; Глистные инвазии | Нарушение |
Наследственная Приобретённая | Нарушение | |
Алкоголизм | Комбинация Недостаточное | |
Нарушение | Нерациональное Голодание; Вегетарианская Искусственное | Недостаточное |
Избыточные | Повышенное |
Нередко действуют комбинации указанных
факторов, вызывающих отрицательный
баланс железа. Примером ЖДА, развивающейся
вследствие комплексного влияния
нескольких факторов, является хлороз
(от греч. «хлорос» — бледно-зеленый, или
«бледная немочь»). Название связано со
специфическим цветом лица таких больных.
При ЖДА уменьшается содержание железа
в плазме крови, костном мозге и в тканевых
депо.
Патогенез.
Основным звеном патогенеза заболевания
является снижение содержания железа в
депо, сыворотке крови и костном мозгу.
В результате нарушается синтез
гемоглобина, возникают гипохромная
анемия и трофические расстройства в
тканях, признаками которых являются:
сухость и вялость кожи, ломкость ногтей,
выпадение волос, атрофия слизистой
оболочки языка, повышенное разрушение
зубов, дисфагия, извращение вкуса,
мышечная слабость и др.. В патогенезе
клинических проявлений болезни имеет
значение: нарушение активности
железосодержащих ферментов в тканях
организма (цитохром С, цитохромоксидаза,
сукцинатдегидрогеназа, пероксидаза,
митохондриальная моноаминооксидаза,
α-глицерофосфатоксидаза) и недостаточное
снабжение тканей кислородом. Признаки
гипоксии тканей появляются лишь при
значительной выраженности малокровия,
когда наступает истощение компенсаторных
механизмов, обеспечивающих на ранних
этапах развития дефицита железа
нормализацию отдачи кислорода из
гемоглобина тканям.
Клиническая картинаскладывается
из двух основных синдромов: общеанемического
и сидеропенического.
Общеанемический синдром проявляется
симптомами, характерными для всех видов
анемии: бледность, общая слабость,
быстрая утомляемость, обмороки, одышка,
тахикардия, систолический шум.Сидеропенический синдром характеризуется
рядом трофических нарушений. Отмечаются:
сухость и трещины кожи, преждевременные
морщины, ломкость ногтей, койлонихия
(катлонихия) — ложкообразные ногти,
ангулярный стоматит, атрофия слизистых
оболочек рта, пищевода, желудка,
дыхательных путей. Нарушается иммунитет,
что приводит к хронизации инфекций,
частым ОРЗ; развивается мышечная
слабость, слабость физиологических
сфинктеров. Может возникнуть извращение
вкуса (поедание несъедобных продуктов
— мела, бумаги и др.), пристрастие к
необычным запахам (ацетон, бензин,
краска). Нарушается память, концентрация
внимания. При дефиците железа резко
усиливается абсорбция свинца, и у детей
на этом фоне развивается необратимая
задержка интеллектуального развития.
Нарушение проницаемости мелких сосудов
ведет к отекам лица. Иногда возникает
«сидеропенический субфебрилитет».
Картина крови.Основным признаком
железодефицитной анемии является
гипохромия со снижением цветового
показателя ниже 0,8 и, соответственно,
уменьшением содержания гемоглобина
ниже 110 г/л. Количество эритроцитов, как
правило, остается на исходном уровне,
но в ряде случаев может оказаться
сниженным до 2,0-1,5×1012/л вследствие
нарушения процессов пролиферации клеток
эритроидного ряда в костном мозгу и
усиления неэффективного эритропоэза
(в норме разрушение эритронормобластов
в костном мозгу не превышает 10-15%).
Ретикулоциты в норме или незначительно
увеличены, при прогрессировании ЖДА их
количество снижается. Важным морфологическим
признаком железодефицитных анемий
является анизоцитоз эритроцитов с
преобладанием микроцитов.
Нередко развивается нейтропения (в
результате уменьшения содержания
железосодержащих ферментов в лейкоцитах).
СОЭ в норме или незначительно увеличена.
Уровень тромбоцитов может быть
незначительно повышен (на фоне
кровотечений).
Исследование костного мозга.В КМ
определяется нормобластическая
гиперплазия с нарушением гемоглобинизации
(преобладание базофильных и
полихроматофильных нормобластов при
снижении оксифильных), снижение индекса
созревания нормобластов, снижение
количества сидеробластов вплоть до
полного их отсутствия. Миелоидный и
мегакариоцитарный ростки не изменены.
Биохимический анализ крови – основной
диагностический критерий при ЖДА,
включающий набор тестов, при помощи
которых подтверждается факт дефицита
железа в организме:
снижение уровня сывороточного железа,
снижение уровня сывороточного ферритина,
снижение степени насыщения трансферрина
железом,увеличение содержания трансферрина в
сыворотке,повышение общей и латентной
железосвязывающей способности сыворотки,увеличение содержания растворимых
рецепторов к трансферритину в сыворотке,повышение свободного протопорфирина
IX в эритроцитах.
Количество железа в сыворотке крови
при выраженной ЖДА падает до 5,4–1,8
мкмоль/л при норме 12,5–30,4 мкмоль/л
(мужчины; у женщин этот показатель на
10–15% ниже. Под общей железосвязывающей
способностью сыворотки понимается
количество железа, которое может
связаться с трансферрином (в норме
54,0–72,0 мкмоль/л). В норме одна треть
трансферрина насыщена железом, а две
трети — свободны. Об уровне депонированного
железа можно судить по содержанию железа
в суточной моче после однократного
введения больному 500 мг десферала
(продукт метаболизма актиномицетов,
избирательно выводящий ион железа из
организма). В норме этот показатель
соответствует 0,6–1,3 мг железа, а при
железодефицитной анемии снижается до
0,2 мг в сутки и менее.
Сывороточный ферритин– очень точный
индикатор резервных запасов железа. Он
содержит примерно 15-20% общего запаса
железа в организме взрослого человека.
Определяется почти во всех тканях,
особенно высока его концентрация и
синтетическая способность в печени,
селезенке и костном мозге. Белок в
свободном от железа виде называется
апоферритином. Ферритин состоит из
белковой оболочки, которая окружает
ядро трехвалентного железа в виде
комплексов окиси и фосфата железа.
Каждая молекула апоферритина может
сорбировать до 5000 атомов железа, однако
большинство молекул ферритина содержат
от 1000 до 3000 атомов железа.
Анемии, ассоциированные с заболеваниями
внутренних органов, включают анемии
при эндокринных заболеваниях, заболеваниях
печени и почек.
К числу анемий при эндокринных
заболеванияхотносятся анемии при
заболеваниях щитовидной и паращитовидных
желез, надпочечников, половых желез,
гипопитуитаризме и др., в основе патогенеза
которых лежит депрессия эритропоэза
при дефиците или, напротив, гиперсекреции
ряда гормонов. В частности, такие гормоны,
как тироксин, кортизол, тестостерон в
очень высоких концентрациях вызывают
угнетение пролиферативной активности
эритроидных прекурсоров. В случае
сгущения крови в результате дегидратации
(при надпочечниковой недостаточности,
гипотиреозе) диагностика анемии может
быть затруднена.
К анемиям при заболеваниях печени
относятся анемии, возникающие при
диффузных поражениях органа (циррозе,
хроническом гепатите, гемохроматозе и
др.).
Патогенез анемии при заболеваниях
печени отличается многообразием
патогенетических факторов, что
определяется особенностями патогенеза
основного заболевания. Выделяют следующие
механизмы развития анемии:
угнетение процессов кроветворения в
костном мозгу вследствие прямого
токсического влияния на клетки-предшественницы
гемопоэза алкоголя (при алкогольном
поражении печени) и эндогенных токсинов
(при нарушениях обезвреживающей и
клиренсной функции печени), при нарушениях
метаболизма железа и депонирования
витамина В12и фолиевой кислоты
в пораженной печени;укорочение продолжительности жизни
эритроцитов в результате прямого
повреждающего действия токсических
продуктов экзогенного (алкоголь) и
эндогенного (при эндотоксемии)
происхождения, гиперспленизма, при
нарушениях внутриклеточного метаболизма
эритроцитов (например, в связи с дефицитом
в клетках НАДФ+) и их способности
к деформации (вследствие патологии
клеточной мембраны при изменениях
фракционного состава фосфолипидов,
снижении содержания сиаловых кислот);кровотечения из расширенных вен
желудочно-кишечного тракта (при циррозе
печени), носовые, геморроидальные и
иной локализации (при формирующейся
недостаточности синтеза факторов
свертывания крови вследствие нарушений
белкового обмена).
В подавляющем большинстве случаев при
заболеваниях печени регистрируется
нормохромная нормоцитарная анемия, при
присоединяющемся дефиците железа –
микроцитарная нормоили гипохромная,
при недостаточности витамина В12и фолиевой кислоты, метастазах рака
желудка в печень – макроцитарная анемия
нормо- или гиперхромного типа.
Анемии при заболеваниях почекмогут
выявляться у больных острым
гломерулонефритом, интерстициальным
нефритом, хронической почечной
недостаточностью. Патогенез анемии при
заболеваниях почек определяется
снижением продукции эритропоэтина
клетками юкстагломерулярного аппарата,
депрессией кроветворения в костном
мозгу (в результате нарушения
пролиферативной активности эритроидных
клеток, торможения процессов синтеза
гема) и сокращением срока жизни эритроцитов
(до 40-50 дней) при действии токсических
продуктов азотистого обмена.
Контрольные вопросы по теме:
Охарактеризуйте типовые формы изменений
общего объема циркулирующей крови.Какова этиология олигоцитемических и
полицитемических гиповолемий?Какова этиология олигоцитемических и
полицитемических гиперволемий?Укажите общие механизмы формирования
компенсаторно-приспособительных
механизмов при кровопотере.Каков механизм формирования экстренных
защитно-приспособительных реакций
организма при кровопотерях?Каков механизм формирования долговременных
защитно-приспособительных реакций
организма при кровопотерях?Дайте определение понятию анемия,
каковы принципы классификации?Назовите основные фонды железа в
организме?Перечислите лабораторные показатели,
характеризующие состояние красной
крови при острой кровопотере?Перечислите лабораторные показатели,
характеризующие состояние красной
крови при хронической кровопотере?Какие Вы знаете анемии, ассоциированные
с заболеваниями внутренних органов,
какие особенности для них характерны?
Темы реферативных сообщений:
Этиологи и патогенез ювенильного
хлороза (у девочек в пубертатный период)
при ЖДА
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Лекция
Заболевания крови. Основные синдромы
Основные синдромы:
1/ Анемический:
– бледность кожи, слизистых;
– алебастровый, зеленоватый оттенок кожи;
– иктеричность;
– ↑ ЧСС, ЧДД;
– расширение границ сердца (относительной сердечной тупости);
– умеренное ↓ АД;
– пастозность нижних конечностей.
2/ Язвенно-некротический:
– афтозный стоматит;
– некротическая ангина;
– лейкозная инфильтрация слизистой рта (набухание десен, увеличение миндалин);
– очаги некроза в ЖКТ.
3/ Геморрагический:
– кровотечения из носа, десен, легочные и т.д.;
– геморрагии на коже, слизистых.
4/ Лимфаденопатия.
Обследование: пальпаторно, биопсия.
Происходит сглаживание, выбухание, обезображивание участков, где расположены лимфоузлы.
Лимфоузлы: плотные, безболезненные, неуклонно увеличиваются, имеют вид «пакетов» и вызывают компрессионные синдромы:
– сдавление бронхов;
– сдавливания средостения: «воротник Стокса» (одышка цианоз, отек лица, отек шеи);
– сдавление общего желчного протока → желтуха;
– сдавление забрюшинных, мезентериальных лимфоузлов дает асцит;
– увеличение лимфоузлов вдоль позвоночника → корешковый синдром.
5/ Гепатомегалия, спленомегалия.
6/ Снижение веса.
7/ Лихорадка – м.б. небольшой, значительной.
8/ Следы расчесов на теле.
9/ Остеоартропатия:
– оссалгия;
– артралгия;
– дисфункция суставов;
– ревматоидоподобные артриты крупных периферических суставов;
– пальцы в виде «барабанных палочек»; на ранней стадии
– ногти в виде «часовых стекол»; заболевания
– фиброзные контрактуры (на поздней стадии заболевания).
10/ Гнойно-септические осложнения.
11/ Трофические изменения кожи, волос, ногтей, костей: истончение и сухость кожи, выпадение волос, ломкость ногтей.
Классификация анемий.
По этиопатогенетическому признаку:
1. Анемии вследствие кровопотерь:
– острые;
– хронические.
2. Анемии вследствие нарушенного кровообразования:
– железодефицитные;
– железонасыщенные (сидероахрестические или сидеробластные);
– В12-фолиево дефицитные;
– В12-ахрестические;
– гипопластические, апластические;
– метапластические.
3. Анемии вследствие усиленного кроверазрушения (гемолитические):
– наследственные;
– приобретенные (связаны с воздействием антител, прямых гемолизинов, других повреждающих факторов).
По цветовому показателю:
– нормохромные;
– гипохромные (ЦП < 0,8);
– гиперхромные (ЦП > 1,1).
По размеру эритроцитов:
– нормоцитраные;
– микроцитарные;
– макроцитарные.
По типу кроветворения:
– нормобластические;
– мегалобластические.
По способности костного мозга к кроветворению:
– регенераторные (ЦП=1) с повышенным эритропоэзом;
– арегенераторные (ЦП=0,2 и <) с временным или полным подавлением эритропоэза;
– гипорегенераторные (ЦП =0,5 и <);
– гиперрегераторные (ЦП=1,5 и >).
Анемии вследствие кровопотерь
Острая постгеморрагическая анемия
Этиология: массивная кровопотеря.
Патогенез: нарушения связаны с уменьшением объема циркулирующей крови и гипоксией.
Компенсаторные механизмы направлены на восстановление объема крови, на борьбу с гипоксией.
Картина крови: через 1-2 суток развивается нормохромная анемия. На 4-5 день – ретикулоцитоз, появляются полихроматофилы, нормобласты (нормоциты). Вследствие недостаточного насыщения эритроцитов гемоглобином анемия становится гипохромной, сопровождается лейкоцитозом со сдвигом влево.
Клиника: симптомы коллапса: резкая слабость, головокружение, бледность, сухость во рту, холодный пот, рвота, ↓ АД, ↑ Рs + слабого наполнения.
Лечение: остановка кровотечения, противошоковые мероприятия, трансфузионная терапия при АД < 90 мм рт.ст. и учащении пульса на 20 и > ударов в 1 минуту.
Кровопотеря < 1 л – плазмозаменители: полиглюкин, желатиноль, альбумин, физраствор, р-р Рингера, эритроцитарная масса + полиглюкин 1:2.
Кровопотеря > 1 л: донорская цитратная кровь (хранение не > 5 дней).
Профилактика: лечение основного заболевания.
Хроническая постгеморрагическая анемия
80% анемий – железодефицитные. Чаще болеют женщины.
Явный и скрытый дефицит железа отмечается у 60% жителей земного шара. В Европе частота железодефицитной анемии – 7-11%, скрытого дефицита железа – 20-25%.
В детском возрасте до 50% детей до 1 года имеют дефицит железа.
Этиология:
– хронические, необильные, скрытые кровопотери (маточные, желудочно-кишечные, легочные, носовые, десневые и т.д.);
– недостаток поступления железа с пищей (чаще в слаборазвитых странах, у детей на искусственном вскармливании, у новорожденных при дефиците железа у беременной);
– усиленный расход железа в период роста, созревания, беременности, лактации;
– пониженное усвоение железа после резекции желудка, тонкого кишечника;
– нарушение утилизации железа при инфекциях, интоксикациях, глистных инвазиях (часто в жарких странах);
– у девочек в период полового созревания в связи с повышенным расходом железа и угнетающим действием эстрогенов на эритропоэз (ювенильный хлороз → «бледная немочь»).
Патогенез: нарушение синтеза гема и насыщения эритроцитов гемоглобином вследствие истинного перераспределительного дефицита железа в организме. Снижается концентрация сывороточного железа, повышается общая и, особенно, латентная железосвязывающая способность сыворотки крови с уменьшением % насыщения железом его переносчика – трансферина (сидерофилин).
Транспорт железа в костный мозг снижается, уменьшается его включение в клетки эритроцитарного ряда.
Картина крови:
– гипохромная анемия – ЦП=0,6 и ниже;
– число эритроцитов м.б. нормальным или снижается, но меньше, чем гемоглобин;
– анизоцитоз, пойкилоцитоз;
– нейтропения (т.к. уменьшается содержание железосодержащих ферментов в лейкоцитах);
– СОЭ ↑ незначительно;
– железо в сыворотке снижено до 2-2,5 мкмоль/л (N = 14-32 мкмоль/л).
Клиника (железодефицитной анемии):
В клинике ведущими являются 2 синдрома:
– анемический;
– сидеропенический.
Степени анемии:
– легкая – Нb 110-90 г/л;
– средняя – Нb 90-70 г/л;
– тяжелая – Нb < 70 г/л.
Клиника: слабость, часто резкая; головокружение, головная боль, мелькание «мушек» перед глазами, обмороки; одышка; секутся, выпадают волосы; ломкость ногтей, их искривление, поперечная исчерченность, ложкообразная форма; извращение вкуса: тяга к мелу, ластику, глине, сырому мясу, льду; привлекают запахи сырости, известки, керосина, ацетона, гуталина; м.б. энурез ночной, недержание мочи; субфебрильная температура; бледность, легкая желтушность ладоней, подошв; атрофия слизистой языка, часто кариес!!!
Диагностика: ОАК (анемия, анизоцитоз, пойкилоцитоз, цветовой показатель < 0,8, лейкопения, тромбоцитопения), БХАК (сывороточное железо), ФГДС (сидоропеническая дисфагия), УЗИ органов брюшной полости, ЭКГ.
Лечение:
Диета: мясо (говядина, телятина, курятина), говяжья печень, рыба, крупа (овсяная, гречневая), овощи, фрукты (яблоки, гранаты) и др.
Анализ крови проводится каждые 3 недели.
Препараты железа:
– per os: ферамид, феррокаль, ферронал, ранферон-12, лактат железа, сульфат железа, ферроплекс, ферроплект, феррум-лек, ферретаб, конферон, ферро-градумент, тардиферон, сорбифер-дурулес, тотема;
– парентерально: феррум-лек, фербитол, ферковен.
Течение: хроническое.
Профилактика: полноценная диета; подростки-девушки – препараты железа весной и осенью, в дни mensis; физкультура, спорт, свежий воздух, при отсутствии соляной кислоты в желудке – реr os.
Ликвидация причин хронической кровопотери.
-В12-фолиеводефицитная анемия
Группа наследственных и приобретенных анемий, общим признаком которых является появление в костном мозге и периферической крови мегалобластов.
Чаще анемия вследствие дефицита витамина В12, реже – фолиевой кислоты.
Комбинированный дефицит встречается редко.
Заболевание чаще встречается во второй половине жизни, пик заболевания приходится на возраст старше 60-ти лет.
Классический вариант В12-дефицитной анемии – это болезнь Аддисона-Бирмера (злокачественная, пернициозная анемия) с триадой симптомов:
1/ нарушение кроветворения;
2/ атрофия слизистой ЖКТ;
3/ изменения со стороны нервной системы (фуникулярный миелоз, невриты, психозы).
Этиология:
Экзогенная недостаточность витамина В12 – редко.
Эндогенная недостаточность – результат уменьшения или отсутствия секреции гастромукопротеина парьетальными клетками желудка, что обусловлено:
а/ наследственным дефектом;
б/ иммунными механизмами – у 50% больных обнаружены антитела против внутреннего фактора или парьетальных клеток желудка;
в/ действием токсинов на слизистую желудка;
г/ гастроэктомией;
д/ раком желудка.
Кроме того, эндогенная недостаточность – это:
– результат нарушения всасывания витамина В12 в кишечнике (энтеропатии, резекция кишечника);
– повышенный расход витамина В12 (беременность, инвазия широкого лентеца).
Патогенез: Витамин В12 (внешний фактор Касла) поступает с пищей, синтезируется флорой толстого кишечника. Для его всасывания необходим гликопротеин (внутренний фактор Касла), вырабатываемый парьетальными клетками желудка (тела, дна). Комплекс «витамин В12 + гликопротеин» всасывается в средней и нижней части подвздошной кишки. Депо витамина В12 – печень.
Витамин В12 участвует в кроветворении и обмене жирных клеток. Без витамина В12 нарушается образование ДНК и нормальное эритробластическое кроветворение становится мегалобластическим.
Без витамина В12 синтезируются ненормальные жирные кислоты и накапливается токсичная метилмалоновая кислота, нарушающая образование миелина.
Картина крови:
– гиперхромная анемия (ЦП=1,0 и > до 1,2-1,5);
– количество эритроцитов падает в большей степени, чем гемоглобин;
– лейкопения с нейтропенией;
– тромбоцитопения.
В мазке крови:
– мегалобласты; до 80-90%
– мегалоциты;
– анизоцитоз, пойкилоцитоз;
– макроцитоз;
– эритроциты с тельцами Жолли, кольцами Кебота, базофильной зернистостью;
– полисегментированные нейтрофилы;
– ретикулоциты – ↓ или N;
– СОЭ увеличена.
Клиника: жалобы связаны с поражением кроветворной, пищеварительной, нервной систем.
Общие жалобы: слабость, утомляемость, одышка, сердцебиение, диспептические расстройства.
Внешне: полнота; одутловатость лица; бледно-желтушная кожа; субиктеричность склер; афты на языке, слизистой щек; «лакированный» язык; печень, селезенка увеличены.
Нервная система: парестезии; чувство «холода», «ползания мурашек», онемение конечностей»; «ватные ноги»; мышечная слабость; атрофия мышц; характерно сегментарное поражение конечностей; потеря вкусовых ощущений, обоняния, слуха; нарушение ФТО; психические расстройства(галлюцинации, бред, Ерт-приступы; кахексия в тяжелых случаях; параличи нижних конечностей; распространенный кариес.
Течение:
– рецидивирующее;
– возможен летальный исход.
При правильном лечении прогноз благоприятный.
Лечение:
Витамин В12 парентерально 400-500 γ ежедневно N 30-40 до нормализации показателей крови.
Поддерживающая терапия: 400-500 γ 1 раз/неделю – 2-3 месяца; затем 2 раза/месяц – 2-3 месяца; затем 250 γ ежемесячно пожизненно.
В нелеченных случаях после 2-3 рецидивов – летальный исход.
Фолиеводефицитная анемия
Дефицит фолиевой кислоты наблюдается при голодании, особенно у детей; при алкоголизме; при беременности; при энтеритах, энтеропатиях.
Клиника: как при В12-дефицитной анемии.
Дифференцировать очень трудно. Поэтому вместе с витамином В12 назначают фолиевую кислоту (10-15 мг/сутки – 6 недель).
Течение – циклическое; прогноз – благоприятный.
Профилактика: новорожденных кормить донорским молоком, смесями, но не козьим молоком.
Дата добавления: 2016-10-23; просмотров: 559 | Нарушение авторских прав | Изречения для студентов
Читайте также:
Рекомендуемый контект:
Поиск на сайте:
© 2015-2020 lektsii.org – Контакты – Последнее добавление
Источник
