Анкета анемии у детей
Терапия железодефицитной анемии должна проводиться препаратами железа. Цель лечения препаратами железа – устранение дефицита железа в организме, а не просто нормализация уровня гемоглобина, поэтому срок лечения длительный.
Препараты железа — группа лекарственных средств, содержащих соли или комплексы двух – и трёхвалентного железа, а также их комбинации с другими препаратами. Каждое из этих препаратов имеет
свою дозировку, форму выпуска, а также сопутствующие вещества.
Дополнительные компоненты повышают усвояемость активного вещества и снижают риск развития побочных эффектов.
Хорошо известно, что неорганические соли двухвалентного железа образуют комплексы с компонентами пищи или лекарствами. Это происходит из-за того, что простые соли железа диссоциируют на двух – или трехвалентные ионы в водных растворах, формируя растворимые и/или нерастворимые комплексы железа. Эти качества приводят к уменьшению всасывания железа. Поэтому, рекомендуется принимать соли железа (II) за 1 час до еды, т. е. натощак. Однако, в этом случае, чаще развиваются такие побочные реакции как раздражение желудка, изъязвление тонкой кишки и др. К данным препаратам относятся Сорбифер Дурулес, Ферроплекс, Тардиферон и др.
Сейчас появились новые высокоэффективные препараты, которые лишены многих побочных действий препаратов предшествующего поколения. Это препараты, в состав которых входит так называемое трехвалентное железо. Неионные соединения железа имеют большую молекулярную массу, что затрудняет их проникновение через мембрану слизистой кишечника. Они поступают из кишечника в кровь в результате активного всасывания, практически не завися от взаимодействия с ворсинками кишечника «напрямую». Это объясняет невозможность передозировки этих препаратов, в отличие от двухвалентного железа. Взаимодействие их с компонентами пищи и лекарственными препаратами не происходит, что позволяет использовать лекарства, содержащие трехвалентное железо, не нарушая режим питания и терапии сопутствующей патологии. Из побочных эффектов в некоторых случаях отмечается лишь чувство переполнения желудка. Представителями таких лекарственных препаратов являются Мальтофер, Ферлатум, Феррум лек.
Данные препараты сходны по структуре с естественным соединением железа с ферритином. Благодаря такому сходству, железо (III) из кишечника поступает в кровь путем активного всасывания. Именно это свойство объясняет невозможность отравления данными препаратами в отличие от простых солей железа. Всосавшееся железо сохраняется в связанном с ферритином виде, главным образом, в печени. Позже, в костном мозге оно включается в состав гемоглобина. Железо, входящее в состав железо (III) – гидроксид полимальтозного комплекса, обладает антиоксидантными свойствами, которые не присущи простым солям железа (II).
1.6. Преимущества современных железосодержащих препаратов:
– обладают низкой токсичностью, высокой безопасностью, при передозировке не приводят к отравлению;
– токсичность препаратов для парентерального (внутримышечного, внутривенного) введения также очень низка;
– по своей терапевтической эффективности не уступают другим препаратам железа, но при этом обладает несомненными преимуществами, такими как хорошая переносимость и минимальное количество побочных эффектов;
– переносятся лучше, чем препараты на основе солей железа;
– при приеме внутрь не взаимодействуют с пищей; компоненты пищи не влияют на степень всасывания, поэтому препараты можно добавлять во фруктовые соки, чай, молоко и принимать его в независимости от диетологического режима, в любое удобное время;
– имеют различные формы выпуска: сиропы, капли, жевательные таблетки, растворы
– при приеме внутрь не окрашивают эмаль зубов, что важно при длительном применении
– высокое содержание элементарного железа
– приемлемая стоимость.
Детям старшего возраста и подросткам назначают таблетки, драже и капсулы, содержащие железо. Детям раннего возраста препараты железа дают в виде сиропа, капель. Дозировка и длительность лечения зависят от степени дефицита железа. Дозу и продолжительность лечения подбирают индивидуально под контролем уровня гемоглобина и железа сыворотки крови. Кратность приема зависит от лекарственной формы конкретного препарата, от содержания элементарного железа в лекарственных препаратах.
Все препараты железа для парентерального применения не назначают одновременно с пероральными препаратами железа, при нормальной абсорбции железа из желудочно-кишечного тракта. Перерыв между парентеральным применением препарата и началом применения пероральных форм железа должен составлять не менее 5 дней. Препараты железа для парентерального питания применяют строго по показаниям: при тяжёлой степени ЖДА, при нарушении всасывания железа, энтеритах, непереносимости или неэффективности перорального приема препаратов железа или при противопоказаниях к нему (язвенной болезни). Назначают следующие препараты железа: Ферковен (для внутривенного введения), Фербитол, Жектофер (для внутримышечного введения), Феррум Лек (для внутривенного и внутримышечного введения).
Неосложненная железодефицитная анемия вследствие алиментарной недостаточности, нарушенного всасывания или повышенного расходования железа, хорошо реагирующая на терапию препаратами железа, не требует для лечения переливаний крови.
Очень важно своевременное лечение анемии, включающее правильную организацию режима питания, отдыха и применение современных железосодержащих препаратов.
1.7. Современные принципы лечения железодефицитной анемии.
1. Невозможно устранить железодефицитную анемию без препаратов железа, с помощью одной лишь диеты, так как всасывание пищевого железа ограничено. Из лечебных препаратов его всасывается значительно больше.
2. Пищевые продукты должны быть полноценными по содержанию белка, микроэлементов, витаминов, так как эти ингредиенты улучшают всасывание медикаментозного железа.
3. Необходимо использовать пероральные препараты железа, парентеральные препараты железа вводятся только по специальным показаниям.
4. Не прибегать к гемотрансфузиям. Переливания эритроцитарной массы используются только по жизненным показаниям.
5. Следует устранить этиологическую причину железодефицитной анемии.
6. Необходимо провести коррекцию нарушений органов и систем.
АНАЛИЗ РЕЗУЛЬТАТОВ ИССЛЕДОВАНИЯ
По данным педиатров, в нашей стране каждый 2 ребенок до года, каждый 3 дошкольник и каждый 4 школьник имеют ЖДА. Так как железодефицитная анемия является таким широко распространенным заболеванием, мы решили исследовать уровень заболеваемости детей ЖДА в нашем Куйбышевском районе.
Исследование включало в себя 3 этапа.
Первый этап – работа в детском отделении ГБУЗ НСО «Куйбышевская ЦРБ». На данном этапе проводилось анкетирование 40 матерей, которые находились в детском отделении по уходу за своими больными детьми, на предмет их информированности по вопросам ЖДА. Анкета состояла из 10 вопросов.
АНКЕТА ИНФОРМИРОВАННОСТИ МАТЕРЕЙ О ЖЕЛЕЗОДЕФИЦИТНОЙ АНЕМИИ
ФИО матери:
Возраст матери:
Образование: среднее, начально-профессиональное, средне-специальное, высшее
Какой по счёту ребёнок:
Возраст ребёнка:
1. Что Вы знаете о железодефицитной анемии:
а) ничего б) повышенная кровоточивость в) малокровие
2. Причины, вызывающие анемию:
а) неправильное питание ребёнка г) обильные менструации
б) острые кровопотери д) заболевания ЖКТ
в) не знаю
3. Связана ли анемия с питанием ребёнка:
а) да б) нет в) не знаю
4. Знаете ли Вы, при каком кормлении чаще всего развивается анемия:
а) при кормлении грудным молоком
б) при кормлении коровьим молоком
в) при кормлении адаптированными смесями
г) вид кормления не имеет значения
д) не знаю
5. Связана ли анемия с полом ребёнка:
а) да б) нет в) не знаю
6. У детей, какого возраста чаще всего возникает анемия:
а) у грудных детей г) не знаю
б) у младших школьников д) возраст значения не имеет
в) у старших школьников
7. Излечима ли анемия:
а) да б) нет в) не знаю
8. Знаете ли Вы, что является основным в лечении железодефицитной анемии:
а) препараты железа в) продукты, богатые железом
б) витамины г) не знаю
9. Знаете ли Вы, какие продукты, богаты железом:
а) мясо говядины д) печень
б) мясо курицы ж) яблоки
в) гречка з) молоко
г) хлеб и) не знаю
10. Влияет ли анемия на качество жизни ребёнка (здоровье, развитие):
а) да б) нет в) не знаю
По результатам проведенного опроса был составлен обобщенный портрет респондента: возраст от 22 до 40 лет; высшее или средне-специальное образование (75%); имеет первого или второго ребенка (87%); возраст ребенка до 3-х лет (65%).
Результаты анкетирования оценивались методом подсчета индикаторов правильных ответов, которые выбрали участники опроса. Полученные данные представлены в диаграммах.
На вопрос о том, что такое анемия (Диаграмма 1) 31 респондент (77,5%) дали правильный ответ – малокровие, 5 человек (12,5%) ответили повышенная кровоточивость и 4 человека (10%) не знают что такое анемия.
Диаграмма 1.

На вопрос о причинах ЖДА (Диаграмма 2) большинство опрашиваемых (45% или 18 человек) основной причиной назвали только неправильное питание, 2 матери (5%) выбрали только кровопотери, 13 участников опроса (32,5%) указали 2-3 причины (заболевания желудочно-кишечного тракта, обильные менструации, неправильное питание). Все причины выбрали только 3 респондента (7,5%) и 10% или 4 человека не знают причины анемии.
Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 |
В статье освещены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий у детей. Представлены основные принципы дифференциальной диагностики и лечения указанных дефицитных анемий у детей.
В настоящей публикации на основании данных литературы и анализа собственных наблюдений представлены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий, а также принципы их лечения у детей. Установлено, что основной формой дефицитных анемий (ДА) в педиатрической популяции является анемия, обусловленная недостаточным содержанием в организме железа. При этом особо подчеркивается, что железодефицитная анемия (ЖДА) не только наиболее распространенная ДА, но и самое частое гематологическое заболевание у детей [1–3]. С учетом того, что другие типы анемий (в т. ч. развивающиеся при дефиците таких витаминов, как фолиевая кислота и В12) хуже известны врачам-педиатрам, их верификация, как правило, запаздывает, т. к. они ошибочно принимаются за ЖДА. Поздняя диагностика и отсутствие адекватной терапии при этом приводят к прогрессированию патологических процессов. Это негативно сказывается на росте и развитии детского организма и ухудшает качество жизни ребенка. Принимая во внимание актуальность данной проблемы, авторы пришли к выводу о необходимости представить для практикующих врачей-педиатров ключевые положения дифференциальной диагностики и лечения анемий, обусловленных дефицитом железа, фолиевой кислоты и витамина В12 у детей.
Дифференциальная диагностика ДА у детей
Критерием анемии, независимо от этиологии, является снижение уровня гемоглобина (Hb) ниже возрастной нормы. Так, синдром анемии констатируют, если концентрация Hb в капиллярной крови ниже: 110 г/л — у детей в возрасте от 1 мес. до 5 лет, 115 г/л — у детей 6–12 лет, 120 г/л — у детей старше 12 лет и подростков. Кроме этого, зная уровень Hb, можно определить тяжесть анемического синдрома. Так, для детей, достигших месячного возраста и старше, снижение Нb до 90 г/л является признаком анемии легкой степени, уровень Нb в пределах 70–90 г/л характерен для анемии средней тяжести, а падение Нb ниже 70 г/л определяет тяжелую степень анемии [1–4].
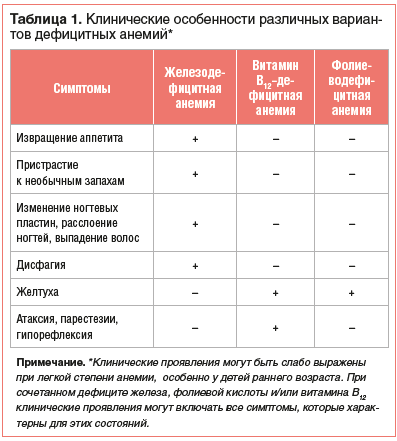
Нозологическая верификация характера анемии проводится на основе анализа клинико-анамнестических данных, результатов лабораторного и, если необходимо, инструментального обследования пациента. Общими клиническими проявлениями анемии, независимо от этиологии, являются повышенная утомляемость, снижение работоспособности, склонность к инфекциям. Среди дополнительных симптомов, которые могут отмечаться при ЖДА, — извращение аппетита и пристрастие к необычным запахам, изменение ногтевых пластин, расслоение ногтей, выпадение волос, атрофия сосочков языка, дисфагия. В свою очередь, при витамин В12-дефицитной анемии имеют место неврологические нарушения (атаксия, парестезии, гипорефлексия и другие проявления фуникулярного миелоза), «лакированный» язык и желтуха. Непрямая гипербилирубинемия может также отмечаться и при фолиеводефицитной анемии (табл. 1).
Наличие желтухи и анемии при этом нередко становится причиной ошибочного заключения о гемолитическом характере анемии, если врач не обращает внимания на отсутствие ретикулоцитоза. Следует отметить, что иктеричность при анемиях, обусловленных дефицитом витамина В12 или фолиевой кислоты, связана с неэффективным эритропоэзом и повышенным разрушением предшественников эритроцитов в костном мозге [1–3, 5–7].
Несмотря на описанные выше симптомы, типичные для конкретных ДА, их клинические проявления могут быть слабо выражены при легкой степени анемии, особенно у детей раннего возраста. В связи с этим этиологическая верификация генеза анемического синдрома проводится на основании не только клинических проявлений и анамнестических данных. Обязательным условием установления диагноза является корректная трактовка результатов лабораторного обследования. При этом минимально достаточным уровнем лабораторного обследования является проведение клинического и биохимического анализов крови.
Хорошо известно, что показаниями к исследованию клинического анализа крови для исключения анемии у детей являются анамнестические (недоношенность, задержка внутриутробного развития, исключительно грудное вскармливание ребенка, если мать имеет хронические заболевания кишечника или является вегетарианкой и др.) и/или клинические факторы риска (геморрагический синдром, синдром мальабсорбции, инфекционно-воспалительные заболевания, желтуха, лимфаденопатия, гепато- или спленомегалия и другие патологические состояния). При оценке результатов клинического анализа крови нельзя ограничиваться только поиском лабораторных признаков анемии. Обязательно должны быть проанализированы все параметры гемограммы (эритроциты и их индексы, ретикулоциты, тромбоциты и их индексы, общее количество лейкоцитов, лейкоцитарная формула, а также абсолютное количество нейтрофилов, лимфоцитов, моноцитов и эозинофилов, СОЭ). Это позволяет уже при первичном обращении пациента очертить круг основных причин выявленной анемии и наметить основные диагностические мероприятия для расшифровки генеза заболевания [1–4].
Так, для ЖДА типичными признаками являются: гипохромия и микроцитоз эритроцитов при нормальном уровне ретикулоцитов, если недостаточное содержание железа в организме обусловлено алиментарными факторами или синдромом мальабсорбции. В тех же случаях, когда ЖДА имеет постгеморрагический генез, гипохромия и микроцитоз эритроцитов будут сопровождаться ретикулоцитозом [1–4]. В свою очередь для анемий, обусловленных недостатком в организме как фолиевой кислоты, так и витамина В12, характерны гиперхромия и макроцитоз эритроцитов, а также ретикулоцитопения (табл. 2).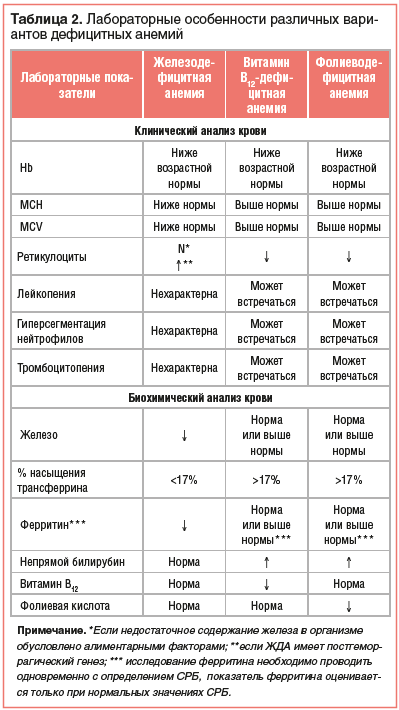
Кроме этого, при фолиево- и витамин В12-дефицитной анемиях могут встречаться лейко- и тромбоцитопения, гиперсегментация нейтрофилов. С учетом того, что в ряде случаев ДА имеет комбинированный генез, при котором дефицит железа сочетается с дефицитом фолиевой кислоты или витамина В12, типичные гематологические признаки могут не выявляться или быть разнонаправленными. Это определяет необходимость обязательного проведения биохимического анализа крови с определением, кроме общепринятых показателей, таких параметров, как железо, железосвязывающая способность, процент насыщения трансферрина, ферритин, фолиевая кислота и витамин В12 [6, 7]. Особо следует подчеркнуть, что ферритин должен определяться вместе с С-реактивным белком (СРБ). При этом оценивать уровень ферритина можно только в тех случаях, когда значения СРБ находятся в пределах нормативных. Это объясняется тем, что ферритин относится к протеинам воспаления и его уровень повышается при воспалительных процессах в организме. В связи с этим нормальный или высокий уровень ферритина при повышенных значениях СРБ может стать причиной ошибочного заключения об отсутствии железодефицитного состояния [2–4]. Особенности биохимического анализа крови при различных вариантах ДА представлены в таблице 2.
Лечение ДА у детей
Корректная трактовка клинико-анамнестических данных и результатов лабораторного обследования позволяет верифицировать причину ДА и своевременно назначить адекватную терапию. Принципиально важным при этом является положение о том, что компенсировать дефицитные состояния невозможно только за счет нормализации рациона питания. Основная роль в купировании дефицита железа, фолиевой кислоты и витамина В12 принадлежит заместительной фармакотерапии [1–7]. При этом для лечения ЖДА используются солевые препараты железа или препараты на основе железа гидроксид полимальтозата. Суточная доза препаратов зависит от массы тела и возраста ребенка, расчет при этом проводится по элементарному железу. Так, для солевых препаратов железа, назначаемых внутрь, используются следующие дозы (расчет по элементарному железу!): для детей до 3 лет — 3 мг/кг/сут, для детей старше 3 лет — 45–60 мг/сут, для подростков —
до 120 мг/сут. При использовании пероральных форм железа гидроксид полимальтозата рекомендованные дозы составляют 5 мг/кг/сут (расчет по элементарному железу!). Продолжительность терапии препаратами железа зависит от степени тяжести ЖДА. При легкой ЖДА курс лечения составляет 3 мес., при среднетяжелой форме — 4,5 мес., при тяжелой — до 6 мес. [3].
В случае диагностики фолиеводефицитной анемии заместительная терапия проводится препаратами фолиевой кислоты. Рекомендовано использовать следующие суточные дозы фолиевой кислоты: для детей до 1 года — 0,25–0,5 мг/сут, для детей старше 1 года — 1,0 мг/сут. При синдроме мальабсорбции доза может быть повышена до 5–15 мг фолиевой кислоты в сутки. Терапия проводится в указанных дозах ежедневно на протяжении 4–6 нед. Через 7 дней от начала лечения необходимо выполнить клинический анализ крови с обязательным подсчетом ретикулоцитов (рис. 1). Повышение уровня ретикулоцитов на фоне приема фолиевой кислоты указывает на правильно установленный диагноз и является обоснованием для продолжения терапии. Купирование анемии достигается через 4–6 нед. от начала лечения [6].
Для лечения витамин В12-дефицитной анемии используют препараты цианокобаламина для парентерального введения. При этом рекомендовано придерживаться следующего режима дозирования: для детей до 1 года — 5 мкг/кг/сут, для детей старше 1 года — 100 мкг/сут, для подростков — 200 мкг/сут. Препарат вводится внутримышечно 1 р./сут ежедневно. На 7–10-й день терапии проводят клинический анализ. Выявление ретикулоцитоза позволяет сделать вывод об эффективности проводимого лечения. Терапию следует продолжить в том же режиме дозирования еще в течение 3–4 нед. В дальнейшем, при достижении нормализации уровня гемоглобина, переходят на поддерживающее лечение: цианокобаламин вводят в терапевтической дозе 1 раз в 7 дней в течение 2 мес., а затем 1 раз в 14 дней в течение 6 мес. (рис. 2). Учитывая, что дефицит витамина В12, как правило, редко обусловлен алиментарными факторами, одновременно проводят поиск причин данного патологического состояния (болезнь Крона, целиакия, инвазия широким лентецом, наследственные нарушения всасывания и/или транспортировки витамина В12 и др.) [7]. В тех случаях, когда имеют место полидефицитные состояния с развитием анемического синдрома, оправданно комбинированное заместительное лечение. Чаще всего у детей встречается сочетанный дефицит железа и фолиевой кислоты, что требует одновременного назначения препаратов железа и фолиевой кислоты.
Заключение
Таким образом, выявление анемии у ребенка определяет необходимость обязательного уточнения причин указанного патологического состояния. Своевременная верификация этиологии анемии позволяет без промедления начать адекватную терапию, что определяет ее эффективность и улучшает качество жизни ребенка. Авторы выражают надежду, что информация, представленная в настоящей публикации, будет полезна практикующим врачам-педиатрам.
