Апластическая анемия это рак крови
Апластическая анемия – тяжёлое гематологическое заболевание, сопровождающиеся малокровием, резким снижением иммунитета, а также нарушениями процессов свертывания крови. Она возникает вследствие подавления кроветворной функции костного мозг (или аплазии костного мозга).
Болезнь впервые описана известным немецким врачом и ученым Паулем Эрлихом, в 1888 году. Неизвестная ранее патология, обнаруженная у молодой беременной женщины, сопровождалась тяжёлой анемией, снижением числа лейкоцитов, лихорадкой, кровоточивостью и быстро привела к смерти больной. Проведенное патологоанатомическое исследование обнаружило замещение красного костного мозга жировой тканью. Позднее, в 1907 году, Анатоль Шоффар, французский врач, предложил назвать это заболевание апластической анемией.
Апластическая анемия – достаточно редкое заболевание. Средняя заболеваемость – 3-5 на 1 млн. всего населения за год. Большинство больных – дети и молодые люди.
Различают наследственную (генетически обусловленную) и приобретенную апластическую анемию.
80% случаев заболевания обусловлены приобретенной формой патологии, 20% вызваны генетическими факторами.
Медики пользуются классификацией патологии по МКБ-10 (Международная Классификация Болезней 10 пересмотра). Различают следующие виды апластических анемий:
D61.0 Конституциональная апластическая анемия
D61.1 Медикаментозная апластическая анемия
D61.2 Апластическая анемия, вызванная другими внешними агентами
D61.3 Идиопатическая апластическая анемия
D61.8 Другие уточненные апластические анемии
D61.9 Апластическая анемия неуточненная
У детей в большинстве случаев заболевание носит приобретенный характер. Частота встречаемости составляет 2-3 случая на 1 млн. детей (пик заболеваемости приходится на подростковый возраст). В 70% случаев непосредственную причину болезни установить не удаётся, принято считать, что наибольшее значение имеют вирусные инфекции, химикаты и лекарственные препараты.
Чаще всего диагноз устанавливают случайно, при общем анализе крови. При правильном лечении и своевременной диагностике прогноз благоприятный. Апластическая анемия у детей хорошо лечится. Результаты применения трансплантации костного мозга и иммуносупрессивной терапии примерно одинаковы по эффективности, однако следует отдавать предпочтение пересадке костного мозга от подходящего (в идеале брат или сестра) донора. Современные методы лечения апластической анемии в детском возрасте позволяют сохранить здоровье и не влияют на способность иметь детей в будущем.
Генетически обусловленные нарушения кроветворной функции отмечают при некоторых наследственных патологиях, таких как семейная анемия Фанкони, синдром Швахмана-Даймонда, истинная эритроцитарная аплазия, врождённый дискератоз.
Мутации в критически важных генах, отвечающих за регуляцию клеточного цикла, синтез белков, защиту и восстановление повреждений ДНК, ведут к образованию дефектных стволовых (гемопоэтических) клеток. Ошибки в генетическом коде инициируют запуск апоптоза – механизма запрограммированной клеточной смерти. При этом пул стволовых клеток сокращается гораздо быстрее, чем у здоровых людей.
Приобретенная форма патологии возникает в результате прямого токсического воздействия на гемопоэтические клетки. К таким факторам относят:
· Воздействие ионизирующей радиации. От апластической анемии погибла Мария Склодовская-Кюри – физик, дважды лауреат Нобелевской премии, полученной за работы в области исследования радиоактивности и за открытие новых радиоактивных элементов;
· Пестициды, инсектициды, производные бензола, соли тяжёлых металлов, мышьяк обладают прямым токсическим эффектом на костный мозг, угнетают продукцию форменных элементов крови и приводят к гибели стволовых клеток;
· Схожим эффектом обладают некоторые лекарства. Нестероидные противовоспалительные средства, противоопухолевые препараты, анальгин, левомицетин (вызывает наиболее тяжёлую форму заболевания, которая по статистике возникает в 1 из 30 тыс. курсов лечения левомицетином), мерказолил, карбамазепин, хинин способны вызвать апластическую анемию у некоторых людей;
· Пусковым фактором для болезни могут быть вирусы. Вирусные гепатиты, некоторые виды парвовирусов, ЦМВ, вирус Эпштейна-Барр и ВИЧ обладают способностью вызывать сбой в иммунной системе, вследствие чего она начинает атаковать собственные ткани организма. Например, у 2% пациентов с острым вирусным гепатитом – выявляют апластическую анемию;
· Аутоиммунные заболевания (ревматоидный артрит, СКВ) также может сопровождать аплазия костного мозга;
· Апластическая анемия при беременности, предположительно, также возникает из-за нарушений в иммунной системе.
В более 50% случаев непосредственную причину заболевания не находят, тогда говорят об идиопатической апластической анемии.
Красный костный мозг – основной и самый важный кроветворный орган, в котором происходит образование и созревание элементов крови. Стволовые гемопоэтические клетки в нем дают начало эритроцитам (отвечают за перенос О2 и СО2), лейкоцитам (обеспечивают иммунитет) и тромбоцитам (участвуют в процессах свёртывания крови). Количество гемопоэтических клеток ограничено и постепенно уменьшается на протяжении всей жизни человека.
При апластической анемии происходит массовая гибель стволовых клеток костного мозга, и, как результат, – резкое снижение содержания эритроцитов, тромбоцитов и лейкоцитов в кровеносном русле больного. Недостаток эритроцитов приводит к малокровию, уменьшение количества лейкоцитов вызывает резкое угнетение иммунной системы, уменьшение числа тромбоцитов – причина кровоточивости и, как следствие, повышенного риска неконтролируемого кровотечения.
Результаты последних исследования дают основание полагать, что приобретенная форма заболевания почти всегда – аутоиммунная патология. Ключевой момент в развитии аплазии красного костного мозга – прямое цитотоксическое действие Т-лимфоцитов. Однако причина, по которой Т-лимфоциты начинают распознавать гемопоэтические стволовые клетки как цели для атаки, до сих пор неизвестна. Пусковым фактором могут служить точечные мутации в генах, кодирующих человеческие лейкоцитарные антигены (HLA система), и объясняющий искажённый иммунный ответ (как и при других аутоиммунных патологиях).
Также полагают, что для развития патологии необходима комбинация нескольких факторов – как внутренних (неизвестные дефекты в ДНК стволовых клеток, мутации генов системы HLA, иммунные нарушения), так и внешних (лекарственные препараты, вирусные инфекции, экзотоксины и антигены).
Симптомы, характерные для заболевания:
· Необъяснимая слабость, утомляемость, сонливость;
· Низкая работоспособность;
· Одышка, возникающая даже при легком физическом напряжении;
· Головокружение, головные боли;
· Перебои в сердце, сердцебиение, тахикардия;
· Бледность кожи;
· Удлинение времени свертывания крови, кровоизлияния в мягкие ткани, головной мозг, образование синяков и кровоподтёков при незначительном воздействии, кровотечение из носа, затяжные изнуряющие менструации у женщин;
· Мелкоточечные кровоизлияния в кожу и слизистые оболочки, кровоточивость десен;
· Частые инфекции (дыхательных путей, кожи, слизистых оболочек, мочевыводящих путей), сопровождающиеся лихорадкой;
· Безболезненные язвы на слизистой рта;
· Потеря массы тела, похудание.
Течение болезни может быть постепенным или молниеносным (с быстрым развитием крайне тяжелой анемии, иммунодефицита, нарушениям процессов свертывания крови с соответствующими осложнениями).
Для диагностики используют развернутый анализ крови и гистологическое исследование материала, добытого из костного мозга.
Лабораторные признаки патологии, обнаруживаемые в периферической крови:
· Снижение концентрации эритроцитов и гемоглобина в крови без дефицита железа;
· Снижение концентрации лейкоцитов всех видов в крови больного;
· Дефицит тромбоцитов;
· Низкое количество ретикулоцитов – незрелых форм эритроцитов;
· Увеличение скорости оседания эритроцитов (до 40-60 мм/ч).
В очень тяжелых случаях концентрация гемоглобина падает ниже 20-30 гр/л. Цветовой показатель, уровни сывороточного железа, эритропоэтина обычно в норме или повышены. Количество тромбоцитов ниже нормы, в тяжёлых случаях они полностью отсутствуют.
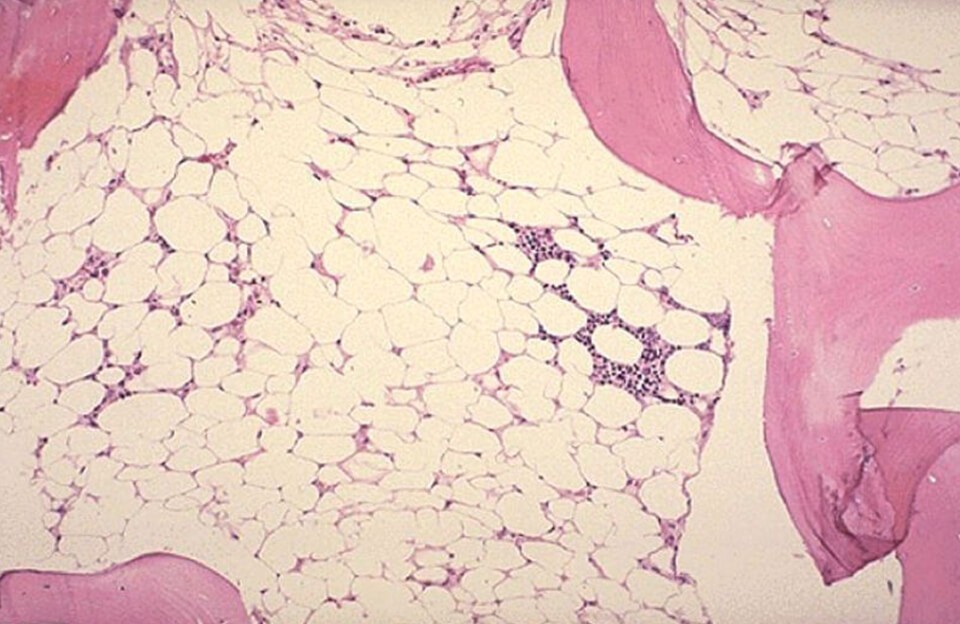
Диагноз подтверждается с помощью биопсии костного мозга. Гистология пунктата показывает большое содержание жира на фоне снижения количества гемопоэтических клеток. Клеточность (общее содержание гемопоэтических стволовых клеток) – ниже 30%, могут отсутствовать мегакариоциты – клетки-предшественники тромбоцитов.
По результатам биопсии различают апластическую анемию лёгкой, тяжёлой и крайне тяжелой степени.
Тяжёлая форма болезни: клеточность – ниже 25%; в периферической крови: нейтрофилов – < 0,5х109/л, тромбоцитов – < 20х109/л, ретикулоцитов – < 20х109/л.
Крайне тяжелая форма болезни: клеточность – ниже 25; в периферической крови: нейтрофилов – < 0,2х109/л, тромбоцитов – < 20х109/л, ретикулоцитов – < 20х109/л.
Легкая форма патологии отклонения от нормы не достигают таких критических показателей.
Тактика лечения зависит от нескольких факторов: от степени тяжести, возраста больного, возможности провести пересадку костного мозга от подходящего донора (в идеале – близкие единокровные родственники больного).
Оптимальным методом лечения тяжелой и крайне тяжелой формы патологии принято считать трансплантацию костного мозга от подходящего донора. Максимальный эффект наблюдается у пациентов молодого возраста. При пересадке костного мозга от подходящего донора 10-летняя выживаемость может достигать 85-90%.
При наличии противопоказаний к трансплантации костного мозга или отсутствии возможности провести её (отсутствие подходящего донора) используется иммуносупрессивная терапия.
Основные препараты, использующиеся для консервативной терапии – антитимоцитарный иммуноглобулин (АТГ) и циклоспорин А.
АТГ – это сыворотка, содержащая антитела против человеческих Т-лимфоцитов, полученная из лошадиной крови. Введение приводит к сокращению популяции Т-лимфоцитов в организме больного, в результате снижается цитотоксическое воздействие на стволовые клетки, улучшается кроветворная функция.
Циклоспорин А – селективный иммунодепрессант, избирательно блокирующий активацию Т-лимфоцитов и высвобождение интерлейкинов, включая интерлейкин-2. В результате блокируется аутоиммунный процесс, разрушающий стволовые клетки, улучшается кроветворная функция. Циклоспорин А не подавляет кроветворную функцию костного мозга и не приводит к тотальной иммуносупрессии.
Показания к назначению глюкокортикостероидов при апластической анемии ограничены профилактикой осложнений при терапии АТГ. Во всех остальных случаях стероидные гормоны имеют посредственную эффективность и являются причиной целого ряда осложнений.
Несмотря на высокую эффективность иммуносупрессивной терапии наиболее радикальное лечение – это пересадка костного мозга. Применение АТГ и циклоспорина А увеличивает риск развития миелодиспластического синдрома и лейкозов, не гарантирует отсутствие рецидивов заболевания.
При неэффективности иммуносупрессивной терапии проводится пересадка костного мозга от донора, не состоящего в родстве с больным. Результаты операции могут быть разными. В 28-94% случаев отмечают 5-летняя выживаемость, в 10-40% случаев происходит отторжение трансплантата.
Пациенты с тяжёлой апластической анемией получают препараты крови в качестве экстренной медицинской помощи. Переливание эритроцитарной массы позволяет быстро компенсировать анемию, а переливание тромбоцитарной массы предупреждает угрожающие жизни кровотечения.
Даже при стойкой ремиссии необходимо проходить периодические обследования (прежде всего, сдавать анализы крови) и по возможности – избегать воздействия негативных факторов.
В период лечения следует помнить, что больные с апластической анемией имеют слабую иммунную систему. Необходимо избегать посещения мест массового скопления людей, регулярно мыть руки, не есть приготовленную в сомнительных местах еду (из-за риска инфекции). Своевременная вакцинация может предупредить некоторые заболевания (в том числе гриппа).
Высокий риск кровотечения или кровоизлияния ограничивает занятия спортом, особенно травмоопасными видами. Несмотря на это, активный образ жизни с регулярными дозированными физическими нагрузками положительно влияют на самочувствие и психоэмоциональное состояние больных.
Сбалансированное питание, богатое витаминами, минералами и белками способствует быстрому восстановлению кроветворения. Не следует употреблять скоропортящиеся продукты (из-за риска возникновения пищевых токсикоинфекций). При лечении циклоспорином А следует ограничить потребление соли.
Оппортунистические инфекции (вирусные, грибковые, бактериальные), обусловленные иммунодефицитом;
Кровотечения, кровоизлияния, нарушения свертывания крови (обусловленные низким числом тромбоцитов);
Осложнения, обусловленные побочными эффектами лекарственных средств для лечения апластической анемии (вторичный гемохроматоз, сывороточная болезнь);
Трансформация болезни в миелодиспластический синдром, лейкемию и другие гематологические заболевания.
До выяснения причин и механизмов развития патологии смертность от апластической анемии достигала 90%. За последние 20-30 лет удалось значительно снизить летальность заболевания. Современные методы лечения значительно улучшили прогноз – 85% пациентов достигают 5-летнего порога выживаемости.
У детей и молодых людей при адекватном лечении прогноз благоприятный и пятилетняя выживаемость достигает 90% (для больных старше 40 лет – 75%).
Эффективные меры профилактики генетически обусловленной апластической анемии отсутствуют в настоящее время.
Профилактика приобретенной апластической анемии заключается в адекватной защите от воздействия токсических веществ, пестицидов и ионизирующего излучения. Следует избегать самостоятельного приема лекарственных средств, особенно длительного и в высоких дозах.
Источник
Апластическая анемия – это крайне неприятное заболевание, способное кроме проблем со здоровьем устроить и финансовые проблемы (лечение очень дорогое). Суть заболевания сводится к нарушению производства крови. На языке медицины – нарушается гемопоэз (кроветворение). Точнее – форменные элементы крови (лейкоциты, эритроциты, тромбоциты) либо производятся в недостаточном количестве, либо их производство прекращается вовсе.
Болезнь достаточно редкая. Сложность лечения связана с тем, что самым простым разделом кроме лекарственной является заместительная трансфузионная терапия эритроцитарной и/или тромбоцитарной массы. Для сложных случаев остается только пересадка костного мозга – дорогая, с целым рядом осложнений операция.
По статистике в зоне риска апластической анемии молодые люди до 20 лет (преобладает вирусная природа патологии), а также люди старше 65-ти лет (накопленные возрастные сбои биохимических процессов как причина).
Внимание. Болезнь имеет высокую летальность – превышает 80%.
Статистику можно посмотреть в видео в конце статьи.
Что такое апластическая анемия
Справочно. Апластическая анемия – это опасное заболевание, при котором нарушается образование клеток крови на уровне костного мозга.
В зависимости от степени выраженности угнетения кроветворения различают две формы:
- гипопластическая анемия (при этой форме функция кроветворения сохранена, но значительно снижена),
- апластическая анемия (полное угнетение кроветворения).
По сути они являются одним и тем же заболеванием разной степени выраженности. Нарушается продукция эритроцитов, тромбоцитов и лейкоцитов.
Клинические проявления могут быть разнообразными и на первых этапах напоминать общее недомогание за счет снижения эритроцитов – возникают слабость, головокружения, могут появиться обмороки.
За счет нехватки тромбоцитов развиваются кровотечения, кожные геморрагические высыпания.
Внимание. Сниженное содержание лейкоцитов в крови сказывается на развитии воспалительных процессов, включая гнойные.
Апластическая анемия – причины
Выделить единственную причину невозможно, так как вызвать апластическую анемию могут различные факторы. Они разительно отличаются друг от друга, но могут приводить к одинаково тяжелым последствиям.
Справочно. Выделяют два основных типа заболевания – врожденный и приобретенный. В первом случае ребенок первоначально содержит генную мутацию, которая приводит к нарушению кроветворной функции. Во втором варианте нарушение выработки клеток крови происходят под влиянием внутренних (эндогенных) или внешних (экзогенных) факторов.
Клиническая картина этих вариантов отличается. Во-первых, врожденные формы часто проявляются на ранних сроках жизни. Во-вторых, они могут сочетаться с аномалиями развития различных органов.
Внимание. В зависимости от вида хромосомной мутации, может наблюдаться снижение производства лишь одного вида кровяных клеток.
При манифестации во взрослом возрасте первыми симптомами могут быть общее недомогание и головокружение, которые являются неспецифичным и возникают при многих заболеваниях. Скорость прогрессирования апластической анемии зависит от выраженности нарушения кроветворной функции.
Апластическая анемия у детей (врожденная)
Врожденные формы включают в себя следующие варианты:
- Синдром Даймонда-Блекфена. При данной патологии происходит нарушение на уровне клеток-предшественников эритроцитов. Фенотипическим симптомом является бледная кожа. Увеличение печени и селезенки не характерно, но может развиваться с течением времени.
- Анемия Фанкони. Наследственное заболевание, которое проявляется на пятом десятке жизни. Возникает острый лейкоз и апластическая анемия. Для данной генной мутации характерны аномалии развития, которые проявляются уже на ранних сроках жизни. В основном это аномалии костной системы (низкий рост, маленький череп, недоразвитие первого пальца верхних конечностей, лучевой кости, тяжелая дисплазия бедра, дополнительное ребро) и неврологический дефицит (аномалии глазных яблок, косоглазие, птоз, нарушение слуха, умственные нарушения развития).
- Синдром Эстрена-Дамешека. Помимо нарушения кроветворения для данных детей характерна определенная внешность – светлые волосы, широко расставленные глаза, курносый нос. Апластическую анемию в этом варианте сопровождает увеличение печени и селезенки.
Приобретенная апластическая анемия
Приобретенные формы различают по факторам, которые вызывают апластическую анемию.
- Внешние (экзогенные) факторы:
- Медикаментозное влияние – прием сульфаниламидов, антибактериальных средств (тетрациклин, левомицитин, стрептомицин), средств для лечения туберкулеза (изониазид, ПАСК), анальгина, цитостатиков.
- Воздействие химических агентов – наиболее опасны нефтепродукты, бензольные производные, ртуть.
- Радиоактивное воздействие.
- Инфекции. Наиболее опасными являются вирус, вызывающий гепатит С, цитомегаловирус, герпес-вирус. Чаще всего они оказывают выраженное повреждающее действие лишь при активно перенесенном заболевании.
- Внутренние (эндогенные) факторы:
- Аутоиммунное поражение костного мозга. Чаще наблюдается в пожилом возрасте.
- Эндокринное влияние. Выявлена связь с нарушением функции щитовидной железы, и с заболеваниями яичников у женщин.
Внимание. Данное разделение условное, так как даже экзогенные факторы могут влиять на костный мозг опосредованно через запуск аутоиммунной агрессии.
Апластическая анемия – механизм развития
В настоящее время существует три теории, объясняющих механизм развития апластической анемии. Каждая из них получила подтверждение в ходе исследований.
Внимание. В некоторых случаях ни одна из имеющихся теорий не может объяснить возникновение заболевания. При таком варианте используют название «идиопатическая апластическая анемия».
Поэтому официально теории приняты, но изучение механизмов возникновения апластической анемии продолжается.
Теории патогенеза (возникновения) апластической анемии:
- аутоиммунная;
- стромальная;
- преждевременный апоптоз.
Аутоиммунная теория
Справочно. В аутоиммунной теории за основу берется развитие иммунного ответа к клеткам костного мозга.
Возникла она в результате исследования материала биоптата костного мозга после развития апластической анемии.
В большом количестве случаев ученые увидели присутствие клеточного иммунитета (моноциты, Т-киллеры), а также факторов воспаления – фактор некроза опухолей, интенферон альфа и гамма.
После более детального изучения стало понятно, что скапливаются они из-за генной мутации. В результате нарушения работы гена PIG-A возникает дефицит специального гликопротеина, который необходим для того, чтобы снижать активность системы комплемента, входящей в состав иммунной системы.
В результате этой поломки защита собственных клеток костного мозга слабеет, они начинают восприниматься, как чужеродные и развивается аутоиммунная реакция. В зависимости от количества поврежденных клеток степень выраженности симптомов разнится.
Важно. Чем больше вовлечено ткани, тем более агрессивная анемия наблюдается у пациента.
Стромальная теория
Нормальное функционирование механизма кроветворения во многом зависит от стромы, то есть специального соединительнотканного основания, в котором находятся клетки костного мозга.
Строма отвечает за выработку специальных веществ (интерлейкины и факторы стволовых клеток), которые необходимы для направления недифференцированных молодых клеток по пути образования эритроцитов, тромбоцитов или лейкоцитов.
Стимулируется эта выработка эритропоэтином.
В случае нарушения выделения факторов роста на уровне стромы возникают низкодифференцированные клетки, которые не могут выполнять свои функции. Они не достигают дифференцировки, достаточной для определения в крови при анализе.
Справочно. Подтверждается данная теория при биопсии костного мозга – определяются предшественники клеток в большом количестве. А также определяется повышенный уровень эритропоэтина в крови. Такие изменения характерны не более чем для 20% случаев.
Теория преждевременного апоптоза
Термином апоптоз в медицине обозначают естественный процесс гибели клетки, когда она в полном объеме выполнила свою функцию. Происходит это во всех тканях организма. После определенного времени клетки подвергаются мутации, начинают восприниматься организмом, как старые, и удаляются.
В норме процесс представляет собой защитный механизм, который способствует обновлению тканей. Мутировавшие клетки могут переродиться в опухолевый процесс, и функция апоптоза – не допустить этого. Однако, если этот процесс начинает происходить раньше времени, возможно чрезмерное удаление клеток ткани. При недостаточном синтезе новых клеток этот процесс приводит к нарушению функции.
Справочно. Причиной слишком раннего удаления здоровых и молодых клеток является мутация гена, отвечающего за выработку протеина Р-450.
Изучение механизмов развития апластической анемии до сих пор является зоной научных интересов исследователей всего мира. Однако это может внести вклад в лечение заболевания в будущем, но никак не сказывается на современных пациентах.
Дело в том, что на сегодняшний момент самым эффективным методом лечения апластической анемии остается пересадка костного мозга. Для замедления процесса используют стероидные гормоны.
Внимание. Ни один из методов лечения не учитывает патогенез процесса.
Апластическая анемия – симптомы
Учитывая угнетение выработки кровяных телец, выделяют следующие синдромы апластической анемии:
- Анемический (возникает за счет недостаточности эритроцитов и, соответственно, гемоглобина);
- Геморрагический (возникает в результате нехватки тромбоцитов, которые в норме останавливают кровотечение, образовывая тромботические массы);
- Токсико-инфекционный (недостаточность лейкоцитов – клеток иммунитета, в результате чего даже незначительная инфекция может развиться до гнойного процесса).
Клиническая картина каждого синдрома отличается. Может наблюдаться как сочетание всех синдромов, так и превалирование одного.
- При анемическом синдроме преобладают:
- повышенная утомляемость;
- головокружение;
- тошнота;
- одышка даже при минимальной нагрузке;
- тахикардия;
- потемнение в глазах.
- При геморрагическом:
- Множественные, легко образующиеся синяки;
- Излишне замедленная остановка любого кровотечения;
- Возникновение носовых кровотечений;
- Обильные месячные;
- Кровоточивость из десен;
- Возникновение специфических высыпаний – тромбоцитопеническая пурпура (является по факту пропитыванием кожи кровью).
- При токсико-инфекционном:
- Тяжелое течение легких инфекционных заболеваний;
- Медленное заживление ран, часто с нагноением.
Эти признаки более характеры для развития апластической анемии во взрослом возрасте. Эти пациенты могут анализировать свое состояние и предъявлять жалобы на приеме у врача.
Апластическая анемия у детей имеет свои особенности. При возникновении заболевания в совсем раннем возрасте они не могут объяснить свои ощущения, но существуют так называемые стигмы (или особенности), которые позволяют заподозрить различные наследственные формы анемии и провести генетическое тестирование.
Обычно у детей при наличии апластической анемии отмечаются следующие особенности:
- маленькая голова,
- укорочение первого пальца верхних конечностей,
- дисплазия тазобедренного сустава при синдроме Фанконе,
- специфический фенотип (светлые волосы, курносый нос, широко поставленные глаза при синдроме Эстрена-Дамешека),
- гепато- и спленомегалия.
Апластическая анемия – диагностика
Сбор жалоб и осмотр пациента является первым звеном в постановке диагноза и дает врачу первоначальный вектор для дальнейшего
подтверждения диагноза.
Самым важным этапом является инструментальная и лабораторная диагностика, которая включает в себя:
- Стернальную пункцию костного мозга;
- Трепанобиопсию;
- биохимический анализ крови;
- общий анализ крови.
Справочно. Стернальная пункция представляет собой забор материала из грудины с помощью специальной иглы. Элементы костного мозга помещают на стекла и изготавливают миелограмму, по которой могут сказать, какие клетки содержит костный мозг, соответствует ли их количественный и качественный состав норме.
С помощью трепанобиопсии производят забор костного мозга из крыла подвздошной кости. Данный метод помогает помимо анализа клеток (цитологического) провести гистологический анализ. Это помогает получить информацию о строме, ее представленности, а также соотношении желтого (неактивного) и красного костного мозга.
Биохимический анализ позволяет получить информацию о:
- содержании сывороточного железа (необходимо для подтверждения анемии),
- эритропоэтина (повышается при недостаточной выработке факторов роста стромой), – антителах к вирусам (которые могут быть причиной заболевания),
- С-реактивного белка (высокоспецифичный показатель воспалительного процесса).
Общий анализ крови показывает количественное содержание клеток крови (эритроциты, тромбоциты, лейкоциты), а также оценивает качественные характеристики клеток.
Апластическая анемия – лечение
На первых этапах апластическую анемию стараются лечить глюкокортикоидами и цитостатиками. Выбран данный метод в связи с преобладанием аутоиммунной агрессии по отношению к костному мозгу. Данный подход приносит положительные результаты, однако часто они являются временными.
Для симптоматического лечения синдромов могу применяться антибиотики, препараты для коррекции артериального давления, ферментные препараты.
Иммуносупрессивную терапию в качестве единственного лечения применяют лишь в начале апластической анемии. Далее стараются комбинировать с цитостатиками и препаратами для симптоматического лечения в зависимости от преобладания синдромов.
Справочно. На данный момент наиболее эффективным лечением апластической анемии является пересадка (трансплантация) костного мозга.
К сожалению, она не всегда проходит гладко. Выделяют несколько наиболее частых осложнений процедуры.
Осложнения пересадки костного мозга
К основным осложнениям относят следующие:
- инфекционные осложнения. Как и при любом оперативном вмешательстве существует риск нагноения места пункции. У пациентов с апластической анемией снижен иммунитет, поэтому даже при должном соблюдении правил асептики и антисептики не исключено появление данного осложнения.
- Отторжение трансплантата. Любой пересаженный орган воспринимается иммунными клетками организма, как чужеродный. Возникает иммунная реакция с попыткой уничтожить инородную ткань.
- Реакция трансплантата против организма пациента. При пересадке стволовых клеток возникает образование клеточного иммунитета донора. Новые клетки начинают агрессивно себя вести по отношению к лимфоцитам пациента. Этот процесс приводит к образованию высыпаний, нарушениями работы сердечно-сосудистой системы и желудочно-кишечного тракта.
- отказ работы жизненно важных органов. Возникает из-за массивного стресса, оказываемого на организм процессом пересадки костного мозга, а также приемом большого количества препаратов.
Несмотря на возможность тяжелых осложнений, трансплантация костного мозга остается самым эффективным методом лечением апластической анемии.
Справочно. Для минимизации рисков осложнений используются различные препараты до и после процедуры.
Апластическая анемия – прогноз
Врожденные формы часто сложнее поддаются лечению, так как костный мозг первоначально генетически не полноценен. Так, при анемии Фалкони, медикаментозное лечение протекает крайне сложно, а пересадка костного мозга может иметь противопоказания из-за аномалий развития.
Справочно. Приобретенные виды анемии легче поддаются лечению, особенно в случае устранения повреждающего фактора, если он был определен. Успех лечения во многом зависит и от времени выявления. Ранняя диагностика существенно повышает шансы на излечение.
Кроме того, выраженность симптомов может варьировать в зависимости от выраженности повреждения костного мозга. При медленно текущем процессе с минимальными повреждениями, даже медикаментозное лечение протекает легче и приносит существенное облегчение.
Источник
