Аутоиммунная гемолитическая анемия цирроз
Что такое аутоиммунная гемолитическая анемия?
Аутоиммунная гемолитическая анемия — это аутоиммунное заболевание, характеризующееся преждевременным разрушением здоровых эритроцитов (клеток крови) аутоантителами.
Аутоиммунные заболевания возникают, когда естественная защита организма от чужеродных организмов (например, лимфоцитов, антител) разрушает здоровые ткани по неизвестным причинам. Обычно эритроциты имеют продолжительность жизни около 120 дней, прежде чем будут удалены селезенкой.
Медицинским термином для низких уровней циркулирующих эритроцитов является анемия. Анемия может вызывать усталость, бледный цвет кожи, пожелтение кожи и белых глаз (желтуха) и отток крови в моче (гемоглобинурия), что придаст моче темно-коричневый цвет.
Признаки и симптомы
Симптомы аутоиммунной гемолитической анемии обычно развиваются медленно в течение периода от нескольких недель до месяцев, но в некоторых случаях могут развиваться внезапно в течение нескольких дней.
Конкретные симптомы, которые возникают, могут варьироваться от одного человека к другому и могут зависеть от скорости возникновения, скорости разрушения здоровых эритроцитов и наличия основного расстройства.
Некоторые люди, особенно те, у кого постепенно развивается анемия, могут не иметь каких-либо явных симптомов. У пострадавших людей могут в конечном итоге развиться:
- ненормальная бледность кожи;
- усталость;
- затрудненное дыхание при физической нагрузке;
- головокружение;
- учащенное сердцебиение.
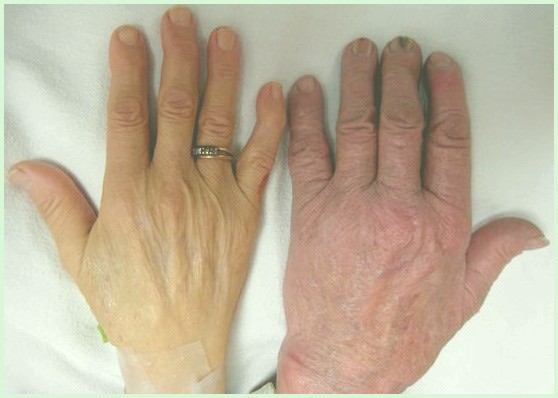
Желтизна кожи и белых глаз (желтуха) и увеличение селезенки (спленомегалия) также часто встречаются у людей с аутоиммунной гемолитической анемией.
Спленомегалия может привести к тому, что у пострадавшего появится вздутие живота или ощущение полного отека в животе. Иногда у некоторых людей может происходить увеличение печени (гепатомегалия).
У людей с тяжелыми случаями, особенно с быстрым (острым) началом, могут развиться более серьезные осложнения, в том числе потеря сознания (обмороки), боль в груди (стенокардия), аномально быстрое сердцебиение (тахикардия) и сердечная недостаточность.
Причины аутоиммунной гемолитической анемии
Причина аутоиммунной гемолитической анемии обычно неизвестна (т. е. идиопатическая). Однако расстройство может возникать как часть более крупного расстройства, эти случаи известны как вторичная аутоиммунная гемолитическая анемия.
Аутоиммунная гемолитическая анемия является аутоиммунным расстройством — расстройством, при котором естественная защита организма от вторжения организмов (например, лимфоцитов, антител) разрушает здоровые ткани по неизвестным причинам. Антитела ошибочно атакуют здоровые эритроциты, вызывая преждевременное разрушение клеток, состояние, называемое гемолизом.
Антитела (которые также известны как иммуноглобулины) представляют собой специализированные белки, которые связываются с инвазивными организмами и вызывают их разрушение. Существует пять основных классов антител – IgA, IgD, IgE, IgG и IgM.
Большинство случаев данной анемии происходят из-за антител IgG, которые по ошибке атакуют здоровые эритроциты. Реже антитела IgM или IgA вызывают расстройство. Когда антитела атакуют здоровые ткани, их можно назвать аутоантителами.
Несколько основных расстройств связанных с гемолитической анемией, включают другие аутоиммунные расстройства, такие как системная красная волчанка и расстройства, характеризующиеся перепроизводством лейкоцитов (лимфопролиферативные расстройства), такие как лейкемия или лимфома.
Вторичная аутоиммунная гемолитическая анемия также может возникнуть как побочный эффект некоторых лекарств.
Затронутые группы населения
Гемолитическая анемия поражает мужчин и женщин в равных количествах. По оценкам, аутоиммунные гемолитические анемии затрагивают 1-3 человека на 100 000 населения в целом. У людей любого возраста, включая детей, может развиться данная болезнь, однако чаще она встречается у взрослых с пиковой заболеваемостью в возрасте 50-70 лет.
Диагностика
Диагноз гемолитической анемии можно заподозрить на основании тщательной клинической оценки, детальной истории болезни, выявления характерных симптомов и различных анализов, таких как анализы крови, которые измеряют гемоглобин и гематокрит. Гемоглобин — белок в красных кровяных клетках, который переносит кислород. Гематокрит — процент от общего объема крови, занимаемый эритроцитами.
Анализы крови могут также показать повышенный уровень незрелых эритроцитов (ретикулоцитов), который происходит, когда организм вынужден производить дополнительные эритроциты, чтобы восполнить те, которые преждевременно разрушились. Некоторые люди с гемолитической анемией имеют повышенный уровень билирубина в крови (гипербилирубинемия). Билирубин — желтоватый продукт, образующийся при метаболизме гемоглобина в печени.
Когда предполагается, что анемия вызвана дисфункцией иммунной системы (т. е. аутоиммунная гемолитическая анемия), могут проводиться специализированные тесты, такие как проба Кумбса. Этот анализ проводиться для обнаружения антител, которые действуют против эритроцитов. Образец крови берется и затем подвергается воздействию реагента Кумбса. Если эритроциты слипаются в присутствии реагента то, это указывает на наличие у пациента заболевания.
Лечение аутоиммунной гемолитической анемии
Лечение аутоиммунной гемолитической анемии является симптоматическим и поддерживающим. Пострадавших людей обычно лечат кортикостероидными препаратами, такими как преднизон, и обычно они контролируют болезнь при правильном лечении. Первоначально может быть рекомендована высокая доза этих лекарств с последующим постепенным снижением дозы в течение следующих нескольких недель или месяцев.
Людям, которые не отвечают на терапию кортикостероидами или развивают непереносимые побочные эффекты, могут быть назначены иммунодепрессанты или хирургическое удаление селезенки (спленэктомия). Иммуносупрессивные лекарственные средства, такие как циклофосфамид, представляют собой лекарственные средства, которые подавляют или блокируют иммунную систему, и помогают некоторым людям с гемолитической анемией, которые не реагируют на преднизон или спленэктомию.
Спленэктомия обычно используется у людей с тяжелыми случаями, которые требуют постоянного преднизона для контроля. У пациентов с основным нарушением лечение этого расстройства обычно приводит к заметному улучшению анемии.
Ритуксимаб — это моноклональное антитело, искусственно созданное антитело, которое нацелено на определенные лейкоциты, которые создают антитела, которые преждевременно разрушают эритроциты. Ритуксимаб оказался полезным для некоторых пациентов с аутоиммунной гемолитической анемией, которые не реагировали на преднизон. Уровень ответов может достигать 80% у взрослых и 60% у детей. Ритуксимаб может быть использован до спленэктомии или может использоваться у людей, у которых наблюдается рецидив после спленэктомии.
Переливание эритроцитов также может быть необходим для поддержания надлежащего уровня эритроцитов у людей с тяжелыми случаями. Этот поддерживающий метод обеспечивает временное облегчение состояния, но не лечит основную причину расстройства.
Профилактика
Предотвратить аутоиммунную гемолитическую анемию не возможно, но врачи могут помочь людям, у которых есть вирусная инфекция или которые используют определенные лекарства, чтобы болезнь не развивалась.
Тяжелая анемия может усугубить многие проблемы, такие как болезни сердца и легких. Люди должны обратиться к врачу, если они испытывают какие-либо симптомы, которые могут указывать на гемолитическую анемию.
Разделяют идиопатические аутоиммунные анемии и вторичные аутоиммунные анемии.
Вторичные аутоиммунные гемолитические анемии развиваются на фоне следующих заболеваний: ревматоидного артрита, склеродермии, синдроме Сьегрена, лимфопролиферативных заболеваниях, других злокачественных заболеваниях, грибковых инфекциях, тимомах, язвенном колите, В12-дефицитной анемии, болезни Кавасаки, первичном биллиарном циррозе печени.
При отсутствии причин для аутоиммунной гемолитической анемии верифицируют идиопатическую АИГА.
АИГА — гемолитическая анемия, возникающая в результате изменения функции иммунной системы организма, вследствие чего против собственных неизмененных антигенов эритроцитов вырабатываются AT.
Этиология.
Причины развития АИГА, как и многих других аутоиммунных заболевании, не ясны. Обсуждается воздействие некоторого триггерного агента (возможно, вируса или микроорганизма), вследствие которого происходит срыв иммунологической толерантности к собственному антигену.
Патогенез.
Характер патогенетических механизмов при АИГА зависит, главным образом, от характера AT, вырабатывающихся против собственных неизмененных антигенов эритроцитов.
Нагруженные антителами (агглютининами или преципитинами) эритроциты разрушаются в селезенке, печени и костном мозге, гемолиз осуществляется по внутриклеточному типу.
AT класса гемолизинов при фиксации на поверхности эритроцита вызывают гибель клетки внутри сосуда.
Проявления заболевания будут в первую очередь определяться механизмом разрушения эритроцитов — внутриклеточным или внутрисосудистым.
Классификация AT: по механизму действия (агглютинины, гемолизины, преципитины); по температурному оптимуму активности (тепловые, холодовые); по серологической характеристике (полные, неполные).
Клиническая картина.
Наиболее частым вариантом является АИГА, обусловленная неполными тепловыми агглютининами (анемия с внутриклеточной гибелью эритроцитов).
Жалобы вызваны развитием гипоксии тканей (резкая слабость, сонливость, обмороки, одышка, сердцебиение).
Часто отмечается субфебрильная или фебрильная температура тела.
У некоторых больных, особенно пожилых, возможно развитие анемической прекомы и комы.
У больных с поражением сердца высока вероятность острой левожелудочковой недостаточности.
При осмотре: резкая бледность кожи и видимых слизистых оболочек. Образование из НЬ разрушающихся эритроцитов большого количества непрямого билирубина ведет к развитию желтухи.
У 2/3 больных выявляется увеличение селезенки и более чем у половины больных — печени.
При АИГА, обусловленной образованием AT класса гемолизинов (анемия с внутрисосудистой гибелью эритроцитов), больные жалуются на боли в поясничной области, повышение температуры тела, появление мочи черного цвета, а также предъявляют жалобы, связанные со снижением содержания НЬ (анемический синдром).
Кожа и видимые слизистые оболочки бледные.
Увеличение селезенки встречается нечасто, и размеры ее невелики. Диагностика.
Сочетание анемического синдрома, желтушности кожи и (или) слизистых оболочек, а также увеличение селезенки должно заставить врача в первую очередь заподозрить АИГА с внутриклеточным механизмом разрушения эритроцитов.
Такое предположение требует незамедлительного исследования периферической крови с обязательным определением количества ретикулоцитов.
В крови отмечается значительное снижение содержания эритроцитов и НЬ. Цветовой показатель близок к единице, СКО эритроцитов находится в пределах 80—95 фл (нормоцитоз).
Содержание ретикулоцитов значительно увеличено.
В тяжелых случаях возможно появление в периферической крови нормобластов.
Количество лейкоцитов и тромбоцитов находится в пределах нормы. Лейкоцитарная формула не изменена, хотя могут наблюдаться и лейкемоидные реакции по нейтрофильному типу.
СОЭ значительно увеличена. При исследовании мочи может быть зафиксировано появление уробилина.
Кал у больных с АИГА с внутриклеточным механизмом разрушения эритроцитов приобретает более темную, по сравнению с обычной, окраску.
Для верификации диагноза АИГА с внутриклеточным механизмом разрушения эритроцитов используют тест, определяющий наличие AT на поверхности эритроцитов — положительная прямая проба Кумбса (проба Кумбса: антиглобу- линовую сыворотку кролика, полученную путем его сенсибилизации у-глобулином человека, добавляют к исследуемым эритроцитам.
Сыворотка не вызывает агглютинацию нормальных отмытых эритроцитов, но при присоединении антиглобулиновой сыворотки к эритроцитам, содержащим на своей поверхности неполные AT, белковые молекулы укрупняются и эритроциты агглютинируют).
Более чувствительная проба — реакции агрегатогемагтлютинации.
При появлении у больного мочи черного цвета, боли в поясничной области и анемических жалоб необходимо предположить наличие АИГА с внутрисосудистым вариантом разрушения эритроцитов.
Это предположение усиливается при выявлении нормохромной (нормоцитарной) анемии с увеличением количества ретикулоцитов.
При исследовании мочи выявляется свободный гемоглобин, а при исследовании мочевого осадка отмечается увеличение количества клеток эпителия почечных канальцев с включениями гемосидерина.
Патоморфология костного мозга: гиперплазия красного ростка кроветворения различной выраженности.
При тяжелых гемолитических кризах костный мозг способен увеличивать продукцию эритроцитов в 6—8 раз.
Дифференциальная диагностика.
АИГА с внутриклеточным механизмом разрушения эритроцитов необходимо дифференцировать от других анемических состояний, сопровождающихся увеличением количества ретикулоцитов: постгеморрагической анемией; ЖДА на фоне терапии препаратами железа; В12ДА на фоне терапии витамином В12; ФДА на фоне терапии фолиевой кислотой.
Для разграничения этих состояний большое значение имеет внимательное изучение анамнеза и анализ имеющихся документальных данных о течении заболевания. Важным подспорьем является проба Кумбса, АИГА с внутрисосудистым разрушением эритроцитов необходимо дифференцировать от ПНГ (отрицательные сахарозная проба и проба Хема при АИГА и положительные — при ПНГ).
Лечение.
АИГА требует незамедлительного лечения.
Препараты первой линии — ГКС — преднизолон внутрь в дозе 1-2 мг/кг массы тела в сутки.
Признаками эффективности лечения являются прекращение падения НЬ, уменьшение ретикулоцитоза, нормализация температуры тела, улучшение самочувствия больного.
Гемоглобин начинает повышаться на 3—4-й день от начала лечения.
После нормализации показателей периферической крови дозу преднизолона начинают медленно снижать до полной отмены.
Рекомендуемая доза преднизолона для пациентов старше 70 лет с признаками остеопороза — 0,6 мг/кг веса/день.
Если в силу каких-либо обстоятельств больной не может получать ГКС перорально, то при парентеральном введении их дозу необходимо увеличить.
Если преднизолон вводят в/м, его доза должна быть увеличена в два раза, а при в/в введении — в три раза по сравнению с дозой, получаемой перорально.
Следует также учитывать, что при парентеральном введении преднизолон действует кратковременно.
Использование ГКС-терапии позволяет получить стойкий эффект у половины больных.
У остальных лечение преднизолоном дает временный эффект; снижение дозы или полная отмена препарата приводят к развитию рецидива заболевания.
Такие больные нуждаются в постоянном приеме поддерживающей дозы преднизолона или проведении повторных курсов терапии.
Спленэктомия в качестве второй линии терапии показана в следующих случаях:
1) отсутствие эффекта на преднизолон;
2) зависимость от преднизолона в дозе 20 мг/день и более;
3) ранний рецидив после отмены преднизолона.
При АИГА с внутрисосудистой гибелью эритроцитов эффект от спленэктомии меньше и может быть отсроченным.
Терапевтическое действие в этом случае связано с выключением селезенки из процесса синтеза AT.
Для пациентов старше 70 лет и детей спленэктомия не является терапией второй линии в связи с высоким риском развития иммунодефицита и инфекционных осложнений.
Терапия третьей линии.
В случае неэфективности спленэктомии назначаются иммунодепрессанты.
В последние годы получен хороший эффект при лечении АИТА циклоспорином А (сандиммун).
Начальная доза 2,5 мг/кг х 2 раза в день в течение 6 дней с последующим снижением дозы циклоспорина до 3 мг/кг день и добавлением 5 мг/день преднизолона.
Применение циклоспорина А позволяет получать длительные и стойкие ремиссии заболевания.
Микофенолат также показал свою эффективность в терапии АИГА.
Ритуксимаб (Мабтера) 375 мг/м2 1 раз в нед — в течение 4 нед. Некоторые исследователи показывают 100% ответа.
Имуран (азатиолрин — 1,5 мг/кг/день в течение 3 мес) или малые дозы циклофосфамида (2 мг/кг/день х 3 мес). Ответ наблюдается у 50% пациентов.
Высокие дозы циклофосфана (50 мг/кг в день х 4 дня) индуцировали продолжительные ремиссии (15 мес) у 66% пациентов.
Прогноз.
При адекватной терапевтической тактике ведения прогноз у больных с АИГА благоприятный.
Профилактика. Эффективной профилактики АИГА не существует.
Под термином «гемолитическая анемия» подразумевается группа наследственных или приобретенных заболеваний, которым свойственно повышенное внутрисосудистое или внутриклеточное разрушение эритроцитов. Гемолитическая анемия может быть иммунной, идиопатической и аутоиммунной. Но чаще всего встречаются именно аутоиммунные гемолитические анемии (АГА) – 1 случай на 75 тысяч населения.
Все аутоиммунные гемолитические анемии включают заболевания, характеризующиеся образованием антител к собственным антигенам эритроцитов.
Причины аутоиммунных гемолитических анемий
Как и любое аутоиммунное заболевание, аутоиммунная анемия является результатом сбоя работы иммунной системы. Причиной такого сбоя может послужить мутация генов и повреждение цепочки ДНК под влиянием различных вредоносных факторов.
Как известно, ДНК – это молекула, которая обеспечивает хранение и передачу информации, а потому анемия может передаваться по наследству. Именно поэтому профилактика и успешное лечение аутоиммунной гемолитической анемии, прежде всего, заключаются в оптимизации работы иммунной системы.
Классификация аутоиммунных гемолитических анемий
В зависимости от причины развития аутоиммунная гемолитическая анемия может быть симптоматической и идиопатической. В первом случае она развивается как осложнение какого-либо иного заболевания. Во втором случае явной причины развития заболевания нет.
В зависимости от антител, атакующих эритроциты, данная болезнь классифицирует на 4 подвида. Итак, бывает аутоиммунная гемолитическая анемия:
- С неполными тепловыми агглютининами: когда эритроциты атакуют иммуноглобулины A и G – молекулы белкового происхождения. Заболевание, как правило, развивается быстро и остро. Основные симптомы: повышение температуры, общая слабость, одышка, боль в пояснице. Разрушение крови происходит в основном в селезенке;
- С тепловыми гемолизинами: разрушение эритроцитов происходит под действием гемолизинов (клеток, повреждающих клетки крови) в кровеносных сосудах. На фоне этого вида болезни повышается свертываемость крови, в результате чего у пациента образуются микротромбы, часто развивается острая почечная недостаточность;
- С полными холодовыми антителами: плохая переносимость холода – главный признак этой формы заболевания. Также больные жалуются на быструю утомляемость, слабость, одышку. Летом болезнь может вообще не давать о себе знать, но обостряется в холодное время года. Наиболее часто страдают люди преклонного возраста;
- С двухфазными антителами-гемолизинами – очень редкий вид анемии, для которого характерно закрепление двухфазного гемолизина на поверхности эритроцита. Данный процесс возможен только при холоде, поэтому гемолизу всегда предшествует переохлаждение.
Хроническая форма аутоиммунной гемолитической анемии обычно протекает практически бессимптомно, периодически обостряясь. На фоне ремиссии при пальпации определяется увеличение селезенки и печени, иногда возникает желтуха.
Развернутый анализ крови у больных АГА показывает увеличение СОЭ, нормальный уровень тромбоцитов, повышенный или нормальный гемоглобин. При обострении хронической анемии или при болезни в острой форме количество лейкоцитов увеличивается (в стадии ремиссии этот показатель находится в норме).
Диагностировать аутоиммунную гемолитическую анемию довольно сложно, для этого проводят ряд специфических диагностических исследований.

Лечение аутоиммунной гемолитической анемии
Лечение аутоиммунной гемолитической анемии проводят глюкокортикостероидными препаратами, чаще всего это преднизолон. Его назначают в суточной дозе 40-60 мг в течение трех недель. Если этот курс не приводит к ремиссии, дозировку медикамента увеличивают в два раза. К признакам ремиссии относят увеличение содержания в крови ретикулоцитов, после чего либо повышается и уровень гематокрита, либо хотя бы намечается тенденция к положительной динамике. Резистентность к такой схеме лечения считается плохим прогностическим признаком.
Поскольку прямой антиглобулиновый тест длительный период может оставаться положительным, даже несмотря на явные признаки улучшения состояния, больным рекомендуется проводить непрямой антиглобулиновый тест– он чутко реагирует на эффективность терапии.
В стадии ремиссии заболевания, а так же с целью предупреждения рецидивов суточную дозу кортикостероидов постепенно снижают на 2,5-5 мг в сутки и до полной отмены.
При отсутствии желаемого эффекта от терапии препаратами этой группы, а также при повышенной устойчивости к гормональным средствам пациентам, течение болезни у которых практически не поддается медикаментозной коррекции и сопровождается частыми рецидивами, рекомендуют спленэктомию – хирургическую операцию по удалению селезёнки. Такая радикальная мера позволяет значительно улучшить качество их жизни.
В случаях отсутствия результата от применения кортикостероидов больным также могут назначить иммуносупрессирующие медикаменты, к примеру, 6-меркантопурин (из расчета 2 мг на 1 кг веса в сутки) или азатиоприн (1,5-3,0 мг на кг/сутки).
При тяжелых гемолитических кризах, угрожающих жизни человека, показана инфузионная терапия: гемодез, индивидуально подобранная эритроцитарная масса. В некоторых случаях переливают плазму крови, замороженные или отмытые эритроциты. Иногда при аутоиммунной гемолитической анемии прибегают к методу плазмафереза и гемодиализу.
Стоит отметить, что кортикостероидные препараты проявляют малую терапевтическую эффективность при лечении гемолитических анемий, вызванных холодовыми антителами. По этой причине основу профилактики этой формы заболевания составляет предупреждение переохлаждения организма. При тяжелом течении болезни назначают иммуносупрессирующие лекарства (хлорбутин, циклофосфан и др.).
Лечение аутоиммунной гемолитической анемии в хронической стадии проводят преднизолоном в суточной дозировке 20-25 мг. По мере улучшения показателей крови дозу постепенно снижают до поддерживающей, которая составляет 5-10 мг/сутки.
Несмотря на довольно высокий уровень развития современной медицины, лечение всех видов гемолитических анемий – сложный процесс, а диагноз, к сожалению, часто неблагоприятный.
