Аутоиммунная гемолитическая анемия при хроническом лимфолейкозе
Аутоиммунные осложнения при хроническом лимфолейкозе – аутоиммунная гемолитическая анемия (АИГА)
Аутоиммунные осложнения возникают при хроническом лимфолейкозе (ХЛЛ) значительно чаще, чем при других лимфопролиферативных процессах. Аутоиммунная гемолитическая анемия (АИГА) развивается в течение заболевания у 10—25 % больных хроническом лимфолейкозе, что в 8 раз превышает ее частоту при неходжкинских лимфомах.
С. Engelfriet и соавт. в большой работе об аутоиммунной гемолитической анемии показали, что хронический лимфолейкоз является самой частой причиной ее развития. При хроническом лимфолейкозе частота аутоиммунного гемолиза в 2 раза выше, чем при системной красной волчанке, занимающей второе место среди заболеваний, при которых часто развивается аутоиммунная гемолитическая анемия. Положительный антиглобулиновый тест (проба Кумбса) выявляется еще чаще—у 20—35 % больных.
Аутоиммунные осложнения могут развиться в любом периоде болезни. Имеются наблюдения, в которых аутоиммунная гемолитическая анемия явилась первым симптомом хронического лимфолейкоза. Так же, как инфекции, аутоиммунные процессы чаще возникают у больных с развернутой клинико-гематологической картиной ХЛЛ. Среди больных с аутоиммунными анемиями и тромбоцитопениями мы наблюдали 72 % больных с выраженными клинико-гематологическими проявлениями ХЛЛ.
Эти данные подтверждаются наблюдениями других исследователей. Так, Т. Hamblin и соавт. обнаружили положительную пробу Кумбса у 2,9 % больных в стадии А, у 10,5 % в стадии В и у 18,2 % при прогрессировании заболевания. В наблюдениях F. Mauro и соавт., включивших 1203 больных ХЛЛ, 90 % больных с АИГА имели признаки прогрессирования. Частота АИГА в их наблюдениях достоверно коррелировала с высотой лейкоцитоза.
Аутоиммунный гемолиз эритроцитов может иметь характер остро и бурно развившегося гемолитического криза, сопровождаясь повышением температуры тела, появлением желтушного окрашивания кожи и темной окраской мочи, повышением содержания непрямого билирубина в сыворотке крови. Однако такие кризы составляют небольшую часть от общего количества случаев аутоиммунного гемолиза. Нередко аутоиммунный гемолиз развивается постепенно, и анемия выражена не так значительно, как у больных с острым гемолитическим кризом.
В подобных случаях, как правило, в костном мозге нет значительного увеличения эритрокариоцитов и заметного ретикулоцитоза крови. Иногда ретикулоцитоз отсутствует и при бурных проявлениях гемолитической анемии, особенно если гемолизу подвергаются эритрокариоциты. Антитела, обнаруживаемые на эритроцитах при АИГА, чаще относятся к классу IgG и только у 10—15 % больных — к классу IgM. Показано, что при обнаружении IgG прогноз значительно лучше. Значительно реже, чем АИГА, развивается анемия, обусловленная парциальной красноклеточной аплазией (ПКА).
По данным Т. Hamblin и соавт., ПКА развивается в 1 %, по данным G. Chikkappa и соавт. — в 6 % случаев хронического лимфолейкоза. ПКА характеризуется тяжелой анемией со снижением гематокрита до 25—20 %, отсутствием ретикулоцитов в крови и практически полным отсутствием эритрокариоцитов в костном мозге. Нет достаточного количества исследований, позволяющих установить причину развития ПКА при ХЛЛ.

Иммунная тромбоцитопения встречается реже, чем АИГА, всего у 2-3 % больных хроническим лимфолейкозом. Она, тем не менее, может представлять большую опасность, чем АИГА, из-за возможных и действительно часто имеющих место жизненно опасных кровотечений или кровоизлияний в головной мозг, служащих причиной смерти больных. Аутоиммунная тромбоцитопения может развиться как самостоятельное осложнение, но часто она сочетается с АИГА.
Еще реже встречается аутоиммунная нейтропения. Описано обнаружение антител к нейтрофилам, однако аутоиммунный характер нейтропении пока убедительно не доказан.
Существуют разные гипотезы о причинах аутоиммунных конфликтов при хроническом лимфолейкозе, в частности о причинах аутоиммунной гемолитической анемии. Увеличение CD5+-лимфоцитов при ревматоидном артрите и других аутоиммунных заболеваниях позволило высказать предположение о роли этих лимфоцитов в возникновении аутоиммунного гемолиза, тем более что они могут продуцировать аутореактивные IgM-антитела. Однако этой гипотезе противоречит поликлоновый характер антиэритроцитарных антител при ХЛЛ.
Описаны случаи аутоиммунного гемолиза после лечения флударабином, который подавляет преимущественно продукцию CD4 -лимфоцитов. В связи с этим ряд авторов высказывают предположение о нарушении соотношения популяций Т-лим-фоцитов как причине развития антиэритроцитарных антител при ХЛЛ. Однако хорошо известно, что в ряде случаев аутоиммунный гемолиз развивался у больных после лечения алкилирующими препаратами, не вызывающими избирательного подавления каких-либо фракций Т-лимфоцитов. Таким образом, в настоящее время нет убедительной концепции о причине столь частого развития аутоиммунного гемолиза эритроцитов при ХЛЛ.
Точно так же нет каких-либо данных, позволяющих предположить причины аутоиммунной тромбоцитопении.

Редким аутоиммунным осложнением при хроническом лимфолейкозе является паранеопластическая пузырчатка. Этот синдром описан в 1990 г. G. J. Anhalt и соавт.. Ими же впервые доказана его аутоиммунная природа. До сих пор в связи с редкостью этого осложнения публикуется практически каждое наблюдение. Нам пришлось наблюдать лишь одного больного с этим осложнением.
В клинической картине преобладающими являются поражения слизистых оболочек и кожи. Они могут быть очень сходными с поражениями кожи при истинной пузырчатке, но чаще напоминают изменения, наблюдаемые при многоформной эритеме, пемфигоиде, плоском лишае или болезни «трансплантат против хозяина». Иногда на коже туловища или конечностей образуются вялые пузыри небольшого размера с прозрачным содержимым. Они часто располагаются в области гениталий.
Еще более выраженными являются поражения слизистой оболочки полости рта: утолщение и эрозии слизистых оболочек щек и языка, красной каймы губ. Эти изменения часто затрудняют речь и прием пищи. Такие же эрозии можно обнаружить на слизистых оболочках глотки, пищевода, трахеи. Как правило, имеется яркий безболезненный коньюнктивит. У некоторых больных развивается поражение бронхов и бронхиол, заканчивающееся облитерирующим бронхиолитом.
Аутоиммунный характер поражения кожи и внутренних органов доказан обнаружением в тканях отложений, представляющих собой комплекс IgG и комплемента. Иммунологические исследования показали, что это антитела к белкам семейства плакина. Белки этого семейства (периплакин, енвоплакин, десмоплакин, плектин, десмоглеин) обеспечивают адгезию клеток к окружающим тканям и между собой. Образование антител к этим белкам ведет к разрушению клеточной мембраны и некрозу клеток. Поскольку такие комплексы обнаружены во многих органах и тканях: почках, мочевом пузыре, мышцах, был предложен термин «паранеопластический аутоиммунный мультиорганный синдром» — ПАМС. Он более полно характеризует заболевание, однако яркая картина поражения кожи и слизистых оболочек послужила причиной сохранения прежнего названия.
Паранеопластическая пузырчатка описана при разных опухолях, наиболее часто при неходжкинских лимфомах, хронический лимфолейкоз и болезни Кастлемана. На хронический лимфолейкоз приходится около 30 % всех описанных случаев. Причины развития аутоиммунного конфликта неизвестны.
Лечение включает кортикостероидные гормоны (в расчете на преднизолон по 1 мг/кг в сутки), циклоспорин А, мабтеру, плазмаферез, но главным является незамедлительное лечение онкологического заболевания, которым страдает больной. Даже после успешного лечения основного заболевания симптомы паранеопластической пузырчатки исчезают очень медленно. Может наступить рецидив при ухудшении течения основного заболевания. При легочном поражении единственным эффективным методом лечения является трансплантация. Из описанных разными клиниками случаев 90 % закончились летально.
– Также рекомендуем “Инфекционные осложнения при хроническом лимфолейкозе – причины”
Оглавление темы “Клиника хронического лимфолейкоза (ХЛЛ)”:
- Влияние мутации гена ТР53 на течение и прогноз хронического лимфолейкоза (ХЛЛ)
- Нарушение апоптоза клеток при хроническом лимфолейкозе (ХЛЛ)
- Влияние экспрессии гена BCL-2 и белка p27 на течение и прогноз хронического лимфолейкоза (ХЛЛ)
- Влияние b2-микроглобулина (b2М) на течение и прогноз хронического лимфолейкоза (ХЛЛ)
- Влияние антигена CD23 на течение и прогноз хронического лимфолейкоза (ХЛЛ)
- Влияние тимидинкиназы и лактатдегидрогеназы (ЛДГ) на течение и прогноз хронического лимфолейкоза (ХЛЛ)
- Сипмтомы хронического лимфолейкоза (ХЛЛ) – анализы
- Аутоиммунные осложнения при хроническом лимфолейкозе – аутоиммунная гемолитическая анемия (АИГА)
- Инфекционные осложнения при хроническом лимфолейкозе – причины
- Опухоли при хроническом лимфолейкозе – частота, причины
Источник
Что такое аутоиммунная гемолитическая анемия?
Аутоиммунная гемолитическая анемия — это аутоиммунное заболевание, характеризующееся преждевременным разрушением здоровых эритроцитов (клеток крови) аутоантителами.
Аутоиммунные заболевания возникают, когда естественная защита организма от чужеродных организмов (например, лимфоцитов, антител) разрушает здоровые ткани по неизвестным причинам. Обычно эритроциты имеют продолжительность жизни около 120 дней, прежде чем будут удалены селезенкой.
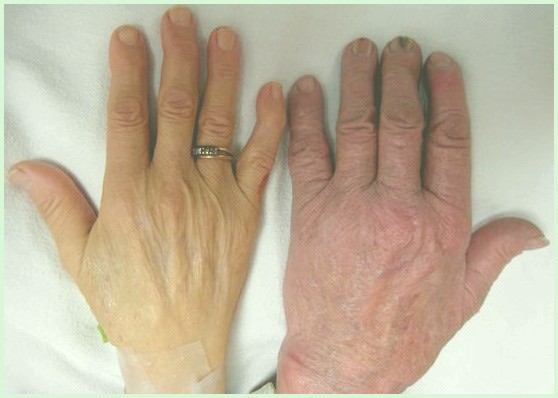
Медицинским термином для низких уровней циркулирующих эритроцитов является анемия. Анемия может вызывать усталость, бледный цвет кожи, пожелтение кожи и белых глаз (желтуха) и отток крови в моче (гемоглобинурия), что придаст моче темно-коричневый цвет.
Признаки и симптомы

Симптомы аутоиммунной гемолитической анемии обычно развиваются медленно в течение периода от нескольких недель до месяцев, но в некоторых случаях могут развиваться внезапно в течение нескольких дней.
Конкретные симптомы, которые возникают, могут варьироваться от одного человека к другому и могут зависеть от скорости возникновения, скорости разрушения здоровых эритроцитов и наличия основного расстройства.
Некоторые люди, особенно те, у кого постепенно развивается анемия, могут не иметь каких-либо явных симптомов. У пострадавших людей могут в конечном итоге развиться:
- ненормальная бледность кожи;
- усталость;
- затрудненное дыхание при физической нагрузке;
- головокружение;
- учащенное сердцебиение.
Желтизна кожи и белых глаз (желтуха) и увеличение селезенки (спленомегалия) также часто встречаются у людей с аутоиммунной гемолитической анемией.
Спленомегалия может привести к тому, что у пострадавшего появится вздутие живота или ощущение полного отека в животе. Иногда у некоторых людей может происходить увеличение печени (гепатомегалия).
У людей с тяжелыми случаями, особенно с быстрым (острым) началом, могут развиться более серьезные осложнения, в том числе потеря сознания (обмороки), боль в груди (стенокардия), аномально быстрое сердцебиение (тахикардия) и сердечная недостаточность.
Причины аутоиммунной гемолитической анемии
Причина аутоиммунной гемолитической анемии обычно неизвестна (т. е. идиопатическая). Однако расстройство может возникать как часть более крупного расстройства, эти случаи известны как вторичная аутоиммунная гемолитическая анемия.
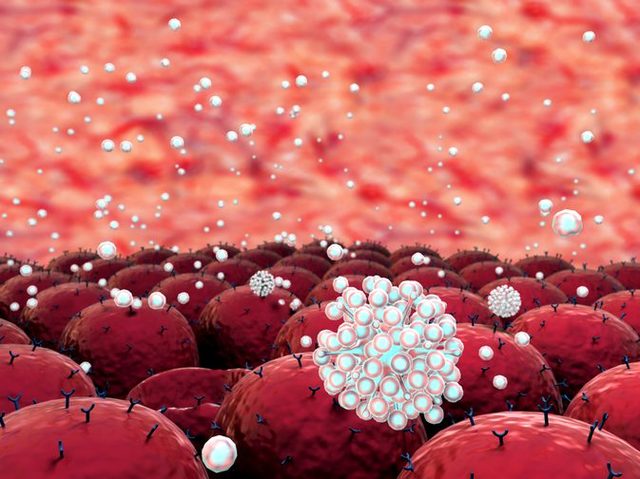
Аутоиммунная гемолитическая анемия является аутоиммунным расстройством — расстройством, при котором естественная защита организма от вторжения организмов (например, лимфоцитов, антител) разрушает здоровые ткани по неизвестным причинам. Антитела ошибочно атакуют здоровые эритроциты, вызывая преждевременное разрушение клеток, состояние, называемое гемолизом.
Антитела (которые также известны как иммуноглобулины) представляют собой специализированные белки, которые связываются с инвазивными организмами и вызывают их разрушение. Существует пять основных классов антител – IgA, IgD, IgE, IgG и IgM.
Большинство случаев данной анемии происходят из-за антител IgG, которые по ошибке атакуют здоровые эритроциты. Реже антитела IgM или IgA вызывают расстройство. Когда антитела атакуют здоровые ткани, их можно назвать аутоантителами.
Несколько основных расстройств связанных с гемолитической анемией, включают другие аутоиммунные расстройства, такие как системная красная волчанка и расстройства, характеризующиеся перепроизводством лейкоцитов (лимфопролиферативные расстройства), такие как лейкемия или лимфома.
Вторичная аутоиммунная гемолитическая анемия также может возникнуть как побочный эффект некоторых лекарств.
Затронутые группы населения
Гемолитическая анемия поражает мужчин и женщин в равных количествах. По оценкам, аутоиммунные гемолитические анемии затрагивают 1-3 человека на 100 000 населения в целом. У людей любого возраста, включая детей, может развиться данная болезнь, однако чаще она встречается у взрослых с пиковой заболеваемостью в возрасте 50-70 лет.
Диагностика
Диагноз гемолитической анемии можно заподозрить на основании тщательной клинической оценки, детальной истории болезни, выявления характерных симптомов и различных анализов, таких как анализы крови, которые измеряют гемоглобин и гематокрит. Гемоглобин — белок в красных кровяных клетках, который переносит кислород. Гематокрит — процент от общего объема крови, занимаемый эритроцитами.
Анализы крови могут также показать повышенный уровень незрелых эритроцитов (ретикулоцитов), который происходит, когда организм вынужден производить дополнительные эритроциты, чтобы восполнить те, которые преждевременно разрушились. Некоторые люди с гемолитической анемией имеют повышенный уровень билирубина в крови (гипербилирубинемия). Билирубин — желтоватый продукт, образующийся при метаболизме гемоглобина в печени.
Когда предполагается, что анемия вызвана дисфункцией иммунной системы (т. е. аутоиммунная гемолитическая анемия), могут проводиться специализированные тесты, такие как проба Кумбса. Этот анализ проводиться для обнаружения антител, которые действуют против эритроцитов. Образец крови берется и затем подвергается воздействию реагента Кумбса. Если эритроциты слипаются в присутствии реагента то, это указывает на наличие у пациента заболевания.
Лечение аутоиммунной гемолитической анемии
Лечение аутоиммунной гемолитической анемии является симптоматическим и поддерживающим. Пострадавших людей обычно лечат кортикостероидными препаратами, такими как преднизон, и обычно они контролируют болезнь при правильном лечении. Первоначально может быть рекомендована высокая доза этих лекарств с последующим постепенным снижением дозы в течение следующих нескольких недель или месяцев.
Людям, которые не отвечают на терапию кортикостероидами или развивают непереносимые побочные эффекты, могут быть назначены иммунодепрессанты или хирургическое удаление селезенки (спленэктомия). Иммуносупрессивные лекарственные средства, такие как циклофосфамид, представляют собой лекарственные средства, которые подавляют или блокируют иммунную систему, и помогают некоторым людям с гемолитической анемией, которые не реагируют на преднизон или спленэктомию.
Спленэктомия обычно используется у людей с тяжелыми случаями, которые требуют постоянного преднизона для контроля. У пациентов с основным нарушением лечение этого расстройства обычно приводит к заметному улучшению анемии.
Ритуксимаб — это моноклональное антитело, искусственно созданное антитело, которое нацелено на определенные лейкоциты, которые создают антитела, которые преждевременно разрушают эритроциты. Ритуксимаб оказался полезным для некоторых пациентов с аутоиммунной гемолитической анемией, которые не реагировали на преднизон. Уровень ответов может достигать 80% у взрослых и 60% у детей. Ритуксимаб может быть использован до спленэктомии или может использоваться у людей, у которых наблюдается рецидив после спленэктомии.
Переливание эритроцитов также может быть необходим для поддержания надлежащего уровня эритроцитов у людей с тяжелыми случаями. Этот поддерживающий метод обеспечивает временное облегчение состояния, но не лечит основную причину расстройства.
Профилактика
Предотвратить аутоиммунную гемолитическую анемию не возможно, но врачи могут помочь людям, у которых есть вирусная инфекция или которые используют определенные лекарства, чтобы болезнь не развивалась.
Тяжелая анемия может усугубить многие проблемы, такие как болезни сердца и легких. Люди должны обратиться к врачу, если они испытывают какие-либо симптомы, которые могут указывать на гемолитическую анемию.
Источник
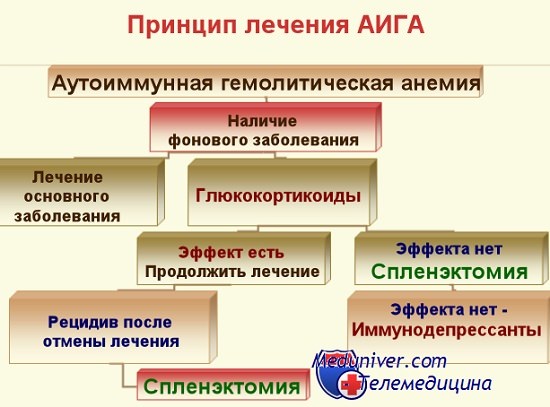
Лечение аутоиммунной гемолитической анемии – схемаПоскольку аутоиммунная гемолитическая анемия делится на генуинную и вторичную формы по возможности лечение должно учитывать соответствующие особенности, и тем самым взаимодействовать с механизмами образования антител. При вторичных формах за счет лимфопролиферации следует лечить последнюю в целях пресечения и дальнейшего угнетения разрастания массы злокачественных клеток, сецернирующих аутоантитела. Правильно проводимая терапия ХЛЛ, ЛС, PC защищает больного от тяжелых приступов расплавления крови, естественно поскольку имеются длительные межпрнступные периоды. При аутоиммунной гемолитической анемии, за счет иммунного дефицита или гиперреактивного состояния с дисгаммаглобулинемией, лечить эти явления для устранения условий аутоиммунного гемолиза или даже его предупреждения. Хирургическое вмешательство, облучение или даже лечение цитостатическими средствами — когда это возможно при отдельных видах рака — устраняют причину развития аутоиммунной гемолитической анемии. Однако наиболее часто периоды расплавления крови при вторичных формах заболевания — за исключением заболеваний за счет отсутствия антител — требуют лечение патогенетического характера в целях приостановления процесса. При генуинной аутоиммунной гемолитической анемии с холодовыми или тепловыми антителами, когда не выявляется определенная этиологическая причина, в основном на острых периодах или формах хронического течения методы патогенетической терапии представляются единственно возможными. В подобных случаях заболевания удовлетворительные результаты дает кортизонотерапия, при этом среднесуточная доза преднизона равняется 40—50 мг. При весьма тяжелых формах со сверхострым расплавлением крови, понижением показателя гемоглобина до 3—4 г, продолжительности жизни гематий от 5 до 10 дней назначать большую дозу от 80 до 100 мг в сутки, из расчета примерно 1—1,5 мг на кг веса тела. В большинстве наблюдаемых нами случаях (Берчану и сотр.) при генуинных формах гемолитический процесс был приостановлен на 2—4 неделях лечения. Течение вторичной формы аутоиммунной гемолитической анемии (ДКВ или лимфопролиферация) зависит от реакции первичного заболевания на проводимую терапию. Даже если назначение кортикоидов обусловливает обратное течение гемолитического процесса, в случае неподдающейся лечению злокачественной лимфопролиферации или сложности ее терапии — например в устарелых формах РКВ — расплавление крови возобновляется непосредственно после уменьшения дозы кортизона. По Leddy кортизонотерапия дает положительный результат примерно в 2/3 случаев с первичными заболеваниями, а в 1/3 — лишь относительный результат, причем из них 5—10% составляют безответные случаи. В группе случаев, не реагирующих на лечение или дающих посредственный результат с повторными рецидивами после непрерывной 5—6-месячной кортикотерапии, показана спленэктомия. Этот хирургический метод лечения дает хорошие результаты у больных, у которых наблюдается преимущественно селезеночная секвестрация.
Тем не менее удаление селезенки следует применять и больным с преимущественно печеночной секвестрацией, поскольку этим приемом устраняются важная иммунологическая система выделения аутоантител и значительная масса макрофаговой ткани гемолитичской активности. Спленэктомия также показана при тяжелом гемолитическом заболевании за счет гиперспленизма в результате злокачественной лимфомы и даже при РКВ или хроническом агрессивном гепатите, конечно когда это допускает общее состояние больного. Во всех отмеченных случаях силен-эктомия рассматривается как биологический иммуносупрессорный метод, устраняющий значительную массу лимфоретикулярных клеток с иммуной патологической реакцией. Известно, что, в отдельных случаях, наличие антител отмечается и после удаления селезенки, даже если процесс расплавления крови не возобновляется. Итак, положительный результат объясняется, в основном, устранением пожирающей эритроциты макрофаговой ткани. В нашем опыте, охватившем 100 случаев спленэктомии у страдающих гемолитической анемией (Теодореску и Берчану) в 25% случаев гемоцитопений по различным причинам наблюдались положительные результаты. При гемолитической анемии с холодовыми антителами, развивающейся после вирусной инфекции, нередко специфическая терапия оказывается лишней, поскольку гемолитический эпизод исчезает по истечении периода выздоровления, когда сокращается число аутоантител. При генуинных или первичных, равно как и вторичных послевирусных формах, которые самоподдерживаются, также в заболеваниях за счет злокачественной лимфомы показана кортикотерапия крупными дозами, в связи с тем, что в этих случаях реакция слабее, чем при формах болезни с холодовыми антителами. По истечении 5—6-месячного периода лечения испробовать спленэктомию, хотя положительный результат редкое явление. После непродолжительного улучшения гемолитической анемии процесс расплавления крови возобновляется, болезнь продолжает свое течение и антитела остаются неизменными. В большинстве случаев гемолитической анемии с холодовыми антителами, не поддающейся кортикотерапии и спленэктомии назначать, в принципе, краткосрочную умеренную иммуносупрессорную терапию. Так, иммуран 100 мг в сутки, эндоксан 50—100 мг и лейкеран 4—6 мг за 1—3 месяца сокращают коэффициент антител и интенсивность расплавления крови, вообще устраняя острые приступы. Болезнь приобретает хроническое течение, чередуются периоды хорошого состояния и умеренного гемолиза, что напоминает хроническую гемолитическую желтуху с компенсированной или умеренной анемией. Иные виды терапии симптоматического или патогенетического характера в аутоиммунной гемолитической болезни не оправдываются положительными результатами. В хронических, устойчивых к лечению формах, которые в основном развиваются за счет холодовых антител, следует избегать способствующие усугублению гемолиза условия, в том числе, инфекции, большую физическую нагрузку и стресс от волнения. В частности избегать воздействие холода, холодные ваны и даже контакт с определенными холодными предметами. При аутоиммунной гемолитической анемии с богатым эритробластами регенеративным костным мозгом переливание крови в принципе не представляется необходимым. Когда в костном мозге, особенно на остром периоде, отмечаются заниженный ретикулоцитоз и мегалобластические отклонения назначать фолиевую кислоту и витамин В12, способствующих восстановлению процесса регенерации костного мозга. В очень тяжелых случаях, с острым гемолизом, падением гемоглобина до 3—4 г., когда тканевая аноксия ставит под угрозу жизнь больного помимо кортизонотерапии крупными дозами, включительно внутривенным введением гемисукцината гидрокортизона, также назначать переливание массы промытых гематий, которые, вообще, хорошо переносимы. В периоды приступов эритробластопении проводить повторные переливания промытыми эритроцитами, одновременно с кортикотерапией до восстановления нормального кроветворения, роста показателей гемоглобина, гематокрита и ретикулоцитов. Противопоказано переливание цельной крови, поскольку подвоз ею комплемента и собственно жидкая плазматическобелковая среда усугубляют явления агглютинации и внутрисосудистого расплавления крови. Более сложные условия лечения при аутоиммунных антителах с характеристикой паиагглютинина и пангемолизина, отмечены нами, в основном, при острой анемии лекарственных средств, острой недифференцированной лейкемии и волчанке. На остром периоде болезни больной не переносит ни одной из групп красных кровяных телец, в связи с чем, в первую очередь, помимо кортикоретапии крупными дозами, проводить характерную для злокачественного разрастания цитостатическую терапию — особенно непродолжительными комбинациями синхронизирующего эффекта, в целях быстрого сокращения массы злокачественных клеток. В принципе это обусловливает ослабление процесса аутогемолиза, сокращение коэффициента паиагглютинина и делает возможным переливание промытыми гематиями после их тщательного отбора от доноров, посредством прямого испытания. Впрочем, проведение любого переливания страдающим острым аутоиммуным расплавлением крови требует особой осторожности и наблюдения непосредственного результата гемолиза, наступающего с началом переливания. Значительная концентрация гемолитических антител у больного может обусловить развитие резкого расплавления переливаемых гематий в условиях оптимального испытания в пробирке. Появление клинических признаков даже незначительного гемолиза требует немедленной проверки выделяемого в кровообращение гемоглобина и прекращения переливания при любом незначительном росте. – Также рекомендуем “Пароксизмальная гемолитическая анемия в условиях холода – клиника, диагостика, лечение” Оглавление темы “Гемолитические анемии”:
|
Источник