Бластные клетки при анемии

Лабораторная диагностика миелодиспластического синдрома – анализы
Диагноз миелодиспластического синдрома (МДС) основывается на обнаружении качественных нарушений кроветворения в одном или нескольких ростках гемопоэза (дизэритропоэз, дизгрануломоноцитопоэз, дизмегакариоцитопоэз). Вариант заболевания определяется на основании анализов крови и костного мозга.
Анализ периферической крови при миелодиспластическом синдроме. У больных миелодиспластическим синдромом (МДС) выявляются различные варианты цитопении: в 60-70% случаев — панцитопения (анемия, лейкои нейтропения, тромбоцитопения), у 30-40% пациентов — двуростковая цитопения, у 5% — одноростковая цитопения.
Анемия наблюдается более чем у 90% больных, имеет нормо- или макроцитарный характер, сопровождается умеренным анизо- и пойкилоцитозом. Уровень ретикулоцитов обычно снижен. Качественные изменения эритроцитов (дизэритропоэз) характеризуются наличием мегалоцитов, эритроцитов с базофильной пунктацией, тельцами Жолли; могут встречаться единичные нормоциты.
Лейко- и нейтропения отмечаются у 60% больных миелодиспластическим синдромом (МДС). В 10-20% случаев количество лейкоцитов в норме или повышено (при хроническом миеломоноцитарном лейкозе). Дизгранулоцитопоэз проявляется прежде всего псевдопельгеровской аномалией (пельгеризацией), которая наблюдается более чем у 80% пациентов. Наряду с этим могут встречаться гиперсегментированные и двуядерные нейтрофилы, а также клетки, содержащие фрагменты ядра.
В цитоплазме нейтрофилов выявляется либо резкое снижение зернистости (вплоть до полной дегрануляции), либо, напротив, аномально большие гранулы. При определенных формах миелодиспластического синдрома (МДС) в периферической крови выявляются бластные клетки. Для хронического миеломоноцитарного лейкоза характерен абсолютный моноцитоз (более 1 • 109/л).
У большинства пациентов в периферической крови выявляется тромбоцитопения. Дизмегакариоцитопоэз характеризуется появлением в периферической крови качественно измененных тромбоцитов (гигантские клетки с бедным грануломером), а также фрагментов мегакариоцитов.

Миелограмма при миелодиспластическом синдроме
При исследовании аспирата костного мозга в большинстве случаев выявляется его нормальная или повышенная клеточность. Уменьшение количества миелокариоцитов отмечается менее чем у 15% больных. Основное при анализе миелограммы у больных миелодиспластическим синдромом — выявление качественных изменений гемопоэза и подсчет количества бластных клеток.
В первую очередь страдает эритропоэз, что проявляется гиперплазией эритроидного ростка, признаками мегалобластоидного кроветворения, наличием гигантских эритроидных клеток (до 20 мкм и более), многоядерных нормоцитов с фрагментами ядра, тельцами Жолли, кариорексисом и пикнозом ядер; цитоплазма клеток содержит базофильную пунктацию и вакуолизацию.
У больных с рефрактерной анемией с кольцевыми сидеробластами (РАКС) увеличено количество сидеробластов, имеются их кольцевидные формы. Дизэритропоэз является самой ранней находкой при миелодиспластическом синдроме и доминирует при рефрактерной анемии (РА) и РАКС.
Количество бластных клеток в пунктате костного мозга зависит от формы миелодиспластического синдрома и колеблется от нормального количества до 20%.
Дизгранулопоэз характеризуется псевдопельгеровской аномалией, гипо- и агрануляцией цитоплазмы или, напротив, появлением аномально крупных гранул. Количество мегакариоцитов в норме или уменьшено. Признаки дизмегакариоцитопоэза включают появление микромегакариоцитов, клеток с однои двулопастными ядрами или с множеством отдельно расположенных ядер небольших размеров с гигантскими аномальными гранулами. Может отмечаться плазмоцитарная реакция костного мозга (4-8%).
Трепанобиопсия дает более полное представление о клеточности костного мозга и признаках дизмегакариоцитопоэза (микромегакариоциты обнаруживаются чаще, чем в миелограмме). Выявляются также признаки дизэритро- и дизгранулоцитопоэза.
Биохимигеские исследования не имеют патогномоничного значения для диагностики миелодиспластического синдрома. В ряде случаев отмечается снижение уровня пируваткиназы, увеличение фетального гемоглобина в крови и лизоцима — в крови и моче.
Цитогенетические нарушения отмечаются у 50% больных первичным миелодиспластическим синдромом и более чем у 80% пациентов со вторичным миелодиспластическим синдромом. Для первичного миелодиспластического синдрома характерны del 5q, +8 и -7. При вторичном миелодиспластическом синдроме чаще выявляются del 7q и del 5q.
Изолированные хромосомные аберрации могут иметь благоприятное (del 5q и del 20q), неблагоприятное значение (del 7q) либо существенно не влиять на прогноз. Выявление любых множественных (не менее 3) цитогенетических аномалий сопровождается неблагоприятным прогнозом.
Дифференциальный диагноз миелодиспластического синдрома (МДС)
Некоторые формы миелодиспластического синдрома (МДС) (РА и РАКС) необходимо дифференцировать от апластической и В12-дефицитной анемии. Цитологическое и гистологическое исследование костного мозга, выявляющее выраженную дисплазию клеток миелоидного ростка при отсутствии аплазии кроветворения, позволяют поставить правильный диагноз.
Трудности могут возникнуть при дифференциальной диагностике МДС и острого эритромиелоза (М6 по FAB-классификации острого лейкоза), поскольку для обоих заболеваний характерны выраженный анемический синдром, бицитопения или панцитопения, гиперплазия и дисплазия эритроидного ростка костного мозга. В то же время при остром эритромиелозе в крови определяются ретикулоцитоз и нормоцитоз, в миелограмме выявляется 20% и более бластных клеток, а также уродливые нормоциты и многоядерные эритробласты при отсутствии качественных изменений гранулоцитарного ряда.
Дифференциальный диагноз РАИБ с другими вариантами острых лейкозов основывается на количестве бластов в миелограмме (при миелодиспластическом синдроме — всегда менее 20%).
– Также рекомендуем “Классификация миелодиспластического синдрома (МДС)”
Оглавление темы “Лейкозы”:
- Прогноз лечения острого лимфобластного лейкоза – прогностические факторы
- С чего начать лечение острого лимфобластного лейкоза? – современная терапия
- Профилактика поражения центральной нервной системы (нейролейкоза) при остром лимфобластном лейкозе
- Лечение рецидива острого лимфобластного лейкоза – схемы терапии
- Миелодиспластические синдромы (МДС) – эпидемиология, причины, клиника
- Лабораторная диагностика миелодиспластического синдрома – анализы
- Классификация миелодиспластического синдрома (МДС)
- Прогноз миелодиспластического синдрома (МДС)
- Лечение миелодиспластического синдрома (МДС) – современные методы
- Хронический миелолейкоз – причины, механизмы развития
Источник
Определение типа бластных клеток при остром лейкозе
Определение типа бластных клеток и соответственно варианта острого нелимфобластного лейкоза (ОНЛЛ) базируется на комплексной характеристике морфологических, цитохимических и иммунофенотипических особенностей лейкемических элементов.
К морфологическим критериям характеристики бластов относятся размер клеток (соотношение макро-, мезо- и микроформ), форма ядер (округлая, складчатая, моноцитоидная), наличие зернистости и/или палочек Ауэра, ядерно-цитоплазматическое отношение (высокое, умеренное или низкое). Именно на основании морфологических признаков лейкемические миелобласты и монобласты разделяются на клетки с наличием или отсутствием признаков созревания.
Цитохимическими маркерами бластов гранулоцитарного ряда служат пероксидаза, липиды, выявляемые Суданом черным В, и ASD-хлорацетатэстераза. Содержание этих маркеров в миелобластах значительно варьирует, иногда выявляется только один из них. В случае сомнительного ответа необходимо обязательно проводить две цитохимические реакции — на пероксидазу и липиды, чтобы избежать возможной ошибки.
Активность ASD-хлорацетатэстеразы существенно ниже, чем пероксидазы, поэтому определение этого фермента представляет меньшую диагностическую ценность. Низкая активность пероксидазы в миелобластах является плохим прогностическим признаком.
Признаки бластов при различных вариантах острого нелимфобластного лейкоза (ОНЛЛ)
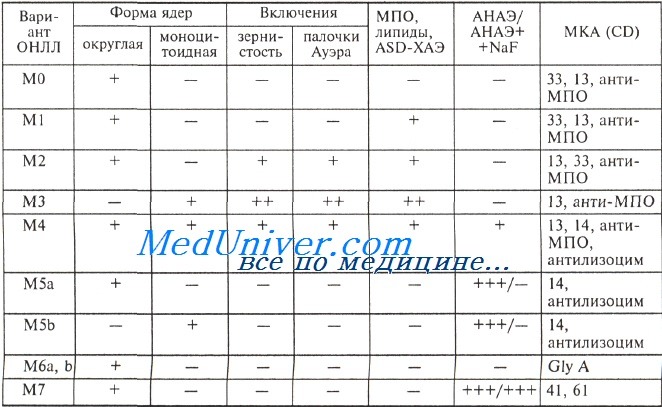
Условные обозначения: МПО — миелопероксидаза; ASD-ХАЭ— ASD-хлорацетатэстераза (гранулоцитарная эстераза); АНАЭ — а-нафтилацетатэстераза (неспецифическая эстераза); анти-МПО — МКА к миелопероксидазе; антилизоцим — МКА к лизоциму; Gly A — гликофорин А.
Исследование а-нафтилацетатэстеразы играет главную роль в диагностике монобластов М5a и М5b. Этот фермент обнаруживается в большинстве гемопоэтических клеток, однако его изоформа, подавляемая фторидом натрия, характерна только для клеток моноцитарно-макрофагальной линии. При определении неспецифической эстеразы с равным успехом используют различные субстраты: а-нафтилацетат, бутират, AS-хлорацетат и др. Диагностическая ценность их близка.
Активность фермента в монобластах без созревания и с созреванием, как правило, одинаково высокая. В то же время, используя панель различных субстратов для неспецифической эстеразы, можно проводить предположительную дифференциальную диагностику моно-бластных и мегакариобластных лейкозов до иммуно-фенотипирования.
Определенное диагностическое значение имеет результат PAS-реакции, так как особенностью большинства бластов миелоидного ряда является диффузное расположение PAS-положительного материала в отличие от лимфобластов, для которых характерно расположение продукта реакции в виде гранул. Результаты этого исследования помогают различать МО ОНЛЛ и ОЛЛ. В отдельных случаях в миелобластах типа МО и эритробластах PAS-положительное вещество может иметь форму гранул.
Различные типы бластных клеток при остром нелимфобластном лейкозе (ОНЛЛ) отличаются по антигенной структуре их мембран. Для клеток гранулоцитарной линии характерна экспрессия антигенов CD33, CD13, они реагируют с МКА к пероксидазе. Бласты моноцитарной линии взаимодействуют с МКА к лизоциму. Для эритроидных клеток характерно наличие молекул гликофорина А, для мегакариоцитов — CD41 и CD61.
Иммунологические данные не позволяют провести дифференциальный диагноз типов бластов гранулоцитарной линии, однако использование данных иммунофенотипирования имеет принципиальное значение для диагностики вариантов М0, М6 и М7, поскольку морфологические и цитохимические показатели этих клеток не позволяют установить тип бластов.
– Также рекомендуем “Острый нелимфобластный лейкоз с повторяющимися цитогенетическими аномалиями – формы, диагностика”
Оглавление темы “Диагностика острого лейкоза”:
- Диагностика острого промиелоцитарного лейкоза – М3 по классификации FAB
- Острый миеломонобластный лейкоз (M4 по классификации FAB) – диагностика
- Острый монобластный лейкоз (M5a по классификации FAB) – диагностика
- Острый эритромиелоз и эритроидный лейкоз (M6a и M6b по классификации FAB) – диагностика
- Острый мегакариобластный лейкоз (M7 по классификации FAB) – диагностика
- Острый миелобластный лейкоз с миелофиброзом (панмиелоз с миелофиброзом по классификации ВОЗ) – диагностика
- Миелосаркома – морфология, диагностика
- Определение типа бластных клеток при остром лейкозе
- Острый нелимфобластный лейкоз с повторяющимися цитогенетическими аномалиями – формы, диагностика
- Острый нелимфобластный лейкоз с мультилинейной дисплазией – формы, диагностика
Источник
При подозрении на лейкоз врачи назначат анализ крови на бласты. Это исследование помогает своевременно выявить опасное заболевание и приступить к лечению как можно раньше. Как правильно подготовиться к взятию пробы? И как расшифровать результаты анализа? Эти вопросы мы рассмотрим в статье.
Что это такое?
Бласты представляют собой незрелые кровяные клетки, которые продуцируются в костном мозге. В дальнейшем они преобразуются в эритроциты, лейкоциты и тромбоциты. Бластные клетки являются предшественниками зрелых кровяных телец.
У здорового человека бласты в костном мозге составляют не более 5 % клеток. При инфекционных заболеваниях их концентрация может возрастать до 10 %. Однако в норме незрелые клетки не должны попадать в кровоток. Они могут находиться только в пределах костного мозга.
При тяжелых гематологических патологиях у пациента появляются бласты в крови. Что это значит? Такой результат анализа указывает на онкологические болезни системы кроветворения. При этих патологиях в костном мозге образуется чрезмерное количество незрелых элементов. Избыток бластов выбрасывается в кровоток. Их наличие в анализе является тревожным признаком.
В начальной стадии рака крови в костном мозге может находиться около 40 % бластных клеток. В дальнейшем из этих незрелых элементов образуется злокачественная опухоль.
Анализ крови
Как выявить присутствие в кровотоке бластов? Это можно сделать с помощью общего анализа крови. Это исследование показывает количество зрелых и незрелых клеток.
Для пробы берут кровь из пальца или из вены. Биоматериал изучают под световым микроскопом. Это устройство имеет специальную сетку для подсчета кровяных клеток. С ее помощью и определяют концентрацию бластов. В расшифровке анализа количество незрелых клеток указывается в процентах.
Показания к исследованию
В каких случаях врачи назначают анализ на бласты? Это исследование показано, если у пациента отмечаются следующие симптомы:
- увеличение лимфатических узлов;
- беспричинное повышение температуры;
- увеличение печени и селезенки;
- слабость;
- воспаление миндалин в тяжелой форме;
- красные точки на коже;
- повышенная кровоточивость.

Очень часто пациенты принимают эти проявления за признаки ангины и других инфекционных болезней. Однако такие симптомы могут свидетельствовать о наличии тяжелой патологии костного мозга. С целью дифференциальной диагностики врачи назначают анализ на наличие бластов в крови.
Подготовка к анализу
Пробу на бластные клетки обычно берут утром, натощак. Результаты анализа чаще всего бывают готовы уже на следующий день.
Какие правила нужно соблюдать перед взятием биоматериала на бласты? Это исследование не требует сложной подготовки. Нужно придерживаться следующих рекомендаций:
- прекратить прием еды за 8 часов до теста;
- не употреблять алкоголь накануне исследования;
- за 2 часа до взятия крови исключить курение.
Рекомендуется также прекратить прием лекарств за 3 дня до анализа. Если же больной не может прервать курс медикаментозного лечения, то нужно рассказать врачу обо всех принимаемых препаратах.
Расшифровка
В норме бласты должны отсутствовать в анализе. В этом случае в результатах исследования указано, что их показатель равен 0 %. У здорового человека в крови могут находиться только зрелые элементы.
Если в анализе присутствует даже малый процент бластов, то это является опасным признаком. Результаты пробы нужно обязательно показать врачу и немедленно приступить к лечению.

Причина отклонений: лейкоз
Основной причиной появления в пробе бластных клеток является лейкоз. Это заболевание иначе называется лейкемией или раком крови. Патология сопровождается неконтролируемым делением незрелых клеток в костном мозге, которые в дальнейшем образуют опухоль.
Врачи выделяют две формы лейкоза:
- острую;
- хроническую.
При острой лейкемии в крови обнаруживается огромное количество бластных клеток. Их концентрация может быть более 20 %. При хронической форме рака крови показатель незрелых элементов обычно не превышает 5-10 %.
Другие показатели крови
При изучении результатов анализа врач обязательно обращает внимание и на другие показатели клинического исследования. Наличие бластных клеток в биоматериале всегда рассматривается в сочетании с другими параметрами крови. На наличие лейкоза могут указывать следующие данные:
- Лейкоцитоз. Примерно у 15 % больных острой формой лейкемии показатель белых кровяных телец превышает норму в десятки раз.
- Низкий гемоглобин. У пациентов с раком крови отмечается тяжелая анемия и снижение числа эритроцитов.
- Падение уровня тромбоцитов. По этой причине у больных лейкемией отмечается повышенная кровоточивость.
- Снижение ретикулоцитов. Эти клетки являются молодыми формами эритроцитов. Их малое количество приводит к анемии.
- Полное отсутствие эозинофилов и базофилов. Это становится причиной резкого снижения иммунитета.
Вышеперечисленные признаки вместе с появлением бластных клеток в крови позволяют врачу поставить диагноз “лейкоз”.
Исследование костного мозга
Если у пациента в крови обнаружены бласты, то врачи обычно назначают пункцию костного мозга. Исследование проводят под местным обезболиванием. Специальной длинной иглой делают прокол в области грудины или позвоночника и берут на исследование кусочек ткани костного мозга.
Пунктат исследуют при помощи микроскопа. В биоматериале определяют количество зрелых и незрелых элементов крови. Повышение бластных клеток до 10 % не всегда указывает на лейкемию. Такой результат исследования возможен при сильном стрессе или инфекционном заболевании. Если же концентрация бластов превышает 30 %, то это чаще всего является признаком рака крови. При этом у больного уменьшается количество эритроцитов, тромбоцитов и лейкоцитов в пункционном материале.
При подозрении на лейкоз также проводят цитохимический анализ пунктата. Он позволяет выявить уровень ферментов бластных клеток. Эти вещества вступают в реакцию с некоторыми красителями, что и используется при лабораторном исследовании. Положительные результаты пробы указывают на лейкоз. С помощью измерения уровня каждого бластного фермента можно определить форму рака крови.
Лечение
Что делать, если анализ крови показал наличие бластных клеток? В этих случаях врач обычно назначает ряд дополнительных анализов. Самым информативным из них является пункция костного мозга. Чрезмерно высокое количество бластов в пунктате является признаком лейкемии.
Если диагноз “лейкоз” подтвердился, то необходимо немедленно приступать к лечению. Важно помнить, что на ранних стадиях рака крови вполне возможно достичь полной или частичной ремиссии. В наши дни применяются следующие методы лечения лейкемии:
- Химиотерапия. Пациенту назначают цитостатики, которые подавляют рост новообразования в костном мозге. Такое лечение может занимать довольно длительное время.
- Переливание крови. Пациенту вводят внутривенно эритроциты и тромбоциты, полученные от донора. Это помогает поднять уровень гемоглобина и уменьшить кровоточивость.
- Радиотерапия. Такой вид лечения показан при хроническом лейкозе. Пациенту облучают увеличенные лимфоузлы и область селезенки.
- Антибактериальная терапия. Пациенты с лейкозом очень подвержены инфекционным патологиям. С целью предотвращения таких заболеваний назначают курсы приема антибиотиков.
- Пересадка костного мозга. Такая операция помогает полностью избавиться от лейкоза. Сложность трансплантации заключается в том, что чужой орган кроветворения не всегда приживается.
После комплексной терапии проводят повторную пункцию костного мозга. Если концентрация бластов снизилась до 5 %, то врачи говорят о полной ремиссии. Если же показатель незрелых клеток не превышает 20 %, то ремиссия считается частичной. В любом случае пациенту необходимо пожизненно соблюдать рекомендации врача. Лейкоз относится к опасным и тяжелым заболеваниям. Даже при полной ремиссии нельзя исключать рецидивы патологии.
Источник
