Буферная система гемоглобина ph
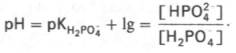
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 28 августа 2018;
проверки требуют 15 правок.
Бу́ферные систе́мы кро́ви (от англ. buffer, buff — «смягчать удар») — физиологические системы и механизмы, обеспечивающие заданные параметры кислотно-основного равновесия в крови[1]. Они являются «первой линией защиты», препятствующей резким перепадам pH внутренней среды живых организмов.
Циркулирующая кровь представляет собой взвесь живых клеток в жидкой среде, химические свойства которой очень важны для их жизнедеятельности. У человека за норму принят диапазон колебаний pH крови 7,37—7,44 со средней величиной 7,4. Буферные системы крови слагаются из буферных систем плазмы и клеток крови и представлены следующими системами[1][2]:
- бикарбона́тная (водородкарбонатная) бу́ферная систе́ма;
- фосфа́тная бу́ферная систе́ма;
- белко́вая бу́ферная систе́ма;
- гемоглоби́новая бу́ферная система;
- эритроциты.
Помимо этих систем также активно участвуют дыхательная и мочевыделительная системы[1].
Бикарбонатная буферная система[править | править код]
Одна из самых мощных и вместе с тем самая управляемая система[2] внеклеточной жидкости и крови, на долю которой приходится около 53 % всей буферной ёмкости крови. Представляет собой сопряжённую кислотно-основную пару, состоящую из молекулы угольной кислоты H2CO3, являющейся источником протона, и бикарбонат-аниона HCO3−, выполняющего функцию акцептора протона:
Вследствие того, что концентрация гидрокарбоната натрия в крови значительно превышает концентрацию H2CO3, буферная ёмкость этой системы будет значительно выше по кислоте. Иначе говоря, гидрокарбонатная буферная система особенно эффективно компенсирует действие веществ, увеличивающих кислотность крови. К числу таких веществ прежде всего относят молочную кислоту, избыток которой образуется в результате интенсивной физической нагрузки. Гидрокарбонатная система наиболее «быстро» отзывается на изменение pH крови[2].
Фосфатная буферная система[править | править код]
В крови ёмкость фосфатной буферной системы невелика (составляет около 2 % общей буферной ёмкости), в связи с низким содержанием фосфатов в крови. Фосфатный буфер выполняет значительную функцию в поддержании физиологических значений рН во внутриклеточных жидкостях и моче.
Буфер образован неорганическими фосфатами. Функцию кислоты в этой системе выполняет однозамещённый фосфат (NaH2PО4), а функцию сопряженного основания — двузамещённый фосфат (Na2HPО4). При рН 7,4 соотношение [НРО42-/Н2РО4-] равняется поскольку при температуре 25+273,15K pKa, ортоII=7,21[3], при этом средний заряд аниона ортофосфорной кислоты < q >=((-2)*3+(-1)*2)/5=-1,4 единиц заряда позитрона.
Буферные свойства системы при увеличении в крови содержания водородных ионов реализуются за счет их связывания с ионами НРО42- с образованием Н2РО4-:
а при избытке ионов ОН- — за счет связывания их с ионами Н2РО4-:
Фосфатная буферная система крови тесно взаимосвязана с бикарбонатной буферной системой.
Белковая буферная система[править | править код]
В сравнении с другими буферными системами имеет меньшее значение для поддержания кислотно-основного равновесия (7—10 % буферной ёмкости).
Белки́ плазмы крови благодаря наличию кислотно-основных групп в молекулах белков (белок—H+ — кислота, источник протонов и белок− — сопряжённое основание, акцептор протонов) образуют буферную систему, наиболее эффективную в диапазоне pH 7,2—7,4[1].
Основную часть белков плазмы крови (около 90 %) составляют альбумины и глобулины. Изоэлектрические точки этих белков (число катионных и анионных групп одинаково, заряд молекулы белка равен нулю) лежат в слабокислой среде при pH 4,9—6,3, поэтому в физиологических условиях при pH 7,4 белки находятся преимущественно в формах «белок-основание» и «белок-соль».
Буферная ёмкость, определяемая белками плазмы, зависит от концентрации белков, их вторичной и третичной структуры и числа свободных протон-акцепторных групп. Эта система может нейтрализовать как кислые, так и основные продукты. Однако вследствие преобладания формы «белок-основание» её буферная ёмкость значительно выше по кислоте.
Буферная ёмкость свободных аминокислот плазмы крови незначительна как по кислоте, так и по щелочи. При физиологическом значении pH их мощность мала. Практически только одна аминокислота — гистидин — обладает значительным буферным действием при значении pH, близком к плазме крови.[2]
Эритроциты[править | править код]
Во внутренней среде эритроцитов в норме поддерживается постоянное значение pH, равное 7,30. Здесь также действуют гидрокарбонатная и фосфатная буферные системы. Однако их мощность отличается от таковой в плазме крови. Кроме того, в эритроцитах белковая система гемоглобин-оксигемоглобин играет важную роль как в процессе дыхания (транспортная функция по переносу кислорода к тканям и органам и удалению из них метаболической CO2), так и в поддержании постоянства pH внутри эритроцитов, а в результате и в крови в целом. Эта буферная система в эритроцитах тесно связана с гидрокарбонатной системой.[2]
Гемоглобиновая буферная система[править | править код]
Буферная система крови (75 % буферной ёмкости). Играет важную роль как в процессе дыхания (транспортная функция по переносу кислорода к тканям и органам и удалению из них метаболической CO2), так и в поддержании постоянства pH внутри эритроцитов, а в результате и в крови в целом.[2]
См. также[править | править код]
- Буферный раствор
Примечания[править | править код]
- ↑ 1 2 3 4 Березов Т. Т., Коровкин Б. Ф. Биологическая химия: Учебник — 1990 г. — стр. 452—455.
- ↑ 1 2 3 4 5 6 Ершов. Общая химия.Биофизическая химия.Химия биогенных элементов. — Издание восьмое, стериотипное. — Москва: Высшая школа, 2010. — 559 с. — ISBN 978-5-06-006180-2.
- ↑ И.Т.Гороновский, Ю.П.Назаренко, Е.Ф.Некряч. Краткий справочник по химии. — Пятое издание, исправленное и дополненное. — Киев: Наукова Думка, 1987. — С. 348. — 828 с.
Литература[править | править код]
- Березов Т. Т., Коровкин Б. Ф. [www.xumuk.ru/biologhim/ Биологическая химия: Учебник] / Под. ред. акад. АМН СССР С. С. Дебова.— 2-е изд., перераб. и доп.— М.: Медицина,— 1990.— 528 с., С. 452—455. ISBN 5-225-01515-8.
- Ершов. Общая химия.Биофизическая химия.Химия биогенных элементов. — Издание восьмое,стереотипное. — Москва: Высшая школа, 2010. — 559 с. — ISBN 978-5-06-006180-2.
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист. Эти сайты могут нарушать авторские права, быть признаны неавторитетными источниками или по другим причинам быть запрещены в Википедии. Редакторам следует заменить такие ссылки ссылками на соответствующие правилам сайты или библиографическими ссылками на печатные источники либо удалить их (возможно, вместе с подтверждаемым ими содержимым). |
Источник
Установлено,
что состоянию нормы соответствует определенный диапазон колебаний рН крови – от
7,37 до 7,44 со средней величиной 7,40 . Кровь представляет собой взвесь
клеток в жидкой среде, поэтому ее кислотно-основное равновесие поддерживается
совместным участием буферных систем плазмы и клеток крови. Важнейшими буферными
системами крови являются бикарбонатная, фосфатная, белковая и наиболее мощная
гемогло-биновая.
Бикарбонатная буферная система – мощная и, пожалуй, самая управляемая система внеклеточной
жидкости и крови. На долю бикарбонатного буфера приходится около 10% всей
буферной емкости крови. Бикарбонатная система
представляет собой сопряженную кислотно-основную пару, состоящую из молекулы
угольной кислоты Н2СО3, выполняющую роль донора протона,
и бикарбонат-иона НСО3–, выполняющего роль акцептора
протона:
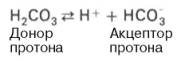
Для данной
буферной системы величину рН в растворе можно выразить через константу
диссоциации угольной кислоты (рКН2СО3) и логарифм концентрации
недиссоциированных молекул Н2СО3 и ионов HCO3–:
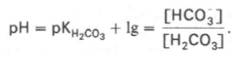
Истинная
концентрация недиссоциированных молекул Н2СО3 в крови
незначительна и находится в прямой зависимости от концентрации растворенного
углекислого газа (СО2 + Н2О <=> Н2СО3).
Поэтому удобнее пользоваться тем вариантом уравнения, в котором рКH2СО3
заменена «кажущейся» константой диссоциации Н2СО3,
учитывающей общую концентрацию растворенного СО2 в крови:
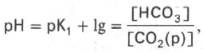
где K1– «кажущаяся» константа диссоциации Н2 С О3 ; [СО2(р)]
– концентрация растворенного СО2.
При
нормальном значении рН крови (7,4) концентрация ионов бикарбоната НСО3
в плазме крови превышает концентрацию СО2 примерно в 20 раз.
Бикарбонатная буферная система функционирует как эффективный регулятор в
области рН 7,4.
Механизм
действия данной системы заключается в том, что при выделении в кровь
относительно больших количеств кислых продуктов водородные ионы Н+
взаимодействуют с ионами бикарбоната НСО3–, что приводит
к образованию слабодиссоциирующей угольной кислоты Н2СО3.
Последующее снижение концентрации Н2СО3 достигается в
результате ускоренного выделения СО2 через легкие в результате их
гипервентиляции (напомним, что концентрация Н2СО3 в плазме
крови определяется давлением СО2 в альвеолярной газовой смеси).
Если в крови
увеличивается количество оснований, то они, взаимодействуя со слабой угольной
кислотой, образуют ионы бикарбоната и воду. При этом не происходит
сколько-нибудь заметных сдвигов в величине рН. Кроме того, для сохранения
нормального соотношения между компонентами буферной системы в этом случае
подключаются физиологические механизмы регуляции кислотно-основного равновесия:
происходит задержка в плазме
крови некоторого количества СО2 в результате гиповентиляции легких
. Как будет показано далее, данная буферная система тесно связана с
гемоглобиновой системой.
Фосфатная буферная система представляет собой сопряженную кислотно-основную пару,
состоящую из иона Н2РО4– (донор протонов) и
иона НРО42– (акцептор протонов):
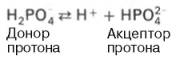
Роль кислоты
в этой системе выполняет однозамещенный фосфат NaH2PO4,
а роль соли двузамещенный фосфат – Na2HPO4.
Фосфатная
буферная система составляет всего лишь 1% от буферной емкости крови. В других
тканях эта система является одной из основных. Для фосфатной буферной системы
справедливо следующее уравнение:
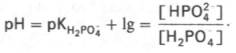
Во
внеклеточной жидкости, в том числе в крови, соотношение [НРО42–]:
[Н2РО4–] составляет 4:1. Величина рКН2РО4–
равна 6,86.
Буферное
действие фосфатной системы основано на возможности связывания водородных ионов
ионами НРО42– с образованием Н2РО4–
(Н+ + + НРО42– —> Н2РО4–),
а также ионов ОН– с ионами Н2РО4–
(ОН– + + Н2 Р О4– —> HPO42–+ H2O). Буферная пара (Н2РО4––НРО42–)
способна оказывать влияние при изменениях рН в интервале от 6,1 до 7,7 и может
обеспечивать определенную буферную емкость внутриклеточной жидкости, величина
рН которой в пределах 6,9–7,4. В крови максимальная емкость фосфатного буфера
проявляется вблизи значения рН 7,2. Фосфатный буфер в крови находится в тесном
взаимодействии с бикарбонатной буферной системой. Органические фосфаты также
обладают буферными свойствами, но мощность их слабее, чем неорганического
фосфатного буфера.
Белковая буферная система имеет меньшее значение для поддержания КОР в плазме крови,
чем другие буферные системы.
Белки
образуют буферную систему благодаря наличию кислотно-основных групп в молекуле
белков: белок–Н+ (кислота, донор протонов) и белок (сопряженное
основание, акцептор протонов). Белковая буферная система плазмы крови
эффективна в области значений рН 7,2–7,4.
Гемоглобиновая буферная система – самая мощная буферная система крови. Она в 9 раз мощнее
бикарбонатного буфера; на ее долю приходится 75% от всей буферной емкости
крови.
Участие
гемоглобина в регуляции рН крови связано с его ролью в транспорте кислорода и
углекислого газа. Константа диссоциации кислотных групп гемоглобина меняется в
зависимости от его насыщения кислородом. При насыщении кислородом гемоглобин
становится более сильной кислотой (ННbО2). Гемоглобин, отдавая
кислород, превращается в очень слабую органическую кислоту (ННb).
Итак,
гемоглобиновая буферная система состоит из неионизированного гемоглобина ННb
(слабая органическая кислота, донор протонов) и калиевой соли
гемоглобина КНb (сопряженное основание, акцептор протонов). Точно так же может
быть рассмотрена оксигемоглобиновая буферная система. Система гемоглобина и
система оксигемоглобина являются вза-имопревращающимися системами и существуют
как единое целое. Буферные свойства гемоглобина прежде всего обусловлены
возможностью взаимодействия кисло реагирующих соединений с калиевой солью
гемоглобина с образованием эквивалентного количества соответствующей калийной
соли кислоты и свободного гемоглобина:
КНb + Н2СO3—> КНСO3 + ННb.
Именно таким образом
превращение калийной соли гемоглобина эритроцитов в свободный ННb с
образованием эквивалентного количества бикарбоната обеспечивает поддержание рН
крови в пределах физиологически допустимых величин, несмотря на поступление в
венозную кровь огромного количества углекислого газа и других кисло реагирующих
продуктов обмена.
Гемоглобин
(ННb), попадая в капилляры легких, превращается в окси-гемоглобин (ННbО2),
что приводит к некоторому подкислению крови, вытеснению части Н2СО3
из бикарбонатов и понижению щелочного резерва крови . Перечисленные буферные
системы крови играют важную роль в регуляции кислотно-основного равновесия. Как
отмечалось, в этом процессе, помимо буферных систем крови, активное участие
принимают также система дыхания и мочевыделительная система.
Источник
Буферные системы
Буферные системы – это соединения, противодействующие резким изменениям концентрации ионов Н+. Любая буферная система – это кислотно-основная пара: слабое основание (анион, А–) и слабая кислота (Н-Анион, H-А). Они минимизируют сдвиги количества ионов Н+ за счет их связывания с анионом и включения в плохо диссоциирующее соединение – в слабую кислоту. Поэтому общее количество ионов Н+ изменяется не так заметно, как это могло бы быть.
Существует три буферные системы жидкостей организма – бикарбонатная, фосфатная, белковая (включая гемоглобиновую).Они вступают в действие моментально и через несколько минут их эффект достигает максимума возможного.
Фосфатная буферная система
Фосфатная буферная система составляет около 2% от всей буферной емкости крови и до 50% буферной емкости мочи. Она образована гидрофосфатом (HPO42–) и дигидрофосфатом (H2PO4–). Дигидрофосфат слабо диссоциирует и ведет себя как слабая кислота, гидрофосфат обладает щелочными свойствами. В норме отношение HРO42– к H2РO4– равно 4 : 1.
При взаимодействии кислот (ионов Н+) с двузамещенным фосфатом (HPO42‑) образуется дигидрофосфат (H2PO4–):
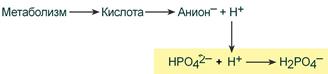
Удаление ионов H+ фосфатным буфером
В результате концентрация ионов Н+ понижается.
При поступлении в кровь оснований (избыток ОН–‑групп) они нейтрализуются поступающими в плазму от H2PO4– ионами Н+:
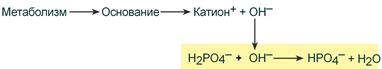
Удаление щелочных эквивалентов фосфатным буфером
Роль фосфатного буфера особенно высока во внутриклеточном пространстве и в просвете почечных канальцев. Кислотно-основная реакция мочи зависит только от содержания дигидрофосфата (H2PO4–), т.к. бикарбонат натрия в почечных канальцах реабсорбируется.
Бикарбонатная буферная система
Эта система самая мощная, на ее долю приходится 65% всей буферной мощности крови. Она состоит из бикарбонат-иона (НСО3–) и угольной кислоты (Н2СО3). В норме отношение HCO3– к H2CO3 равно 20 : 1.
При поступлении в кровь ионов H+ (т.е. кислоты) ионы бикарбоната натрия взаимодействуют с ней и образуется угольная кислота:
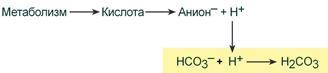
При работе бикарбонатной системы концентрация водородных ионов понижается, т.к. угольная кислота является очень слабой кислотой и плохо диссоциирует. При этом в крови не происходит параллельного значимого увеличения концентрации НСО3–.
Если в кровь поступают вещества с щелочными свойствами, то они реагируют с угольной кислотой и образуют ионы бикарбоната:
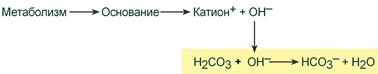
Работа бикарбонатного буфера неразрывно связана с дыхательной системой (с вентиляцией легких). В легочных артериолах при снижении плазменной концентрации СО2 и благодаря присутствию в эритроцитах фермента карбоангидразы угольная кислота быстро расщепляется с образованием CO2, удаляемого с выдыхаемым воздухом:
Н2СО3→ Н2О + СО2↑
Кроме эритроцитов, значительная активность карбоангидразы отмечена в эпителии почечных канальцев, клетках слизистой оболочки желудка, коре надпочечников и клетках печени, в незначительных количествах – в центральной нервной системе, поджелудочной железе и других органах.
Белковая буферная система
Белки плазмы, в первую очередь альбумин, играют роль буфера благодаря своим амфотерным свойствам. Их вклад в буферизацию плазмы крови около 5%.
В кислой среде подавляется диссоциация СООН‑групп аминокислотных радикалов (в аспарагиновой и глутаминовой кислотах), а группы NH2 (в аргинине и лизине) связывают избыток Н+. При этом белок заряжается положительно.
В щелочной среде усиливается диссоциация COOH‑групп, поступающие в плазму ионы Н+ связывают избыток ОН–‑ионов и pH сохраняется. Белки в данном случае выступают как кислоты и заряжаются отрицательно.
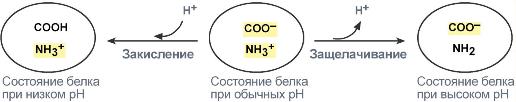
Изменение заряда буферных групп белка при различных рН
Гемоглобиновая буферная система
Высокой мощностью в крови обладает гемоглобиновый буфер, на него приходится до 28% всей буферной емкости крови. В качестве кислой части буфера выступает оксигенированный гемоглобин H‑HbO2. Он имеет выраженные кислотные свойства и в 80 раз легче отдает ионы водорода, чем восстановленный Н‑Нb, выступающий как основание. Гемоглобиновый буфер можно рассматривать как часть белкового, но его особенностью является работа в теснейшем контакте с бикарбонатной системой.
Изменение кислотности гемоглобина происходит в тканях и в легких, и вызывается связыванием соответственно H+ или О2. Непосредственный механизм действия буфера заключается в присоединении или отдаче иона H+ остатком гистидина в глобиновой части молекулы (эффект Бора).
В тканях более кислый pH в норме является результатом накопления минеральных (угольной, серной, соляной) и органических кислот (молочной). При компенсации pH данным буфером ионы H+ присоединяются к пришедшему оксигемоглобину (HbО2) и превращают его в H‑HbО2. Это моментально вызывает отдачу оксигемоглобином кислорода (эффект Бора) и он превращается в восстановленный H‑Hb.
НbO2+ Н+ → [H-HbO2] → Н-Hb + O2
В результате снижается количество кислот, в первую очередь Н2СО3, продуцируются ионы НСО3‑ и тканевое пространство подщелачивается.
В легких после удаления СО2 (угольной кислоты) происходит защелачивание крови. При этом присоединение О2 к дезоксигемоглобину H-Hb образует кислоту более сильную, чем угольная. Она отдает свои ионы Н+ в среду, предотвращая повышение рН:
Н-Hb + O2 → [H-HbO2] → НbO2 + Н+
Работу гемоглобинового буфера рассматривают неотрывно от бикарбонатного буфера:
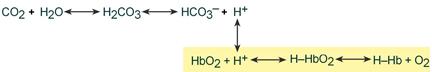
Эффективность гемоглобинового буфера напрямую зависит от активности дыхательной системы (Газообмен в легких и тканях).
Источник
