Факторы влияющие на сродство гемоглобина к кислороду
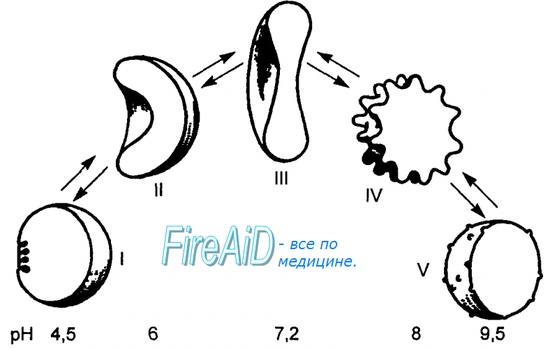
Оглавление темы “Вентиляция легких. Перфузия легких кровью.”: Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
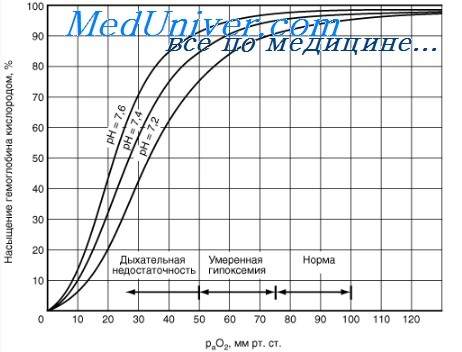
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц. Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН. Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани. Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей. – Также рекомендуем “Углекислый газ. Транспорт углекислого газа.” |
Источник
Динамика кривой зависит от нескольких факторов. Кривая может сдвигаться относительно оси абсцисс вправо или влево (эффект Бора) в зависимости от сопутствующего парциального давления двуокиси углерода и величины рН. При этом реальная физиологическая кривая имеет S-образную форму. При увеличении содержания двуокиси углерода и закис-лении крови кривая диссоциации оксигемоглобина сдвигается вправо и, напротив, при снижении РСо2 и защелачивания крови кривая сдвигается влево.
Биологическое значение кривой диссоциации оксигемоглобина.Кривая диссоциации оксигемоглобина имеет важное биологическое значение для переноса кислорода кровью. Участок кривой, соответствующий низким парциальным значениям кислорода, характеризует содержание оксигемоглобина в капиллярах тканей, а фрагмент кривой, лежащий в области высокого парциального давления кислорода 80—100 мм рт.ст., соответствует крови в легочных капиллярах.
Эффективность транспорта кислородак тканям определяют два фактора: количество оксигемоглобина, образовавшегося в легких, и количество кислорода, отдаваемого тканям, что зависит от степени распада оксигемоглобина в восстановленный гемоглобин. Процесс наиболее эффективного переноса кислорода к тканям соответствует S-образной форме кривой диссоциации оксигемоглобина. В области высокого парциального давления кислорода кривая близка к насыщению кислородом крови, а в области низких значений парциального давления кислорода в тканях значительная часть оксигемоглобина отдает кислород и превращается в восстановленную форму.
Эффект Бора. Огромное биологическое значение для транспорта кислорода и двуокиси углерода имеет эффект Бора.
При увеличении парциального давления двуокиси углерода в тканях кривая диссоциации оксигемоглобина, сдвигаясь вправо, отражает повышение способности оксигемоглобина отдавать кислород тканям и тем самым высвобождаться для дополнительного связывания двуокиси углерода и переноса ее избытка из тканей в легкие.
Напротив, при снижении парциального давления двуокиси углерода и смещении рН крови в основную сторону (алкалоз) сдвиг кривой диссоциации оксигемоглобина влево означает снижение способности оксигемоглобина отдавать кислород тканям и поглощать двуокись углерода для транспорта ее к легким.
Сдвиг кривой диссоциации оксигемоглобина иллюстрирует взаимосвязь транспорта кислорода и двуокиси углерода в крови и сродство гемоглобина к этим газам.
#82 Объясните мех-мы транспорта углекислого газа кровью, роль карбоангидразы. Проанализируйте роль дыхания в регуляции рН крови.
Перенос углекислого газа. Двуокись углерода, образующаяся в тканях, переносится с кровью к легким и выделяется с выдыхаемым воздухом в атмосферу. В отличие от транспорта кислорода она транспортируется кровью тремя способами.
Формы транспорта углекислого газа. Во-первых, так же как и кислород, двуокись углерода переносится в физически растворенном состоянии. Содержание физически растворенной двуокиси углерода в артериальной крови составляет 0,026 мл в 1 мл крови, что в 9 раз превышает количество физически растворенного кислорода. Это объясняется гораздо более высоким коэффициентом растворимости двуокиси углерода.
Во-вторых, двуокись углерода транспортируется в виде химического соединения с гемоглобином — карбогемоглобина.
В третьих — в виде гидрокарбоната НСОз, образующегося в результате диссоциации угольной кислоты.
Механизм переноса двуокиси углерода. Перенос двуокиси углерода из тканей в легкие осуществляется следующим образом. Наибольшее парциальное давление двуокиси углерода в клетках тканей и в тканевой жидкости — 60 мм рт.ст.; в притекающей артериальной крови оно составляет 40 мм рт.ст. Благодаря этому градиенту двуокись углерода движется из тканей в капилляры. В результате ее парциальное давление возрастает, достигая в венозной крови 46—48 мм рт.ст. Под влиянием высокого парциального давления часть двуокиси углерода физически растворяется в плазме крови.
Роль карбоангидразы. Большая же часть двуокиси углерода претерпевает химические превращения. Благодаря ферменту карбоангидразе она соединяется с водой, образуя угольную кислоту Н2СО3. Особенно активно эта реакция идет в эритроцитах, мембрана которых хорошо проницаема для двуокиси углерода.
Угольная кислота (Н2СО3) диссоциирует на ионы водорода Н+ и гидрокарбоната (НСОз), которые проникают через мембрану в плазму.
Наряду с этим двуокись углерода соединяется с белковым компонентом гемоглобина, образуя карбоаминовую связь.
В целом 1 л венозной крови фиксирует около 2 ммоль двуокиси углерода. Из этого количества 10 % находится в виде карбоаминовой связи с гемоглобином, 35 % составляют ионы гидрокарбоната в эритроцитах, и оставшиеся 55 % представлены угольной кислотой в плазме.
Источник
Факторы влияющие на КДО. Влияние температуры на кривую диссоциации оксигемоглобина (КДО)
Обсуждению этого вопроса посвящена обширная литература. Считается, что наибольшее влияние на положение КДО оказывает кислотность среды (эффект Бора). Было установлено, что при Ph больше 6,0 в крови преобладает оксигемоглобин, при Ph менее 6,0 — восстановленный гемоглобин.
Было установлено также, что на величину Р50 влияет находящееся в эритроците фосфорное соединение 2,3 дифосфоглицерат (2,3-ДФГ) и что концентрация этого вещества увеличивается по мере снижения Ph. Высказывалось даже предположение, что на положение кривой диссоциации оксигемоглобина Ph влияет через 2,3-ДФГ. Это предположение в дальнейшем частично подтвердилось, что позволило окончательно прояснить роль Ph в изменениях положения КДО.
Ph, изменяя структуры групп гемоглобина, связанных с кислородом, непосредственно влияет на аффинитет гемоглобина с кислородом. Кроме того, Ph оказывает на положение КДО опосредованное влияние через содержание в эритроците 2,3-ДФГ, поскольку кислая среда активирует образование этого фосфата, а щелочная среда его ингибирует.
Однако 2,3-ДФГ и сам может непосредственно влиять на положение КДО. Воздействуя на атомы железа в молекулах гемоглобина, 2,3-ДФГ снижает сродство гемоглобина к кислороду и способствует ускорению диссоциации оксигемоглобина. Установлено, что увеличение 2,3-ДФГ на 1 ммоль/л повышает Р50 на 1,23 мм Нд. На содержание в эритроците 2,3-ДФГ оказывают непосредственное влияние неорганические фосфаты, тиреоидные и некоторые гипофизарные гормоны.
Основная роль напряжения углекислоты в регуляции положения КДО реализуется через влияние ее на кислотность среды. При гиперкапнии Ph снижается, при гипокапнии — повышается.
Температура крови оказывает серьезное влияние на положение кривой диссоциации оксигемоглобина. Установлено, что при гипертермии КДО смещается вправо, при гипотермии — влево.
Этот феномен имеет серьезный физиологический смысл. В альвеоле притекающая кровь контактирует с охлажденным альвеолярным воздухом, что способствует смещению КДО влево и повышению аффинитета гемоглобина с кислородом. Ускоряется оксигенация крови.
В тканях, особенно в функционирующей мышечной ткани, температура всегда повышена. Это способствует смещению КДО вправо и снижению сродства гемоглобина к кислороду, что облегчает переход кислорода в клетки.
Воздействие температуры на положение КДО усиливается под влиянием 2,3-ДФГ. При низком содержании этого фосфата в эритроците, при прочих равных условиях, влияние гипотермии на увеличение аффинитета гемоглобина к кислороду существенно повышается и способствует большему смещению кривой влево.
Данный феномен создает серьезные проблемы для реаниматолога в случаях переохлаждения организма пострадавшего (длительное нахождение в холодной воде, замерзание при отрицательной температуре воздуха, особенно в состоянии алкогольного опьянения). В этой ситуации сродство гемоглобина к кислороду может быть столь высоким, что на тканевом уровне практически прекращается газообмен.
Противоположная ситуация возникает при гипертермии, при которой на фоне резкого увеличения потребности в кислороде в силу низкого аффинитета гемоглобина к кислороду (смещение КДО вправо) возникают сложности в оксигенации крови в легких.
– Также рекомендуем “Значение положения кривой диссоциации оксигемоглобина (КДО). Механизм формирования КДО”
Оглавление темы “Параметры потребления кислорода и гемодинамики”:
1. Кривая диссоциации оксигемоглобина (КДО). Физиологический смысл КДО
2. Кислородтранспортная функция крови. Нормальная кривая диссоциации оксигемоглобина (КДО)
3. Факторы влияющие на КДО. Влияние температуры на кривую диссоциации оксигемоглобина (КДО)
4. Значение положения кривой диссоциации оксигемоглобина (КДО). Механизм формирования КДО
5. Гемодинамические параметры. Кислородный поток и потребление кислорода
6. Факторы влияющие на потребление кислорода. Предупреждение критической тканевой гипоксии
7. Законы Старлинга. Сердечный выброс по Старлингу
8. Регуляция сердечного выброса по кислороду. Влияние венозного притока на сократимость миокарда
9. Современный взгляд на сердечный выброс. Взаимоотношение факторов влияющих на сократимость миокарда
10. Неконтролируемая внутривенная инфузия. Кривая венозного притока
Источник

Динамика кривой зависит от нескольких факторов. Кривая может сдвигаться относительно оси абсцисс вправо или влево (эффект Бора) в зависимости от сопутствующего парциального давления двуокиси углерода и величины рН. При этом реальная физиологическая кривая имеет S-образную форму. При увеличении содержания двуокиси углерода и закис-лении крови кривая диссоциации оксигемоглобина сдвигается вправо и, напротив, при снижении РСо2 и защелачивания крови кривая сдвигается влево.
Биологическое значение кривой диссоциации оксигемоглобина. Кривая диссоциации оксигемоглобина имеет важное биологическое значение для переноса кислорода кровью. Участок кривой, соответствующий низким парциальным значениям кислорода, характеризует содержание оксигемоглобина в капиллярах тканей, а фрагмент кривой, лежащий в области высокого парциального давления кислорода 80—100 мм рт.ст., соответствует крови в легочных капиллярах.
Эффективность транспорта кислорода к тканям определяют два фактора: количество оксигемоглобина, образовавшегося в легких, и количество кислорода, отдаваемого тканям, что зависит от степени распада оксигемоглобина в восстановленный гемоглобин. Процесс наиболее эффективного переноса кислорода к тканям соответствует S-образной форме кривой диссоциации оксигемоглобина. В области высокого парциального давления кислорода кривая близка к насыщению кислородом крови, а в области низких значений парциального давления кислорода в тканях значительная часть оксигемоглобина отдает кислород и превращается в восстановленную форму.
Эффект Бора. Огромное биологическое значение для транспорта кислорода и двуокиси углерода имеет эффект Бора.
При увеличении парциального давления двуокиси углерода в тканях кривая диссоциации оксигемоглобина, сдвигаясь вправо, отражает повышение способности оксигемоглобина отдавать кислород тканям и тем самым высвобождаться для дополнительного связывания двуокиси углерода и переноса ее избытка из тканей в легкие.
Напротив, при снижении парциального давления двуокиси углерода и смещении рН крови в основную сторону (алкалоз) сдвиг кривой диссоциации оксигемоглобина влево означает снижение способности оксигемоглобина отдавать кислород тканям и поглощать двуокись углерода для транспорта ее к легким.
Сдвиг кривой диссоциации оксигемоглобина иллюстрирует взаимосвязь транспорта кислорода и двуокиси углерода в крови и сродство гемоглобина к этим газам.
№ 33 Транспорт газов кровью: перенос углекислого газа. Формы транспорта углекислого газа. Роль карбоангидразы. Роль дыхания в регуляции рН крови.
Перенос углекислого газа. Двуокись углерода, образующаяся в тканях, переносится с кровью к легким и выделяется с выдыхаемым воздухом в атмосферу. В отличие от транспорта кислорода она транспортируется кровью тремя способами.
Формы транспорта углекислого газа. Во-первых, так же как и кислород, двуокись углерода переносится в физически растворенном состоянии. Содержание физически растворенной двуокиси углерода в артериальной крови составляет 0,026 мл в 1 мл крови, что в 9 раз превышает количество физически растворенного кислорода. Это объясняется гораздо более высоким коэффициентом растворимости двуокиси углерода.
Во-вторых, двуокись углерода транспортируется в виде химического соединения с гемоглобином — карбогемоглобина.
В третьих — в виде гидрокарбоната НСОз, образующегося в результате диссоциации угольной кислоты.
Механизм переноса двуокиси углерода. Перенос двуокиси углерода из тканей в легкие осуществляется следующим образом. Наибольшее парциальное давление двуокиси углерода в клетках тканей и в тканевой жидкости — 60 мм рт.ст.; в притекающей артериальной крови оно составляет 40 мм рт.ст. Благодаря этому градиенту двуокись углерода движется из тканей в капилляры. В результате ее парциальное давление возрастает, достигая в венозной крови 46—48 мм рт.ст. Под влиянием высокого парциального давления часть двуокиси углерода физически растворяется в плазме крови.
Роль карбоангидразы. Большая же часть двуокиси углерода претерпевает химические превращения. Благодаря ферменту карбоангидразе она соединяется с водой, образуя угольную кислоту Н2СО3. Особенно активно эта реакция идет в эритроцитах, мембрана которых хорошо проницаема для двуокиси углерода.
Угольная кислота (Н2СО3) диссоциирует на ионы водорода Н+ и гидрокарбоната (НСОз), которые проникают через мембрану в плазму.
Наряду с этим двуокись углерода соединяется с белковым компонентом гемоглобина, образуя карбоаминовую связь.
В целом 1 л венозной крови фиксирует около 2 ммоль двуокиси углерода. Из этого количества 10 % находится в виде карбоаминовой связи с гемоглобином, 35 % составляют ионы гидрокарбоната в эритроцитах, и оставшиеся 55 % представлены угольной кислотой в плазме.
Дата добавления: 2018-11-12; просмотров: 117 | Нарушение авторских прав | Изречения для студентов
Читайте также:
Рекомендуемый контект:
Поиск на сайте:
© 2015-2020 lektsii.org – Контакты – Последнее добавление
Источник

