Федеральные рекомендации по лечению анемии
Син.: анемия воспаления
Код по МКБ-1 D63.8
Анемия хронических болезней (АХБ) является второй по распространенности после
ЖДА и наблюдается у пациентов с острой или хронической активацией иммунной
системы вследствие различных как инфекционных, так и неинфекционных заболеваний
(см. рисунок).

Рисунок 1. Наиболее частые причины анемий в клинической практике.
Наиболее частые состояния, которые могут приводить к развитию АХБ, представлены в таблице (см. таблицу).
В настоящее время считается, что образование гепцидина – ключевой механизм развития АХБ. Являясь гормоном, секретируемым гепатоцитами в условиях воспаления, гепцидин блокирует всасывания железа в кишечнике и реутилизацию железа из депо (депонирование железа в клетках моноцитарно-макрофагальной системы), тем самым снижая концентрацию железа в плазме крови, что способствует развитию железодефицитного эритропоэза. Другим важным фактором развития АХБ является неадекватно низкая продукция ЭПО вследствие избыточной продукции провоспалительных цитокинов. Таким образом, ведущую роль в развитии АХБ играет
комплекс факторов, основными из которых являются нарушение гомеостаза железа
вследствие повышенной продукции гепцидина и нарушение эритропоэза в виде
неадекватно низкой продукции ЭПО степени анемии, что является патогенетическим
обоснованием терапевтического применения при них эритропоэзстимулирующих
препаратов (ЭСП).
АХБ развивается не только при хронических, но и острых воспалительных заболеваниях. Снижение уровня Hb можно обнаружить уже менее, чем через 2 недели
от начала заболевания. Обычно это умеренная, микроцитарная анемия с уровнем Hb
90-130 г/л и гематокритом 30-40%. Лишь у 20% пациентов гематокрит может снижаться меньше 25%. При хроническом течении анемии, она становится более
гипохромной с более выраженным воспалительным компонентом в ее этиологии. При
острой инфекции, когда анемия развивается быстро, она часто нормохромная.
| Заболевания, ассоциируемые с анемией хронических болезней | Предположительная распространенность анемии при данном заболевании (%) |
|---|---|
Инфекции (острые и хронические)
| 18 – 95 |
Рак
| 30 – 77 |
Аутоиммунные реакции
| 8 – 71 |
Хроническая реакция трансплантат против | 8 – 70 |
Хронические заболевания почек | 23 – 50 |
1.1. Особенности диагностики анемии хронических болезней
Принципиальное различие между ЖДА и АХБ заключается в том, что ЖДА имеет
отношение к абсолютному дефициту железа, тогда как патофизиология АХБ является
мультифакторной. С высокой долей вероятности об АХБ следует думать, если анемия
развилась на фоне тяжелых заболеваний. АХБ необходимо также исключить в случаях,
когда перо-ральная ферротерапия в течение 4 нед не привела к повышению НЬ >10 г/л.
С этой целью проводится определение биохимических показателей обмена железа с расчетом коэффициента НТЖ и концентрации сывороточного ферритина СФ (см. клинические рекомендации по ЖДА, дифференциальная диагностика). Следует
учитывать, что уровень СФ повышается в условиях воспаления (острые и хронические
инфекции, болезни печени, аутоиммунные и онкологические заболевания), что может
маскировать наличие дефицита железа (ДЖ). Поэтому при повышенном уровне СРБ
(>10 мкг/л) ДЖ констатируется при СФ <50 мкг/л.
Для выявления ДЖ в случаях часто встречающегося сочетания ЖДА и АХБ, при
котором ФС, как правило, нормальный или повышен, в клинической практике
рекомендуется использование коэффициента НТЖ. У пациентов с АХБ в сочетании с
ДЖ НТЖ меньше возрастного уровня, представленного в таблице см. таблицу.
Насыщение трансферрина железом, % | – 1–2 года – < 9% – 3–5 лет – < 13% – 6–15 лет – < 14% – старше 15 лет- <16% |
* не имеют самостоятельного значения для диагностики ДЖ
Нормальный уровень сывороточного трансферринового рецептора 1 (сТФР) и высокая концентрация гепцидина, характерные для АХБ, вероятно, имеют высокую
диагностическую ценность. Однако их применение в клинической практике ограничивается отсутствием доступных коммерческих тест-систем и стандартизации в
педиатрической практике.
1.2. Лечение АХБ
Адекватное лечение основного заболевания – наиболее эффективный способ лечения
АХБ. Однако лечение АХБ необходимо при всех хронических заболеваниях трудно
поддающихся терапии (системные заболевания соединительной ткани, хронические
воспалительные заболевания кишечника, ВИЧ-инфекция и др.), поскольку анемия
значительно ухудшает прогноз и исходы этих заболеваний и является независимым
фактором риска повышенной летальности. Поскольку гепцидин блокирует всасывания
железа в кишечнике, лечение АХБ пероральными препаратами железа не эффективно.
Частичный эффект от пероральной ферротерапии может наблюдаться у пациентов с АХБ, развившейся на фоне ДЖ. Внутривенная ферротерапия с патогенетической точки
зрения более целесообразна при АХБ, однако если она используется в виде
монотерапии (только в случаях доказанного при АХБ ДЖ по низкому уровню НТЖ или
ФС) следует ожидать высокого уровня резистентности (около 50%) к терапии. Это
связано с неадекватно низкой продукцией ЭПО степени тяжести анемии, характерной
для АХБ. Поэтому наиболее эффективной схемой лечения АХБ является
комбинированное использование ЭСП и внутривенных препаратов железа.
Использование пероральных препаратов железа вместо внутривенной ферротерапии
допустимо, но может снижать ответ на рчЭПО терапию.
В настоящее время самый большой опыт применения рч ЭПО у детей и подростков
имеется у пациентов с хронической почечной недостаточностью (см. соответствующие
клинические рекомендации). В литературе доступны немногочисленные публикации о
эффективности рч ЭПО в сочетании с препаратами железа при АХБ у детей.
С практической точки зрения уровень сывороточного ЭПО (с-ЭПО), определяемый у
пациента с анемией, не может просто сравниваться с нормальным значением ЭПО.
Продукция ЭПО почками увеличивается обратно пропорционально степени гипоксии
(снижения концентрации Hb). Поэтому уровень с-ЭПО следует оценивать
относительно степени тяжести анемии. В каждой лаборатории рекомендуется на
основании анализа данных обследования популяции пациентов с анемией (чаще с
ЖДА) рассчитать уравнение регрессии Hb-ЭПО, которое будет моделью адекватности
продукции ЭПО степени тяжести анемии.
Для врача-клинициста важно все анемии разделить на две большие группы: I – анемии
с адекватной продукцией ЭПО и II – анемии с неадекватно низкой продукцией ЭПО
степени тяжести анемии.
Оценку адекватности продукции ЭПО проводят на основании определения отношения
логарифма, определяемого (О) уровня ЭПО (в исследуемой сыворотке) к логарифму предполагаемого (П) уровня ЭПО (в контрольной сыворотке пациента с ЖДА с тем же уровнем Hb) – коэффициент О/П (log ЭПО). Продукцию ЭПО считают неадекватно низкой степени анемии при О/П (log ЭПО) < 0,8.
При анемии с адекватной продукцией ЭПО выявляется высокая степень обратной зависимости уровня Hb от концентрации сывороточного ЭПО. То есть, чем ниже уровень Hb, тем выше концентрация ЭПО в сыворотке крови. Моделью адекватной продукции ЭПО степени анемии является ЖДА (верхняя прямая см.рисунок). При анемиях с неадекватно низкой продукцией ЭПО обратная зависимость уровня Hb от концентрации ЭПО низкая (нижняя прямая см.рисунок). Уровень эндогенного ЭПО при этом виде анемии, если и повышается, то незначительно, и не соответствует
степени снижения уровня Hb (неадекватно низкая степени анемии продукция ЭПО). В группу ЭДА относятся: анемия при хронической почечной недостаточности, АХБ,
ранняя анемия недоношенных, анемия при злокачественных новообразованиях, анемия при хронической сердечной недостаточности, анемия беременных.

Рисунок 2. Зависимость между уровнем Hb и концентрацией сывороточного эритропоэтина (ЭПО) (Log шкала) при анемии с адекватной (верхняя прямая) и неадекватно низкой (нижняя прямая) продукцией ЭПО.
В клинической практике уровень с-ЭПО <100 МЕ/л при НЬ <100 г/л может служить
индикатором неадекватно низкой продукции ЭПО степени тяжести анемии и
предиктором эффективного ответа на рчЭПО-терапию.
Уменьшение продукции ЭПО при ЭДА приводит к гипопролифера-тивному эритропоэзу. Получен ряд убедительных данных, что неадекватно низкая продукция ЭПО является следствием воздействия провоспалительных цитокинов (IJ.-1.TNF-аи INF-y). Повышенные плазменные концентрации этих цитокинов описаны у пациентов с различными ЭДА. Выявление неадекватно низкой продукции ЭПО у пациента с анемией.
1.3. Протокол применения рекомбинантного человеческого эритропоэтина для лечения АХБ у детей и подростков
Показания к применению:
Hb < 100 г/л
Противопоказания к применению:
гематокрит свыше 0,6;
лейкоцитоз свыше 40×109/л;
тромбоцитоз свыше 700×109/л;
индивидуальная непереносимость препарата
Сроки лечения:
продолжительность терапии до 12 недель.
Режимы дозирования:
150-300 МЕ/кг 3 раза в неделю подкожно или 600 МЕ/кг 1 раз в неделю внутривенно.
Терапевтический режим:
стартовая доза рч ЭПО – 150 МЕ/кг
на фоне лечения рчЭПО необходимо дополнительно назначать внутрь
или внутривенно препараты железа в суточной дозе не более 5 мг/кг для
профилактики функционального дефицита железа.
Лабораторный контроль:
общий анализ крови с подсчетом количества эритроцитов, гемоглобина,
гематокрита, ретикулоцитов, тромбоцитов перед началом терапии и на фоне
лечения каждые 7-10 дней.
Требования к результатам лечения:
целевой уровень Hb – 110 г/л
Коррекция дозы рч ЭПО:
При отсутствии полного терапевтического ответа через 2 недели применения рч-
ЭПО в дозе 150 МЕ/кг, определяемого как повышение уровня гемоглобина на ≥ 10 г/л
от исходного при отсутствии трансфузий эритроцитарной массы, разовая доза препарата увеличивается на 50 МЕ/кг. Последующее увеличение дозы рч-ЭПО
предусматривается каждые 2 недели на 50 МЕ/кг при условии недостаточной скорости
прироста уровня гемоглобина (< 5 г/л в неделю), максимально 300 МЕ/кг. Если доза в
300 МЕ/кг не дает эффекта, дальнейшее повышение дозы нецелесообразно.
Максимальная продолжительность введения рч-ЭПО – 12 недель. Если уровень Hb
повышается чрезмерно быстро (более чем на 20 г/л в неделю) или если его концентрация превышает 120 г/л, следует прекратить введение препарата.
Применение ЭСП при АХБ у детей патогенетически обосновано, однако имеет недостаточную доказательную базу. Необходимы многоцентровые рандомизированные
исследования для того, чтобы высказаться за или против применения ЭСП при АХБ в педиатрической практике. До этих пор применение ЭСП возможно в рамках исследовательских протоколов, а также в некоторых исключительных случаях, например, по религиозным убеждениям, как альтернатива гемотрансфузиям.
Диспансерное наблюдение
Учитывая симптоматический характер анемического синдрома, продолжительность наблюдения определяется клиникой основного заболевания.
Источник
Железодефицитная анемия (ЖДА) представляет собой клинико–гематологический синдром, возникающий при развитии дефицита железа вследствие различных патологических (физиологических) процессов и характеризующийся снижением уровня гемоглобина (в меньшей степени эритроцитов) наряду с клиническими признаками анемии и сидеропении.
Клинические рекомендации ведения больных ЖДА включают: – выявление причины ЖДА и при необходимости – ее коррекция; – обучение больных ЖДА; – принятие решения о назначении лекарственных препаратов железа (ПЖ); – выбор лекарственного ПЖ; – путь введения ПЖ (внутрь или парентерально); – длительность лечения и необходимость поддерживающей терапии; – контроль переносимости ПЖ и коррекция при плохой переносимости; – оценку эффективности и выявление причин отсутствия или недостаточного эффекта; – коррекцию выявленных причин неэффективности.
Выявление причины ЖДА и возможности ее коррекции
После верификации железодефицитного характера анемии, т.е. синдрома ЖДА, необходимо выявление причины, лежащей в основе данного варианта анемического синдрома (нозологическая диагностика). Для клинициста этот этап является не менее важным и вместе с тем наиболее трудным и ответственным, поскольку в основе имеющейся ЖДА могут лежать потенциально курабельные заболевания. Наличие в МКБ–10 рубрики «Железодефицитная анемия неуточненная» оставляет для врача «лазейку» в случаях отсутствия явной причины анемии, «освобождая» его от тщательности и углубления диагностического поиска на этапе нозологической диагностики. Следует особо подчеркнуть роль врача–интерниста на этапах синдромной и нозологической диагностики, поскольку подавляющее большинство больных ЖДА (независимо от конкретной причины) обращаются прежде всего, как и многие другие пациенты, к терапевту, а не к гематологу или другому специалисту. При выявлении причины ЖДА лечение должно быть направлено на устранение этой причины (по возможности) или коррекцию имеющихся нарушений – лечение эрозивно–язвенных процессов в желудке, оперативные лечения при опухолях ЖКТ, миоме матки, лечение энтеритов, коррекция алиментарной недостаточностии т.д.
Обучение больных
Существенным компонентом ведения больных ЖДА является повышение их образовательного уровня в отношении данной патологии, создание мотивации к лечению, вовлечение пациентов в контроль за своим состоянием и лабораторными показателями. Необходимо разъяснение сущности ЖДА, причин ее возникновения, реальных возможностей коррекции дефицита железа и нормализации уровня гемоглобина. Особое значение имеют обучающие программы у беременных женщин с наличием ЖДА и пациенток, страдающих меноррагиями. У беременных должна создаваться мотивация необходимости коррекции дефицита железа с целью предотвращения недостатка железа у плода. Больные должны быть осведомлены о возможных побочных эффектах при лечении лекарственными препаратами железа, необходимости соблюдения врачебных назначений, в том числе и регулярности приема ПЖ. Следует обязательно указать на недопустимость попыток коррекции дефицита железа с помощью различных пищевых продуктов, а также на строгие показания к назначению инъекционных форм ПЖ.
Принятие решения о назначении лекарственных препаратов железа
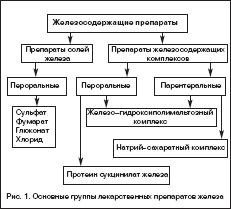
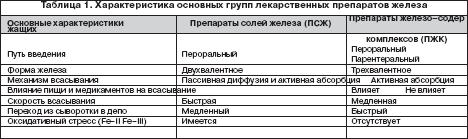
Всем больным ЖДА показана патогенетическая терапия препаратами железа. Следует подчеркнуть ошибочность мнения о возможности коррекции дефицита железа с помощью пищевых продуктов с высоким содержанием железа, что является одним из мифов в представлениях о ведении больных ЖДА. Об этом должны быть осведомлены больные, что следует считать важным образовательным компонентом ведения данной категории пациентов. Разумеется, пища должна быть богата продуктами, содержащими железо. Однако следует иметь в виду неодинаковую степень всасываемости железа из различных продуктов. Так например, железо, содержащееся в мясе в виде гема, всасывается на 40–50%, в то время как из растительных продуктов, овощей, фруктов всасывается всего 3–5% содержащегося в них железа. Поэтому средством выбора для коррекции дефицита железа и уровня гемоглобина у больных ЖДА являются лекарственные препараты железа. На фармацевтическом рынке России в настоящее время имеется большой арсенал ПЖ в различных лекарственных формах, с неодинаковым содержанием в них железа, наличием дополнительных компонентов, влияющих на биодоступность железа, различной стоимостью (рис. 1). Из ПСЖ железо всасывается в двухвалентной форме, в последующем превращается в трехвалетное, которое связывается с трансферрином и используется для построения молекулы гемоглобина. В ПЖК железо находится в трехвалентной форме и всасывается как бы в готовом виде. В ПЖК, в частности, в гидрооксиполимальтозном комплексе, связано как в физиологическом состоянии в молекуле ферритина. Существуют различия в механизмах всасывания железа из ПСЖ и ПЖК. Всасывание железа из ПСЖ происходит главным образом в виде пассивной диффузии согласно градиенту концентрации и в меньшей степени активно, в то время как абсорбция железа из ПЖК является активным процессом в виде конкурентного обмена. Это ведет к различному уровню железа в сыворотке, объему распределения, константам элиминации после абсорбции. Всасывание железа из ПЖК и нарастание его концентрации в сыворотке происходит медленно, но оно быстро поступает в запасы. При применении ПСЖ могут возникать нарушения окислительных процессов (оксидативные повреждения) вследствие превращения ионов двухвалентного железа в трехвалентное, которое соединяется с трансферрином и включается в молекулу гемоглобина. При окислении образуются свободные радикалы, которые вызывают клеточные повреждения, такие как перекисное окисление липидов, нарушение структуры мембранных и клеточных белков, повреждение клеточной ДНК и РНК. ПЖК в отличие от ПСЖ не вызывают «оксидативного стресса», поскольку ионы железа не меняют свою валентность в процессе всасывания (табл. 1). Для лучшей абсорбции ПСЖ рекомендуется принимать за час до еды т.е. на пустой желудок, что может вызывать нарушения со стороны желудка, кишечника и другие побочные эффекты. Современные технологии производства препаратов железа позволяют производить ПСЖ с замедленным высвобождением железа в тонком кишечнике, что уменьшает токсическое воздействие ионов железа на слизистую желудка. Частота побочных эффектов при лечении ПЖК меньше по сравнении с ПСЖ, что обеспечивает лучший комплайенс больных ЖДА. ПСЖ взаимодействуют с некоторыми пищевыми продуктами (танин, фитаты, соли кальция) и медикаментами (пленкообразующие препараты, тетрациклины, препараты кальция), снижающими биодоступность железа. В связи с этим ПСЖ не следует принимать одновременно с указанными пищевыми продуктами и лекарственными препаратами. В то же время пища и медикаменты не оказывают влияния на всасывание железа из ПЖК. Темпы прироста показателей гемоглобина при применении ПСЖ и ПЖК примерно одинаковые.
Путь введения препаратов железа
В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний ПЖ следует назначать внутрь. Путь введения ПЖ у больных ЖДА определяется конкретной клинической ситуацией, в частности, состоянием кишечного всасывания и переносимостью пероральных ПЖ.
Основными показаниями для парентерального введения ПЖ являются: – патологии кишечника с нарушением всасывания (различные энтериты, синдром недостаточности всасывания); – резекция тонкой кишки; – резекция желудка по Бильрот II с формированием «слепой петли»; – эрозивно–язвенные процессы в желудке (обострение язвенной болезни и др.); – непереносимость ПЖ для приема внутрь. Многие врачи обосновывают назначение парентеральных ПЖ выраженностью анемического синдрома в расчете на якобы больший их эффект, что также не имеет достаточных оснований и не подтверждается клинической практикой. Темпы прироста уровня гемоглобина при назначении ПЖ внутрь и парентерально оказались приблизительно одинаковыми, в связи с чем предпочтение ПЖ в инъекционных формах при необходимости более быстрой нормализации содержания гемоглобина (например, при подготовке к оперативному вмешательству) следует считать неоправданным. ПЖ для парентерального введения могут назначаться при плохой переносимости пероральных ПЖ, однако большинство современных ПСЖ и ПЖК переносятся сравнительно удовлетворительно. В связи с этим принятие решения о назначении парентерального ПЖ должно осуществляться только после ряда «врачебных маневров» (снижение дозы ПЖ, прием вместе с пищей, смена ПЖ для приема внутрь и т.д.).
Выбор лекарственного препарата железа
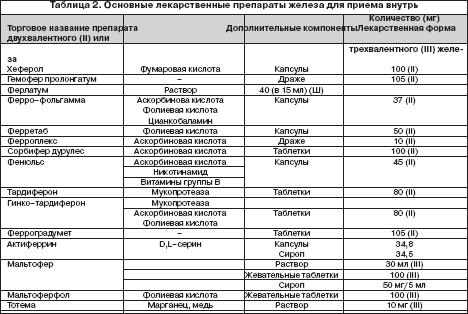
Выбор ПЖ и оптимального режима его дозирования должен определяться количеством и биодоступностью содержащегося в нем железа, переносимостью, стоимостью. При этом необходимо иметь в виду, что адекватный прирост показателей гемоглобина у больных ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг элементарного железа . Учитывая, что при развитии ЖДА всасывание железа увеличивается по сравнению с нормой и составляет 25–30% (при нормальных запасах железа – всего 3–7%), необходимо назначать от 100 до 300 мг элементарного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. С учетом этого при выборе ПЖ следует ориентироваться не на содержание в нем общего количества соединения железа, а на количество элементарного железа. Например, при назначении препаратов сульфата железа с низким содержанием элементарного железа (менее 100 мг) количество принимаемых таблеток должно быть от 3 и выше (в зависимости от содержания железа в каждой таблетке), в то время как препараты сульфата, фумарата или гидроксиполимальтозного комплекса железа с содержанием 100 мг элементарного железа можно принимать в количестве 1–2 таблеток в сутки. Основные ПСЖ представлены сульфатом железа, глюконатом, хлоридом, фумаратом, глицин сульфатом. Наибольшей степенью абсорбции обладают препараты сульфата железа, а наименьшей – глицин сульфата. Многие из ПСЖ содержат вещества, например, аскорбиновую кислоту, усиливающие всасывание железа и улучшающие биодоступность препарата, а также витамины (фолиевую кислоту, цианкобаламин). Среди ПЖК на отечественно рынке имеются гидроксиполимальтозный комплекс, железо–сорбитоловый комплекс, протеин сукцинилат железа, железо–сахарозный комплекс. К новым высокоэффективным и безопасным препаратам железа относятся препараты, представляющие собой неионные соединения железа на основе гидроксиполимальтозного комплекса (ГПК) трехвалентного железа. Структура комплекса состоит из многоядерных центров гидроксида Fe (III), окруженных нековалентно связанными молекулами полимальтозы. Комплекс имеет большой молекулярный вес, что затрудняет его диффузию через мембрану слизистой кишечника. Химическая структура комплекса максимально приближена к структуре естественных соединений железа с ферритином. Абсорбция железа в виде ГПК имеет принципиально иную схему по сравнению с его ионными соединениями и обеспечивается поступлением Fe (III) из кишечника в кровь путем активного всасывания. Неионная структура комплекса обеспечивает его стабильность и перенос железа с помощью транспортного белка, что предотвращает в организме свободную диффузию ионов железа, т.е. прооксидантные реакции. Данные по безопасности, полученные во время клинических исследований препарата железа на основе гидроксида Fe (III) с полимальтозой, свидетельствуют о более низкой частоте побочных эффектов по сравнению с солевыми препаратами железа. Для лучшей переносимости ПСЖ следует принимать во время еды, хотя следует иметь в виду, что всасывание железа лучше при приеме лекарственных препаратов перед едой. Всасываниежелеза может уменьшаться под влиянием содержащихся в некоторых пищевых продуктах веществ – фитинов (рис, соя), фосфатов (рыба, морепродукты), танина (чай, кофе). Многие больные склонны запивать лекарства чаем, что в случаях приема ПЖ в виде солей недопустимо, поскольку образуются плохо растворимые комплексы с низкой их абсорбцией в кишечнике. Кроме того, всасывание железа из ПЖ в виде солей ухудшается при одновременном приеме ряда медикаментов (тетрациклины, антациды, соли магния). С учетом этого следует рекомендовать прием препаратов солей железа в различное время с другими вышеуказанными медикаментами. Препараты ПЖК, в частности, гидроксиполимальтозный комплекс лишены подобных недостатков, поскольку пищевые продукты и медикаменты не оказывают влияние на всасываемость железа (в виде трехвалентной формы) из железосодержащих комплексов. В таблице 2 представлены основные зарегистрированные в России лекарственные ПСЖ и ПЖК для приема внутрь.
Оценка эффективности лечения
В случаях назначения ПЖ в достаточной дозе на 7–10–й день от начала лечения наблюдается повышение количества ретикулоцитов. Достоверное повышение уровня гемоглобина отмечается через 3–4 нед. от начала лечения. Нормализация показателей гемоглобина обычно происходит в сроки 4–9 нед. Иногда наблюдается резкое скачкообразное повышение гемоглобина. Эти индивидуальные колебания могут быть обусловлены, с одной стороны, выраженностью ЖДА, степенью истощения запасов железа, а с другой – эффективностью назначенного ПЖ (количество содержащегося железа, биодоступность и др.). Имеет также значение некомплаентность больных (нерегулярность приема ПЖ, побочные эффекты).
Длительность лечения и поддерживающая терапия
Оптимальная тактика ведения больных ЖДА предполагает насыщающую и поддерживающую терапию ПЖ. Длительность насыщающей терапии зависит от темпов прироста и сроков нормализации показателей гемоглобина, составляя в среднем 4–6 недель. Поддерживающая терапия показана в тех ситуациях, когда причина дефицита железа сохраняется (меноррагии, беременность) или в силу различных ситуаций является трудноустранимой (патология кишечника, носовые и другие кровотечения при геморрагических диатезах). Женщинам, страдающим ЖДА на фоне меноррагий, после нормализации показателей гемоглобина рекомендуется поддерживающая терапия ПЖ в течение 5–7 дней после очередной менструации. Больным надо разъяснять необходимость поддерживающего лечения в связи с продолжающимися избыточными потерями железа. Беременные с ЖДА должны получать ПЖ до конца беременности в целях обеспечения адекватной потребности плода в железе.
Переносимость препаратов железа
Среди побочных эффектов на фоне применения ПЖ внутрь наиболее часто возникают тошнота, анорексия, металлический вкус во рту, запоры, реже – поносы. Развитие запоров обусловлено, по всей вероятности, связыванием в кишечнике сероводорода, являющегося одним из стимулов кишечной перистальтики. В большинстве случаев современные ПЖ вызывают незначительные побочные явления, не требующие их отмены и перехода на парентеральный путь введения. Диспептические расстройства могут уменьшаться при приеме препаратов после еды или уменьшения суточной дозы препарата. Чаще побочные эффекты регистрируютсяпри приеме ПСЖ, в то время как препараты ПЖК (гидроксиполимальтозный комплекс) переносятся лучше и имеют в связи с этим определенные преимущества. В случаях сохраняющейся плохой переносимости пероральных ПЖ показано назначение ПЖ парентерально (внутримышечно или внутривенно). На фоне лечения парентеральными ПЖ, особенно для внутривенного введения, могут возникать аллергические реакции в виде крапивницы, лихорадка, флебиты, анафилактический шок. Кроме того, при внутримышечном введении ПЖ возможно потемнение кожи в местах инъекций, инфильтраты, абсцессы. Если ПЖ для парентерального введения назначают больным гипохромной анемией, не связанной с дефицитом железа, имеется повышенный риск возникновения тяжелых нарушений из–за «перегрузки» железом различных органов и тканей (печень, поджелудочная железа и др.) с развитием гемосидероза.
Причины неэффективности лечения препаратами железа
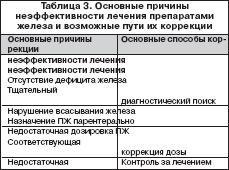
В случае отсутствия или недостаточного эффекта от лечения ПЖ следует выяснить причину с целью возможности ее коррекции. Возможные причины неэффективности лечения ПЖ и способы их коррекции представлены в таблице 3. Необходима убежденность в правильной трактовке всех клинико–лабораторных признаков и в достоверности синдрома ЖДА. Причиной отсутствия или недостаточной эффективности ПЖ может быть недостаточная суточная доза железа, что обычно связано с назначением ПЖ с низким содержанием в нем железа и малым количеством принимаемых таблеток. Так, например, при лечении препаратом, в котором содержится всего лишь 10 мг двухвалентного железа, число принимаемых таблеток должно быть не менее 10 в сутки. Такой режим дозирования неудобен для больных, чем и объясняется, вероятнее всего, невыполнение ими врачебного назначения. С учетом вышесказанного для обеспечения комплаентности следует назначать ПЖ с высоким содержанием железа (не менее 100 мг). Препараты с низким содержанием железа целесообразно использовать в педиатрической практике. Одной из причин неэффективности ПЖ при назначении внутрь может быть нарушение всасывания железа, в частности, у больных с невыявленной или недооцененной кишечной патологией. В этих случаях показано назначение парентеральных ПЖ. В ряде случаев вследствие улучшения самочувствия больные начинают нерегулярно принимать ПЖ или вообще прекращают лечение. В результате показатели гемоглобина не достигают нормальных значений и ЖДА при этом остается фактически недолеченной. С учетом этого длительность насыщающей терапии ПЖ должна определяться сроками достижения нормального уровня гемоглобина, что требует постоянного лабораторного мониторинга. Ряд больных не всегда выполняют назначение врача (регулярность приема ПЖ, достаточная продолжительность и т.д.). В некоторых случаях это может быть обусловлено развитиемпобочных эффектов от ПЖ и самостоятельным прекращением лечения. Поэтому необходим контроль за лечением, эффективностью, переносимостью ПЖ со стороны врача, среднего медперсонала, родственников больных. Отсутствие эффекта от ПЖ может быть связано с неустраненными причинами ЖДА, среди которых клинически наиболее значимыми являются скрытые кровопотери из желудочно–кишечного тракта, чаще из кишечника (невыявленная опухоль!). С учетом этого в подобных ситуациях при исключении других возможных причин неэффективности ПЖ необходимо тщательное эндоскопическое исследование кишечника (в ряде случаев – повторное). Таким образом, у больных ЖДА наряду с устранением причины обязательна патогенетическая терапия ПЖ (ПСЖ и ПЖК), которые должны назначаться преимущественно внутрь. Тактика лечения ПЖ предусматривает выбор пути введения ПЖ с учетом клинической ситуации, оптимального ПЖ с достаточным содержанием в нем железа, оценку эффективности и переносимости препарата, длительность насыщающей и обоснованность поддерживающей терапии. Своевременная верификация синдрома ЖДА и выявление ее причины, адекватная патогенетическая терапия с назначением ПЖ с оптимальными фармакокинетическими свойствами, клинической эффективностью, переносимостью позволяет корригировать анемический синдром и обеспечивать достаточный уровень качества жизни у данной категории пациентов.
Источник