Где происходит распад гемоглобина

Происходит в мононуклеарных фагоцитах (в селезенке и печени). Сначала происходит разрыв связи между I-м и II-м кольцами. Фермент – НАДзависимая оксигеназа. После ее действия образуется пигмент зеленого цвета – вердоглобин. В его составе сохраняется и железо и белок. В дальнейшем вердоглобин распадается на составные части: белок, железо и пигмент-биливердин. Железо образует комплекс с белком трансферрином, и этот комплекс поступает в ткани, где оно снова может быть использовано для синтезов или депонироваться в виде комплекса с белком ферритином.
Билирубин плохо растворим в воде, поэтому он адсорбируется на альбумине крови. Такой комплекс называется СВОБОДНЫМ или НЕПРЯМЫМ БИЛИРУБИНОМ. Он свободный, потому что не связан ни с каким другим веществом ковалентными связями; непрямой, потому что не дает прямой реакции с диазореактивом Эрлиха (для определения этого вида билирубина необходимо предварительно осадить альбумины).
В печени непрямой билирубин подвергается обезвреживанию путем связывания с глюкуроновой кислотой. В реакции расходуется УТФ. При этом к молекуле билирубина присоединяются 2 молекулы глюкуроновой кислоты (образование билирубиндиглюкуронида). Это вещество малотоксично и хорошо растворяется в воде, называется ПРЯМЫМ СВЯЗАННЫМ БИЛИРУБИНОМ, т.к. определяется в прямой реакции с диазореактивом Эрлиха и связан ковалентно с глюкуроновой кислотой. В таком виде билирубин поступает в желчь и вместе с ней выводится из организма.
При определении содержания билирубина используют диазореактив Эрлиха, который дает розовую окраску с билирубином и по ее интенсивности судят о концентрации билирубина в крови.
В крови человека примерно 75% непрямого билирубина от его общего количества. Общее содержание билирубина в норме (прямой+непрямой) от 8 до 20 мкмоль/л.
Билирубин – это конечный продукт распада гемоглобина у человека. Однако, поступив с желчью в кишечник, он превращается под действием ферментов микрофлоры кишечника. Сначала от него отщепляется глюкуроновая кислота, затем происходит частичное восстановление и образуется вещество, называемое “мезобилиноген”, а затем стеркобилиноген. Стеркобилиноген в основном выводится с калом и на воздухе (в кале) превращается в стеркобилин, а мезобилиноген частично всасывается из кишечника по системе v.portae, т.е. попадает в печень и там разрушается. Поэтому его нет у здоровых людей в крови. Небольшая часть стеркобилиногена тоже всасывается из кишечника через систему геморроидальных вен, т.е. попадает сразу в большой круг кровообращения, минуя печень, поэтому часть его выводится с мочой.
Значит, стеркобилиноген является компонентом мочи в норме.
В НОРМЕ:
Кровь:
Билирубин (в основном непрямой) – в норме (8-17мкмоль/л)
Гемоглобин – в норме (мужчины – 130-145 г/л; женщины – 110-130 г/л
Моча: светло-желтого цвета, стеркобилиноген – в норме, мезобилиногена нет.
Кал: нормальной окраски, стеркобилиноген – в норме
135.
ГЕМОЛИТИЧЕСКАЯ ЖЕЛТУХА Наблюдается при усилении распада эритроцитов. Билирубина образуется больше, чем в норме и скорость экскреции тоже увеличивается. Непрямой билирубин повышается в крови. В моче билирубина нет, а содержание стеркобилина в кале и в моче повышено.
136.
ПАРЕНХИМАТОЗНАЯ ЖЕЛТУХА (паренхиматозная). Наблюдается при повреждении гепатоцитов (например, при вирусном гепатите). Билирубин не обезвреживается. Желчные пигменты поступают не только в кишечник, но и в кровь. Т.е. в крови повышается содержание не только прямого, но и непрямого билирубина. Наблюдается билирубинурия. В моче обнаруживают мезобилиноген.
137.
ОБТУРАЦИОННАЯ ЖЕЛТУХА (механическая) Наблюдается при закупорке желчных протоков (например, при желчнокаменной болезни). Желчь продолжает вырабатываться, но поступает не только в желчные протоки, а также в кровь. В крови повышается уровень билирубина, в основном – прямого билирубина. Наблюдается билирубинурия. Содержание стеркобилина в моче и в кале снижено (кал становится светлым, а моча темнеет за счет прямого билирубина).
138.
Распад гемоглобина может влиять на функционирование печени человека. В чем же тут может быть опасность для пациента?

Организм человека – сложная саморегулирующаяся система, которая для достижения оптимальных условий работы и существования сама себе помогает.
Вся работа тканей и органов держится на активных обменных процессах, проходящих в них. Основной связывающей средой между ними является кровь. С ее помощью происходит насыщение тканей кислородом, поступающим от легких. Взамен кровь транспортирует от клеток продукты их жизнедеятельности и образованный углекислый газ.
Молекулы в организме человека
В крови содержится довольно много молекул, обеспечивающих подобный транспорт. Главной из них является молекула гемоглобина, основная функция которой – доставка кислорода и удаление СО2.
Гемоглобин – сложная молекула, состоящая из двух больших, двух малых белковых субъединиц и находящегося между ними и связывающего их в единую молекулу атома железа.
 В огромном количестве гемоглобин находится в эритроцитах – красных кровяных клетках, отвечающих за транспортную функцию. Чем эритроцитов больше, тем обычно больше гемоглобина.
В огромном количестве гемоглобин находится в эритроцитах – красных кровяных клетках, отвечающих за транспортную функцию. Чем эритроцитов больше, тем обычно больше гемоглобина.
Как и любая структура организма, эритроциты не вечны. После образования их в костном мозгу, они покидают его, некоторое время циркулируют по кровотоку и спустя определенное время (средняя продолжительность жизни эритроцита составляет около 120 дней) они попадают в селезенку, где проходит утилизация изношенных или поврежденных эритроцитов с их последующим распадом.
Частичный распад эритроцитов происходит и в кровяном русле.
Расшифровка схемы
В результате, чтобы не терять имеющееся в организме железо, старые эритроциты расщепляются на более простые структуры, которые впоследствии принимают участие в образовании новых эритроцитов. Процесс их образования довольно сложен. Он включает в себя достаточно большое количество стадий и для его протекания необходимо очень много вспомогательных веществ.
Соответственно, если разрушается эритроцит, то происходит и распад содержащегося в нем гемоглобина. Схема распада данного белка следующая:

- Под воздействием кислорода и молекулы, осуществляющей транспортировку протонов водорода, происходит превращение гемоглобина в вердоглобин (если изучать данный процесс под контролем зрения, можно заметить, что происходит смена цвета (гемоглобин дает красную окраску, в то время как вердоглобин окрашивает все в зеленый цвет)).
- В последующих реакциях происходит отщепление атома двухвалентного железа, которое после используется для синтеза нового гема, и белковых субъединиц, которые последовательно распадаются до аминокислот и в дальнейшем используются для синтеза новых белков. В результате от молекулы гемоглобина остается только одно вещество – биливердин. Гем при помощи белка-трансферрина переносится в печень, где находится депо железа. Оно используется в дальнейшем как для повторного синтеза молекулы гемоглобина, так и новых молекул.
- Воздействуя на биливердин специальным ферментом – редуктазой, происходит превращение его в новую молекулу – билирубин, который, в свою очередь, дает оранжевую окраску.
Данное вещество является достаточно токсичным и при большом количестве его в кровотоке приводит к развитию различных состояний, таких как желтуха. В тяжелых случаях может приводить к поражению нервной системы и развитию печеночной комы.
Оно используется в основном для синтеза желчных кислот в печени, поэтому после его образования дальнейшая схема утилизации гемоглобина может идти в двух направлениях.
Первое из них основывается на реакции конъюгации.
В крови билирубин может содержаться в трех формах – чистый билирубин, не связанный ни с одной молекулой, свободный, связанный преимущественно с альбуминами крови, и несвободный, или конъюгированный, составляющий комплекс билирубина с глюкуроновой кислотой.
Реакция конъюгации билирубина происходит преимущественно в печени.
 Оттуда связанный с глюкуроновой кислотой билирубин попадает по системе желчных протоков в кишечник, где происходит дальнейшее превращение данной молекулы.
Оттуда связанный с глюкуроновой кислотой билирубин попадает по системе желчных протоков в кишечник, где происходит дальнейшее превращение данной молекулы.
Некоторая часть уробилиногена всасывается в кровь и транспортируется с ее током в печень, где происходит образование сложных спиртов, необходимых для некоторых реакций метаболизма.
Большая же часть оставшегося в кишечнике уробилиногена под действием ферментов и пигментных молекул микроорганизмов окисляется до стеркобилиногена, придающего окраску калу и выводящегося с ним.
Малая часть стеркобилиногена по системе вен прямой кишки (кровоток от которой осуществляется по широко развитой системе геморроидальных вен) всасывается в кровь и транспортируется к почкам. В них происходит выделение стеркобилиногена с током мочи. Во внешней среде, за счет реакции с атомами кислорода, стеркобилиноген превращается в уробилин и стеркобилин, которые придают моче характерный цвет.
Таким образом выглядит схема реакции распада молекулы гемоглобина.
Искусственный метод распада гемоглобина
Все данные реакции протекают в крови под воздействием эндогенных ферментов. Подобную схему распада гемоглобина можно спроектировать и в лабораторных условиях, чтобы получить более наглядное представление о протекании данной реакции.
Как было сказано выше, эритроциты подвергаются разрушению с целью их повторного использования в дальнейшем. Данный механизм осуществляется по принципу физиологической смерти клеток, однако есть еще один механизм, вызывающий распад эритроцитов и образование желчных пигментов.
 Данный механизм носит название апоптоза и активируется обычно в случае несостоятельности эритроцитов или ошибок во время их синтеза.
Данный механизм носит название апоптоза и активируется обычно в случае несостоятельности эритроцитов или ошибок во время их синтеза.
Схема распада эритроцита и гемоглобина, если имеет место нарушение синтеза, ничем не отличается от таковой как при физиологической утилизации. Единственным нюансом является то, что часть клеток распадается непосредственно в селезенке, а другая – в кровяном русле. Существенным изменениям молекула билирубина не подвергается, однако за счет наличия в крови огромного количества ионов, иных молекул и клеток системы крови реакция расщепления может пойти несколько непредсказуемо.
Если иммунная система организма в норме, подобный внутрисосудистый распад гемоглобина обычно никак не сказывается на состоянии здоровья человека. Если же имеются и какие-либо нарушения в работе системы иммунитета, то реакция может пойти несколько непредсказуемо, и сложно предугадать ее последствия.
Для чего же следует знать схему распада молекулы гемоглобина
Дело в том, что в норме в крови содержится определенное количество желчных пигментов. При развитии того или иного патологического процесса, который может проходить как в печени, так и селезенке, показатели билирубина могут значительно меняться и изменяться. При увеличении их количества судят о либо повышенной активности клеток крови и селезенки, либо же о значительных проблемах с печенью. Если такое поражение пустить на самотек и своевременно не обратиться к врачу, состояние может привести к летальному исходу или развитию печеночной комы.
Увеличение количества непрямого билирубина обычно является провоцирующим фактором развития желчнокаменной болезни, которая чаще всего приводит к нарушению работы пищеварительной системы, но может проявить себя и в виде ургентного состояния (печеночная колика).
Снижение же продуктов распада гемоглобина в крови говорит о нарушении работы транспортных систем организма или же о несостоятельности костного мозга, что может говорить за развитие онкологического процесса.
Любое увеличение количества билирубина чаще всего проявляется в виде желтухи, поэтому уже на стадии осмотра пациента можно заподозрить имеющиеся метаболические нарушения.
Именно поэтому крайне важно знать о возможных изменениях количества гемоглобина в крови и уметь правильно распознать имеющуюся патологию.
https://www.youtube.com/watch?v=Kr_vZTauVlc
Для определения количества данных веществ назначается специальный анализ – биохимия крови. Исследование количества гемоглобина и билирубина проводится в лабораториях специально обученным персоналом. На основании полученных ими данных удается сделать вывод об имеющихся нарушениях и предпринять соответствующие меры.
Тема 3 (вопрос 4 и 5).
Гем состоит из иона двухвалентного железа и порфирина. В основе структуры порфиринов находится порфин. Порфин представляет собой четыре пиррольных кольца, связанных между собой метеновыми мостиками. С наибольшей скоростью гем синтезируется в костном мозге (для синтеза гемоглобина ретикулоцитами) и в печени (для образования цитохрома Р-450).
Синтез гема происходит в несколько стадий:
1. На первой стадии в митохондриях сукцинил-КоА взаимодействует с глицином с образованием δ-аминолевулиновой кислоты. Эту реакцию катализирует специфический пиридоксальзависимый фермент δ-аминолевулинатсинтаза. Фермент активируется стероидами и ингибируется по типу обратной связи конечным продуктом – гемом. Продукт реакции из матрикса митохондрий переходит в цитозоль.
2. На второй стадии, в цитозоле, происходит конденсация 2-х молекул
δ-аминолевулиновой кислоты с образованием порфобилиногена. Фермент – порфобилиногенсинтаза – ингибируется конечным продуктом.
3. Из 4-х молекул порфобилиногена синтезируется протопорфирин IX, являющийся предшественником гема.
4. Протопорфирин IX присоединяет молекулу Fe при участии феррохелатазы (гемсинтаза) и образуется гем. Источником железа в этой реакции является белок ферритин, который депонирует железо.
Механизм регуляции синтеза тема в неэритроидных клетках имеет определенные отличия. Так, в клетках печени, где синтез гема происходит на высоком уровне, гем является отрицательным регулятором синтеза δ-аминолевулинатсинтазы по механизму репрессии-депрессии в процессе транскрипции. Главный регуляторный эффект гема состоит в том, что синтез фермента значительно ускоряется в отсутствии гема и замедляется в его присутствии.
Синтез белковой части гемоглобина происходит на рибосомах. Цепи α и β глобина синтезируются на полисомах, образованных, как правило, пятью рибосомами. Цепь α освобождается первой, присоединяется к β-цепи, еще связанной с рибосомой и отделяет ее, образуя димер αβ. Два димера соединяются в молекулу гемоглобина α2β2.
Соединение гема с глобином может происходить или в процессе синтеза полипептидных цепей, или после окончания синтеза глобина. Синтез полипептидных цепей происходит только в присутствии гема. При низкой концентрации гема синтез глобина замедляется. Отсюда следует, что синтез гема и глобина происходит координировано и ни один из этих компонентов не образуется в избыточном или недостаточном количестве.
Катаболизм гемоглобина
Эритроциты имеют короткое время жизни (примерно 120 дней). При физиологических условиях в организме взрослого человека разрушается около 1 – 2×1011 эритроцитов в сутки. Их катаболизм происходит, главным образом, в ретикулоэндотелиальных клетках селезёнки (РЭС), лимфатических узлов, костного мозга и печени. При распаде гемоглобина образуется билирубин. Билирубин является основным желчным пигментом у человека. При распаде 1 г гемоглобина образуется 35 мг билирубина, а в сутки у взрослого человека – примерно 250-350 мг. Дальнейший метаболизм билирубина происходит в печени.
Билирубин, образованный в клетках РЭС селезёнки и костного мозга, называется свободным (неконьюгированным)или непрямым, поскольку вследствие плохой растворимости в воде он легко адсорбируется на белках плазмы крови (альбуминах) и для его определения в крови необходимо предварительное осаждение белков спиртом. После этого билирубин определяют реакцией с диазореактивом Эрлиха. Свободный (непрямой) билирубин не проходит через почечный барьер и в мочу не попадает.
Каждая молекула альбумина связывает 2 (или 3) молекулы билирубина. При низком содержании альбумина в крови, а также при вытеснении билирубина из центров связывания на поверхности альбумина высокими концентрациями жирных кислот, лекарственных веществ (например, сульфаниламиды) увеличивается количество билирубина, не связанного с альбуминами. Он может проникать в клетки мозга и повреждать их.
Комплекс альбумин-билирубин с током крови попадает в печень, где происходит его превращение в прямой билирубин путем коньюгации с глюкуроновой кислотой. Реакцию катализирует УДФ-глюкуронилтрансфераза. Образующийся билирубиндиглюкуронид получил название прямого(коньюгированного) билирубина или связанного. Он растворим в воде и дает прямую реакцию с диазореактивом Эрлиха.
Прямой билирубин – это нормальный компонент желчи, попадающий в кровь в незначительном количестве. Он может проходить через почечный барьер, но в крови в норме его мало, поэтому в моче обычными лабораторными методами он не определяется.
Вместе с желчью прямой билирубин выводится в тонкий кишечник. В кишечнике билирубинглюкурониды гидролизуются специфическими бактериальными ферментами β-глюкуронидазами. Освободившийся билирубин под действием кишечной микрофлоры восстанавливается с образованием сначала мезобилирубина, а затем мезобилиногена(уробилиногена). Небольшая часть уробилиногенов, всасываясь в тонком кишечнике и верхнем отделе толстого, через систему воротной вены попадает в печень, где практически полностью разрушается до дипиррольных соединений. Уробилиноген при этом в общий кровоток не поступает и в моче не определяется.
Основная часть уробилиногена поступает в толстый кишечник, где под влиянием микрофлоры подвергается дальнейшему восстановлению с образованием стеркобилиногена. Образовавшийся стеркобилиноген почти полностью выделяется с калом. На воздухе он окисляется и превращается в стеркобилин, являющийся одним из пигментов кала. Небольшая часть стеркобилиногена попадает путем всасывания через слизистую толстого кишечника в систему нижней полой вены (через геморроидальные вены), доставляется в почки и выводится с мочой (4 мг/сутки).
За сутки у человека распадается около 9 г гемопротеинов, в основном это гемоглобин эритроцитов.
Эритроциты в норме живут 90-120 дней, после чего лизируются в клетках ретикулоэндотелиальной системы – макрофагах селезенки (главным образом), купферовских клетках печени и макрофагах костного мозга. При разрушении эритроцитов в кровеносном русле высвобождаемый гемоглобин образует комплекс с белком-переносчиком гаптоглобином (фракция α2-глобулинов крови) и также переносится в клетки РЭС селезенки, печени и костного мозга.
Синтез билирубина
В клетках РЭС гем в составе гемоглобина окисляется молекулярным кислородом. В реакциях последовательно происходит разрыв метинового мостика между 1-м и 2-м пиррольными кольцами гема с их восстановлением, отщеплением железа и белковой части и образованием оранжевого пигмента билирубина. Высвобождаемое железо может либо запасаться в клетке в комплексе с ферритином, либо выделяться наружу и связываться с трансферрином.
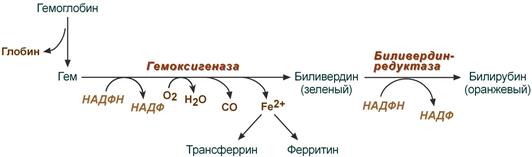
Реакции распада гемоглобина и образования билирубина
Билирубин – токсичное, жирорастворимое вещество, способное разобщать окислительное фосфорилирование в клетках. Особенно чувствительны к нему клетки нервной ткани.
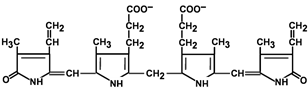
Строение билирубина
Выведение билирубина
Из клеток ретикуло-эндотелиальной системы билирубин попадает в кровь. Здесь он находится в комплексе с альбумином плазмы, в гораздо меньшем количестве – в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами. Образование таких комплексов не позволяет выделяться билирубину с мочой. Билирубин в комплексе с альбумином называется свободный (неконъюгированный) или непрямой билирубин.
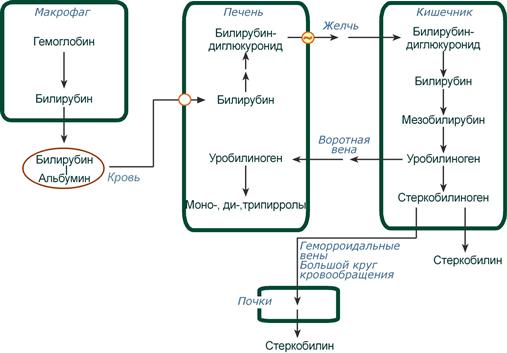
Этапы метаболизма билирубина в организме
Из сосудистого русла в гепатоциты билирубин попадает с помощью белка-переносчика (транспортный белок органических анионов) или по механизму флип-флоп. Далее при участии цитозольного связывающего белка лигандина (Y-протеин) билирубин транспортируется в ЭПР, где протекает реакция связывания билирубина с УДФ-глюкуроновой кислотой, при этом образуются моно- и диглюкурониды. Кроме глюкуроновой кислоты, в реакцию конъюгации могут вступать сульфаты, фосфаты, глюкозиды.
Билирубин-глюкуронид получил название связанный (конъюгированный) или прямой билирубин.
После образования билирубин-глюкурониды АТФ-зависимым переносчиком секретируются в желчные протоки и далее в кишечник, где при участии бактериальной β-глюкуронидазы превращаются в свободный билирубин. Одновременно, даже в норме (особенно у взрослых), некоторое количество билирубин-глюкуронидов может попадать из желчи в кровь по межклеточным щелям.
Таким образом, в плазме крови обычно присутствуют две формы билирубина: свободный (непрямой), попадающий сюда из клеток РЭС (80% и более всего количества), и связанный (прямой), попадающий из желчных протоков (в норме не более 20%).
Термины “связанный“, “конъюгированный“, “свободный“, “несвязанный” отражают взаимодействие билирубина и глюкуроновой кислоты (но не билирубина и альбумина!).
Термины “прямой” и “непрямой” введены, исходя из возможности химической реакции билирубина с диазореактивом Эрлиха. Связанный билирубин реагирует с реактивом напрямую, без добавления дополнительных реагентов, т.к. является водорастворимым. Несвязанный (жирорастворимый) билирубин требует добавочных реактивов, реагирует не прямо.
Превращение в кишечнике
В кишечнике билирубин подвергается восстановлению под действием микрофлоры до мезобилирубина и мезобилиногена (уробилиногена). Часть уробилиногена всасывается и с кровью портальной вены попадает в печень, где либо распадается до моно-, ди- и трипирролов, либо окисляется до билирубина и снова экскретируется. При этом при здоровой печени в общий круг кровообращения и в мочу мезобилирубин и уробилиноген не попадают, а полностью задерживаются гепатоцитами.
Оставшаяся в кишечнике часть пигментов ферментами бактериальной флоры толстого кишечника восстанавливается до стеркобилиногена. Далее
- малая часть стеркобилиногена может всасываться и катаболизировать в печени, подобно уробилиногену,
- незначительное количество стеркобилиногена через геморроидальные вены попадает в большой круг кровообращения, отсюда в почки и в мочу. После окисления на воздухе из стеркобилиногена образуется стеркобилин мочи,
- однако основное количество стеркобилиногена достигает нижних отделов толстого кишечника и выделяется. В прямой кишке и на воздухе стеркобилиноген окисляется в стеркобилин, окрашивая кал,
- аналогично уробилиноген, появляющийся в моче при патологии печени, окисляется в уробилин.
Очень часто стеркобилиноген, содержащийся в нормальной моче, называют уробилиногеном. И в клинической практике обычно не проводят различий между стеркобилиногеном и уробилиногеном мочи, их рассматривают как один пигмент – урохромы (уробилиноиды), что может создавать некоторую путаницу при оценке результатов анализа.
