Гемоглобин с соляной кислотой
Для проведения данных исследований необходимо следующее оснащение рабочего места:
- Гемометр Сали (ГС-3) с комплектом принадлежностей.
- Концентрированная соляная кислота.
- Дистиллированная вода.
- Набор для взятия крови из пальца.
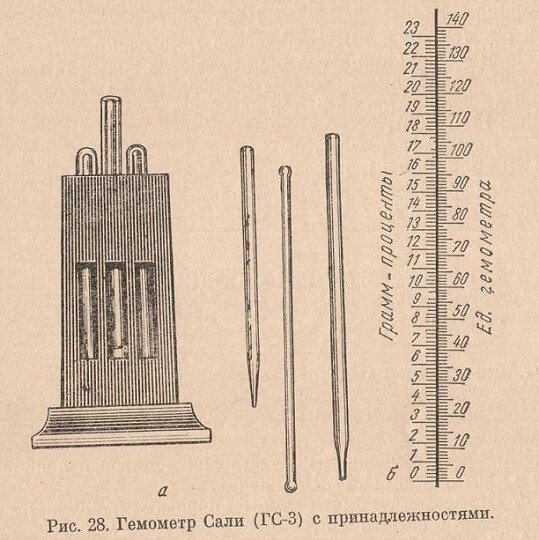
Для определения количества гемоглобина используют гемометр ГС-3 (рис. 28), особенностью которого является наличие точных стандартов и пробирки со шкалой, градуированной в грамм-процентах (рис. 28).
Сущность метода
Гемоглобин крови под воздействием 0,1 N раствора соляной кислоты превращается в солянокислый гематин, интенсивность окраски которого сравнивают с цветом стандартов. Для определения гемоглобина необходим 0,1 N раствор соляной кислоты, который готовят следующим образом. В мерную колбу емкостью 1 л помещают 8,24 мл концентрированной соляной кислоты и доливают дистиллированной водой до метки; такой раствор можно также приготовить из фиксанала.
Техника определения гемоглобина
В градуированную пробирку до круговой метки (2 г%) наливают 0,1 N раствор соляной кислоты. Пробирку вставляют в гемометр. После нанесения укола в палец первую каплю крови удаляют ваткой или фильтровальной бумагой. В свежевыступнвшую каплю крови вносят кончик чистого сухого капилляра. Плавно, без перерывов, с помощью резиновой трубки с мундштуком насасывают кровь в капилляр до круговой метки 0,02 мл. Уровень крови в капилляре регулируют, прикасаясь к его кончику кусочками фильтровальной бумаги. Вытирают кончик капилляра от крови и вносят его в 0,1 N раствор соляной кислоты, находящийся в градуированной пробирке. Кровь выпускают в реактив тонкой струйкой, не взмучивая жидкости. Не вынимая капилляр из пробирки, его прополаскивают 2-3 раза надосадочным прозрачным 0,1 раствором соляной кислоты, затем извлекают из жидкости, прикасаясь его кончиком к стенкам пробирки, выдувают остаток жидкости и выносят из пробирки. Кровь с соляной кислотой немедленно смешивают, постукивая по дну пробирки. Пробирку ставят в прибор на 5 минут.

Вследствие гемолиза эритроцитов и образования солянокислого гематина жидкость буреет и становится прозрачной. Через 5 минут к испытуемой жидкости небольшими порциями прибавляют дистиллированную воду, каждый раз тщательно перемешивая жидкость с помощью стеклянной палочки. Стекающая с палочки жидкость должна полностью остаться в пробирке. В момент, когда цвет жидкости приблизится к цвету стандартов, воду начинают прибавлять осторожно, по каплям. Разведение заканчивают, как только цвет испытуемой жидкости совсем сравняется с цветом стандартов. Цвет жидкости и стандартов сравнивают при дневном освещении в проходящем свете, держа гемометр в вытянутой руке на уровне глаз. Определяют, на каком делении шкалы находится нижний мениск жидкости. Цена деления шкалы равна 0,2 г% (см. рис. 28).
Количество гемоглобина при оформлении в бланке анализа записывают в грамм-процентах и единицах. Грамм-проценты переводят в единицы, умножая их количество на 6, так как 1 г% соответствует 6 ед. (100: 16,67 = 6). В норме содержание гемоглобина от 11,7 г% (70 ед.) до 18 г% (108 ед.). После определения гемоглобина пробирку и капилляр промывают дистиллированной водой и высушивают, а гемометр укладывают в футляр.
Источник
Гемоглобин выполняет, в организме важную роль переносчика
кислорода и принимает участие в транспорте углекислоты.
Гемоглобин представляет собой сложное химическое соединение
(молекулярный вес 68 800). Он состоит из белка глобина и четырех молекул гема.
Молекула гема, содержащая атом железа, обладает способностью соединять и
отдавать молекулу кислорода. При этом валентность железа, к которому
присоединяется кислород, не изменяется, т. е. железо остается двухвалентным.
Если обработать гемоглобин раствором соляной кислоты, то от
глобина отщепляется гем. Вступая в соединение с соляной кислотой, он
превращается в гемин
(С34Н32N4O4FeCl), образующий
кристаллы характерной формы. Проба на образование гемина производится для
доказательства присутствия крови при судебномедицинских исследованиях.
В состав молекулы гема входят четыре пиррольных кольца (два из них имеют
характер щелочи, а два – кислоты). Атом железа, содержащийся в геме, связывает
гем с белковой частью глобином. Если гем теряет атом железа, а пирроловая его
структура сохраняется, то получается гематопорфирин. Это вещество в больших
количествах образуется в организме при некоторых отравлениях или нарушениях
обмена и может выделяться с мочой.
Гем является активной, или так называемой простатической, группой
гемоглобина, а глобин — белковым носителем гема. Гемоглобин, присоединивший
кислород, превращается в оксигемоглобин (его обозначают символом
НbO2). Оксигемоглобин, отдавший кислород, называется восстановленным,
или редуцированным, гемоглобином (Нb). Оксигемоглобин, гемоглобин и
некоторые другие соединения и производные гемоглобина дают характерные полосы
поглощения лучей спектра.
Так, пропуская луч света через раствор оксигемоглобина, можно Рис. 5. Спектры поглощения оксигемоглобина (сверху) и Оксигемоглобин несколько отличается по цвету от гемоглобина, поэтому |
Значительно большее поглощение световых лучей с длиной волны 620—680 ммк
гемоглобином по сравнению с оксигемоглобином легло в основу методики измерения
степени насыщения крови кислородом — оксигемометрии. При этой методике ушную
раковину или кювету с кровью просвечивают небольшой электрической лампой и
определяют с помощью фотоэлемента интенсивность светового потока указанной длины
волны, проходящего через ткань уха или кювету с кровью. По показаниям
фотоэлемента определяют степень насыщения гемоглобина кислородом.
Кровь взрослых людей содержит в среднем 14—15% гемоглобина (у мужчин
13,5—16%, у женщин 12,5—14,5%). Общее содержание гемоглобина равно примерно 700
г.
В эмбриональном периоде в крови человека имеются разные типы гемоглобина,
отличающиеся способностью присоединять кислород в некоторыми другими химическими
свойствами. Для определения и разделения разных типов гемоглобина применяют
методику измерения оптической плотности растворов гемоглобина до и после
денатурации его едкой щелочью. Разные типа гемоглобина условно обозначают НbA,
HbF, НbР, Гемоглобин НbР встречается только в первые 7—12 недель внутриутробного
развития зародыша. На 9-й неделе появляется в крови зародыша гемоглобин HbF и
гемоглобин взрослых НbA. Существенно важным представляется тот факт, что
эмбриональный гемоглобин HbF обладает более высоким сродством к кислороду и
может насыщаться на 60% при таком напряжении кислорода, когда гемоглобин матери
насыщается всего на 30%. У разных видов позвоночных животных имеются различия в
структуре гемоглобина. Гем разных типов гемоглобина при этом одинаков, глобины
же различаются по своему аминокислотному составу.
В организме постоянно происходит синтез и распад гемоглобина, связанные с
образованием и разрушением эритроцитов. Синтез гемоглобина совершается в
эритробластах красного костного мозга. При разрушении эритроцитов, которое
происходит в ретикуло-эндотелиальной системе, главным образом в печени и
селезенке, из красных кровяных клеток выходит гемоглобин. В результате
отщепления железа от гема и последующего окисления образуется из гемоглобина
пигмент билирубин, который затем с желчью выделяется в кишечник, где
превращается в стеркобилин и уробилин, которые выводятся с калом и мочой. За
сутки разрушается и превращается в желчные пигменты около 8 г гемоглобина, т. е.
несколько более 1 %.
В организме человека и животных могут образовываться и другие соединения
гемоглобина, при спектральном анализе которых обнаруживаются характерные спектры
поглощения. К числу таких соединений гемоглобина относятся метгемоглобин и
карбокенгемоглобин. Вещества эти образуются в результате некоторых
отравлений.
Метгемоглобин (MetHb) представляет собой прочное соединение
гемоглобина с кислородом; при образовании метгемоглобина меняется валентность
железа: двухвалентное железо, входящее в молекулу гемоглобина, превращается в
трехвалентное. В случае накопления в крови больших количеств метгемоглобина
отдача кислорода тканям становится невозможной и наступает смерть от
удушення.
Метгемоглобин отличается от гемоглобина коричневым цветом и наличием полосы
поглощения в красной части спектра. Метгемоглобин образуется при действии
сильных окислителей: феррицианида (красной кровяной соли), марганцовокислого
калия, амил- и пропилнитрита, анилина, бертолетовой соли, фенацетина.
Карбоксигемоглобин (НbСО) представляет собой соединение железа
гемоглобина с окисью углерода (СО) — угарным газом. Это соединение примерно в
150—300 раз прочнее, чем соединение гемоглобина с кислородом. Поэтому примесь
даже 0,1 % угарного газа во вдыхаемом воздухе ведет к тому, что 80% гемоглобина
оказываются связанными окисью углерода и не присоединяют кислород, что является
опасным для жизни.
Слабое отравление угарным газом — обратимый процесс. Прп дыхании свежим
воздухом СО постепенно отщепляется от карбоксигемоглобнна и
выделяется.
Вдыхание чистого кислорода увеличивает скорость расщепления
карбоксигемоглобина в 20 раз. В тяжелых случаях отравления необходимо
искусственное дыхание (стр. 171) газовой смесью с 95% содержания 02 и 5% СО2, а
также переливание крови.
Миоглобин. В скелетной и сердечной мышце находится мышечный
гемоглобин, называемый миоглобином. Его простетическая группа — гем — идентична
этой же группе молекулы гемоглобина, а белковая часть — глобин — обладает
меньшим молекулярным весом, чем белок гемоглобина.
Миоглобин человека способен связывать до 14% от общего количества кислорода в
организме. Это его свойство играет важную роль в снабжении кислородом работающих
мышц. Если при сокращении мышцы кровеносные капилляры ее сжимаются и кровоток в
некоторых участках мышцы прекращается, то все же благодаря наличию кислорода,
связанного с миоглобином, в течение некоторого времепп сохраняется снабжение
мышечных волокон кислородом.
Источник
Количественное определение гемоглобина
Определение количества гемоглобина в крови производится колориметрическим путем. Простейший тип – гемометр.
Принцип действия.
Гемоглобин крови под действием децинормального раствора соляной кислоты превращается в солянокислый гематин. Полученный раствор бурого цвета разбавляется в градуированной пробирке водой до совпадения его цвета с цветом стандартов гемометра. Количество гемоглобина отсчитывается по уровню разбавленного раствора в градуированной пробирке согласно делению шкалы прибора.
Конструкция гемометра.
Гемометр состоит из корпуса стойки с тремя смотровыми окошками. Снизу корпус закрывается крышкой, привинчивающейся двумя винтами. В два гнезда снизу вставляются одинаковые запаянные пробирки со стандартной жидкостью и закрываются крышкой. В среднее гнездо вставляется градуированная пробирка. Цвет жидкости заполненных пробирок-стандартов установлен соответственно цвету раствора солянокислого гематина, полученного из крови с концентрацией гемоглобина в 17,3г%. В задней стенке корпуса смонтировано прозрачно-матовое или молочного цвета стекло. Состав стандартных жидкостей гемометра: 200мм3 децинормальной соляной кислоты смешивают с 20мм3 крови, а затем объем раствора доводится добавлением дистиллированной воды до 2мл. Гемоглобин крови при этом распадается на белок глобин и гем: последний, соединяясь с соляной кислотой, образует солянокислый гематин, имеющий коричневую окраску. В таком стандартном растворе содержится 17,3г% гемоглобина.
Измерительная пробирка и единицы измерения гемоглобина
Градуированная пробирка гемометра может иметь шкалу: с делением от 2 до 23. которая показывает количество гемоглобина в граммах на 100 мл крови, т.е. концентрация гемоглобина в гр%, по СИ – г/л.
Ход работы.
В градуированную пробирку наливают децинормальный раствор соляной кислоты до метки с цифрой 2 г%. Капиллярной пипеткой набирают 20 мм крови, путем осторожного насасывания через резиновую трубку в мундштук. Обычно кровь насасывают на несколько миллиметров выше круговой метки, вынимают мундштук и обтирают ватой кровь, прилипшую снаружи на кончик пипетки. Столбик крови обычно доводится до метки посредством дотрагивания до кончика пипетки ватой. При этом пипетку необходимо держать горизонтально. Затем пипетку с кровью опускают в градуированную пробирку так, чтобы кончик ее прогрузился в соляную кислоту, и кровь осторожно, не взмучивания жидкости, выдавливается из пипетки. После этого пипетка промывается путем насасывания 2 или 3 раза соляной кислоты из верхнего слоя ее в пробирке. Затем пипетка приподнимается, окончательно освобождается от жидкости выдуванием при прикосновении к стенкам пробирки и осторожно удаляется из пробирки. Полученная смесь крови с соляной кислотой тщательно перемешивается посредством легкого постукивания по дну пробирки. Полученную смесь красновато-бурого цвета оставляют в спокойном состоянии в течение 5 минут, поместив пробирку в корпус гемометра. За это время произойдет образование солянокислого гематина (или гемина). По истечении этого времени жидкость осторожно разбавляют дистиллированной водой (пипеткой) до тех пор, пока не будет одинакового цвета со стандартами. Во время разбавления жидкость в пробирке тщательно перемешивается стеклянной палочкой. Сравнение цветов проводится путем сличения при рассмотрении их при дневном свете на вытянутой руке против окна. Количество гемоглобина отсчитывается после совпадения цвета жидкости с цветом стандартов, причем отсчет производится нижнему мениску жидкости в пробирке.
Количество гемоглобина у животных
| Вид животного | г/100мл, г% | г/л |
| КРС | 9-12 | 90-120 |
| Лошади | 8-14 | 80-140 |
| Овцы, козы | 0-14 | 100-140 |
| Свиньи | 9-11 | 90-110 |
| Кролики | 10,5-12,5 | 105-125 |
| Собаки | 13-16 | 130-160 |
| Человек: женщины | 12-14 | 120-140 |
| мужчины | 13-16 | 130-160 |
Качественное определение гемоглобина
Гемоглобин обладает характерным спектром поглощения, отличающим его от других химических соединений. Спектральный анализ позволяет выяснить наличие в каком-либо растворе гемоглобина или его производных.
Ход работы.
К 10 мл дистиллированной воды в пробирке прибавьте 1-2 капли крови, происходит гемолиз крови (т.е. разрушение эритроцитов, которое сопровождается выходом из них красящего пигмента). Гемолизированная кровь исследуется с помощью карманного спектроскопа на проходящем свете. Если между целью спектроскопа и источником света поместить окрашенную среду (гемолизированная кровь), то окрашенный раствор пропускает не все лучи белого цвета, задерживая некоторые из них. Та часть спектра, лучи которой не пропускаются, представляются наблюдателю в виде темных полос.
В нашем опыте в поле зрения спектра обнаруживаются две полоски поглощения в желто-зеленой части спектра, между фраунгоферовыми Д и Е слева более узкая и справа более широкая, характерные для оксигемоглобина.
Спектр восстановленного гемоглобина имеет одну широкую диффузную полосу поглощения между линиями Д и Е, ближе к линии Д.
Спектр метгемоглобина имеет 4 полосы поглощения. Наиболее характерной для метгемоглобина является полоса поглощения в красной части спектра, между линиями С и Д, ближе к С. Две другие полосы между линиями Д и Е, четвертая полоса широкая, расположена в сине-зеленой части спектра.
Спектр поглощения карбоксигемоглобина имеет две полосы поглощения, сходные с полосами поглощения оксигемоглобина, но полосы несколько сдвинуты к фиолетовой части спектра.
Источник
Общеклинический анализ крови – это первоочередное исследование, назначаемое больным при поступлении в муниципальные или частные клиники. Любые патологические изменения со стороны различных органов отражаются на составе крови.
Общеклинический анализ исследует количественные и качественные свойства красных форменных элементов и содержание в них белка гемоглобина. Квантитативное (количественное) определение гемоглобина в крови – важная составляющая работы лабораторных сотрудников, направленная на своевременное выявление анемии.
Красные форменные клетки вырабатываются (с помощью животных белков, железа и витаминов) в красном костном мозге и разрушаются под действием ферментов селезенки. Они выполняют жизненно важные функции – транспорт кислорода к тканям и утилизацию оксидов углерода. Повышенный или пониженный гемоглобин указывает на патологии органов различной этиологии. В предложенном ниже видео показан процесс переноса оксидов.
Строение и физиология гемоглобина
Гемоглобин – это четвертичная глобула, которая занимается утилизацией и поставкой оксидов в организме человека. Данное пептидное соединение является тетрамером, состоящим из четырех субъединиц. Одна полипептидная структура способна переносить через кровоток до четырех молекул кислорода.
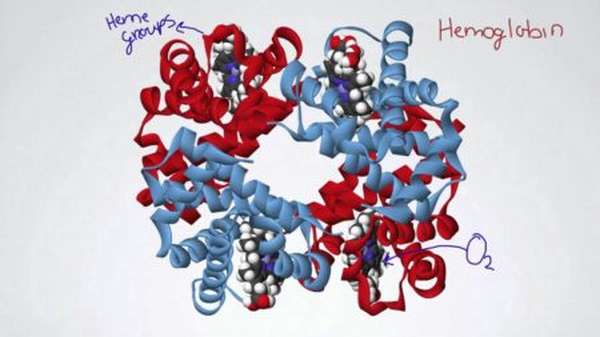
Гемоглобин состоит из простетической группы и глобулина. Простетическую группу железосодержащего пептида принято называть «гемом». Благодаря гему кровь приобретает свойственный ей окрас – алый или синевато-красный. Простетическая группа содержит железо, которое участвует в восстановительно-окислительных процессах.
Различают несколько основных видов гемоглобина:
- Оксигемоглобин,
- Карбоксигемоглобин,
- Дезоксигемоглобин,
Оксигемоглобин образуется при присоединении кислорода к гемоглобину в условиях высокого парциального давления. При отщеплении кислорода от железосодержащего белка образуется устойчивая форма – дезоксигемоглобин. Карбоксигемоглобин появляется в результате присоединения монооксида или диоксида углерода. Стоит отметить, что монооксид углерода в 250 раз эффективнее связывается с железосодержащим белком, чем обуславливается его опасность для жизни при вдыхании (угарный газ).
Дезоксигемоглобин сильно токсичен для тканей человеческого организма, поэтому существуют специальные системы «ликвидации» гемоглобина в крови. Этим занимается особое пептидное соединение – гаптоглобин.
Определение количества гемоглобина по методу Сали
Метод базируется на свойстве железосодержащего белка превращаться в хлорид гематита под действием соляной кислоты. Методика Сали считается неинвазивным вмешательством.
Интенсивность цвета жидкости прямо пропорциональна концентрации гемоглобина в крови. Раствор хлоргемина при проведении исследования разводят дистиллированной водой до стандартного цветового спектра.
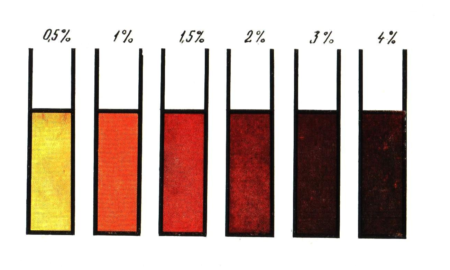
Важно! Стоит отметить, что гемоглобин по Сали не получил широкого распространения на территории РФ.
Метод, который применяется для определения уровня гемоглобина, принято называть «гемометром Сали». Другое название современного метода определения гемоглобина по Сали – гемоглобинометрия. Такой колориметрический аппарат состоит из специального штатива, который имеет три гнезда.
Боковые гнезда держат две склянки с веществами. Среднее гнездо данного прибора необходимо для размещения пронумерованной мензурки из стекла. Градуированная мензурка обладает шкалой с делениями, которые измеряют количество железосодержащего пептидного соединения в граммах на децилитр (г/дл). При клиническом исследовании крови используется специальная пипетка для воды и размешивания содержимого склянки.
При проведении полного анализа по методу Сали вначале в склянку наливается 0.10% раствор соляной кислоты. Потом выполняется забор исследовательского материала из кончика пальца в пипетку до отметки «0.04 мл». Впоследствии пипетку обтирают стерилизованной ваткой и размещают в мензурку с раствором HCl.
Медицинский сотрудник несколько раз встряхнет содержимое пробирки и поставит отстаиваться. Полное химическое превращение железосодержащего пептидного соединения в растворе соляной кислоты происходит не менее чем за 10-15 минут.
По истечении пяти минут оценивается цвет жидкости в гемометре со стандартными цветами. Как правило, он более темный, нежели в стандартных пробирках. Используя обычную пипетку к раствору постепенно добавляют чистую воду, попеременно перемешивая содержимое и сравнивая со стандартным цветом. На окончательном этапе цвет материала должен сравняться с нормативом. После всего вышеперечисленного замеряют уровень жидкости и проводят соответствующие подсчеты.
В промышленном масштабе выпускаются гемометры, которые содержат исключительно грамм-процентную градуированную шкалу. Нормой гемоглобина у мужчин и женщин принято считать значения 15 г%, или 168 г/дл. Но даже при соблюдении определенных правил наблюдаются небольшие погрешности в измерениях. В некоторых случаях разные результаты могут в значительной мере исказить данные о болезни.
Цианметгемоглобиновый метод определения содержания гемоглобина в крови
Стандартизированным и наиболее точным методом определения гемоглобина принято считать гемоглобинцианидный анализ. Такая методика базируется на свойстве железосодержащего пептидного соединения превращаться в цианметгемоглобин при добавлении к биологическому материалу определенного вещества.
Содержание цианметгемоглобина замеряют фотометрически. При анализе крови в роли реактива применяется раствор Драбкина. Железосодержащий белок под влиянием синеродисто-железистого калия превращается в метгемоглобин, который потом преобразуется в присутствии цианина калия в гемиглобинцианид.
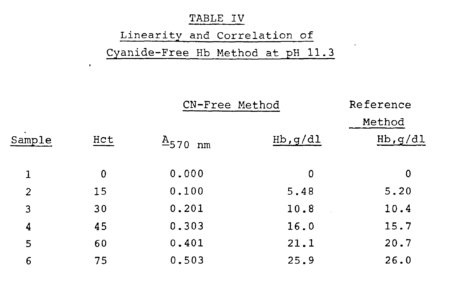
Типичное соотношение разведения биологического материала с реагентом — 2 : 500 (0,04 миллилитров капель крови и 10 мл реактива). По истечении 30 минут, которые нужны для полного преобразования железосодержащего пептида в гемиглобинцианид, измеряют «гашение» при длине волны в 550 нанометров и плюс толщине слоя в 2 см против воды на спектрофотометре СФ или на ФЭК и ему похожей технике. С помощью СФ также измеряют уровень свободного железосодержащего пептида в плазме.
На данный момент разработаны гемиглобинцианидные цветовые стандарты в ампулах, которые точно соответствуют определенному уровню железосодержащего белка. Растворы, полученные в результате определенных реакций, исследуют с помощью колориметрии. После всего рисуют рабочие таблицы и узнают, какое количество железосодержащего пептидного соединения содержится в кровотоке.
Есть устройства, специально созданные для определения количества гемоглобина. Зачастую используются именно циангемоглобиновые методы определения гемоглобина. Как правило, гемоглобинометрические приборы могут работать самостоятельно. Широкое применение такие тест-устройства для определения гемоглобина в крови получили в домашних условиях. Однако в ряде ситуаций больные не учитывают влияние внешних факторов в доме (стресса, еды).
Другой набор методов диагностики уровня гемоглобина в крови
Значительную известность и распространение среди различных лабораторий получила методика гемихром (или гемихромный метод). Принцип данного метода основан на преобразовании всех форм железосодержащего пептида в гемихром, который имеет красноватый цвет. Преимущество гемихромного метода заключается в том, что он не является токсичным.
Иногда назначают прохождение биохимического исследования на гликированный гемоглобин. Стоит отметить, что важное значение гликозилированный гемоглобин и глюкометр имеют при диагностике сахарного диабета.
При определенных состояниях в моче может содержаться гемоглобин, поэтому нередко данная биологическая жидкость и ее анализы являются важными частями диагностики различных заболеваний. Такое случается при переливании несовместимой крови от донора, в особенности у ребенка.
Загрузка…
Источник
