Гемолитическая анемия минковского шоффара симптомы
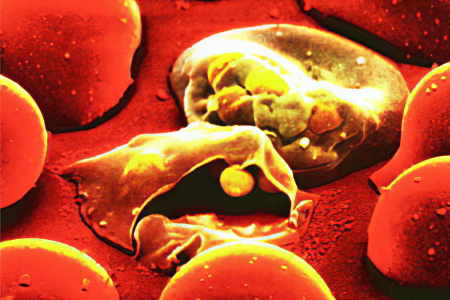
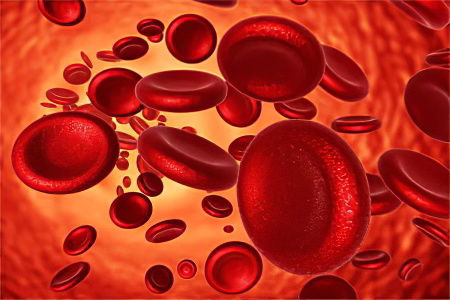
Анемия характеризуется снижением уровня гемоглобина в крови. Это заболевание имеет широкое распространение. От него страдают люди самых разных возрастов. Нередко анемия диагностируется в детском возрасте.
Анемия – это не какое-то одно заболевание. Существует множество разновидностей патологии. Самой частой причиной анемии выступают погрешности в питании, когда организм человека испытывает дефицит витаминов и питательных веществ. Устранить такое состояние можно с помощью медикаментозной коррекции, однако, предварительно нужно уточнить причину его развития.
Гемолитическая анемия Минковского-Шоффара является серьезной патологией. Она представляет опасность для здоровья и жизни человека. Именно об этой разновидности анемии речь пойдет далее.
Содержание:
- Анемия – что это?
- В чем отличительная особенность гемолитической анемии?
- Причины анемии Минковского-Шоффара
- Симптомы анемии Минковского-Шоффара
- Диагностика анемии Минковского-Шоффара
- Лечение анемии Минковского-Шоффара
- Осложнения анемии Минковского-Шоффара
- Меры профилактики
Анемия – что это?
Анемия характеризуется снижением уровня эритроцитов и гемоглобина в крови. В ряде случаев ниже нормы падает не только численный состав эритроцитов, но и изменяется их форма. По мере прогрессирования заболевания, красные кровяные тельца не в состоянии выполнять свои функции.
Анемия развивается на фоне иных нарушений в организме, сама по себе она не манифестирует. Поэтому для избавления от болезни следует установить причину, которая привела к изменению в составе крови.
В чем отличительная особенность гемолитической анемии?
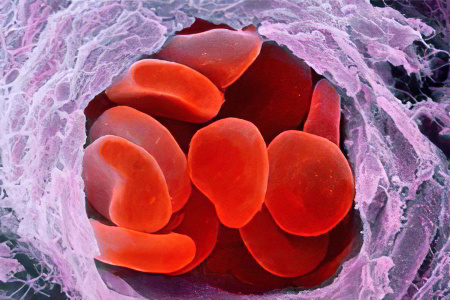
Гемолитическая анемия объединяет в себе сразу несколько заболеваний, но причины их развития едины. Эритроциты в крови разрушаются слишком быстро, поэтому красный костный мозг начинает их усиленно вырабатывать. В результате, цикл их роста нарушается. По мере прогрессирования анемии, эритроциты подвергаются массовой гибели.
Гемолитические анемии могут передаваться от родителей детям, а могут развиваться в течение жизни. Анемия Минковского-Шоффара является наследственной патологией.
Также это заболевание называют микросфероцитарной анемией и наследственным сфероцитозом. Однако чаще всего используется термин «анемия Минковского-Шоффара» по имени ученых, которые впервые открыли эту патологию.
Нельзя назвать данную разновидность анемии редкой, она поражает каждого 5000-ого жителя планеты. Чаще всего от нее страдает люди, населяющие Северную Европу. Впервые анемия Минковского-Шоффара дает о себе знать еще в детстве. Если оставить это нарушение без лечения, то пострадает организм в целом.
Причины анемии Минковского-Шоффара

При анемии Минковского-Шоффара структура эритроцитов претерпевает патологические изменения, что отражается на их функционировании. Красные кровяные тельца становятся хрупкими и гораздо легче разрушаются. Из них выходит гемоглобин, который в свободной форме циркулирует в крови.
Если в норме эритроциты имеют форму двояковыпуклого диска, то при анемии Минковского-Шоффара они становятся круглыми, что не позволяет им проникать в мелкие кровеносные сосуды. При попытке сделать это, эритроциты сильно повреждаются и разрушаются. Их уровень в крови снижается, что становится причиной развития анемии.
Если от анемии Минковского-Шоффара страдал один из родителей, то это заболевание будет унаследовано ребенком. Редко больные дети появляются на свет от абсолютно здоровых родителей. Если это случается, то причиной специалисты называют повреждения в структуре ДНК. Гены мутируют в то время, когда малыш находится в утробе женщины.
Патогенными факторами выступают:
Воздействие на организм женщины радиоактивного или рентгеновского излучения.
Отравление организма беременной женщины солями тяжелых металлов, наркотиками, табачным дымом.
Перенесенные вирусные заболевания.
Следует принять во внимание, что эти патогенные факторы способны спровоцировать не только анемию, но и иные серьезные нарушения в организме растущего плода. Поэтому относиться к своему здоровью нужно очень бережно.
Симптомы анемии Минковского-Шоффара

Чем ниже в крови уровень нормальных эритроцитов, тем сильнее будут симптомы болезни. Первые признаки патологии развиваются у ребенка еще в дошкольный период, либо во время раннего школьного возраста. Анемия имеет волнообразное течение, периоды ремиссии сменяются периодам обострения.
Во время гемолитического криза происходит массовая гибель эритроцитов. При этом все симптомы набирают силу. Когда криз минует, человек будет чувствовать себя удовлетворительно. Возможно чрезмерная бледность кожных покровов и слизистых оболочек.
Симптомами криза являются:
Высокая температура тела.
Головные боли.
Общая слабость и недомогание.
Желтушность кожных покровов.
Спазмы и боли в животе.
Увеличение печени в размерах.
Воспаление селезенки.
Развиваться заболевание может также и во взрослом возрасте. Первым признаком на который человек чаще всего обращает внимание – это пожелтение кожных покровов. Хотя в ряде случаев объективные симптомы нарушения могут вовсе отсутствовать. Зачастую диагностировать анемию удается только во время случайного осмотра, когда человек сдает кровь на анализ.
Диагностика анемии Минковского-Шоффара
Выявить заболевание, как правило, не составляет труда. Доктор выслушает жалобы пациента и осуществит его осмотр. Обязательно нужно уточнить, страдали ли от анемии ближайшие кровные родственники человека. Кроме внешнего осмотра кожи и слизистых оболочек, доктор пальпирует живот, чтобы уточнить, увеличена ли печень и селезенка больного в размерах. В обязательном порядке назначают УЗИ этих органов.
Без лабораторных исследований подтвердить диагноз не удастся, поэтому врач направляет пациента сдать следующие анализы:
Анализ мочи. В ней может быть выявлен билирубин, белок и уробилин в высоких концентрациях.
Кровь на биохимический анализ. При этом удастся обнаружить снижение уровня холестерина, повышение уровня непрямого билирубина и лактатдегидрогеназы.
Кровь на клинический анализ. При этом будет обнаружено повышение уровня ретикулоцитов, сами эритроциты уменьшаются в размерах. Кроме того, повышается СОЭ, может отмечаться снижение уровня тромбоцитов и лейкоцитов. Цветовой показатель крови будет ниже нормы.
Чтобы подтвердить диагноз, потребуется изучить белки мембран эритроцитов методом двумерного электрофореза.
Обязательно нужно проводить дифференциальную диагностику анемии Минковского-Шоффара с аутоиммунными заболеваниями. В первую очередь, необходимо тщательно изучить семейный анамнез, так как анемия Минковского-Шоффара чаще всего передается по наследству. Кроме того, у больных детей имеются определенные изменения в строении черепа. Если у доктора остаются сомнения, то пациенту выполняют пробу Кумбса. Когда эта проба дает отрицательный результат, диагноз подтверждают.
Лечение анемии Минковского-Шоффара

В зависимости от тяжести течения болезни, будут различаться способы его медикаментозной коррекции. В период ремиссии анемии терапию не проводят. Во время обострения патологии пациента необходимо госпитализировать.
Лечение сводится к следующим мероприятиям:
При снижении уровня гемоглобина до 70 г/л пациенту переливают эритроцитарную массу.
При высоком уровне билирубина в крови больному вводят альбумин.
Для снятия интоксикации с организма больному проводят инфузионную терапию.
Желчегонные препараты позволяют улучшить самочувствие пациента при гемолитическом кризе.
Тяжелое течение анемии Минковского-Шоффара требует оперативного вмешательства. Для этого больному удаляют селезенку. Это не даст возможности полностью избавиться от анемии, но состояние человека улучшается, так как жизненный цикл эритроцитов удается продлить.
После удаления селезенки больному больше не будут грозить гемолитические кризы. Однако эта процедура противопоказана в возрасте младше 5 лет, так как малышам спленэктомия грозит летальным исходом. Кроме того, отсутствие в организме селезенки способствует снижению иммунитета. Человек становится восприимчивым к различным инфекциям.
Еще один оперативный метод лечения анемии – это эндоваскулярная окклюзия. Данная процедура является альтернативой спленэктомии. Во время процедуры пациенту вводят препарат, который вызывает инфаркт селезенки. Ее определенная часть не погибает, а продолжает функционировать, поэтому состояние больного улучшается, но иммунитет при этом не падает.
Если заболевание протекает легко и больной получает качественное и своевременное лечение, то прогноз на жизнь благоприятный. Удаление селезенки позволяет избежать кризов. Без проведения операции средняя продолжительность ремиссии между гемолитическими кризами составляет 2 года.
Осложнения анемии Минковского-Шоффара

В детском возрасте анемия Минковского-Шоффара способна стать причиной задержки умственного и физического развития. Чаще всего это наблюдается в том случае, когда ребенок не получает лечения, либо его начинают слишком поздно.
Во взрослом возрасте самым частым осложнением анемии Минковского-Шоффара является желчнокаменная болезнь, которая развивается на фоне повышенного уровня билирубина в крови. Зачастую гемолитический криз путают с механической желтухой, поэтому адекватную терапию больному не проводят. Если у пациента в желчном пузыре обнаруживаются камни, то его удаляют вместе с селезенкой.
Меры профилактики
Анемия Минковского-Шоффара – это заболевание, которое передается по наследству, поэтому предотвратить его развитие невозможно. Людям, страдающим от данной патологии нужно состоять на учете у гематолога.
Вероятность появления на свет ребенка с гемолитической анемией у больной матери приравнивается к 50%. Поэтому такие дети должны с рождения быть качественно обследованы.

Автор статьи: Шутов Максим Евгеньевич | Гематолог
Образование:
В 2013 году закончен Курский государственный медицинский университет и получен диплом «Лечебное дело». Спустя 2 года окончена ординатура по специальности «Онкология». В 2016 году пройдена аспирантура в Национальном медико-хирургическом центре имени Н. И. Пирогова.
Наши авторы
Источник
Медицинский эксперт статьи

х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Наследственный сфероцитоз (болезнь Минковского-Шоффара) – это гемолитическая анемия, в основе которой лежат структурные или функциональные нарушения мембранных белков, протекающая с внутриклеточным гемолизом.
Немецкий терапевт О. Минковский (1900) первым дал описание семейной гемолитической анемии; М.А. Шоффар (1907), французский терапевт, обнаружил у больных снижение резистентности эритроцитов и связанное с этим усиление гемолиза.
Заболевание распространено повсеместно, частота встречаемости составляет 1:5 000 в популяции. Передается по аутосомно-доминантному типу; около 25 % случаев спорадические, обусловленные возникновением новой мутации.
Чаще встречается у жителей Северной Европы, где распространённость заболевания составляет 1 на 5000 населения.
Аутосомно-доминантный тип наследования встречается примерно в 75% случаев заболевания. У членов семьи пациента тяжесть анемии и степень сфероцитоза может варьировать. В 25% случаев семейный анамнез отсутствует. У части пациентов изменения лабораторных показателей минимальны, что предполагает аутосомно-рецессивный тип наследования, остальные случаи – результат спонтанных мутаций.
 [1], [2]
[1], [2]
Код по МКБ-10
D58.0 Наследственный сфероцитоз
Как развивается болезнь Минковского-Шоффара?
Связан с наследственным дефектом мембраны эритроцитов в виде дефицита определённых структурных белков (спектрины, анкирины, актины). Эти белки служат для поддержания двояковогнутой формы эритроцитов и в то же время позволяют им деформироваться при прохождении через узкие капилляры. Выделяют изолированный парциальный дефицит спектрина, комбинированный дефицит спектрина и анкирина (30-60% случаев), парциальный дефицит белка полосы 3 (15-40% случаев), дефицит белка 4,2 и других, менее значимых белков. Дефицит этих белков приводит к дестабилизации липидной структуры мембраны эритроцитов, нарушается работа натрий-калиевого насоса мембраны. Повышается проницаемость эритроцита для ионов натрия. Поступая в клетку, натрий тянет за собой воду. Набухая, эритроцит приобретает сферическую форму – наиболее энергетически выгодную. При этом он уменьшается в диаметре, но увеличивается его толщина. Такой эритроцит вследствие изменённой структуры мембраны не способен к трансформации при прохождении мелких межсинусоидальных пространств селезёнки, где снижена концентрация глюкозы и холестерина, что способствует ещё большему набуханию эритроцита. Это прохождение сопровождается отрывом липидных структур. Эритроцит становится всё более дефектным и маленьким. Такой эритроцит воспринимается макрофагами селезёнки как чужеродный, захватывается и разрушается. Таким образом, происходит внутриклеточный гемолиз. Продолжительность жизни эритроцитов резко сокращается (до 12-14 дней) вследствие их сильного изнашивания, так как требуется больше энергии для удаления из клетки ионов натрия, в избытке поступающих внутрь клетки. Компенсаторно в костном мозге усиливается эритроуоэз. Вследствие гемолиза в крови увеличивается количество непрямого билирубина, но резкого его нарастания не происходит, так как печень значительно увеличивает свою функциональную активность: усиливает образование прямого билирубина, вследствие чего нарастает его концентрация в жёлчи и содержание в жёлчных ходах. При этом часто образуются билирубиновые камни в жёлчном пузыре и протоках – развивается желчнокаменная болезнь. Как следствие может появиться механическая желтуха: увеличивается количество стеркобилиногена и содержание уробилина. После возраста 10 лет камни жёлчного пузыря встречаются у половины больных, не подвергнутых спленэктомии.
Патогенез наследственного сфероцитоза (болезни Минковского-Шоффара)
Симптомы болезни Минковского-Шоффара
Тяжесть и разнообразие клинической картины обусловлены видом структурного белка, отсутствующего на мембране эритроцита (недостаточность а-цепи спектрина наследуется аутосомно-доминантно и протекает легко, а недостаточность бета-цепи вызывает тяжёлое заболевание, наследуемое аутосомно-рецессивно). В половине случаев наследственный сфероцитоз проявляется уже в периоде новорождённости, имитируя картину гемолитической болезни новорождённых или затяжной конъюгационной гипербилирубинемии. Клиническая картина гемолитического криза складывается из триады симптомов: бледности, желтухи, спленомегалии. Кризы могут быть спровоцированы инфекционными заболеваниями, приёмом ряда лекарственных препаратов, но могут быть спонтанными. В межкризовый период больные не жалуются, но увеличенная селезёнка у них пальпируется всегда. Чем тяжелее протекает заболевание, тем отчётливее выражены определённые фендтипические особенности, а именно: башенный череп, готическое нёбо, широкая переносица, большие расстояния между зубами. Эти изменения костной ткани связаны с компенсаторной гиперплазией костного мозга (эритроидного ростка), и, как следствие, остеопорозом плоских костей. В зависимости от тяжести наследственного сфероцитоза степень выраженности клинических симптомов может быть различной. Иногда желтуха может быть единственным симптомом, по поводу которого больной обращается к врачу. Именно к этим лицам относится известное выражение М.А. Шоффара: «Они более желтушны, чем больны». Наряду с типичными классическими признаками заболевания встречаются формы наследственного сфероцитоза, когда гемолитическая анемия может быть настолько хорошо компенсирована, что пациент узнает о заболевании лишь при проведении соответствующего обследования.
Симптомы наследственного сфероцитоза (болезни Минковского-Шоффара)
Осложнения болезни Минковского-Шоффара
Наиболее частое осложнение при наследственном сфероцитозе – развитие желчнокаменной болезни вследствие нарушения билирубинового обмена. Часто за гемолитический криз принимают развитие механической желтухи при желчнокаменной болезни. При наличии камней в жёлчном пузыре показана холецистэктомия вместе со спленэктомией. Выполнение только холецистэктомии нецелесообразно, так как продолжающийся гемолиз рано или поздно приведёт к образованию камней в жёлчных протоках.
Образование трофических язв – достаточно редкое осложнение, встречающееся у детей. Язвы возникают из-за разрушения эритроцитов, вследствие чего происходит тромбирование сосудов, развивается ишемия.
Очень редко возникают так называемые арегенераторные, или апластические, кризы, когда повышенный гемолиз в течение нескольких дней не сопровождается усиленным эритропоэзом. В результате этого ретикулоциты исчезают из крови, быстро нарастает анемия, уровень непрямого билирубина падает. Сейчас ведущая этиологическая роль при данном осложнении отводится парвовирусу (В 19).
 [3], [4]
[3], [4]
Как распознать наследственный сфероцитоз?
Диагностика этого заболевания достаточно проста. Диагноз наследственного сфероцитоза делают несомненным следующие признаки: желтуха, деформация лицевого черепа, увеличенная селезёнка, сфероцитоз эритроцитов, их пониженная осмотическая стойкость, высокий ретикулоцитоз. Большую помощь в постановке правильного диагноза играет тщательный сбор анамнеза. Как правило, аналогичные симптомы удаётся обнаружить у одного из родителей больного, хотя их выраженность может быть иной (например, периодическая иктеричность склер). В редких случаях родители совершенно здоровы. Трудности диагностики часто обусловлены желчнокаменной болезнью, обычно сопровождающей наследственный микросфероцитоз (из-за образования в протоках и жёлчном пузыре билирубиновых камней). Свойственная гемолизу непрямая билирубинемия при холелитиазе сменяется прямой – возникает механическая желтуха. Болезненность в области жёлчного пузыря, некоторое увеличение печени – обычные признаки при наследственном микросфероцитозе. Нередко в течение многих лет больных ошибочно рассматривают как лиц, страдающих заболеванием желчевыводящих путей или печени. Одна из причин ошибочного диагноза в данном случае – отсутствие сведений о ретикулоцитах.
Лабораторная диагностика включает ряд исследований.
Клинический анализ крови – определяется нормохромная гиперрегенераторная анемия, микросфероцитоз эритроцитов. В период криза может быть нейтрофильный лейкоцитоз со сдвигом влево. Характерно увеличение СОЭ.
Биохимический анализ – крови отмечают повышение непрямого билирубина, сывороточного железа, ЛДГ.
Обязательно исследование осмотической резистентности эритроцитов в растворах натрия хлорида различной концентрации. При наследственном сфероцитозе отмечают снижение минимальной осмотической резистентности, когда гемолиз наименее стойких эритроцитов начинается уже при концентрации натрия хлорида 0,6-0,7% (норма 0,44-0,48%). Максимальная стойкость может быть повышена (норма 0,28-0,3%). Среди больных наследственным сфероцитозом встречаются лица, у которых, несмотря на явные изменения морфологии эритроцитов, в обычных условиях осмотическая стойкость эритроцитов нормальная. В этих случаях необходимо её исследовать после предварительной суточной инкубации эритроцитов.
К морфологическим особенностям эритроцитов при наследственном сфероцитозе относятся шарообразная форма (сфероциты), уменьшение диаметра (средний диаметр эритроцита
Содержание гемоглобина в эритроцитах остается в пределах физиологической нормы или несколько выше. Цветовой показатель близок к 1,0. Эритроцитометрическая кривая Прайс-Джонса растянута, сдвинута влево.
Костно-мозговая пункция не обязательна. Она проводится только в неясных случаях. В миелограмме должно быть компенсаторное раздражение эритроидного ростка кроветворения.
Для проведения дифференциальной диагностики с иммунными гемолитическими анемиями необходимо ставить пробу Кумбса. При наследственном сфероцитозе она отрицательная.
Окончательно и достоверно подтвердить диагноз наследственного сфероцитоза позволяет проведение электрофореза белков мембраны эритроцита в сочетании с количественным определением белков.
Дифференциальный диагноз
Сфероцитоз эритроцитов и другие признаки гемолиза (желтуха, увеличение селезёнки, ретикулоцитоз) встречаются и при аутоиммунных гемолитических анемиях. Однако в отличие от наследственного микросфероцитоза при последних не бывает изменений костей черепа, признаков наследственного микросфероцитоза у кого-либо из родителей; при первых клинических проявлениях аутоиммунного гемолиза ещё не отмечается существенного увеличения селезёнки, болезненности в области жёлчного пузыря, но анизоцитоз и пойкилоцитоз эритроцитов выражены больше, чем при микросфероцитозе. В сомнительных случаях необходимо проводить пробу Кумбса, которая бывает положительной (прямая проба) в большинстве случаев аутоиммунной гемолитической анемии и отрицательной при наследственном микросфероцитозе.
Диагностика наследственного сфероцитоза (болезни Минковского-Шоффара)
 [5], [6], [7], [8], [9], [10], [11], [12], [13], [14], [15]
[5], [6], [7], [8], [9], [10], [11], [12], [13], [14], [15]
Какие анализы необходимы?
Лечение болезни Минковского-Шоффара
Лечение в период гемолитического криза заключается в проведении заместительной терапии эритроцитарной массой при снижении гемоглобина ниже 70 г/л. В ряде случаев требуется проведение инфузионной терапии с дезинтоксикационной целью. При высоких показателях билирубина показано лечение альбумином. Во внекризовый период следует проводить лечение желчегонными препаратами. В случае тяжёлого течения заболевания в сочетании с задержкой физического развития, сопровождающегося частыми кризами, требующими постоянного проведения заместительной терапии, показано проведение спленэктомии. Помимо этого показанием к спленэктомии служит развитие гиперспленизма. Спленэктомия не приводит к излечению от данной патологии, но после удаления селезёнки исчезает основной плацдарм для раз-рушения эритроцитов и продолжительность их жизни удлиняется. Как правило, у детей с удалённой селезёнкой гемолитические кризы не повторяются. Существуют и отрицательные стороны спленэктомии. Удаление селезёнки отрицательно влияет на иммунологическую реактивность организма ребёнка, происходит снижение фагоцитарной активности лейкоцитов, повышается восприимчивость к паразитарным, грибковым и вирусным инфекциям. Есть мнение, что удаление селезёнки приводит к развитию синдрома гипоспленизма, проявляющегося в снижении жизненного тонуса, явлениях психической лабильности и снижении трудоспособности. Потенциальными факторами риска спленэктомии являются технические сложности во время операции у больных, имеющих большие размеры органа, развитие кровотечений во время и после операции, а также инфекционно-септические осложнения. Описаны случаи смертельного исхода от бактериальных инфекций в позднем послеоперационном периоде у детей, перенёсших спленэктомию в возрасте до 5 лет. Именно поэтому проведение спленэктомии в возрасте до 5 лет не рекомендуется. Подготовка к спленэктомии включает введение за 2 нед до операции пневмококковой, менингококковой вакцин, назначение глюкокортикоидов, ВВИГ. В течение последующих 2 лет показано ежемесячное введение бициллина-5. В последние годы широко проводят лапароскопическую спленэктомию, которая имеет значительно меньше операционных и послеоперационных осложнений, оставляет минимальный косметический дефект, позволяет сократить время пребывания пациента в стационаре. Альтернативой спленэктомии может считаться эндоваскулярная окклюзия селезёнки – введение в селезёночную артерию веществ, вызывающих её спазм и в последующем приводящих к развитию инфаркта селезёнки. 2-5% ткани после окклюзии органа сохраняют кровоснабжение благодаря коллатералям. Это поддерживает иммунологическую реактивность организма, что важно для педиатрической практики. Данная операция имеет минимальное число осложнений. За рубежом для уменьшения риска развития осложнений после операции чаще всего используют проксимальную эмболизацию селезёнки за несколько дней до спленэктомии.
Как лечится наследственный сфероцитоз (болезнь Минковского-Шоффара)?
Исход
При лёгком течении заболевания, а также при своевременно проведённой спленэктомии исход благоприятный. Течение наследственного сфероцитоза волнообразное. Вслед за развитием криза улучшаются клинико-лабораторные показатели и наступает ремиссия, которая может длиться от нескольких недель до нескольких лет.
Источник
