Гемолитическая анемия при скв

Приобретенная иммунологическая гемолитическая анемия — причина наиболее тяжелых анемических осложнений у больных системной красной волчанкой.
При развитии данной патологии наблюдается падение числа эритроцитов в единичных наблюдениях до 600000. Гемолитическая анемия отмечается, по большим американским статистикам, у 3-10% всех больных.
Гемолитическая анемия с острым началом (кризом) может быть ранним, даже первым проявлением системной красной волчанки. Чаще она развивается уже на фоне развернутого течения заболевания, после провокации, например, гемотрансфузий. Гемолитическая анемия, однако, редко является непосредственной причиной смерти больных. Так, Dubois из 58 смертельных исходов при системной красной волчанке гемолизу приписывает лишь один случай.
Клиника гемолитической анемии при системной красной волчанке обычная для приобретенных иммунологических форм. Она характеризуется нормобластической гиперплазией костного мозга, увеличением селезенки, холодовой аутоагглютинацией эритроцитов, нередко затрудняющей подсчет клеток; положительной реакцией Кумбса, выявляемой, впрочем, у больных не только с клинически выраженной гемолитической анемией, но и у значительного числа всех больных системной красной волчанкой (у всех больных — Rosenfeld), то есть и у больных с гемолизом в скрытом состоянии.

Л.С. Резникова и Л.Я. Трофимова (1961) нашли положительную реакцию Кумбса у 20 из 24 больных системной красной волчанкой, между тем клинически гемолитическая анемия имелась лишь в единичных наблюдениях. Следует подчеркнуть, что реакция Кумбса остается положительной и во время ремиссии, наступающей в результате гормональной терапии.
В виде исключения наблюдают острые гемолитические кризы с гемоглобинемией и гемоглобинурией, гипохолестеринемией и характерным периодом восстановления — максимальной регенераторной реакцией, с колоссальным ретикулоцитозом, эритробластозом (отсюда наименование «эритробластический криз»). Типичное наблюдение приводит Debray.
У 28-летней женщины, страдавшей суставным («ревматическим») синдромом при обилии волчаночных клеток, быстро развилась анемия с падением числа эритроцитов до 1 500 000, а спустя 2 года даже до 600 000, что сопровождалось:
- реактивным компенсаторным эритробластозом (максимально 60 и даже 130 эритробластов на 100 лейкоцитов),
- ретикулоцитозом (максимально 890‰),
- тромбоцитозом (1700000 в 1 мм3),
- нейтрофильным лейкоцитозом (12000 с 6% миелоцитов),
- гемоглобинемией и умеренной желтухой,
- гипохолестеринемией (80 мг%),
- резкой гипергаммаглобулинемией (44,3 отн %).
У больной обнаружен ряд положительных иммунологических реакций:
- аутоагглютинация эритроцитов, обработанных папаином в солевой среде;
- прямая и непрямая реакции Кумбса;
- холодовая агглютинация эритроцитов человека в титре 1:68;
- падение комплемента;
- 100 % поглощение антиглобулина на лейкоцитах, сенсибилизированных сывороткой больной.
Была выявлена также антитромбопластинная активность сыворотки. Быстрое улучшение наступило от назначения гормонов и переливания эритроцитарной массы. Однако в дальнейшем больная перенесла еще 2 тяжелых криза и, несмотря на поддерживающую терапию и должный режим, умерла при очередном кризе.
В другом аналогичном случае число эритроцитов падало до 800000 при 240‰ ретикулоцитов, наблюдались резкая диспротеинемия, положительная реакция Кумбса, холодовая агглютинация, тепловые и холодовые сывороточные антитела, позже развилось поражение почек. Лечение преднизоном (с последующей поддерживающей терапией) дало отличные результаты.

Из других гематологических иммунных синдромов описаны формы с подавлением кроветворения: резкая нейтропения при попытках лечения производными иприта и ТЕМ, смертельный лекарственный агранулоцитоз от пирамидона, апластическая анемия от левомицетина.
Эритроцито-, тромбоцито-, нейтролейкопения у больных системной красной волчанкой, вызванные основным заболеванием или спровоцированные непереносимостью лекарств, перелитой кровью и т. д., могут развиваться независимо друг от друга или одновременно в различных сочетаниях, обусловливая разнообразную картину, как и при других аналогичных гемопатиях.
В общем гематологические осложнения все же не столь часты, как поражение сердца, почек и легких.
Волчанка – хроническое воспалительное аутоиммунное расстройство. Некоторые признаки этого заболевания могут быть временными, такие как боль в суставах и мышцах, усталость, сыпь, вызванная или усугубляемая солнечным светом и др.
Это заболевание часто может ошибочно диагностироваться как другие патологии, из-за возможного поражения внутренних органов. По этой причине волчанку часто называют «великим подражателем». Нет ни одного специфического диагностического теста, который может определить, присутствие у человека волчанки, но существует целый ряд других методов определения этой патологии.
Типы волчанки
Существует несколько основных типов волчанки, каждый из которых влияет на определенные группы пациентов:
Системная волчанка – при которой иммунная система атакует здоровую ткань.
Дискоидная волчанка – необычная кожная сыпь, усугубляемая солнечным светом.
Лекарственная волчанка – обычно наблюдается у пожилых пациентов в возрасте 50-70 лет, с более высокими показателями заболеваемости у тех, кто ежедневно принимает лекарства в дозах более 200 мг в день
Неонатальная волчанка – вызвана антителами матери, которые влияют на плод, и идентифицируется кожными поражениями, обычно на лице или голове, или врожденным пороком сердца.
Клинические признаки волчанки
Специалисты подтверждают диагноз, при наличии у пациентов 4-х из указанных ниже симптомов волчанки.
Внешние признаки
1. Маларовая сыпь – сыпь в форме бабочки на щеках.
2. Кожная сыпь появляется в зонах, подверженных воздействию солнца (фоточувствительность).
3. Потеря волос.
4. Дискоидная сыпь – красные пятна на коже из-за срастания волосяных фолликулов.
5. Артрит – длится несколько недель в нескольких суставах.
7. Язвы во рту или носу, длившиеся более месяца.
8. Признаки серозита – воспаление тканей, покрывающих внутренние органы (в том числе, сердца и легких).
9. Боль в животе.
10. Лихорадка, усталость и потеря веса.
Клинические (лабораторные) симптомы
· Лейкопения (низкий уровень лейкоцитов).
· Тромбоцитопения (низкий уровень тромбоцитов крови).
· Гемолитическая анемия (снижение количества эритроцитов).
· Кровь или белок в моче или анализы, которые определяют плохую функцию почек.
Дополнительная диагностика
Тест на антинуклеарные антитела (ANA) является часто используемым тестом на диагностику волчанки.
Другими диагностическими методами являются:
· Рентгенография грудной клетки – при инфекции оболочек легких, сердца.
· Анализ мочи для мониторинга количества белка или крови в моче, которые могут указывать на проблемы с почками.
· Тесты на креатинин сыворотки, которые измеряют количество креатинина в крови. Этот тест также определяет, насколько хорошо функционируют почки пациента.
Чем опасна системная волчанка?
Заболевание может поражать почти любую часть тела, включая кожу,суставы, почки, легкие, кровеносные сосуды, сердце и мозг. Невозможно узнать, какая часть тела будет затронута.
Иммунная система как правило защищает организм от бактерий и других агентов. При аутоиммунном заболевании, таком как волчанка, иммунная система теряет способность определять разницу между посторонними веществами и ее собственными клетками и тканями.
Затем иммунная система создает антитела, направленные против самого организма. Это вызывает воспаление, боль и повреждение различных органов. Вплоть, до тяжелых (смертельных) форм.
Спасибо, что читаете нас: если понравился материл – поддержите наш канал оценкой.
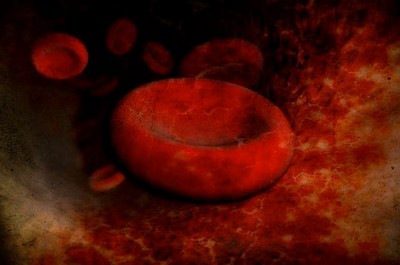
Приобретенная иммунологическая гемолитическая анемия , причина наиболее тяжелых анемических осложнений у больных системной красной волчанкой.
При развитии данной патологии наблюдается падение числа эритроцитов в единичных наблюдениях до 600000. Гемолитическая анемия отмечается, по большим американским статистикам, у 3-10% всех больных.
Гемолитическая анемия с острым началом (кризом) может быть ранним, даже первым проявлением системной красной волчанки. Чаще она развивается уже на фоне развернутого течения заболевания, после провокации, например, гемотрансфузий. Гемолитическая анемия, однако, редко является непосредственной причиной смерти больных. Так, Dubois из 58 смертельных исходов при системной красной волчанке гемолизу приписывает лишь один случай.
Клиника гемолитической анемии при системной красной волчанке обычная для приобретенных иммунологических форм. Она характеризуется нормобластической гиперплазией костного мозга, увеличением селезенки, холодовой аутоагглютинацией эритроцитов, нередко затрудняющей подсчет клеток, положительной реакцией Кумбса, выявляемой, впрочем, у больных не только с клинически выраженной гемолитической анемией, но и у значительного числа всех больных системной красной волчанкой (у всех больных , Rosenfeld), то есть и у больных с гемолизом в скрытом состоянии.

Л.С. Резникова и Л.Я. Трофимова (1961) нашли положительную реакцию Кумбса у 20 из 24 больных системной красной волчанкой, между тем клинически гемолитическая анемия имелась лишь в единичных наблюдениях. Следует подчеркнуть, что реакция Кумбса остается положительной и во время ремиссии, наступающей в результате гормональной терапии.
В виде исключения наблюдают острые гемолитические кризы с гемоглобинемией и гемоглобинурией, гипохолестеринемией и характерным периодом восстановления , максимальной регенераторной реакцией, с колоссальным ретикулоцитозом, эритробластозом (отсюда наименование «эритробластический криз»). Типичное наблюдение приводит Debray.
У 28-летней женщины, страдавшей суставным («ревматическим») синдромом при обилии волчаночных клеток, быстро развилась анемия с падением числа эритроцитов до 1 500 000, а спустя 2 года даже до 600 000, что сопровождалось:
- реактивным компенсаторным эритробластозом (максимально 60 и даже 130 эритробластов на 100 лейкоцитов),
- ретикулоцитозом (максимально 890‰),
- тромбоцитозом (1700000 в 1 мм3),
- нейтрофильным лейкоцитозом (12000 с 6% миелоцитов),
- гемоглобинемией и умеренной желтухой,
- гипохолестеринемией (80 мг%),
- резкой гипергаммаглобулинемией (44,3 отн %).
У больной обнаружен ряд положительных иммунологических реакций:
- аутоагглютинация эритроцитов, обработанных папаином в солевой среде,
- прямая и непрямая реакции Кумбса,
- холодовая агглютинация эритроцитов человека в титре 1:68,
- падение комплемента,
- 100 % поглощение антиглобулина на лейкоцитах, сенсибилизированных сывороткой больной.
Была выявлена также антитромбопластинная активность сыворотки. Быстрое улучшение наступило от назначения гормонов и переливания эритроцитарной массы. Однако в дальнейшем больная перенесла еще 2 тяжелых криза и, несмотря на поддерживающую терапию и должный режим, умерла при очередном кризе.
В другом аналогичном случае число эритроцитов падало до 800000 при 240‰ ретикулоцитов, наблюдались резкая диспротеинемия, положительная реакция Кумбса, холодовая агглютинация, тепловые и холодовые сывороточные антитела, позже развилось поражение почек. Лечение преднизоном (с последующей поддерживающей терапией) дало отличные результаты.
Из других гематологических иммунных синдромов описаны формы с подавлением кроветворения: резкая нейтропения при попытках лечения производными иприта и ТЕМ, смертельный лекарственный агранулоцитоз от пирамидона, апластическая анемия от левомицетина.
Эритроцито-, тромбоцито-, нейтролейкопения у больных системной красной волчанкой, вызванные основным заболеванием или спровоцированные непереносимостью лекарств, перелитой кровью и т. д., могут развиваться независимо друг от друга или одновременно в различных сочетаниях, обусловливая разнообразную картину, как и при других аналогичных гемопатиях.
В общем гематологические осложнения все же не столь часты, как поражение сердца, почек и легких.
Загрузка…
Содержание
- Гемолитическая анемия
- Классификация гемолитических анемий
- Причины гемолитических анемий
- Симптомы гемолитических анемий
- Наследственные мембранопатии, ферментопении и гемоглобинопатии
- Приобретенные гемолитические анемии
- Диагностика гемолитических анемий
- Лечение гемолитических анемий
Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для гемолитических анемий типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения гемолитической анемии используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
Гемолитическая анемия
Гемолитическая анемия — анемия, обусловленная нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Группа гемолитических анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных группах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. При гемолитической анемии жизненный цикл эритроцитов укорочен и их распад (гемолиз) происходит раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).
Классификация гемолитических анемий
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные.
Наследственные гемолитические анемии включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – гемолитические анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – гемолитические анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии — гемолитические анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные гемолитические анемии подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные анемии) – обусловлены воздействием антител
- токсические – гемолитические анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- гемолитические анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Причины гемолитических анемий
Патогенетическую основу наследственных гемолитических анемий составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфо-функциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды.
Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода, прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков). Аутоиммунные реакции с образованием антител, агглютинирующих эритроциты, возможны при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе, миеломной болезни), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии).
В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Механическое повреждение и гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.
Центральным звеном патогенеза гемолитических анемий является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. Эти процессы сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Симптомы гемолитических анемий
Наследственные мембранопатии, ферментопении и гемоглобинопатии
Наиболее распространенной формой данной группы гемолитических анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке.
Манифестация микросфероцитарной гемолитической анемии возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом — обтурационная желтуха. При микросфероцитарной гемолитической анемии во всех случаях увеличена селезенка, а у половины пациентов – еще и печень.
Кроме наследственной микросфероцитарной гемолитической анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические гемолитические анемии связаны с недостатком определенных ферментов эритроцитов (чаще — Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет.
Особенностям клинического течения гемоглобинопатий — талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Приобретенные гемолитические анемии
Среди различных вариантов приобретенных гемолитических анемий чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер.
Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка.
При некоторых формах аутоиммунных гемолитических анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические гемолитические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия.
Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Диагностика гемолитических анемий
Определение формы гемолитической анемии на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки.
Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. При аутоиммунных гемолитических анемиях большое диагностическое значение имеет положительная проба Кумбса. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, гемобластозы.
Лечение гемолитических анемий
Различные формы гемолитической анемии имеют свои особенности и подходы к лечению. При всех формах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной гемолитической анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной гемолитической анемии выполняется спленэктомия.
Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов. При развитии почечной недостаточности прогноз неблагоприятен.
