Несмотря на принятие в большинстве стран мира национальных программ по борьбе с сахарным диабетом (СД), его распространенность и заболеваемость им продолжают увеличиваться. Он является одной из основных причин ранней инвалидизации и высокой летальности населения.
В настоящее время во всем мире насчитывается около 246 миллионов больных диабетом. Учитывая темпы роста этого заболевания, эксперты ВОЗ прогнозируют, что количество больных к 2030 году достигнет 380 миллионов человек. В России в 2008 году официально зарегистрировано 2,834 млн. больных СД. Однако данные контрольно-эпидемиологических исследований показали, что истинная численность больных сахарным диабетом в 3-4 раза выше официально признанной и составляет порядка 8 млн. человек (1) (это 5,5% всего населения России). Проведенная в России в рамках Приоритетного национального проекта «Здоровье» диспансеризация 6,7 млн. здоровых людей в возрасте 35-55 лет выявила порядка 470 тыс. больных СД 2 типа, что составляет 7,1%. На самом деле и эти данные могут оказаться заниженными, так как около 50% больных СД остаются недиагностированными, и следовательно, не получающими никакой сахароснижающей терапии и сохраняющими стабильную гипергликемию – все это создает благоприятные условия для развития осложнений СД.
Доказано, что гипергликемия способствует развитию и прогрессированию микро-, макроангиопатии, полинейропатии с повреждением, дисфункцией и последующей недостаточностью жизненно важных органов и систем организма. Поражение сосудов сетчатой оболочки глаз с быстрой потерей зрения, гломерулосклероз с развитием хронической почечной недостаточности, диабетическая стопа, артериальная гипертензия, острая/хроническая ишемическая болезнь сердца, мозга и их последствия (инфаркт миокарда, сердечная недостаточность, инсульт, атрофия коры мозга со снижением когнитивных функций и развитием слабоумия) – таков далеко не полный перечень ассоциированных с СД болезней и синдромов. Как результат, пациенты с СД умирают в два раза чаще, чем те, кто не имеет этого заболевания. Наибольший удельный вес среди причин смерти имеет сердечно-сосудистая патология, на долю которой приходится не менее 85% всех смертей пациентов с СД 2-го типа. Столь серьезная ситуация во многом определяется поздней диагностикой СД 2-го типа, когда от момента появления заболевания до его обнаружения проходит более 10 лет, а также низким, не превышающим в некоторых странах 16%, уровнем адекватной компенсации гипергликемии. Поэтому повышение эффективности ранней диагностики СД и обеспечение качественного лечения, направленного на достижение целевого уровня гликемии пациента рассматривается сегодня как важнейшая задача, стоящая перед медиками многих стран мира, в том числе и России.
На сегодняшний день общепризнанным показателем выраженности и степени компенсации нарушений углеводного обмена является уровень гликированного гемоглобина (HbA1). Гликированный гемоглобин (гликогемоглобин) — это гемоглобин, в котором углеводный остаток конденсируется с N-концевым валином в бета-цепи молекулы НbА. Гликирование – неферментативный процесс и протекает медленно, в течение всей жизни эритроцита (около 120 дней). Установлено, что оно осуществляется через стадию образования альдимина (так называемые «Шиффовы основания» между альдегидом углеводов и аминогруппой), сравнительно нестойкого, «обратимого» соединения. Далее альдимин посредством химического преобразования (преобразование Амадори) превращается в относительно стойкое, «необратимое» соединение кетоамин. Образовавшийся кетоамин остается присоединенным к белку на весь период его жизни. Гликогемоглобин HbA1 разделяется на подгруппы в зависимости от присоединенного углевода (НbА1а, А1b, A1c). HbA1c – содержит одну молекулу глюкозы, он составляет 70-90% гликированной фракции, остальное количество приходится на HbA1а (имеет форму 1 – с фруктозо-1,6-бифосфатом и форму 2 – с глюкозо-6-фосфатом) и HbA1b (углеводный остаток, точно не идентифицирован).
Содержание гликогемоглобина имеет прямую корреляцию с уровнем глюкозы в крови и является интегрированным показателем компенсации углеводного обмена на протяжении последних 60–90 дней. Скорость образования НbА1с, также как и НbА1, зависит от величины гипергликемии, а нормализация его уровня в крови происходит через 4–6 недель после достижения нормального уровня гликемии. В отдельных случаях при высоком уровне глюкозы в крови могут наблюдаться низкие значения HbA1c. Это происходит при патологиях, сопровождающихся сокращением срока жизни эритроцитов (гемолитическая болезнь) или при значительной недавней потере крови (увеличение доли молодых эритроцитов). Напротив, высокие значения HbA1c при нормальном уровне глюкозы были отмечены при железодефицитной анемии (увеличение доли старых эритроцитов), дефиците витамина В12 и фолиевой кислоты. Эти обстоятельства должны быть учтены при клинической интерпретации значений HbA1c.
В соответствии с рекомендациями ВОЗ и Российской Федеральной целевой программы «Сахарный диабет», определение концентрации гликогемоглобина должно проводиться у каждого больного диабетом с регулярностью 4 раза в год (1,2). При этом определены целевые значения HbA1c, достижение которых позволяет существенно снизить риск возникновения осложнений СД. Практически все национальные диабетические ассоциации, ВОЗ и ВФД (Всемирная федерация диабета – International Diabetes Federation, IDF) рекомендуют поддерживать «строгую» компенсацию углеводного обмена, при которой уровень гликогемоглобина (HbA1c) в крови составлял бы менее 7% и даже ниже 6,5% (при норме 6,0%).
В рекомендациях, разработанных АДА (Американская диабетическая ассоциация – American Diabetes Association, ADA) совместно с ВФД в 2006 году, подчеркивается, что показатель HbA1c более 7,0% следует рассматривать как недостаточную компенсацию углеводного обмена у больного СД 2 типа и как необходимость принятия конкретных действий по улучшению лечения для снижения этого показателя. Такие «жесткие» рекомендации по контролю углеводного обмена являются следствием проспективного исследования UKPDS (United Kingdom Prospective Diabetic Study). Результаты этого исследования, проводившегося в период с 1976 по 1997 гг. в 23 центрах Великобритании с включением 5102 пациентов с впервые выявленным СД 2 типа, четко свидетельствуют о том, что при уменьшении уровня HbA1c на 1% общая летальность при СД 2 типа снижается на 21%, риск развития микрососудистых осложнений – на 37%, а инфаркта миокарда – на 14% (3).
За время прошедшее с 1976 года, когда впервые было предложено использовать определение содержания гликогемоглобина для контроля уровня глюкозы у больных сахарным диабетом (4), было разработано много лабораторных методов, позволяющих определять HbA1c. Разнообразие методов предполагает возникновение дискуссий по поводу преимуществ или недостатков того или иного метода. Так как в настоящее время отсутствует единая международная процедура стандартизации, в соответствии с которой все существующие методы могли быть нормированы, регулярно предпринимаются попытки достижения такого соглашения. Чтобы выработать единый стандарт и преодолеть проблемы связанные с его принятием, Международная федерация клинической химии (IFCC) создала в 1993 году «рабочую группу» по стандартизации определения HbA1c. Эта группа координирует действия национальных групп и изготовителей приборов и тестов для определения HbA1c. В июле 2001 года международным сообществом были утверждены референсные методы определения HbA1c. Таковыми стали высокоэффективная жидкостная хроматография (ВЭЖХ) и капиллярный электрофорез (HPLC/capillary electrophoresis, HPLC-CE) (5).
В результате дальнейших усилий, предпринятых IFCC, был разработан первичный референсный материал высокоочищенного гликогемоглобина и проведены сравнительные исследования относительно других методов и стандартов, в том числе NGSP (Национальная программа по стандартизации гликогемоглобина, США). Установленная между двумя системами измерений взаимосвязь была проверена многочисленными исследованиями и утверждена документально.
Взаимосвязь данных показателей определяется следующим соотношением:
NGSP = (0.915 * IFCC) + 2.15 Так как абсолютные значения NGSP больше значений IFCC всего на 1,5–2 единицы, то одновременное существование двух близких систем оценки вызывает трудности и может явиться предпосылкой к ошибочному истолкованию результатов клиницистами и пациентами. Поэтому следующим этапом работы по стандартизации исследования гликированного гемоглобина стала выработка в октябре 2007 года совместного решения IFCC, с одной стороны, и АДА / ВФД / ЕАИД (Европейская ассоциация по изучению диабета – European Association for the Study of Diabetes, EASD), с другой, о единицах измерения и соотношении между ними. Было принято решение, что при использовании оборудования, стандартизованного в соответствии с требованиями IFCC или диагностических систем, аттестованных с использованием соответствующего референтного материала, содержание гликогемоглобина должно выражаться в единицах IFCC (ммоль HbA1c/моль Hb), и в производных единицах NGSP (%). Кроме того, ожидается, что по окончании широкомасштабного исследования «Average Plasma Glucose Study» должна быть установлена взаимосвязь между концентрацией HbA1c и средним содержанием глюкозы в крови, в результате чего появится новый показатель “А1С-derived average glucose” (ADAG).
Следует отметить, что на сегодняшний день большинство производителей приборов и наборов для определения HbA1c имеют сертификат NGSP. Однако ряд производителей ориентируются на требования IFCC. В нашей стране принято ориентироваться на значения NGSP.
Принимая во внимание строгие требования к определению граничных значений содержания гликогемоглобина у больных СД, были разработаны современные требования к методу измерения гликогемоглобина: - метод должен быть стандартизирован (сертификат NGSP, IFCC или European Reference Laboratory for Glycohemoglobin, ERL);
- межсерийный Сv не должен быть выше 4%;
- исследование должно быть непродолжительным;
- процедура анализа должна быть простой.
За последнее десятилетие для определения содержания гликогемоглобина были разработаны и нашли практическое применение ряд аналитических методов, такие как катионообменная хроматография высокого и низкого давления, ионообменная хроматография, аффинная хроматография; электрофоретический метод и электрофокусирование; колориметрический метод с использованием тиобарбитуровой кислоты и иммунохимические методы, в частности, иммунотурбидиметрия. Высокоэффективная жидкостная хроматография (ВЭЖХ)
Признана референсным методом. При помощи ВЭЖХ определяются НbА1с, НbА1а, НbА1в. Содержание отдельной фракции пропорционально площади соответствующего пика. Расчет проводится анализатором автоматически, результат выдается в процентах, так как пики калибраторов уже имеют процентное выражение. Процедура определения предусматривает удаление Шиффовых оснований. Исключена интерференция с гемоглобинами (F, S, С, D, Е) и карбогемоглобинами. Калибровка осуществляется по двум стандартам гликогемоглобина. Недостатком данного метода является необходимость приобретения специализированного дорогостоящего оборудования. Ионообменная хроматография низкого давления
Данный метод получил широкое распространение в лабораториях благодаря оптимальному сочетанию аналитических характеристик и потребительских качеств. Так, например, в анализаторе DS-5 Glycomat, производства компании Drew Scientific (Великобритания) избирательно определяется процентное содержание НbА1с в присутствии гемоглобинов А1а, А1b или F, определяется наличие в пробе гемоглобинов C и S. Результаты имеют хорошую корреляцию с референсным методом ВЭЖХ. Процесс пробоподготовки стандартизирован и не требует много времени. Процедура измерения занимает 5 минут. Анализатор можно использовать как для выполнения единичных измерений, так и серии проб.
Ионообменная хроматография (ручная процедура)
Цельная кровь смешивается с лизирующим раствором, содержащим детергент и борат-ионы в высокой концентрации. В процессе гемолиза достигается устранение лабильных Шиффовых оснований. Затем гемолизат в течение 5 минут смешивается со слабосвязанной катион-обменной смолой. За это время HbA0 связывается со смолой. Для отделения смолы от супернатанта, в котором содержится HbA1, используется специальный сепаратор. Процентное содержание гликогемоглобина от общего содержания гемоглобина в крови рассчитывается после измерения оптической плотности гликогемоглобиновой фракции и общего гемоглобина при длине волны 415 нм или 405 нм относительно стандартного раствора гликогемоглобина. В качестве примера использования данного метода в диагностических тест-системах можно привести набор Glycohemoglobin HbA1 производства компании Human GmbH (ФРГ), который содержит все необходимое для выполнения 20 или 100 тестов. Любая лаборатория, в которой имеется полуавтоматический биохимический анализатор или фотометр, с помощью этого набора может определять содержание гликогемоглобина в пробах пациентов.
Портативные анализаторы гликогемоглобина
В последнее время получило развитие направление по созданию компактных систем для определения важнейших биохимических показателей «у постели больного» (Point оf Сare Testing, POCT). Для гликогемоглобина также были разработаны подобные системы, использующие одноразовые картриджи: NycoCard (Axis-Shield), DC2000+ (Bayer), A1cNow (Metrika), TRIstat (Trinity Biotech) и др. Достоинствами этих систем являются простота использования и скорость получения результатов анализа. Однако высокие стоимость теста и вариабельность результатов существенно ограничивают их применение. Иммунотурбидиметрия
По данным CAP (College of American Pathologists) в 1995 году при исследовании содержания гликогемоглобина 54% лабораторий использовали метод аффинной хроматографии, тогда как в 2007 году основными методами стали иммунотурбидиметрия (65%) и ионообменная хроматография (32% лабораторий). Данные представлены ниже на диаграмме (7). 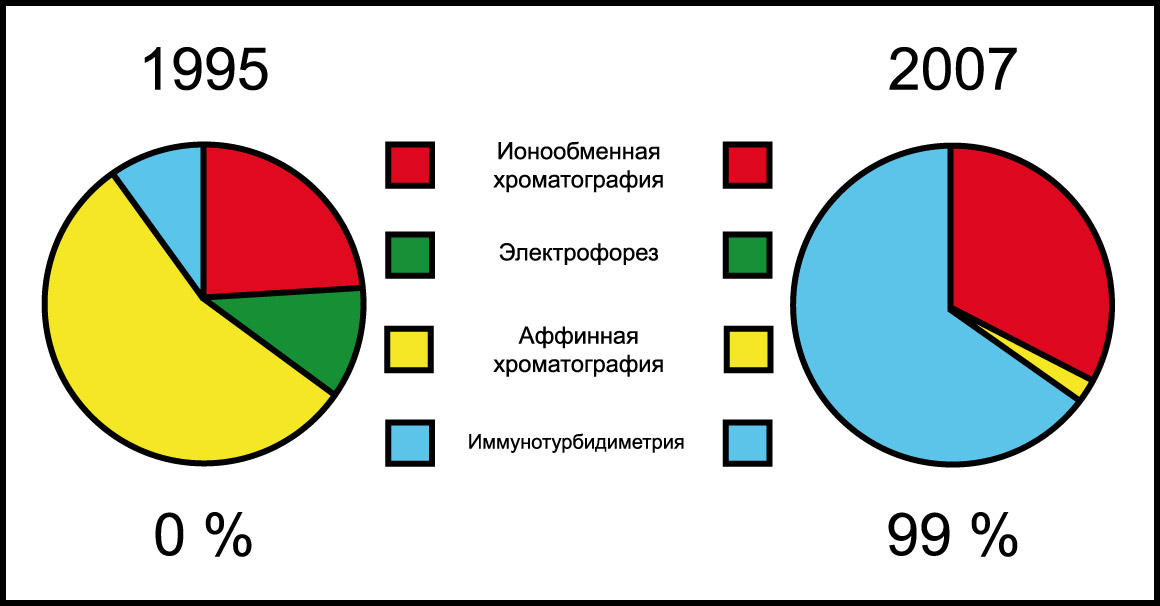
Популярность иммунотурбидиметрического метода объясняется тем, что он позволяет напрямую (без предварительного определения негликированной фракции) определять процентное содержания НbА1с в цельной крови. Этот двустадийный метод основан на конкурентном связывании общего гемоглобина и HbА1с со специфическими латексными частицами пропорционально их концентрации. Затем происходит связывание гликогемоглобина и специфических мышиных моноклональных антител, которые, в свою очередь, взаимодействуют с козьими поликлональными антителами к IgG мыши, вызывая агглютинацию латексных частиц. Степень агглютинации зависит от количества связанного с латексными частицами гликогемоглобина HbА1с. Увеличение мутности смеси измеряется фотометрически. Процентное содержание HbА1с в пробах вычисляется по калибровочной зависимости, установленной при измерении калибраторов (6).
Ниже в таблицах представлены результаты оценки внутрисерийной и межсерийной вариации, полученные при измерении содержания гликогемоглобина в контрольных растворах трех уровней с использованием набора HbA1с% Liquidirect производства компании Human GmbH (ФРГ). Внутрисерийная вариация (n=20) | Контроль | Среднее HbA1c,% | SD HbA1c,% | Cv, % | | Низкий | 4.76 | 0.060 | 1.26 | | Средний | 7.29 | 0.075 | 1.04 | | Высокий | 10.9 | 0.160 | 1.46 |
Межсерийная вариация (n=20) | Контроль | Среднее HbA1c,% | SD HbA1c,% | Cv, % | | Низкий | 4.72 | 0.062 | 1.30 | | Средний | 7.36 | 0.083 | 1.12 | | Высокий | 11.1 | 0.167 | 1.51 |
В сравнении с референсным методом ВЭЖХ (Tosoh A1c 2.2 Plus), а также относительно коммерческого набора для иммунотурбидиметрического определения гликогемоглобина (Roche TinaQuant HbA1c II) набор HbA1с% Liquidirect показал хорошую корреляцию результатов при измерении проб пациентов, как с нормальным, так и с высоким содержанием HbА1с. Результаты представлены ниже в таблице и на диаграмме. | Параметр | ВЭЖХ //Human HbA1с% Liquidirect | TinaQuant HbA1c II //Human HbA1с% Liquidirect | | Число измерений, n | 40 | 60 | | Коэфф. корреляции, r2 | 0,993 | 0,942 | | Уравнение регрессии | 0,95 х + 0,055 | 1,074х – 0,366 | | Xср | 7,33% | 6,28% | | Yср | 7,02% | 6,38% |
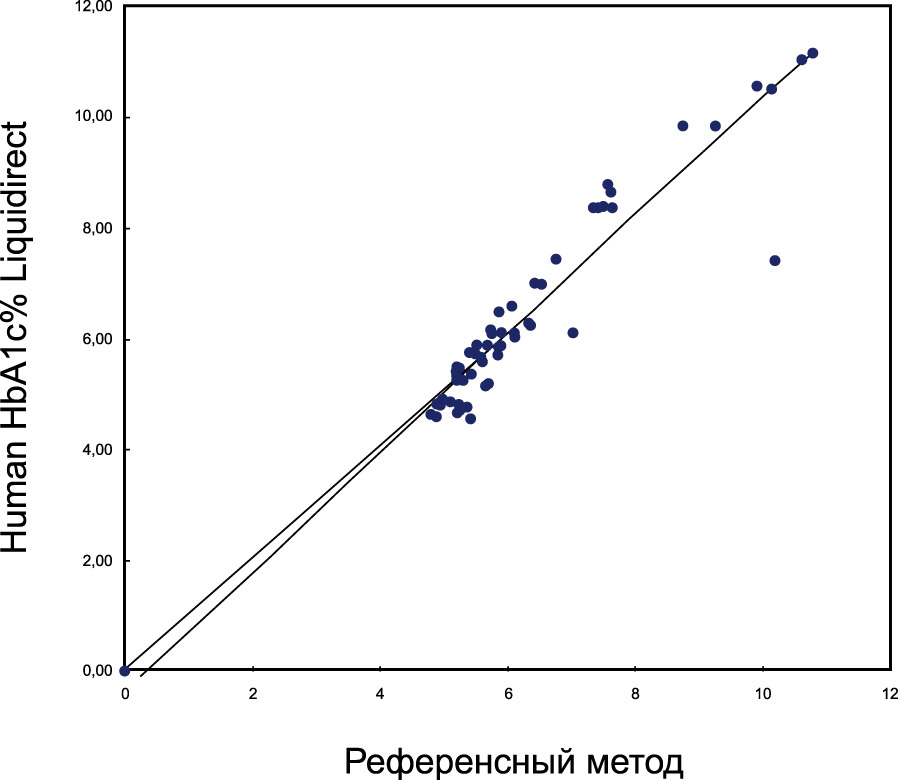
Наряду с хорошими аналитическими характеристиками преимуществом турбидиметрического метода является: возможность выполнения измерений на автоматических и полуавтоматических биохимических анализаторах, которые, как правило, уже имеются в лабораториях; представление результата в виде процентного отношения; небольшое количество образца (20 мкл); короткое время исследования (10 минут). При использовании современных биохимических автоанализаторов, для которых минимальный объем реакционной смеси составляет 150–200 мкл, стоимость одного анализа почти в 1.5 раза меньше, чем при использовании специализированных анализаторов.
Очевидно, что расходы на регулярный контроль гликемии выше, чем на приобретение сахароснижающих препаратов. Однако проведение постоянного мониторинга состояния углеводного обмена у больных СД является необходимым условием для профилактики сосудистых осложнений, отсрочки их прогрессирования, сохранения работоспособности больных, поддержания нормального качества их жизни и снижения частоты инвалидизации. Это, в свою очередь, приводит к уменьшению общих затрат на медицинское обслуживание больных СД. Последние рекомендации ВОЗ, ВФД и ЕАИД еще раз подчеркивают необходимость своевременной диагностики данного заболевания, а также проведения постоянного качественного контроля терапии и профилактики сосудистых осложнений СД, что возможно лишь при использовании современных методов и диагностической аппаратуры. Список литературы.
1. Федеральная целевая программа “Сахарный диабет”. Методические рекомендации. М., 2002.
2. American Diabetes Association: Clinical Practice Recommendation (Position Statement). Diabetes Care, 24 (Suppl. 1): S33-S55, 2001.
3. Association of glycaemia with macro vascular complications of type 2 diabetes (UKPDS 35): prospective observational study. BMJ, 321, p. 405-412, 2000.
4. R.J. Koenig, et.al. Hemoglobin A1c as an indicator of the degree of glucose intolerance in diabetes. Diabetes, N 25 (3), p. 230-232, 1976.
5. Jeppsson J.-O. et. al., Approved IFCC Reference Method for the Measurement of HbA1c in Human Blood. Clin. Chem. Lab. Med., 40, p. 78-89, 2002.
6. Chang J. et. al., Evaluation and interference study of hemoglobin A1c measured by turbidimetric inhibition immunoassay. Am. J. Clin. Pathol., 109, p. 274-278, 1998.
7. Molinaro R. J. Targeting HbA1c: standardization and clinical laboratory measurement. Med. Lab. Obs., 1, p. 10-19, 2008. Андрей Владимирович Багаев канд. мед. наук, ведущий специалист по продукции ЗАО «Аналитика» Июнь, 2009 (материал подготовлен для журнала “Клинико-лабораторный консилиум” № 3-2009) |


