Инфаркт миокарда при анемии
Анемии (малокровие) — состояние, характеризующееся уменьшением количества Hb в единице объёма крови, часто при одновременном уменьшении количества эритроцитов. Это самый распространённый гематологический синдром. По данным ВОЗ, во всём мире около 2 млрд человек страдают анемией, и приблизительно в 50% случаев она связана с дефицитом железа.
Анемия – самостоятельное заболевание системы крови, однако она может быть симптомом лейкоза, тромбоцитопении, геморрагических состояний и т.д. Кроме того, анемия может возникать или усугубляться при миелосупрессивной химиотерапии или радиационном облучении.
При анемии в основе патологии сердечно-сосудистой системы лежат глубокие биологические изменения в миокарде, обусловленные тканевой и гемической гипоксией. Гипоксия развивается в результате снижения кислородной ёмкости крови, а также при нарушении регуляции NO-зависимого расширения сосудов вследствие патологии переноса эритроцитами оксида азота. В патогенезе железодефицитной анемии имеет значение нарушение обмена железа — одного из основных микроэлементов, необходимых для нормальной жизнедеятельности человеческого организма. Железо входит в состав Нb, миоглобина, цитохромов, каталазы, пероксидазы и других ферментов, участвует в тканевом дыхании, обменных процессах, синтезе гормонов и т.д.
При острой анемии вследствие быстрого снижения Нb и циркулирующих эритроцитов (резкая и обильная кровопотеря, острый гемолиз) уменьшается доставка кислорода к тканям. Наибольшая относительная способность переноса кислорода сохранена при гематокрите 30-33%. По мере уменьшения концентрации Нb и содержания кислорода, обеспечение общей доставки кислорода происходит за счёт увеличения сердечного выброса. Компенсаторно возникает тахикардия, укорачивается диастола, уменьшается системное сосудистое сопротивление, снижается АД. В норме при здоровом сердце и большом резерве миокардиального кровотока перечисленные реакции компенсируют острую анемию без развития ишемии миокарда. Этому способствует возникающее в ответ на острую гипоксию увеличение уровня эритропоэтина, который оказывает кардиопротективное действие. В то же время при поражении коронарных артерий устойчивость миокарда к низкому уровню Нb значительно снижена. Это приводит к ишемии, а ишемизированный или гипертрофированный миокард более чувствителен, чем неизменённый, даже к незначительному снижению уровня Нb, в результате нарушение функций сердца может иметь серьёзные последствия.
При хронической анемии выявляют и другие компенсаторные реакции: увеличение сердечного выброса и преднагрузки, уменьшение постнагрузки, увеличение хронотропных и инотропных эффектов. Однако при длительном существовании даже умеренной анемии существующая при этом гипоксия приводит к более глубоким изменениям, проявляющимся в нарушении структуры и функции биологических мембран, в том числе мембран кардиомиоцитов. В миокарде происходят диффузио-дистрофические и структурные изменения (жировая дегенерация), появляются субэидокардиальные зоны ишемии, вплоть до мелкоочаговых некрозов, расширяются полости, что в конечном итоге приводит к нарушению диастолической и систолической функций сердца.
Диастолическая дисфункция ЛЖ и ПЖ характерна для всех видов анемии (особенно для гемолитической и серповидноклеточной). Причиной серповидноклеточной анемии считают окклюзию сосудов серповидными эритроцитами, приводящую к ишемии миокарда, при рецидивирующих гемолитических кризах развивающийся при этом фиброз миокарда. При некоторых гемолитических анемиях возможны микротромбозы коронарных артерий с развитием ИМ.
Определено, что длительное увеличение сердечного выброса при хронической анемии может привести к ремоделированию центральных артерий эластического типа (аорта и сонные артерии), увеличению массы миокарда ЛЖ.
Несмотря на разнообразную этиологию (постгеморрагичекие, гемолитические, а пластические, железодефицитные, В12-дефицитные и др.), анемии имеют общие симптомы: слабость, повышенную утомляемость, бледность кожных покровов и слизистых, боли в области сердца, сердцебиение, одышку и т.д. Длительное течение анемии приводит к развитию так называемого «анемического сердца», которое проявляется указанными выше жалобами, расширением границ относительной сердечной тупости влево, снижением амплитуды зубцов ЭКГ, низкой толерантности к физической нагрузке и депрессией сегмента ST во время проведения стресс-тестов.
В исследованиях последних лет выявлено значение анемии как независимого фактора риска развития ССЗ. В работах ARIC было показано, что снижение Нb на 1 г/дл связано с увеличением риска смерти на 14% и увеличением нарушений функций сердца на 28%. Анемию и высокий уровень гематокрита рассматривают как независимый предиктор острого коронарного синдрома и ИМ и прогностически неблагоприятный признак в отношении «поздней» госпитальной смерти и фатального кардиогенного шока. Снижение Нb коррелирует с выраженностью клинических проявлений ИБС, нарушениями ритма. При остром ИМ низкий уровень Нb может быть экстракардиальным фактором, усиливающим ишемию и провоцирующим систолическую дисфункцию сердца.
Анемия любой этиологии связана с возникновением и развитием застойной сердечной недостаточности. В ряде крупных многоцентровых исследований статистически доказана высокая частота выявления анемии у больных с ХСН, причём наличие анемии связано с худшим клиническим статусом, более тяжёлой систолической и диастолической дисфункцией, высоким уровнем натрийуретического пептида, быстрым ухудшением функции почек, низким качеством жизни и повышенными медицинскими затратами. Фремингемское исследование показало, что анемия — независимый фактор риска смерти больных с застойной сердечной недостаточностью. При снижении гематокрита на каждый 1% риск смерти больных с сердечной недостаточностью увеличивается на 6%.
Своевременное лечение по стандартным схемам, соответствующим опредёленному типу анемии (например, препараты железа назначают при железодефицитной анемии), может привести к уменьшению и устранению описанных изменений, в том числе ишемии, гипертрофии, дилатации и диастолической дисфункции ЛЖ, увеличению фракции выброса, ударного объёма, сердечного выброса и др.
Особое место среди анемий занимает талассемия — наследуемая по рецессивному типу гемолитическая анемия, характеризующаяся нарушением синтеза глобина (белка, входящего в состав Нb). Для неё характерно наличие мишеневидных эритроцитов, гипохромная анемия при повышенном содержании железа в органах, в том числе в сердце, с развитием гемосидероза. При накоплении железа в сердце могут возникать нарушения ритма, кардиомегалия, сердечная недостаточность. Описаны случаи экссудативного перикардита при данной патологии.
Наряду с яркими проявлениями талассемии существуют трудно диагностируемые, маломанифестные формы. В связи с этим следует подчеркнуть опасность применения препаратов железа у данной категории больных и необходимость обязательного исследования показателей обмена железа при выявлении анемии. Для лечения применяют препараты, выводящие избыток железа из организма, трансфузии эритроцитарных препаратов крови.
Поражение сердца при тромбоцитопениях и нарушениях свёртываемости крови.
Тромбоцитопеническая пурпура – группа заболеваний, для которых характерно наличие геморрагического синдрома, развивающегося в результате снижения числа тромбоцитов в периферической крови ниже уровня 155×10х9 г/л (тромбоцитопении).
Идиоматическая тромбоцитопеническая пурпура (болезнь Верльгофа) протекает в острой или хронической форме, проявляясь кровоизлияниями в кожу, слизистые оболочки, а также различными кровотечениями (в том числе в миокард, серозные оболочки, сетчатку и другие отделы глаза). Для болезни Мошковича характерно сочетание тромбоцитопении с геморрагическим синдромом и гемолитической анемией. Развитие симптоматических тромбоцитопений отмечают при других заболеваниях (злокачественные новообразования, лучевая болезнь, гепатит, инфекционные болезни), а также при использовании ряда лекарств. У больных ССЗ существует риск тромбоцитопении, вызванной приёмом клопидогрела, особенно при использовании его в высоких дозах (однократная доза 600 мг), хинидина, НПВС и ряда других средств.
Поражение сердца (микрососудистые тромбы и интрамиокардиальные кровоизлияния) при тромбоцитопенической пурпуре часто выявляют при морфологическом исследовании миокарда. Гистологическое исследование позволяет выявить фокальный миокардит, ассоциированный с тромбоцитарными микротромбами, зоны некроза, нарушения в проводящей системе области синоатриального и атриовентрикулярного узла, ножек пучка Гиса.
Частыми клиническими проявлениями указанных нарушений считают нарушения ритма, различные по характеру и тяжести. В ряде случаев они имеют транзиторный характер. Около 3-8% больных с тромбоцитопенической пурпурой жалуются на боли в области сердца по типу стенокардии. Редко возникает застойная сердечная недостаточность.
Опасными для жизни считают кровоизлияния в сердце, головной мозг. Существуют сообщения о внезапной смерти больных с тромбоцитопенической пурпурой, вызванной очаговыми кровоизлияниями в миокард (в том числе в зонах проводящей системы сердца), приводящими к фатальным нарушениям ритма.
Описаны возможности успешной коррекции и восстановления функции сердца при лечении тромбоцитопенической пурпуры, в частности после применения плазмафереза.
У ряда больных, получавших НФГ, развивается гепарин-индуцированная тромбоцитопения. Риск её возникновения составляет 1-3%. Состояние обычно развивается у больных, перенёсших операцию в условиях искусственного кровообращения. Выделяют два типа гепарин-индуцированной тромбоцитопении. Тромбоцитопения I типа – результат прямой активации гепарином тромбоцитов и их повышенная агглютинация — доброкачественная, без риска тромбозов, существует в течение первых 5-10 дней после операции и склонна к саморазрешению без лечебных мероприятий. Тромбоцитопения II типа – иммунная, вследствие образования антител к гепарину, характеризуется тяжёлым, иногда быстропрогрессирующим течением. При несвоевременной диагностике может возникнуть кровотечение, артериальные и венозные тромбозы, тромбоэмболические осложнения. Состояние требует лабораторного контроля (определяют количество тромбоцитов, степень их агрегации). При несвоевременно установленном диагнозе часто возникает необходимость интенсивной терапии. Прогноз может быть неблагоприятным, особенно у продолжающих получать гепарин после операции, в том числе после кардиохирургического вмешательства (например, протезирование клапанов сердца).
Диагноз гепарин-индуцированной тромбоцитопении следует рассматривать у всех больных с тромбоцитопенией, получавших гепарин в течение последних 14 дней, особенно при наличии признаков тромбоза. Лечение проводят прямыми ингибиторами тромбина с последующим переходом на пероральный прием варфарина, изучают возможности применения фондапаринукса — непрямого ингибитора фактора Ха.
Гемофилия — болезнь системы гемостаза, наследующаяся сцепленно с полом, характеризуется недостаточностью VIII или IX факторов свертывания крови. Болезнь Виллебранда сходна с классической гемофилией (атромбоцитопеническая пурпура) — наследственная болезнь системы гемостаза, характеризуемая количественными или качественными нарушениями синтеза фактора Виллебранда (фактор VIII циркулирует совместно с фактором Виллебранда, который его стабилизирует).
Для данных заболеваний характерен клинически выраженный геморрагический синдром и связанная с ним анемия, проявляющаяся соответствующими изменениями сердечной деятельности. У некоторых пациентов болезнь Виллебранда сочетается с признаками мезенхимальной дисплазии, выражающейся в числе прочего пролабированием створок клапанов сердца, артериовенозными шунтами.
Предполагают, что существует связь между фактором Виллебранда и развитием атеросклероза, однако данная теория не получила абсолютного подтверждения.
Необходимо отметить, что для больных с гемофилией состояние сердечной деятельности — важный фактор, определяющий режимы терапии, в частности объёмы переливаемой плазмы. Так, при необходимости переливания свежезамороженной плазмы в ситуации нормальной функции сердца скорость трансфузии может быть около 18 мл/кг в течение часа, в то время как при сердечной недостаточности объёмы переливания должны быть скорректированы в меньшую сторону.
Полицитемия истинная (эритремия, болезнь Вакеза) — болезнь, обусловленная гиперплазией костного мозга (преимущественно эритроцитарного ростка), характерен эритроцитоз, лейкоцитоз, тромбоцитоз, увеличение массы циркулирующей крови и количества Нb. Болезнь проявляется резким покраснением кожных покровов, кожным зудом, склонностью к тромбозам, спленомегалией.
В связи с увеличением массы эритроцитов в кровяном русле для полицитемии характерно повышение свёртывания крови, плеторический синдром, что обусловливает особенности клинических проявлений осложнения заболевания. Для большинства больных характерна АГ. Нарушение микроциркуляции в миокарде вызывает боли в области сердца. В случае тромбоза развивается острый коронарный синдром, ИМ.
Лечение больных с полицитемией при уровне тромбоцитов, превышающем норму, предполагает назначение антиагрегантов: ацетилсалициловая кислота, тиклопидин, клопидогрель в общетерапевтических дозах.
Помимо истинной полицитемии, эритроцитоз может развиться как компенсаторная реакция (так называемый вторичный эритроцитоз) в случаях снижения насыщения крови кислородом. Это характерно для жителей высокогорья (например, живущих в районах Тянь-Шаня, Гималаев, Анд и др.), больных с хроническими неспецифическими заболеваниями легких, лёгочным сердцем. Клинические проявления сходны с истинной полицитемией. Отмечают худший прогноз при ИМ на фоне эритроцитоза в случае лёгочной гипертензии в связи развитием более тяжёлых гемодинамических осложнений. Эритроцитоз повышает риск повторного тромбообразования в постинфарктном периоде, предрасполагает к прогрессированию сердечной недостаточности.
В лечении данной категории больных делают акцент на антиагреганты.
Горохова С.Г., Атаманова М.А.
Поражение сердца при заболеваниях крови
Опубликовал Константин Моканов
Ишемическая болезнь сердца (ИБС) – патология, в основе которой лежит поражение миокарда, обусловленное недостаточным его кровоснабжением. Атеросклеротическое сужение коронарных артерий является патогенетической основой ИБС, но для развития ишемии миокарда требуется еще дополнительный фактор, ведущий к нарушению баланса пропускной способности коронарных артерий и потребности миокарда в кислороде.
Чаще всего это увеличение работы ЛЖ (тахикардия, повышение систолического АД) или недостаточность коронарного кровотока (тромбообразование в венечных артериях, спазм). Реже как факторы, способствующие развитию или прогрессированию ИБС, рассматриваются снижение перфузионного давления (ДАД) или нарушение кислород-транспортной функции крови и т. д.
Для наглядности приводим выписки из историй болезни пациентов, у которых эти факторы играли роль «запускающего механизма». Мнение о том, что штаны принято носить только мужчинам, а женщины должны быть утонченные и элегантные, отдавая предпочтение юбкам и платьям, в нынешнее время абсолютно не актуально.
Клинический случай 1
Больной Ш., 84 года, был госпитализирован в мае 2013 г. с жалобами на давящие боли за грудиной при небольшой физической нагрузке и в покое.
Более 30 лет регистрируются высокие цифры АД (до 200/120 мм рт. ст.), сахарный диабет 2-го типа.
4 мес. назад перенес острый инфаркт миокарда без зубца Q боковой стенки левого желудочка. При коронарографии: передняя межжелудочковая ветвь (ПМЖВ) левой коронарной артерии (ЛКА) стенозирована в проксимальной трети на 50%, в дистальной трети — последовательные стенозы 30–50%; огибающая артерия (ОА) стенозирована в средней трети на 70%, правая коронарная артерия (ПКА) субокклюзирована в передней трети, окклюзирована в средней трети, дистальная часть слабо контрастируется по меж- и интраартериальным анастомозам. Выполнено стентирование средней трети ОА. Реканализацию ПКА выполнить не удалось.
Обращено внимание на наличие гипохромной анемии легкой степени (гемоглобин -106 г/л). Проведенное обследование возможного источника кровотечения не выявило. Выписан в удовлетворительном состоянии с рекомендацией приема ацетилсалициловой кислоты и клопидогрела, сахароснижающей терапии, препаратов железа.
Дома рекомендованные препараты принимал нерегулярно, врача не посещал.

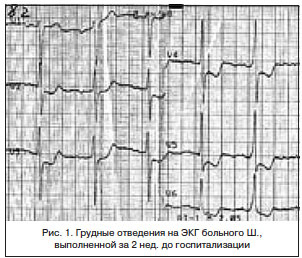
Около 2 мес. назад отметил нарастание слабости. Стали беспокоить редкие приступы загрудинных болей. На ЭКГ от 10.05.13 г.: на фоне синусового ритма с ЧСС 75 уд./мин — выраженная депрессия сегмента ST в отведениях V2-6 (рис. 1). От предложенной госпитализации отказался.
Последние 2 нед. участились приступы загрудинных болей давящего характера, они стали возникать при минимальной физической нагрузке и в покое, сублингвальный прием нитроглицерина оказывал кратковременное действие, появилось чувство нехватки воздуха. Обратился в поликлинику, откуда был доставлен в ЦКБ с диагнозом «ИБС, прогрессирующая стенокардия».
При поступлении: кожные покровы бледные. Отеков нет. ЧД — 18 в 1 мин. Дыхание жесткое. Пульс — 72, АД — 140/70 мм рт. ст. на обеих руках. Систолический шум в точке Боткина и на верхушке, проводящийся в левую подмышечную область.
ЭКГ при поступлении (рис. 2): синусовый ритм с ЧСС 59 уд./мин, замедление атриовентрикулярной проводимости (PQ — 0,24 с). Замедление проводимости по левому предсердию и желудочку. Гипертрофия левого желудочка. Нарушение реполяризации в V2-5.
ЭхоКГ: гипертрофия миокарда ЛЖ (ММЛЖ — 240 г). Утолщение межжелудочковой перегородки (МЖП), более выраженное в базальной части (1,6–1,8 см), без признаков обструкции выходного отдела ЛЖ. Толщина ЗСЛЖ — 1,5 см. Сократительная способность миокарда ЛЖ удовлетворительная (ФВ по Тейхольцу — 63%), КСР — 3,6 см, КДР — 5,5 см, ЛП — 5,1 см. Зон нарушенной кинетики не выявлено. Изменение диастолической функции ЛЖ по первому типу.
В экстренном порядке выполнена коронароангиография (КАГ) (рис. 3): ствол ЛКА не изменен. ПМЖВ стенозирована на границе передней и средней третей на 50%, на протяжении дистальной трети — последовательные стенозы 30–60%. 1ДВ — анатомически некрупная, стенозирована в устье на 80%, окклюзирована в средней трети, дистальная часть слабо контрастируется по интерартериальным коллатералям. ВТК стенозирована в устье до 50%. ОВ анатомически крупная, проходима на всем протяжении, ранее имплантированные стенты — без стенотических изменений. ПКА субокклюзирована в передней трети, окклюзирована в средней трети, дистальная часть слабо контрастируется по меж- и интраартериальным анастомозам. Сбалансированный тип коронарного кровоснабжения.
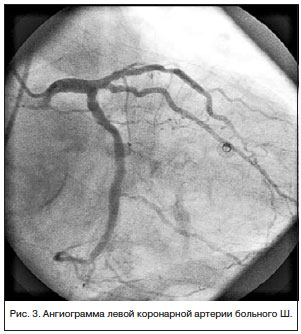
Учитывая отсутствие динамики стенозов-КА по сравнению с КАГ от января 2013 г., чрескожное коронарное вмешательство не проводилось.
В анализе крови: гемоглобин — 61 г/л, эритроциты — 2,30×10*12, ЦП — 0,8, гематокрит — 18,5, лейкоциты — 7,7×10*9.
Кардиоспецифические ферменты (КФК МВ, тропонин Т) находились в пределах референсных значений.
В анализе мочи: удельный вес — 1020, белок — 0,15, лейкоциты — 0–5 в поле зрения, эритроциты — 100–150 в поле зрения.
Дополнительный целенаправленный расспрос позволил выяснить, что на протяжении последних 4 мес. неоднократно были эпизоды выделения темно-красной мочи, иногда длившиеся по несколько дней (макрогематурия?).
Убедительных данных, говорящих об остром очаговом поражении миокарда, на момент госпитализации не получено. Учитывая наличие анемии тяжелой степени, произведена трансфузия отмытых эритроцитов (1150 мл за 2 сут) с положительным эффектом: уровень гемоглобина повысился до 100 г/л, число эритроцитов — до 3,59×10*12, гематокрит — до 29,4.
На ЭКГ через 1 сут после последней гемотранфузии отмечается нормализация конечной части желудочковых комплексов в грудных отведениях (в V4 — зубец Т слабоотрицательный).
Самочувствие пациента значительно улучшилось: в течение последующих 3 сут при расширении двигательного режима до уровня физических нагрузок, соответствующих 3 функциональному классу, боли в грудной клетке не возникали, выраженность одышки существенно уменьшилась, объем нагрузок ограничивался главным образом мышечной утомляемостью. Эпизоды макрогематурии не повторялись. В удовлетворительном состоянии больной переведен для дообследования в урологическое отделение.
Клинический случай 2
Больной К., 50 лет, госпитализирован в стационар в декабре 2014 г. с клиникой прогрессирования стенокардии напряжения, одышки, возникающих при минимальной физической нагрузке, в покое, с нарастанием общей слабости в течение последнего месяца.
В анамнезе: АГ с максимально известными значениями АД 200/100 мм рт. ст. давностью более 15 лет; регулярно принимает антигипертензивные препараты, однако контроль АД нерегулярный. В 2002 г. перенес ОИМ, в этом же году выполнено аортокоронарное шунтирование (АКШ) ПМЖА, ПКА, ОА. В 2009 г. развилась клиника прогрессирующей стенокардии, в связи с чем выполнено стентирование шунта к ОВ ЛКА. В мае 2014 г. — повторный ОИМ задней стенки левого желудочка, проводился системный тромболизис, чрескожное коронарное вмешательство с реканализацией и стентированием АКШ к ОА. После выписки и до настоящей госпитализации — состояние стабильное.
Сопутствующие заболевания: сахарный диабет 2-го типа, мочекаменная болезнь, хронический геморрой, железодефицитная анемия легкой степени регистрируется с 2009 г. (препараты железа не принимал).
При поступлении: кожные покровы бледные, сухие. ЧД — 18 уд./мин. Дыхание жесткое, небольшое количество свистящих хрипов на выдохе. Тоны сердца глухие. ЧСС -76 уд./мин. АД — 150/90 мм рт. ст. на обеих руках.
ЭКГ зарегистрирована на фоне болевого приступа (рис. 4): ритм синусовый, ЧСС — 88 уд./мин, смещение сегмента ST вверх от изолинии в отведениях III, aVF, V1. В отведениях I и aVL смещение сегмента ST книзу от изолинии. Зубец Q длительностью 0,04 с во II, III, aVF отведениях.
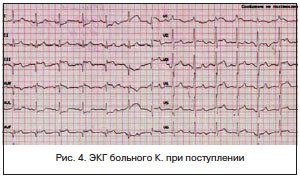
ЭхоКГ: гипертрофия миокарда ЛЖ (ММЛЖ — 213 г, МЖП — 1,5 см, ЗСЛЖ — 1,2 см). Дилатация левого предсердия (5,3×6,1 см). Нарушение диастолической функции левого желудочка по первому типу. Гипокинез диафрагмального, заднебазального и заднебоковых сегментов. ФВ — 54% по Тейхольцу.
В общем анализе крови: гемоглобин — 70 г/л, эритроциты — 4,29×10*12, гематокрит -23,5, ЦП — 0,48, гипохромия, анизоцитоз, пойкилоцитоз (овалоциты, мишеневидные эритроциты), лейкоциты — 5,9×10*9. Сывороточное железо — 1,9.
Кардиоспецифические ферменты (КФК МВ, тропонин Т) находились в пределах референсных значений.
Таким образом, убедительных данных, свидетельствующих об остром очаговом поражении миокарда, на момент госпитализации не получено. Высказано предположение, что причиной прогрессирования стенокардии являлась тяжелая железодефицитная анемия, вероятнее всего, постгеморрагическая. Проведена трансфузия эритроцитной взвеси 630 мл за первые сутки, начато парентеральное введение препаратов железа.
Трансфузионную терапию перенес хорошо. Ангинозные боли не рецидивировали. На ЭКГ, зарегистрированной после гемотрансфузии (рис. 5): ЧСС — 62 уд./мин. Сегмент ST вернулся к изолинии.
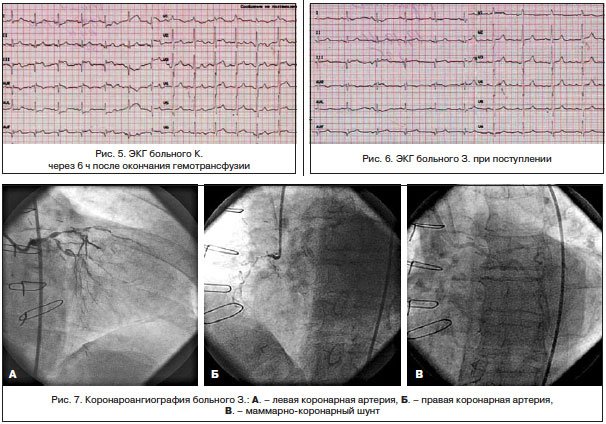
В анализе крови спустя 1 сут: уровень гемоглобина возрос до 105 г/л, число эритроцитов — до 5,71×10*12, гематокрит — 38,3, ЦП — 0,55, гипохромия, анизоцитоз сохраняются. Лейкоциты — 8×10*9.
В течение 3 сут пациент находился в ОРИТ, антиангинальной терапии не требовалось, т. к. приступы стенокардии не рецидивировали.
Проводился поиск возможного источника кровопотери, онкопоиск: при колоноскопии выявлен хронический комбинированный геморрой 3 ст. Другой патологии, которая могла бы объяснить наличие анемии, не найдено.
Проводилось постепенное расширение двигательного режима. Физические нагрузки, соответствующие уровню 3 функционального класса, приступов стенокардии и ЭКГ-признаков ишемии миокарда не вызывают.
Через 12 дней в стабильном состоянии пациент выписан для дальнейшего лечения в амбулаторных условиях. Хирургом рекомендовано выполнение в плановом порядке дезартеризации геморроидальных узлов под ультразвуковым контролем.
Клинический случай 3
Больной З., 82 года, госпитализирован в стационар с жалобами на дискомфорт за грудиной, нехватку воздуха, возникающие без четкой связи с физической нагрузкой, длительностью до 4–5 мин, накануне был затяжной приступ длительностью более 1 ч, выраженную слабость, потливость. Настоящее ухудшение состояния отмечает в течение последних 3 дней на фоне появившейся гипотонии.
В течение 2 нед. до госпитализации принимал по поводу дорсалгии нестероидные противовоспалительные препараты (НПВП) (кеторолак). 4 дня назад отметил появление учащенного жидкого стула темной окраски, необычно низкое АД — 80/40 мм рт. ст.
В 1995 г. перенес ОИМ нижней стенки ЛЖ. В этом же году выполнено маммарно-коронарное шунтирование ПМЖА, АКШ ЗБВ ОА и ПКА. В 2003 г. — линейное аортобедренное шунтирование синтетическим протезом слева. Ранний послеоперационный период осложнился развитием повторного ОИМ нижней стенки ЛЖ.
С 2009 г. — пароксизмы мерцательной тахиаритмии.
Постоянно принимает бисопролол — 2,5 мг/сут, периндоприл — 5 мг/сут, аторвастатин — 20 мг/сут, варфарин — 5 мг/сут. Контроль МНО не проводился более года.
При поступлении: кожные покровы и видимые слизистые бледные. Число дыханий — 20 в 1 мин. Дыхание ослабленное, жесткое. Тоны сердца глухие, ритмичные. ЧСС — 76 уд./мин. АД — 110/70 мм рт. ст.
Лабораторные данные: гемоглобин — 91 г/л, эритроциты — 3,93×10*12, гематокрит — 33,0, ЦП — 0,84, лейкоциты — 10,2–10,6×10*9, тромбоциты — 223×10*9, анизоцитоз, анизохромия.
Кардиоспецифические ферменты: КФК — 268 при поступлении, через 10 ч — 319, КФК МВ — 30 при поступлении, через 10 ч — 42, тропонин Т при поступлении — 177, через 10 ч — 538.
Сывороточное железо — 13 мкмоль, белки транспорта железа в границах нормы. Коагулограмма: АЧТВ — нет коагуляции, МНО — нет коагуляции, фибриноген — 3,3 г/л, Д-димер — 1147.
ЭКГ (рис. 6) при поступлении: синусовый ритм, АВ-блокада I ст., рубцовые изменения нижней стенки ЛЖ, смещение сегмента ST во II, III и avF отведениях, высокий R — в V1-2. Архив ЭКГ не предоставлен.
ЭхоКГ: склероз и кальциноз стенок аорты, кольца и створок АК. ММЛЖ — 204 г, толщина МЖП — 1,0 см, ЗСЛЖ — 1,0 см. Дилатация левых отделов сердца (ЛП — 4,5×5,5 см, левый желудочек: КСО — 92, КДО — 171). Относительная недостаточность МК II степени. Гипокинез среднего заднего и заднебокового сегментов ЛЖ. Снижение глобальной сократительной способности миокарда ЛЖ (ФВ по Тейхольцу — 47%). Диастолическая дисфункция левого желудочка первого типа.
С учетом жалоб, анамнеза, лабораторно-инструментальных данных у больного диагностирован повторный ОИМ диафрагмальной и заднебазальной локализации.
Не исключалось состоявшееся желудочно-кишечное кровотечение на фоне приема НПВП и орального антикоагулянта, в связи с чем экстренно выполнена ЭГДС: эндоскопические признаки хронического эзофагита, язва нижней трети пищевода Forrest II C. Острая язва желудка Forrest II B (без признаков продолжающегося кровотечения). Язва привратника Forrest I B (с признаками продолжающегося кровотечения). После эндоскопического инъекционного гемостаза кровотечение остановлено.
Причиной ОИМ, вероятно, явилась гипотония и анемия на фоне желудочно-кишечного кровотечения. Начата консервативная гемостатическая, противоязвенная терапия. От проведения КАГ с возможным чрескожным коронарным вмешательством решено воздержаться до стабилизации состояния.
На фоне лечения цифры АД стабилизировались на уровне 120/85 мм рт. ст., уровень гемоглобина повысился до 110 г/л, возросло число эритроцитов — до 5,71×10*12, гематокрит — 38,3, ЦП — 0,55, лейкоциты — 8×10*9, гипохромия, анизоцитоз сохраняются.
Уровень активности КФК снизился до 113 ед, МВ КФК — до 12,7, тропонина Т — до 225.
ЭГДС через 2 сут: язва нижней трети пищевода Forrest III, острая язва желудка Forrest III, язва привратника Forrest II С (отсутствие признаков кровотечения, появление в области дна фибрина).
На 3-й день пребывания в стационаре возобновились кратковременные приступы сжимающих болей за грудиной (2 приступа: во время приема пищи и при попытке сесть в кровати).
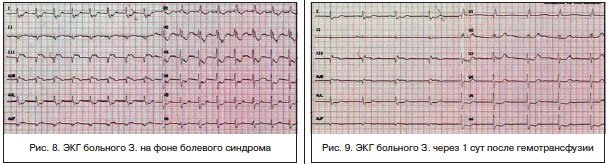
По экстренным показаниям выполнена коронароангиография (рис. 7): ствол ЛКА стенозирован на протяжении передней и средней трети до 70%, субокклюзирован в дистальной трети с переходом на устья ОВ и ПМЖВ; ПМЖВ субокклюзирована в устье, стенозирована в передней трети на 80%, окклюзирована в средней трети, дистальная часть контрастируется по функционирующему маммарно-коронарному шунту. ОВ субокклюзирована в устье, стенозирована в передней трети на 80%; ПКА субокклюзирована на протяжении передней и средней трети, окклюзирована на границе средней и дистальной третей, дистальная часть контрастируется по межартериальным анастомозам.
Правый тип коронарного кровоснабжения.
Маммарно-коронарный шунт из правой маммарной артерии в дистальной трети ПМЖВ проходим. Шунты к ОА и ПКА не визуализируются.
Попытка реканализации стенозированных артерий — без успеха в связи с выраженным кальцинозом.
В течение последующих суток — состояние с отрицательной динамикой: в виде учащения кратковременных приступов стенокардии, сопровождающихся выраженными ЭКГ-признаками ишемии миокарда (рис. 8). Отмечено снижение гемоглобина со 110 до 87 г/л, гематокрита — до 26,0.
Кардиоспецифические ферменты в пределах нормальных значений. ЭхоКГ: размер левых отделов сердца прежний, новых участков нарушения движений стенок ЛЖ не выявлено.
Гастроскопия: активное кровотечение из острого дефекта слизистой кардиоэзофагеального перехода (Forrest I). Эндоскопическая остановка кровотечения.
После переливания 600 мл эритроцитной взвеси состояние с положительной динамикой: ангинозные боли и ЭКГ-признаки ишемии миокарда не рецидивируют (рис. 9), восстановление уровня гемоглобина (110 г/л), эритроцитов (3,85×10*12), гематокрита -33,7.
При контрольной ЭГДС через 10 дней положительная динамика — уменьшение в размерах язвенных дефектов без признаков кровотечения.
На фоне терапии ингибиторами протонной помпы, β-блокаторами, клопидогрелом 75 мг/сут показатели красной крови стабильны, двигательный режим расширен и по уровню нагрузок соответствует 3 ФК.
ХМЭКГ: ритм синусовый, ЧСС (за сут/днем/ночью): 78/77/78 уд/мин, максимальная ЧСС — 99 уд/мин, минимальная — 64 уд/мин. Отмечается появление депрессии сегмента ST при увеличении ЧСС свыше 90 уд/мин.
Приведенные случаи демонстрируют возможность проявления коронарной недостаточности на фоне снижения кислород-транспортной способности крови как у пациентов с тяжелым, так и умеренным поражением коронарного русла. Устранение анемии во всех трех случаях способствовало повышению коронарного резерва и стабилизации состояния.
