Эритроциты их функции виды гемоглобина
Эритроциты (Э) – это высокоспециализированные безъядерные клетки крови. Ядро у них утрачивается в процессе созревания. Эритроциты имеют форму двояковогнутого диска. В среднем их диаметр около 7,5 мкм, а толщина на периферии 2,5 мкм. Благодаря такой форме увеличивается поверхность эритроцитов для диффузии газов. Кроме того, это возрастает их пластичность. За счет высокой пластичности, они деформируются и легко проходят по капиллярам. У старых и патологических эритроцитов пластичность низкая. Поэтому они задерживаются в капиллярах ретикулярной ткани селезенки и разрушаются там. Мембрана эритроцитов и отсутствие ядра обеспечивают их главную функцию – перенос кислорода и участие в переносе углекислого газа. Мембрана эритроцитов непроницаема для катионов, кроме калия, а ее проницаемость для анионов хлора, гидрокарбонат анионов и гидроксил анионов в миллион раз больше. Кроме того она хорошо пропускает молекулы кислорода и углекислого газа. В мембране содержится до 52% белка. В частности, гликопротеины определяют групповую принадлежность крови и обеспечивают ее отрицательный заряд. В нее встроена Nа/К-АТФаза, удаляющая из цитоплазмы натрий и закачивающая ионы калия. Основную массу эритроцитов составляет хемопротеин гемоглобин. Кроме того в цитоплазме содержатся ферменты карбоангидраза, фосфатазы, холинэстераза и другие ферменты.
Функции эритроцитов:
1. Перенос кислорода от легких к тканям.
2. Участие в транспорте СО2 от тканей к легким.
3. Транспорт воды от тканей к легким, где она выделяется в виде пара.
4. Участвуют в свертывании крови, выделяя эритроцитарные факторы свертывания.
5. Переносят аминокислоты на своей поверхности.
6. Участвуют в регуляции вязкости крови, вследствие пластичности. В результате их способности к деформации, вязкость крови в мелких сосудах меньше, чем крупных.
В одном микролитре крови мужчин содержится 4,5-5,0 млн. эритроцитов (4,5-5,0 * 1012 л). Женщин – 3,7-4,7 млн. (3,7-4,7 * 1012 л). Подсчет количества эритроцитов производится в камере Горяева. Для этого кровь в специальном капилляре меланжере (смесителе) для эритроцитов смешивают с 3% раствором хлорида натрия в соотношении 1:100 или 1:200. Затем капелька этой смеси помещается в счетную камеру. Она создается средним выступом камеры и покровным стеклом. Высота камеры 0,1 мм. На среднем выступе нанесена сетка, образующая большие квадраты. Часть этих квадратов разделена на 16 маленьких (табл.). Каждая сторона малого квадрата имеет величину 0,05 мм. Следовательно, объем смеси над малым квадратом будет составлять 1/10 мм * 1/20 мм * 1/20 мм = 1/4000 мм3.
После заполнения камеры, под микроскопом считают количество эритроцитов в 5-ти тех больших квадратах, которые разделены на маленькие, Т.е. в 80 маленьких. Затем рассчитывают количество эритроцитов в одном микролитре крови по формуле:
Где а – общее количество эритроцитов, полученное при подсчете
б – число малых квадратов в которых производился подсчет (80)
в – разведение крови (1:100, 1:200).
4000 – величина обратная объему жидкости на малым квадрате.
Для быстрого подсчета, при большом количестве анализов, используют
фотоэлектрические эритрогемометры. Принцип их действия основан на определении прозрачности взвеси эритроцитов с помощью пучка света проходящего от источника к светочувствительному датчику. Фотоэлектрокалориметры.
Увеличение содержания эритроцитов в крови называется эритроцитозом или эритремией, уменьшаться эритропенией или анемией. Эти изменения могут быть относительными и абсолютными. Например, относительное уменьшение их количества возникает при задержке воды в организме, а увеличение при обезвоживании. Абсолютное уменьшение содержания эритроцитов, т.е. анемия наблюдается при кровопотере, нарушениях кроветворения, разрушении эритроцитов гемолитическими ядами или при переливании несовместимой крови.
Гемолиз это разрушение мембраны эритроцитов и выход гемоглобина в плазму. В результате кровь становится прозрачной.
Различают следующие виды гемолиза.
По месту возникновения:
1. Эндогенный, т.е. в организме.
2. Экзогенный, вне его. Например во флаконе с кровью, аппарате искусственного кровообращения.
По характеру:
1. Физиологический. Он обеспечивает разрушение старых и патологических форм эритроцитов. Имеется два механизма. Внутриклеточный гемолиз происходит в макрофагах селезенки, костного мозга, клетках печени. Внутрисосудистый, в мелких сосудах, из которых гемоглобин с помощью белка плазмы гаптоглобина переносится к клеткам печени. Там гем гемоглобина превращается в билирубин. В сутки разрушается около 6-7 г гемоглобина.
2. Патологический.
По механизму возникновения :
1. 1.Химический. Возникает при воздействии на эритроциты веществ, растворяющих липиды мембраны. Это спирты, эфир, хлороформ, щелочи кислоты и т.д. В частности, при отравлении большой дозой уксусной кислоты возникает выраженный гемолиз.
2. Температурный. При низких температурах в эритроцитах образуются кристаллики льда, разрывающие их оболочку.
3. Механический. Наблюдается при механических разрывах мембраны. Например, при встряхивании флакона с кровью или ее перекачивания аппаратом искусственного кровообращения.
4. Биологический. Происходит при действии биологических факторов. Это гемолитические яды бактерий, насекомых, змей. В результате переливания несовместимой крови.
5. Осмотический. Возникает в том случае, если эритроциты попали в среду с осмотическим давлением ниже, чем у крови. Вода входит в эритроциты, они набухают и лопаются. Концентрация хлорида натрия, при которой происходит гемолиз 50% всех эритроцитов, является мерой их осмотической стойкости. Ее определяют в клинике для диагностики заболеваний печени, анемий. Осмотическая стойкость должна быть не ниже 0,46% НаС1. При помещении эритроцитов в среду, с большим чем у крови осмотическим давлением, происходит плазмолиз. Это сморщивание эритроцитов. Его используют для подсчета эритроцитов.
Гемоглобин. Его разновидности и функции.
Гемоглобин (Нb) – это хемопротеин, содержащийся в эритроцитах. Его молекулярная масса 66000 дальтон. Молекулу гемоглобина образуют четыре субъединицы, каждая из которых включает гем, соединенный с атомом железом, и белковую часть глобин. Гем синтезируется в митохондриях эритробластов, а глобин в их рибосомах. У взрослого человека гемоглобин содержит две - и две -полипептидных цепи. Он называется А-гемоглобином (adult-взрослый). В зрелом возрасте он составляет основную часть гемоглобина. В первые три месяца внутриутробного развития в эритроцитах находится гемоглобин типа GI и G2 (Gover). В последующие периоды внутриутробного развития и в первые месяцы после рождения основную часть составляет фетальный гемоглобин (F-гемоглобин). В его структуре две - и две -полипептидные цепи. При рождении до 50-80% гемоглобина составляет F-гемоглобин, а 20-40 % А-гемоглобин. Ранние гемоглобины имеют большую кислородную емкость.
Гем содержит атом 2-х валентного железа, который легко соединяется с кислородом и легко отдает его. При этом валентность железа не изменяется. Один грамм гемоглобина способен связывать 1,34 мл кислорода. Соединение гемоглобина с кислородом, образующееся в капиллярах легких называется оксигемоглобином (HbO2). Он имеет ярко алый цвет. Гемоглобин, отдавший кислород в капиллярах тканей, называется дезоксигемоглобином или восстановленным (Hb). У него темно-вишневая окраску. От 10 до 30% углекислого газа, поступающего из тканей в кровь, соединяются с амидной группировкой гемоглобина. Образуется легко диссоциирующее соединение карбгемоглобин (HbCO2). В этом виде часть углекислого газа транспортируется к легким.
В некоторых случаях гемоглобин образует патологические соединения. При отравлении угарным газом образуется карбоксигемоглобин (HbCO). Сродство гемоглобина с окисью углерода значительно выше, чем с кислородом, а скорость диссоциации карбоксигемоглобина в 200 раз меньше, чем оксигемоглобина. Поэтому присутствие в воздухе даже 1% угарного газа приводит к прогрессирующему увеличению количества карбоксигемоглобина и опасному угарному отравлению. Кровь теряет способность переносить кислород. Развивается гипоксия мозга и других тканей. Угарное отравление сопровождается сильной головной болью, тошнотой, рвотой, судорогами, потерей сознания и смертью.
При отравлении сильными окислителями, например нитритами, марганцевокислым калием, красной кровяной солью, образуется метгемоглобин (MetHb). В этом соединении гемоглобина железо становится трехвалентным. Поэтому метгемоглобин очень слабо диссоциирующее соединение. Он не отдает кислород тканям.
Все соединения гемоглобина имеют характерный спектр. Восстановленный гемоглобин дает одну широкую полосу поглощения в желто-зеленой части спектра между линиями D и E. Оксигемоглобин дает 2 узких полосы поглощения в желто-зеленой части спектра между линиями D и E. У карбоксигемоглобина такая же спектральная картина, как и оксигемоглобина. Поэтому для диагностики отравления угарным газом, в исследуемую кровь добавляют восстановитель, например реактив Стокса. Под их влиянием оксигемоглобин превращается в дезоксигемоглобин и появляется спектр восстановленного гемоглобина. Карбоксигемоглобин не восстанавливается. Метгемоглобин, в зависимости от рН крови, дает 3-5 полос поглощения. Одна из них находится в красной части, другие в желто-зеленой области спектра.
Гемоглобин образует с соляной кислотой соединение коричневого цвета – солянокислый гематин. Форма его кристаллов зависит от видовой принадлежности крови. В частности, кристаллы солянокислого гематина человека имеют форму прямоугольных пластинок.
Содержание гемоглобина определяют методом Сали. Гемометр Сали состоит из 3 пробирок, находящихся в специальном штативе. Две из них, расположенные сбоку от центральной, заполнены стандартным раствором солянокислого гематина коричневого цвета. Средняя пробирка имеет градуировку в единицах гемоглобина. В нее наливают 0,2 мл соляной кислоты. Затем мерной пипеткой набирают 20 мкл крови и выпускают ее в соляную кислоту. Перемешивают содержимое пробирки и выдерживают 5 мин. Полученный раствор солянокислого гематина разводят водой до тех пор, пока его цвет не станет таким же, как в боковых пробирках. По уровню жидкости в средней пробирке определяется содержание гемоглобина. В норме в крови мужчин содержится 132-164 г/л (13,2-16,4 г %) гемоглобина. У женщин – 115-145 г/л (11,5-14,5 г %). Количество гемоглобина снижается при кровопотерях, интоксикациях, нарушениях эритропоэза, недостатке железа, витамина В12 и т.д.
Кроме этого определяют цветовой показатель. Он отражает степень насыщения эритроцитов гемоглобином. Это отношение содержания гемоглобина в крови к количеству эритроцитов. В норме его величина составляет 0,85-1,05.
Источник
Эритроциты-
это высокоспециализированные безъядерные
клетки крови. Функции эритроцитов:1.
Перенос кислорода от легких к тканям.2.
Участие в транспорте СО2 от тканей к
легким.3. Транспорт воды от тканей к
легким, где она выделяется в виде пара.4.
Участвуют в свертывании крови, выделяя
эритроцитарные факторы свертывания.5.
Переносят аминокислоты на своей
поверхности.6. Участвуют в регуляции
вязкости крови, вследствие пластичности.
В результате их способности к деформации,
вязкость крови в мелких сосудах меньше,
чем крупных.
В
одном микролитре крови мужчин содержится
4,5-5,0 млн. эритроцитов (4,5-5,0 * 1012 л). Женщин
– 3,7-4,7 млн. (3,7-4,7 * 1012 л). Подсчет количества
эритроцитов производится в камере
Горяева. Для этого кровь в специальном
капилляре меланжере для эритроцитов
смешивают с 3% раствором хлорида натрия
в соотношении 1:100 или 1:200. Затем капелька
этой смеси помещается в счетную камеру.
Часть этих квадратов разделена на 16
маленьких. Каждая сторона малого квадрата
имеет величину 0,05 мм. Следовательно,
объем смеси над малым квадратом будет
составлять 1/10 мм * 1/20 мм * 1/20 мм = 1/4000
мм3.После заполнения камеры, под
микроскопом считают количество
эритроцитов в 5-ти тех больших квадратах,
которые разделены на маленькие, Т.е. в
80 маленьких. Затем рассчитывают количество
эритроцитов в одном микролитре крови
по формуле Х = 4000*а*в/б Где а – общее
количество эритроцитов, полученное при
подсчете.б – число малых квадратов в
которых производился подсчет.в –
разведение крови (1:100, 1:200).4000 – величина
обратная объему жидкости на малым
квадрате. Для быстрого подсчета, при
большом количестве анализов, используют
фотоэлектрическиеэритрогемометры.
Принцип их действия основан на определении
прозрачности взвеси эритроцитов с
помощью пучка света проходящего от
источника к светочувствительному
датчику.
Выделяют
четыре формы гемоглобина:1) оксигемоглобин;2)
метгемоглобин;3) карбоксигемоглобин;4)
миоглобин. Оксигемоглобин содержит
двухвалентное железо и способен связывать
кислород. Он переносит газ к тканям и
органам. При воздействии окислителей
(перекисей, нитритов и т. д.) происходит
переход железа из двухвалентного в
трехвалентное состояние, за счет чего
образуется метгемоглобин, который не
вступает в обратимую реакцию с кислородом
и обеспечивает его транспорт.
Карбоксигемоглобин образует соединение
с угарным газом. Он обладает высоким
сродством с окисью углерода, поэтому
комплекс распадается медленно. Это
обусловливает высокую ядовитость
угарного газа. Миоглобин по структуре
близок к гемоглобину и находится в
мышцах, особенно в сердечной. Он связывает
кислород, образуя депо, которое
используется организмом при снижении
кислородной емкости крови. За счет
миоглобина происходит обеспечение
кислородом работающих мышц.
Гемолиз
это разрушение мембраны эритроцитов и
выход гемоглобина в плазму. В результате
кровь становится прозрачной. Различают
следующие виды гемолиза. По месту
возникновения:1. Эндогенный, т.е. в
организме.2. Экзогенный, вне его.
По
характеру:1. Физиологический. Он
обеспечивает разрушение старых и
патологических форм эритроцитов. Имеется
два механизма. Внутриклеточный гемолиз
происходит в макрофагах селезенки,
костного мозга, клетках печени.
Внутрисосудистый, в мелких сосудах, из
которых гемоглобин с помощью белка
плазмы гаптоглобина переносится к
клеткам печени. Там гем гемоглобина
превращается в билирубин. В сутки
разрушается около 6-7 г гемоглобина.2.
Патологический.
По
механизму возникновения :1.ХимическийВозникает
при воздействии на эритроциты веществ,
растворяющих липиды мембраны. Это
спирты, эфир, хлороформ, щелочи кислоты
и т.д.. 2. Температурный. При низких
температурах в эритроцитах образуются
кристаллики льда, разрывающие их
оболочку.3МеханическийНаблюдается при
механических разрывах мембраны. Например,
при встряхивании флакона с кровью или
ее перекачивания аппаратом искусственного
кровообращения.4. Биологический.
Происходит при действии биологических
факторов. Это гемолитические яды
бактерий, насекомых, змей. В результате
переливания несовместимой крови.5.
Осмотический. Возникает в том случае,
если эритроциты попали в среду с
осмотическим давлением ниже, чем у
крови.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
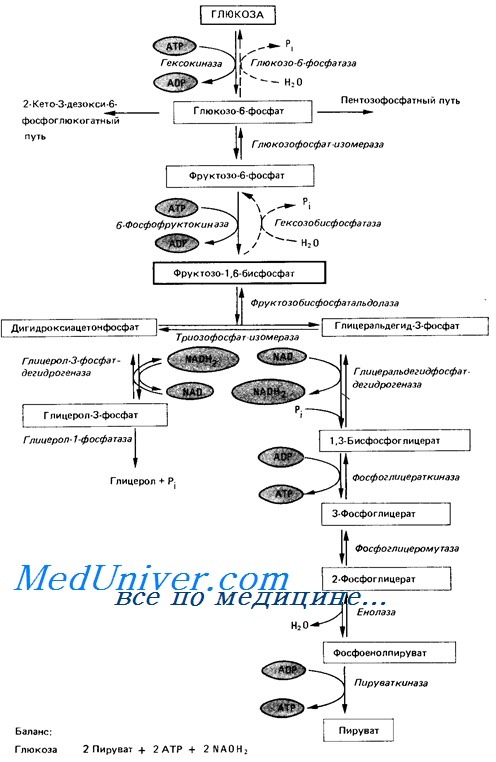
Оглавление темы “Функции клеток крови. Эритроциты. Нейтрофилы. Базофилы.”: Функции клеток крови. Функции эритроцитов. Свойства эритроцитов. Цикл Эмбдена—Мейергофа. Строение эритроцитов.Цельная кровь состоит из жидкой части (плазмы) и форменных элементов, к которым относят эритроциты, лейкоциты и кровяные пластинки — тромбоциты. Функции крови: Функции и свойства эритроцитовЭритроциты переносят 02 содержащимся в них гемоглобином от легких к тканям и С02 от тканей к альвеолам легких. Функции эритроцитов обусловлены высоким содержанием гемоглобина (95 % массы эритроцита), деформируемостью цитоскелета, благодаря чему эритроциты легко проникают через капилляры с диаметром меньше 3 мкм, хотя имеют диаметр от 7 до 8 мкм. Глюкоза является основным источником энергии в эритроците. Восстановление формы деформированного в капилляре эритроцита, активный мембранный транспорт катионов через мембрану эритроцита, синтез глютатиона обеспечиваются за счет энергии анаэробного гликолиза в цикле Эмбдена—Мейергофа. В ходе метаболизма глюкозы, протекающего в эритроците по побочному пути гликолиза, контролируемого ферментом дифосфоглицератмутазой, в эритроците образуется 2,3-дифосфоглицерат (2,3-ДФГ). Основное значение 2,3-ДФГ заключается в уменьшении сродства гемоглобина к кислороду. В цикле Эмбдена—Мейергофа расходуется 90 % потребляемой эритроцитами глюкозы. Торможение гликолиза, возникающее, например, при старении эритроцита и уменьшающее в эритроците концентрацию АТФ, приводит к накоплению в ней ионов натрия и воды, ионов кальция, повреждению мембраны, что понижает механическую и осмотическую устойчивость эритроцита, и стареющий эритроцит разрушается. Энергия глюкозы в эритроците используется также в реакциях восстановления, защищающих компоненты эритроцита от окислительной денатурации, которая нарушает их функцию. Благодаря реакциям восстановления атомы железа гемоглобина поддерживаются в восстановленной, т. е. двухвалентной форме, что препятствует превращению гемоглобина в метгемоглобин, в котором железо окислено до трехвалентного, вследствие чего метгемоглобин неспособен к транспорту кислорода. Восстановление окисленного железа метгемоглобина до двухвалентного обеспечивается ферментом — метгемоглобинредуктазой. В восстановленном состоянии поддерживаются и серусодержащие группы, входящие в мембрану эритроцита, гемоглобин, ферменты, что сохраняет функциональные свойства этих структур. Цикл Эмбден-Мейергоффа эритроцитов Эритроциты имеют дисковидную, двояковогнутую форму, их поверхность — около 145 мкм2, а объем достигает 85—90 мкм3. Такое соотношение площади к объему способствует деформабильно-сти (под последней понимают способность эритроцитов к обратимым изменениям размеров и формы) эритроцитов при их прохождении через капилляры. Форма и деформабильность эритроцитов поддерживаются липидами мембран — фосфолипидами (глицерофосфолипидами, сфинголипидами, фосфотидилэтаноламином, фосфатидилсирином и др.), гликолипидами и холестерином, а также белками их цитоскелета. В состав цитоскелета мембраны эритроцита входят белки — спектрин (основной белок цитоскелета), анкирин, актин, белки полосы 4.1, 4.2, 4.9, тропомиозин, тропомодулин, адцуцин. Основой мембраны эритроцита является липидный бислой, пронизанный интегральными белками цитоскелета — гликопротеинами и белком полосы 3. Последние связаны с частью белковой сети цитоскелета — комплексом спектрин—актин—белок полосы 4.1, локализованным на цитоплазматической поверхности липидного бислоя мембраны эритроцита (рис. 7.1). Взаимодействие белкового цитоскелета с липидным бислоем мембраны обеспечивает стабильность структуры эритроцита, поведение эритроцита как упругого твердого тела при его деформации. Нековалентные межмолекулярные взаимодействия белков цитоскелета легко обеспечивают изменение размеров и формы эритроцитов (их деформацию) при прохождении этих клеток через микроциркуляторное русло, при выходе ретикулоцитов из костного мозга в кровь — благодаря изменению расположения молекул спектрина на внутренней поверхности липидного бислоя. Генетические аномалии белков цитоскелета у человека сопровождаются появлением дефектов мембраны эритроцитов. В результате последние приобретают измененную форму (так называемые сфероциты, элиптоциты и др.) и имеют повышенную склонность к гемолизу. Увеличение соотношения холестерин—фосфолипиды в мембране увеличивает ее вязкость, уменьшает текучесть и эластичность мембраны эритроцита. В результате снижается деформируемость эритроцита. Усиление окисления ненасыщенных жирных кислот фосфолипидов мембраны перекисью водорода или супероксидными радикалами вызывает гемолиз эритроцитов (разрушение эритроцитов с выходом гемоглобина в окружающую среду), повреждение молекулы гемоглобина эритроцита. Постоянно образующийся в эритроците глютатион, а также антиоксиданты (остокоферол), ферменты — глутатионредуктаза, супероксиддисмутаза и др. защищают компоненты эритроцита от этого повреждения.
До 52 % массы мембраны эритроцитов составляют белки гликопротеины, которые с олигосахаридами образуют антигены групп крови. Глико-протеины мембраны содержат сиаловую кислоту, которая придает отрицательный заряд эритроцитам, отталкивающий их друг от друга. Энзимы мембраны — Ка+/К+-зависимая АТФаза обеспечивает активный транспорт Na+ из эритроцита и К+ в его цитоплазму. Са2+-зависимая АТФаза выводит Са2+ из эритроцита. Фермент эритроцита карбоангидраза катализирует реакцию: Са2+ Н20 Н2С03 о Н+ + НСО3, поэтому эритроцит транспортирует часть углекислого газа от тканей к легким в виде бикарбоната, до 30 % С02 переносится гемоглобином эритроцитов в форме карбаминового соединения с радикалом NH2 глобина. – Также рекомендуем “Гемоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина.” |
Источник