Карбоксигемоглобин в крови норма
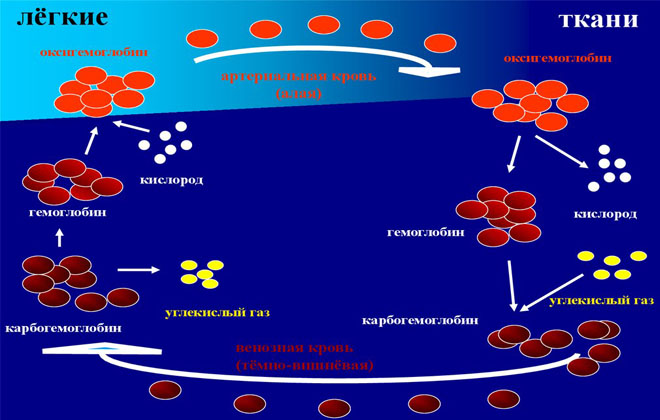
Дыхание — непременное условие жизнедеятельности клеток организма, которые поглощают кислород и выделяют двуокись углерода. Функцию транспортного средства, доставляющего О2 и выводящего СО2, выполняет кровь. Карбогемоглобин — это ее важная составляющая, участвующая в газообмене.

Что это такое
Гемоглобин (Hb) состоит из гема, соединения, содержащего железо, и белкового вещества глобина. Связываясь с О2, поступающим в кровь из легких, Hb снабжает им ткани, а соединяясь с СО2, очищает их от двуокиси углерода и доставляет ее к альвеолам, через которые этот газ удаляется в атмосферу.
Существуют 3 фракции (вида, модификации) гемоглобина, обусловленные физиологическими функциями. Соединяясь с О2, Hb превращается в оксигемоглобин НbО2. Это ярко-красное вещество преобладает в артериальной крови. Кроме того, оно содержится и в миокарде, во всех скелетных мышцах. Мышечный гемоглобин связывает около 10-14% всего О2 в организме. Миоглобин обеспечивает мышцы кислородом, когда они сокращаются, поскольку в это время кровоток приостанавливается.
НbО2, отдав тканям кислород, преобразуется в восстановленный (редуцированный) гемоглобин HНb. Эта субстанция содержится в венозной крови, обуславливая ее темно-вишневую окраску.
Соединение гемоглобина с углекислым газом называется карбогемоглобином. НbСO2 выводит двуокись углерода из клеток и транспортирует в легкие до 20% этого газа. Карбогемоглобин тоже содержится в венозной крови. Hb непрерывно преобразуется из оксигемоглобина в карбогемоглобин и обратно.
Кроме того, Hb образует стойкое соединение с глюкозой, содержащейся в крови. При диабете уровень гликированного гемоглобина HbA1c существенно возрастает. По динамике его концентрации можно судить об эффективности лечения этого заболевания.
Еще одна модификация Hb — фетальный гемоглобин, который содержится в крови новорожденных и исчезает к 1 году. Его наличие у взрослых свидетельствует о нарушениях в организме.
Однако Hb может видоизменяться, образуя и патологические модификации. Соединение гемоглобина с угарным газом называется карбоксигемоглобином. HbСО утрачивает способность транспортировать О2, поэтому клетки испытывают острое кислородное голодание. Анализ на наличие карбоксигемоглобина используется в криминалистике, поскольку позволяет выявить скрытые следы крови. Так, например, отсутствие HbСО в костной ткани трупного материала доказывает, что погибший был уже мертв до начала пожара.
От сильной гипоксии ткани также страдают, когда Hb окисляется и двухвалентное железо в геме замещается трехвалентным Fe. Образующийся при этом метгемоглобин HbMet настолько прочно связывается с О2, что практически не отдает его клеткам. Такое патологическое состояние наступает при отравлении нитратами, нитритами, анилинами, перекисью водорода, марганцовокислым калием, бертолетовой солью и другими веществами-окислителями.
Норма и отклонения
Количество гемоглобина в крови считается оптимальным в следующих пределах (г/л):
- у мужчин: 130-160, после 55-60 лет — 120-140;
- у женщин: 120-140, при беременности — 110-150;
- у детей: до 6 лет — 110-140, до 15 лет — 115-150;
- у жителей высокогорных районов: на 10-20 г/л выше.
Карбоксигемоглобин обнаруживается у некурящих в диапазоне от 0,5 до 1,5%, а у курильщиков — от 4 до 9% от всего объема Hb. О тяжелых отравлениях свидетельствуют показатели более 20%.
Норма в крови метгемоглобина — 0,04-1,52 %. При отравлениях концентрация HbMet достигает более 15%. Летальный исход наступает, если отклонения в показателях превышают 70%.
Проведение и расшифровка анализа
Результаты исследования Hb в медучреждениях нередко отличаются друг от друга, поскольку лаборатории оснащены приборами разных поколений. При проведении анализов крови нередко сказывается и субъективный фактор, зависящий от квалификации лаборанта. Кроме того, следует иметь в виду, что количество гемоглобина максимально вечером и минимально утром.
Сегодня наиболее распространен традиционный метод Сали. Содержание Hb определяют, добавляя к крови соляную кислоту. При этом гем, соединяясь с HCl, преобразуется в кристаллический гемин. Анализы биоматериалов на гемин применяются в судебной медицине для выявления следов крови.
Наиболее точные результаты дает автоматизированный метод с использованием гемометра. Такое исследование проводится гораздо быстрее. Но и при этом методе возможны незначительные расхождения показателей. Однако при расшифровке анализа следует обращать внимание на большие отклонения от нормы Hb, которые свидетельствуют о патологических процессах.
Так, избыток гемоглобина может быть следствием:
- легочной недостаточности;
- обезвоживания организма;
- химических отравлений;
- заболеваний крови, печени, кишечника;
- пороков сердца и др.
Дефицит Hb может быть признаком:
- анемий различной этиологии;
- нарушений менструального цикла;
- эрозий и изъязвлений ЖКТ;
- внутренних кровотечений;
- инфекций;
- воспалительных процессов с отечностью;
- сахарного диабета;
- заболеваний почек;
- злокачественных опухолей и других патологий.
При существенных отклонениях гемоглобина от нормы следует незамедлительно пройти углубленное обследование организма. Вовремя назначенное лечение позволит избежать развития многих опасных заболеваний.
Гемоглобин (Hb)
— кровяной пигмент, роль которого заключается в транспорте кислорода к органам и тканям. Вне эритроцитов (в плазме крови) гемоглобин практически не обнаруживается.
Химически гемоглобин относится к группе хромопротеидов. Его простетическая группа, включающая железо, называется гемом, белковый компонент — глобином. Молекула гемоглобина содержит 4 гема и один глобин. Гем является металлопорфирином — комплексом железа с протопорфирином. Протопорфирин имеет в своей основе четыре пиррольных кольца, соединенных посредством метиловых мостиков (СН) в кольцо порфирина. Гем идентичен для всех разновидностей гемоглобина человека.
В эритроцитах циркулирующей крови гемоглобин находится в состоянии беспрерывной обратимой реакции, то присоединяя молекулу кислорода (в легочных капиллярах), то отдавая ее (в тканевых капиллярах).
При полном насыщении крови кислородом 1 г гемоглобина связывает 1,34—1,36 мл кислорода. При высоком содержании кислорода в окружающей среде (в легких) восстановленный гемоглобин легко и быстро переходит в оксигемоглобин, тогда как при малых концентрациях кислорода в окружающей среде (в тканях, в которых кислород утилизируется) оксигемоглобин легко отщепляет от себя кислород. В случае ухудшения условий артериализации крови вследствие нарушения диффузии кислорода через альвеолярную мембрану или увеличения скорости кровотока в малом круге кровообращения, а также при повышенном потреблении кислорода тканями содержание оксигемоглобина в крови снижается, а количество восстановленного гемоглобина соответственно возрастает. В норме в артериальной крови содержание оксигемоглобина составляет 95—96 % от общего количества гемоглобина. В венозной крови эта величина снижается до 60 %.
Карбоксигемоглобин (HbCO)
— оксиуглеродный гемоглобин — диссоциирует в несколько сотен раз медленнее, чем оксигемоглобин, поэтому даже незначительная концентрация (0,07 %) в воздухе угарного газа (СО), связывая около 50 % имеющегося в организме гемоглобина и лишая его способности переносить кислород, является смертельной.
Образование карбоксигемоглобина начинается с периферии эритроцитов, соприкасающихся в легочных капиллярах с СО. При последующей циркуляции крови перераспределения СО между эритроцитами не происходит. По мере увеличения концентрации СО в воздухе образование карбоксигемоглобина распространяется от периферии эритроцитов к их центру. Каждый грамм глобина способен связывать 1,33—1,34 мл О2 или СО. Эта величина получила название константы Хьюфнера. Однако сродство к СО в 200—290 раз больше, чем к О2-
Константа равновесия этой реакции следующая:

В связи с этим даже при малом содержании СО во вдыхаемом воздухе в организме создаются конкурентные взаимоотношения между этими газами по захвату гемоглобина со значительным преимуществом для СО.
Определение содержания карбоксигемоглобина
(по Л.Э. Горн). Метод основан на фотометрическом определении разницы светопоглощения растворов окси- и карбоксигемоглобина после их денатурации щелочью.
Оборудование и реактивы. Универсальный фотометр ФМ или горизонтальный фотометр; 0,04 % раствор аммиака; 0,2 н. раствор гидратов оксида натрия или калия (едкого кали или натра).
Методика. В 2 пробирки наливают по 4,9 и 5,9 мл 0,04 % раствора аммиака, после чего в каждую вносят по 0,1 мл крови. В первую пробирку, предназначенную для определения светопоглощения исходной денатурированной крови, содержащей искомое количество карбоксигемоглобина (HbO2 + HbCO), быстро добавляют 5 мл 0,2 н. раствора щелочи, быстро перемешивают двукратным опрокидыванием и фотометрируют пробу через 1 мин после внесения щелочи (50—70 с, не более!) при светофильтре № 5 (М-55 или М-52, эффективная длина волны пропускаемого света 550 или 520 нм). Содержимое второй пробирки, в которой определяют общее количество гемоглобина, прямо фотометрируют при светофильтре № 5 (М-50, 496 нм). Фотометрирование ведут по общепринятым правилам в кюветах 10 мм с использованием дистиллированной воды. При использовании светофильтра № 5 (М-55) содержание карбоксигемоглобина вычисляют по формуле:

где Е — экстинкция.
Если светофильтр № 5 имеет марку М-52, а не М-55, то коэффициент 132 заменяют на 123.
Норма и оценка результатов исследования карбоксигемоглобина
В крови лиц, не соприкасающихся в условиях производства с оксидом углерода, карбоксигемоглобин присутствует, как правило, в некотором количестве, что обусловлено практически постоянным загрязнением атмосферы продуктами неполного сгорания всех видов топлива. По данным разных авторов, у городских жителей, не связанных с воздействием оксида углерода, в крови содержится до 15 % карбоксигемоглобина. Средняя его концентрация колеблется, по различным данным, от 2—4 до 6—8 %. Курение ведет к повышению этой величины на 2—3 %. Источником образования карбоксигемоглобина является не только экзогенный оксид углерода, но и в какой-то мере оксид углерода, образующийся в организме в результате неполного окисления некоторых продуктов обмена веществ, в частности гемоглобина. Поскольку при перенесении пострадавшего в чистую атмосферу, особенно при вдыхании кислорода, диссоциация карбоксигемоглобина происходит сравнительно быстро (за первый час содержание карбоксигемоглобина уменьшается вдвое), результаты лабораторного исследования крови, взятой для анализа через некоторое время после оказания первой помощи, могут дать ложное представление об имевшей место начальной максимальной концентрации карбоксигемоглобина и тем самым исказить представление о степени тяжести клинической картины интоксикации. Это является обоснованием необходимости максимального сокращения интервалов между вынесением пострадавшего из отравленной атмосферы и взятием крови для анализа. При хронической интоксикации оксидом углерода диссоциация карбоксигемоглобина в крови значительно замедляется.
Исследование кислотно-щелочного состояния (КЩС) или кислотно-основного состояния (КОС) имеет важное значение в диагностике и лечении различных неотложных состояний, в том числе хирургических.
Под кислотностью и щелочностью понимают концентрацию свободных ионов водорода (Н+) в растворе, т.е. рН крови. Для эффективного протекания процессов жизнедеятельности концентрация свободных ионов водорода (Н+) должна находится в жестких пределах. В действительности исследование КЩС включает наряду с измерением рН определение и физиологически важных газов, присутствующих в крови (кислорода – О2 и углекислого газа – СО2) и еще около 20-ти других параметров. Все эти показатели и их значения тесно взаимосвязаны друг с другом.
У пациентов реанимационного и операционного блоков могут наблюдаться существенные изменения этих показателей в течение коротких промежутков времени. Исследования КЩС, в отличие от всех других видов лабораторных анализов, выполняется на пробах артериальной крови.
Для нормального функционирования всех клеток организма необходим кислород (О2). Решающая роль в транспорте кислорода к тканям принадлежит содержащемуся в эритроцитах гемоглобину. Под термином «гемоглобин» подразумевают несколько форм гемоглобина, которые присутствуют в крови человека, как в норме, так при патологии. Более 98% кислорода, поглощенного легкими из вдыхаемого воздуха, переносится к клеткам организма кровью в виде оксигемоглобина. В норме в крови в небольших количествах присутствуют фракции гемоглобина, не способные переносить О2 – дисгемоглобины (сульфгемоглобин, метгемоглобин, карбоксигемоглобин).
Метгемоглобин постоянно образуется в результате нормального метаболизма клеток организма. Метгемоглобин содержит трехвалентное железо и не способен к транспорту кислорода! При образовании значительных количеств метгемоглобина транспортировочная функция крови резко нарушается. В организме существует механизм регуляции уровня метгемоглобина в крови, который поддерживает долю этой фракции не выше 1,0 – 1,5% от общего гемоглобина.
Карбоксигемоглобин — прочное соединение гемоглобина (Hb) и угарного газа (СО). Карбоксигемоглобин образуется очень быстро, поскольку способность присоединяться к гемоглобину у угарного газа примерно в 200 раз выше, чем у кислорода. Карбоксигемоглобин не способен переносить кислород к тканям организма, поэтому при отравлении окисью углерода у человека может быстро наступить смерть. В больших количествах карбоксигемоглобин образуется при отравлении угарным газом, а в небольших всегда присутствует в крови всех курильщиков и жителей больших городов.
Показания:
Анализа КЩС необходим
· Для постановки диагноза анализ газов крови – неотъемлемая часть постановки диагноза дыхательной недостаточности и первичной гипервентиляции. Он также выявляет метаболический ацидоз и алкалоз.
· Для оценки тяжести заболевания
· Для контроля эффективности лечения такой анализ очень важен для подбора терапии кислородом (О2) для пациентов с хронической дыхательной недостаточностью типа 2 и для оптимизации установок аппарата ИВЛ.
Увеличение метгемоглобина (FMetHb) в крови развивается при:
· отравлении нитритами, нитратами, нитрозосоединениями, анилином, сульфонамидами, ацетанилидом, хлоридами, бромидами и др
· наследственном дефиците НАДН-метгемоглобинредуктазы: низкая активность фермента проявляется в раннем детском возрасте. Клинических последствий, как правило, это заболевание не имеет, проявляясь незначительным косметическим дефектом.
· наличие аномальных вариантах гемоглобина, обозначаемых как гемоглобин М
Увеличение карбоксигемоглобина (FСОHb) в крови развивается при:
· отравлении угарным газом. При уровне FСОHb выше 30% отмечаются сильные головные боли, общая слабость, рвота, одышка, тахикардия, а при уровне 50% – судороги, кома; выше 70% наступает дыхательная недостаточность и возможен летальный исход.
Методика:
Определение газов крови, кислотно-щелочного статуса, параметров оксиметрии проводятся на анализаторе «ABL 800 FLEX» фирмы «RADIOMETR», Дания, определение до 50 параметров.
Подготовка:
Специальной подготовки не требуется!
Автор На чтение 8 мин. Опубликовано 25.07.2020
Карбоксигемоглобин норма в крови
К.В. ФАТКУЛЛИН 1 , А.Ж. ГИЛЬМАНОВ 1 , Д.В. КОСТЮКОВ 2
1 Башкирский государственный медицинский университет,, г. Уфа, ул. Ленина, д. 3
2 НПП «Техномедика»,, г. Москва, п/я 1
Фаткуллин Ким Вилевич — аспирант кафедры лабораторной диагностики ИПО, тел. , e-mail: [email protected] 1
Гильманов Александр Жанович — доктор медицинских наук, профессор, заведующий кафедрой лабораторной диагностики ИПО, тел. , e-mail: [email protected] 1
Костюков Дмитрий Владимирович — инженер, ведущий специалист, тел. , e-mail: [email protected] 2
В статье описаны механизмы образования карбокси- и метгемоглобина в организме в норме, основные причины повышения их концентрации в крови при патологических состояниях (отравлениях), патогенез, особенности клинической картины и диагностики развивающейся интоксикации. Приведена сравнительная характеристика традиционных и современных лабораторных методов определения концентрации указанных дериватов гемоглобина в крови: показаны их принципы, особенности, преимущества и недостатки.
Ключевые слова: карбоксигемоглобин, метгемоглобин, интоксикация, лабораторные методы.
1 Bashkir State Medical University, 3 Lenina St., Ufa, Russian Federation
2 Research and Production Enterprise TEKHNOMEDICA, P.O. Box 1, Moscow, Russian Federation
Качественные пробы на наличие карбоксигемоглобина
Пробы:
Функции и виды гемоглобина
Основная функция гемоглобина — транспортная. Он связывается с кислородом, поступившим в кровь из легочных альвеол, переносит его и затем отдает тканям. Но на этом роль гемоглобина не заканчивается: он забирает углекислый газ и относит его обратно к легким, откуда тот удаляется в окружающую среду. Таким образом, данный белок играет огромное значение для дыхания: без него у клеток человеческого организма нет возможности полноценно осуществлять метаболизм.
Выделяют несколько видов нормального гемоглобина:
Из них А1 и А2 характерны для взрослых (причем HbA1 составляет 96-98% от общего количества), а гемоглобин F — для новорожденных. В первые дни жизни этот показатель составляет до 60-80%, и к четвертому-пятому месяцу жизни снижается до 10%. В крови человека нормальный гемоглобин присутствует в трех химических формах: оксигемоглобин (соединение с кислородом, обозначение — HbO2), карбгемоглобин (соединение с углекислым газом, обозначение — HHbCO2), и восстановленный гемоглобин (обозначается как HHb). Однако данный белок способен образовывать и патологические соединения такие, как карбоксигемоглобин и метгемоглобин.
Карбоксигемоглобин представляет собой соединение с угарным газом. Он не способен переносить кислород и углекислый газ, откуда следует вывод о том, что при его наличии в крови ткани начинают испытывать сильнейшее кислородное голодание. Именно поэтому при пожаре люди гораздо чаще погибают от удушья, чем от самого огня.
Метгемоглобин образуется при окислении гемоглобина, железо в метгемоглобине является трехвалентным (в норме оно двухвалентное). Такое соединение прочно связывает кислород и крайне неохотно отдает его тканям. Вот почему при образовании метгемоглобина ткани также испытывают сильнейшую гипоксию. Метгемоглобин появляется в крови при отравлении окислителями (перманганатом калия, анилином и т.п.), нитратами и нитритами.
Сам по себе анализ крови на гемоглобин не предполагает определения наличия в крови карбоксигемоглобина и метгемоглобина. В этом нет необходимости. Подобное исследование проводится в том случае, если имеют место быть симптомы отравления: тогда кровь берут в токсикологическую лабораторию, где при помощи специальных методик выявляют наличие метгемоглобина или карбоксигемоглобина.
Экстренная медицина
Определение карбоксигемоглобина в крови является ценным показателем, уточняющим диагноз и определяющим рациональную терапию. Так, в случаях, когда по истечении определенного времени в крови пострадавшего наступает равновесие между образованием и удалением окиси углерода, терапия кислородом может утрачивать свое значение.
Качественная реакция на наличие карбоксигемоглобина в крови:
1. Кровь в количестве 0,01 мл берут из пальца уколом иглой и разводят дистиллированной водой в 100 раз (до 1 мл). Пробирку с разведенной кровью помещают перед спектроскопом и наблюдают при естественном или искусственном освещении две полосы поглощения в желто-зеленом (А. =нм) и зеленом (к = нм) участках спектра, совпадающих со спектром оксигемоглобина (А =инм).
Для отличия производят качественную реакцию: в пробирку добавляют вещество, быстро реагирующее с кислородом и превращающее оксигемоглобин крови в восстановленный гемоглобин (1 — 2 капли сернистого аммония NH4S или 4—5 мг дитионита натрия Na2S204). Пробирку встряхивают и снова помещают перед спектроскопом.
При отсутствии карбоксигемоглобина видна лишь одна широкая полоса поглощения, соответствующая восстановленному гемоглобину и располагающаяся в желто-зеленой части спектра (А =нм). В присутствии карбоксигемоглобина изменений в спектре не происходит, и при повторной спектроскопии продолжают определяться две полосы поглощения — в желто-зеленом и зеленом участках спектра.
2. Спектроскопический метод определения карбоксигемоглобина основан на способности карбоксигемоглобина и восстановленного гемоглобина в разной степени поглощать световые лучи при длине волны 534—563 нм. Вычисляют разность между светопоглощением карбоксигемоглобина и светопоглощением восстановленного гемоглобина, который получают путем добавления дитионита натрия.
Из пальца берут на анализ 0,1 мл крови. Кровь насасывают микропипеткой, предварительно сполоснутой раствором цитрата натрия; помещают в мерную пробирку емкостью 10 мл и доводят объем до метки 0,005 н. раствором едкого натра. К 5 мл прозрачного раствора добавляют восстановитель — 8 мг дитионита натрия — и производят спектрометрическое измерение оптической плотности раствора при волнах 534 и 536 нм. Содержание в крови СОНb вычисляют по формуле:
где E1 — оптическая плотность при длине волны 534 нм; Е2 — то же при длине волны 536 нм.
Единого мнения о физиологически допустимых нормах содержания карбоксигемоглобина в крови нет. Так, у городских жителей содержание в крови карбоксигемоглобина может достигать 4 — 7%.
Следует отметить, что у больных с хронической интоксикацией окисью углерода уровень карбоксигемоглобина в крови обычно соответствует нормальным величинам. Определение у них карбоксигемоглобина может иметь место при нарушении функции легких и сердца с отклонениями в обмене угольной кислоты, а также при зритремии, диабете, силикозе и сердечных заболеваниях.
3. В случаях, если под рукой нет спектроскопа, может быть использован ориентировочный, технически простой метод определения карбоксигемоглобина с помощью сульфата меди. На кусок белой бумаги (стекло, поверхность фаянса, фарфора) наносят каплю крови пострадавшего с подозрением на отравление окисью углерода.
Рядом наносят каплю крови здорового человека. В каждую каплю крови вносят по капле 2 % раствора сульфата меди и перемешивают деревянной палочкой (спички). По истечении 30 с — 1 мин в крови, содержащей карбоксигемоглобин, образуется мазеобразная масса серовато-коричневого или шоколадного цвета. Спустя некоторое время она становится красно-коричневого цвета.
Определение метгемоглобина. При интоксикации анилином, нитро- и динитробензолом, бертолетовой солью и другими соединениями, способными окислять железо гемоглобина, происходит образование метгемоглобина с переходом железа из двухвалентного в трехвалентное его соединение.
Существует мнение, что в крови здорового человека и животных всегда имеется определенное (физиологически допустимое) количество метгемоглобина. В организме теплокровных животных постоянно происходят процессы образования и редукции метгемоглобина до окиси гемоглобина. В обычных условиях эти процессы хорошо уравновешены. Уровень метгемоглобина у здорового человека не превышает 1 % по отношению ко всему гемоглобину крови:
1. Качественная реакция на метге-моглобин осуществляется при помощи спектрального анализа. Метгемоглобин дает характерный спектр с широкой полосой поглощения в красной части спектра (к = 630 нм) и две полосы в оранжевой и желтой частях спектра.
2. Большое значение для оценки тяжести интоксикации имеет количественное определение метгемоглобина. Его производят на спектрофотометре. При этом метгемоглобин после предварительного его определения по полосе поглощения света на длине волны 633 нм переводят в цианметгемоглобин, совсем не дающий полосы поглощения в этом месте спектра.
Метод основан на фотометрировании метгемоглобина и цианметгемоглобина в красной части спектра при длине волны 630 нм, в которой они имеют разные спектры поглощения. Изменение интенсивности поглощения света после добавления цианистого калия (для превращения MtHb в цианметгемоглобин) прямо пропорционально концентрации MtHb.
Для исследования берут две пробы крови. Гемоглобин одной пробы переводят в метгемоглобин добавлением капли насыщенного раствора KjFe (CN)6. В другой пробе гемоглобин окисляют за счет растворенного в среде кислорода. Далее определяют степень поглощения света с длиной волны 619 нм в обеих пробах с последующим вычислением разности светопоглоще-ния между метгемоглобином и оксигемоглобином.
3. Количественное определение метгемоглобина может быть проведено и с помощью ручного спектроскопа. Кровь, разведенную в 5 раз дистиллированной водой (0,2 мл крови и 0,8 мл воды), помещают в цилиндр и просматривают через ручной спектроскоп. При наличии полосы поглощения в красном участке спектра раствор разводят водой до тех пор, пока полоса станет чуть видимой.
Отмечают общий объем кровяной соли K3Fe(CN)6, что обусловливает перевод оставшегося оксигемоглобина в метгемоглобин. Вновь появляется полоса поглощения в красной части спектра. Раствор опять, как и в первый раз, разводят водой и получают величину общего объема повторно (Vi). Расчет ведут по формуле:
где V — первый объем в миллилитрах; Vx — второй объем в миллилитрах.
Одним из перспективных методов лабораторной диагностики является газожидкостная хроматография. Она отличается от других прежде всего высокой специфичностью и чувствительностью, а также быстротой проведения анализа (5—15 мин), малым количеством исследуемого материала, сравнительной простотой выполнения исследований и достаточной их объективностью.
Неотложная помощь при профессиональных интоксикациях, Артамонова В.Г., 1981 г.
