Коагулограмма при апластической анемии
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер.
Коагулограмма (скрининг): показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Показания к назначению исследования
Коагулограмма (гемостазиограмма) – комплексное гематологическое исследование, направленное на оценку состояния системы гемостаза (свертывание крови), или показателей свертывания крови. В систему гемостаза входят клетки крови (тромбоциты) и специфические вещества (факторы свертывания), растворенные в плазме крови и содержащиеся в тромбоцитах. При нарушении целостности стенки сосуда происходит активация свертывающей системы и образуется сгусток крови, препятствующий кровопотере.
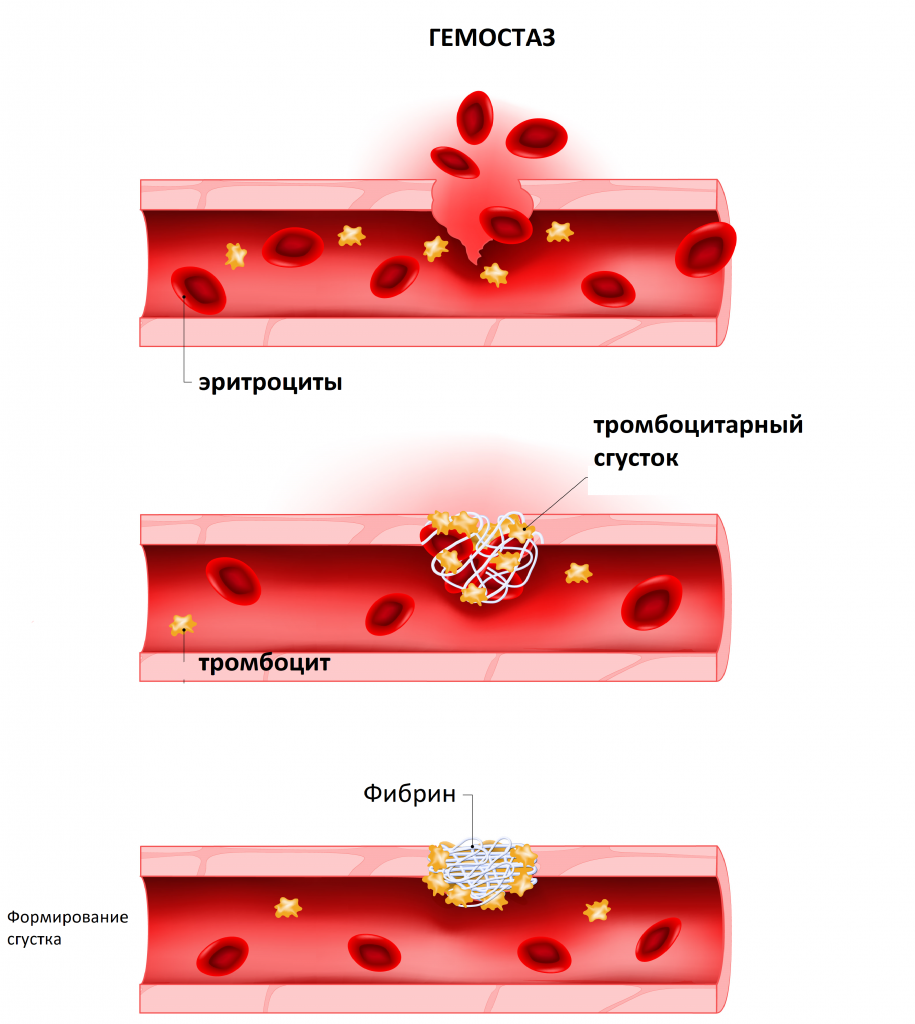
Через некоторое время после остановки кровотечения начинается фибринолиз – процесс растворения тромба после восстановления поврежденной стенки сосуда для возобновления тока крови.
Показаниями к проведению коагулограммы являются состояния, сопровождаемые повышенной кровоточивостью или, наоборот, повышенным тромбообразованием.
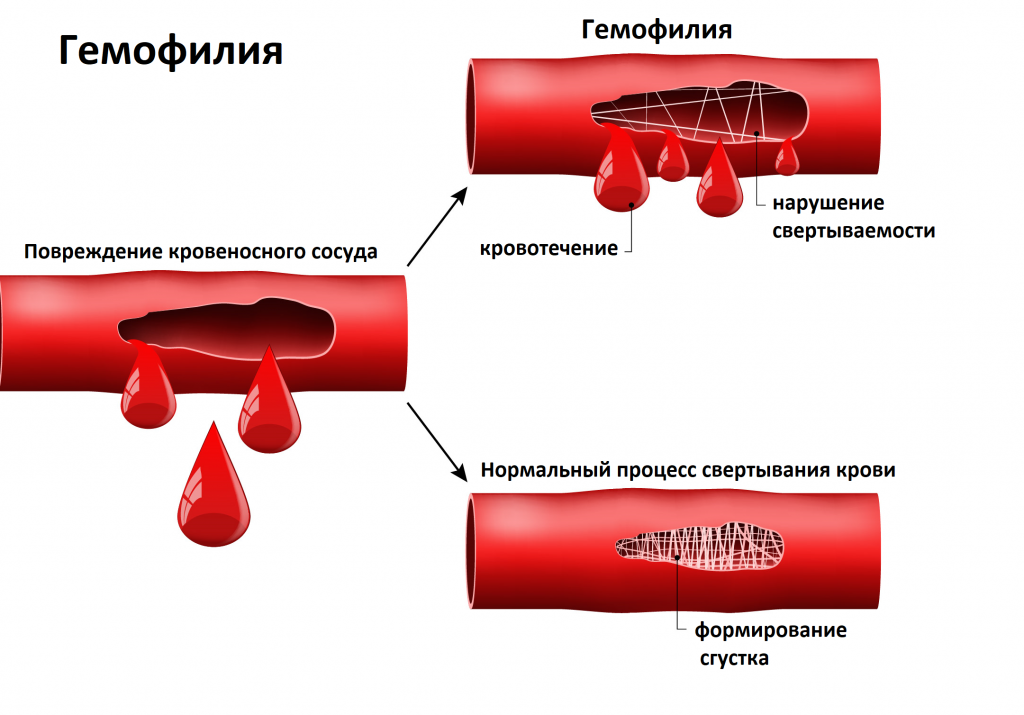
Повышенная кровоточивость приводит к геморрагическому синдрому. Он проявляется образованием гематом, точечных кровоизлияний под кожу (петехий), кровоточивостью слизистых оболочек (носовые кровотечения, кровотечения из десен), появлением примеси крови в кале, моче, длительными менструальными кровотечениями, а также возможными кровоизлияниями во внутренние органы и полости тела. Наиболее грозным проявлением геморрагического синдрома является кровоизлияние в головной мозг – геморрагический инсульт, который может привести к стремительному нарушению функции мозга вплоть до летального исхода. Наследственное заболевание, связанное с нарушением свертывания крови (уменьшение или отсутствие факторов свертывания) называется гемофилия.

Обратная ситуация – тромбоз – это формирование внутри кровеносных сосудов сгустков крови (тромбов), препятствующих свободному току крови.
Риск повышенного тромбообразования имеют люди с ожирением, сахарным диабетом, нарушениями ритма сердца (среди которых наиболее значимы фибрилляция и трепетание предсердий), низкой двигательной активностью, пациенты после крупных операций (например, протезирования суставов, клапанов сердца, экстренных операций и т. п.), с варикозной болезнью, перенесенными инфарктами миокарда, инсультами, с различными аутоиммунными заболеваниями.
Тромбообразование в определенном участке сосудистого русла сопровождается острым или постепенным нарушением кровоснабжения какого-либо органа с нарушением его функций и последующим некрозом тканей.
Помимо вышеперечисленных состояний, коагулограмму выполняют перед операциями для оценки риска кровотечений, при назначении некоторых лекарственных препаратов, а также обязательно при заболеваниях печени, поскольку большая часть белков системы свертывания крови синтезируется именно в этом органе.
Подготовка к процедуре
Суть коагулограммы – оценка активности белков свертывающей системы крови. Поэтому крайне важна правильная подготовка к сдаче данного анализа. Взятие крови осуществляется натощак, последний прием пищи должен быть не менее чем за 8-10 часов до сдачи анализа. Рекомендуется исключить избыточное количество жирной, сладкой и белковой пищи. Питьевой режим остается обычным. Накануне необходимо избегать стрессовых нагрузок, интенсивных занятий спортом.
Если пациент принимает какие-либо лекарственные препараты, влияющие на показатели коагулограммы, то в зависимости от поставленных перед исследованием целей необходимо или продолжить, или за несколько дней прекратить их прием. Это следует обязательно обсудить с лечащим врачом до сдачи анализа.
При необходимости срочного получения результатов можно обратиться в офисы компании ИНВИТРО, где проводится экспресс-диагностика. В этом случае анализ будет готов примерно через 2 часа.
Некоторые из белков свертывающей системы крови относятся к белкам острой фазы. Они вырабатываются во время стресса, к которому относятся не только физическая и эмоциональная нагрузка, но и болезни. Следовательно, любое стойкое или непродолжительное, но интенсивное напряжение организма может приводить к изменению показателей коагулограммы.
Обезвоживание (дегидратация) является одной из причин сгущения крови и увеличения концентрации факторов свертывания, что также приводит к искажению результата.
Состояние свертывающей системы крови меняется во время беременности, как в сторону усиления, так и в сторону ослабления активности ряда белков.
Применение многих лекарственных средств влияет на свертывающую систему крови. Так, первые поколения оральных контрацептивов приводят к повышенному риску тромбообразования, а антикоагулянты – к кровотечениям. Список препаратов, действующих на активность свертывающей системы, огромен. При получении какой-либо медикаментозной терапии предварительно следует проконсультироваться с лечащим врачом о возможном влиянии конкретного препарата на результат исследования.
Прием беременной женщиной некоторых лекарственных препаратов, например, варфарина, рифампицина, фенитоина, барбитуратов, сказывается на выработке факторов свертывания в организме плода. Впоследствии ребенок может быть подвержен высокому риску кровотечений.
Коагулограмма (скрининг)
Гемостазиограмма (коагулограмма), скрининг
Синонимы: Гемостазиограмма, коагулограмма. Coagulation studies (coagulation profile, coag panel, coagulogram).
Краткая характеристика исследования «Гемостазиограмма (коагулограмма), скрининг»
Включает следующие показатели:
Протромбин (протромбиновое время, протромбин (по Квику), МН…
1 360 руб
Гемостазиограмма (коагулограмма) расширенная
Синонимы: Гемостазиограмма.
Coagulation studies (coagulation profile, coag panel, coagulogram).
Краткая характеристика исследования «Гемостазиограмма (коагулограмма) расширенная»
Коагуляционное звено гемостаза:
Протромбин (протромбиновое время, протромбин (по Квику)…
3 790 руб
Сдать коалограмму вы можете в ближайшем медицинском офисе ИНВИТРО. Список офисов, где принимается биоматериал для лабораторного исследования, представлен в разделе «Адреса».
Свертывающая система крови – это в первую очередь ферментативная система, которая обеспечивает внешний, внутренний и общий пути свертывания. Эти механизмы последовательно сменяются, но также они могут протекать независимо друг от друга.
Скрининговая коагулограмма включает в себя следующие показатели:
- протромбин (протромбиновое время, протромбин (по Квику), МНО – международное нормализованное отношение);
- фибриноген;
- АЧТВ (активированное частичное тромбопластиновое время);
- тромбиновое время.
Данные показатели относятся к базовым и позволяют оценить все пути свертывания.
Нормальные показатели
| Показатель | Референсное значение | Единица измерения |
| Протромбиновое время | 9,0–15,0 | сек. |
| Протромбин по Квику | 78–142 | % |
| МНО | зависит от наличия у пациента сопутствующей патологии, по поводу которой он получает терапию антикоагулянтами | |
| АЧТВ | 25,4–36,9 | сек. |
| Тромбиновое время | 10,3–16,6 | сек. |
| Фибриноген | 2,00–4,00 | г/л |
| до 5,6 (2-й и 3-й триместр беременности) | г/л | |
Расшифровка результата
I. Протромбин по Квику, протромбиновое время и международное нормализованное отношение (МНО) отражают активность внешнего пути коагуляции.
- Протромбиновое время – это время свертывания крови после добавления к плазме веществ (тромбопластина с кальцием), запускающих внешний путь свертывания крови. Время измеряется в секундах (сек.). Чем больше протромбиновое время, тем ниже активность факторов свертывания.
- Протромбин по Квику считается более объективным показателем внешнего пути, поскольку в ходе анализа происходит исследование времени свертывания в зависимости от разной концентрации факторов свертывания в крови, получаемой при разведении исследуемого материала в лаборатории. Показатель измеряется в процентах (%). Чем дольше происходит свертывание крови, тем ниже процент протромбина по Квику.
- Международное нормализованное отношение (МНО) – это стандартизованный в соответствии с международными рекомендациями показатель протромбинового теста. Он вычисляется по определенной формуле. Чем выше МНО, тем дольше образуется сгусток крови.
Протромбиновое время, протромбин по Квику и МНО при нормальном содержании и активности фибриногена также отражают активность протромбинового комплекса (II, V, VII, X факторов свертывания крови). При назначении терапии антикоагулянтами из группы антагонистов витамина К (варфарин) происходит увеличение МНО и протромбинового времени и уменьшение протромбина по Квику. Другими причинами данных изменений может быть дефицит витамина К (например, при геморрагической болезни новорожденных), наследственный дефицит II, V, VII, X факторов, заболевания печени и кишечника.
Обратная картина, т. е. снижение МНО, уменьшение протромбинового времени и увеличение протромбина по Квику, имеет место при состояниях, сопровождаемых повышенным свертыванием крови: при тромбозах, сгущении крови при дегидратации, при приеме оральных контрацептивов, барбитуратов.
II. Активированное частичное тромбопластиновое время (АЧТВ) при нормальном содержании и активности фибриногена характеризует внутренний путь свертывания крови, включающий в себя активность II, V, VIII, IX, X, XI, XII факторов. АЧТВ определяют путем добавления в образец крови реагентов, запускающих данный путь свертывания, с измерением времени, необходимого для образования сгустка крови. Измеряется в секундах (сек.). Чем медленнее идет свертывание крови, тем больше АЧТВ.
Данный показатель используют для контроля терапии гепарином (прямой антикоагулянт), при этом отмечается повышение значения АЧТВ. К другим причинам увеличения времени относятся наследственные и приобретенные дефициты факторов свертывания внутреннего пути, например, при гемофилии, геморрагической болезни новорожденных, заболеваниях печени и кишечника, некоторых аутоиммунных болезнях и т. д. Причины повышения АЧТВ те же, что и для протромбина по Квику.
III. Тромбиновое время и фибриноген отражают общий, или конечный путь свертывания крови.
- Фибриноген – фактор свертывания крови I, белок, синтезируемый в печени и превращающийся в фибрин – основу сгустка при свертывании крови. Он также является белком острой фазы. Измеряется в граммах на литр (г/л). При повышенном тромбообразовании, различных воспалительных заболеваниях происходит усиление синтеза этого белка. При заболеваниях печени, наследственном дефиците фибриногена и др. его концентрация снижается.
- Тромбиновое время – время свертывания крови, необходимое для формирования фибринового сгустка при добавлении к плазме тромбина – фермента (фактор IIа), который появляется при взаимодействии факторов свертывания крови при повреждении сосуда. Тромбиновое время зависит от уровня и активности фибриногена. Измеряется в секундах (сек.).
Изменение тромбинового времени в целом коррелирует с уровнем фибриногена. Однако при таком наследственном заболевании, как дисфибриногенемия, т. е. нарушение функциональной активности фибриногена, происходит увеличение тромбинового времени и нарушение свертывания, несмотря на нормальное количество фибриногена в крови.
Дополнительные обследования при отклонении показателей от нормы
При обнаружении отклонений в скрининговой коагулограмме может потребоваться исследование более широкого спектра показателей: Д-димера, антитромбина III, волчаночного антикоагулянта, протеина С, протеина S и т. д.
D-димер (D-dimer)
Синонимы: Фрагмент расщепления фибрина.
D-dimer, Fragment D-dimer, Fibrin degradation fragment.
Краткая характеристика определяемого вещества D-димер
D-димер – маркёр тромбообразования и фибринолиза.
Несмотря на ограниченную специфично…
1 495 руб
Волчаночный антикоагулянт (ВА, Lupus anticoagulants, LA)
Синонимы: Аутоантитела (IgG) против фосфолипидов;
Lupus anticoagulant panel; Lupus inhibitor; LA sensitive PTT; PTT-LA; Dilute Russell viper venom test; DRVVT; Modified Russell viper venom tes; MRVVT.
Краткая характеристика теста «Волчаночный антикоагулянт»
Волчаночный ант…
1 045 руб
Протеин C, % активности (Protein C, % Activity)
Синонимы: Активность протеина C (%); ПС (% активности).
Protein C; PC; Coagulation protein С; Protein C (% Activity).
Краткая характеристика определяемого вещества Протеин C (% активности)
Протеин С – один из наиболее важных физиологических ингибиторов свёртывания. В ак…
1 920 руб
Протеин S свободный (Protein S)
Синонимы: Свободный протеин S; ПрS.
Protein S, Free; Free protein S; fPS. Естественный антикоагулянт, кофактор протеина С.
Краткая характеристика определяемого вещества Протеин S свободный
Протеин S – кофактор протеина C (см. тест № 1263 Протеин C), усиливающий его антикоа…
2 210 руб
Наиболее точную интерпретацию результата коагулограммы может дать врач-гематолог. Однако это исследование для оценки свертывающей системы крови и предупреждения осложнений лечения могут назначить многие специалисты:
терапевт
, педиатр, врач общей практики,
кардиолог
,
акушер-гинеколог
, хирург,
уролог
,
травматолог-ортопед
и пр.
Источники:
- Люлльман Х., Мор К., Хайн Л. Фармакология. Атлас. Пер. с англ. А.А. Свистунова. – Москва: Практическая медицина. 2016.
- Marsdante K.J., Kliegman R.M. Nelson essentials of pediatrics. 8th edition. Elsevier, 2019.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы – 19 лет
Поделитесь этой статьей сейчас
Похожие статьи
ТТГ, тиреотропный гормон
Тиреотропный гормон (ТТГ, тиротропин, Thyroid StimulatingHormone, TSH): показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Атеросклероз
Атеросклероз: причины появления, симптомы, диагностика и способы лечения.
Тремор рук
Тремор рук: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Правила сбора ногтей
Ногти рекомендуется собирать для анализа только в том случае, если отобрать волосы для анализа принципиально невозможно.
Апластическая анемия – угнетение функции кроветворения красного костного мозга (эритроцитопоэза, лейкопоэза и тромбоцитопоэза), приводящее к пангемоцитопении. К основным клиническим проявлениям гематологического синдрома принадлежат головокружение, слабость, обмороки, одышка, покалывание в груди, кожные геморрагии, кровотечения, склонность к развитию инфекционно-воспалительных и гнойных процессов. Заболевание диагностируется на основании характерных изменений гемограммы, миелограммы и гистологического исследования трепанобиоптата. Лечение патологии включает проведение гемотрансфузий, иммуносупрессивной терапии, миелотрансплантации.
Общие сведения
Апластическая (гипопластическая) анемия – тяжелое расстройство гемопоэза (чаще всех его звеньев), сопровождающееся развитием анемического, геморрагического синдромов и инфекционных осложнений. Развивается в среднем у 2 человек на 1 млн. населения в год. Приблизительно с одинаковой частотой патология поражает мужчин и женщин. Возрастные пики заболеваемости приходятся на возраст 10–25 и старше 50 лет. При данной патологии в костном мозге чаще нарушается образование всех трех типов клеточных элементов крови (эритроцитов, лейкоцитов и тромбоцитов), иногда – только одних эритроцитов; в зависимости от этого различают истинную и парциальную апластическую анемию. В гематологии данный вид анемии относится к числу потенциально фатальных заболеваний, приводящих к гибели 2/3 заболевших.

Апластическая анемия
Причины
По происхождению апластическая анемия может быть врожденной (связанной с хромосомными аберрациями) и приобретенной (развившейся в течение жизни). Принято считать, что угнетение миелопоэза связано с появлением в красном костном мозге и крови цитотоксических T-лимфоцитов, производящих фактор некроза опухолей и γ-интерферон, которые в свою очередь подавляют ростки кроветворения. Запускать этот механизм могут различные внешнесредовые (химические соединения, физические явления, лекарственные вещества), а также эндогенные факторы (вирусы, аутоиммунные реакции). К числу наиболее значимых причин относят:
- Прием миелотоксических препаратов. Достоверно установлена связь анемии с приемом некоторых противоопухолевых, противосудорожных, антибактериальных, антитиреоидных, противомалярийных препаратов, транквилизаторов, препаратов золота и др., обладающих потенциальным миелотоксическим эффектом. Лекарственные вещества могут вызывать как прямое повреждение стволовых кроветворных клеток, так и опосредованное – через аутоиммунные реакции. Анемии, связанные с таким механизмом развития, называются лекарственными.
- Контакт с химическими и физическими агентами. Супрессию костного мозга может вызывать взаимодействие с органическими растворителями, соединениями мышьяка, бензольными соединениями, пестицидами, облучение всего тела. В некоторых случаях недостаточность гемопоэза является временной и обратимой – главными факторами здесь являются концентрация/доза вещества и время контакта. супрессию костного мозга.
- Вирусные инфекции. Из вирусных агентов наибольшее значение уделяется возбудителям гепатитов В, С и D. В этом случае гипопластическая анемия обычно развивается в течение полугода после перенесенного вирусного гепатита. При изучении патогенеза было замечено, что репликация вируса происходит в мононуклеарах крови и костного мозга, а также в иммунных клетках. Предполагается, что подавление миелопоэза в этом случае является своеобразным иммунным ответом, возникающим против клеток, несущих на своей поверхности вирусные антигены. Такой вид анемии выделяется в отдельную форму – постгепатитную. Среди других вирусных инфекций называются ЦМВ, инфекционный мононуклеоз, грипп.
Также описаны случаи панцитопении, вызванные инфицированием туберкулезом, интоксикацией, лучевой болезнью, лимфопролиферативными заболеваниями (тимомой, лимфомой, хроническим лимфобластным лейкозом), беременностью. Почти в половине наблюдений причину анемии выявить не удается – такие случаи относят к идиопатической форме.
Патогенез
В основе апластической анемии может лежать либо первичное повреждение гемопоэтических стволовых клеток, либо нарушение их эффективной дифференцировки. При наследственных анемиях недостаточность гемопоэза опосредована кариотипическими аберрациями, приводящими к нарушению репарации ДНК и невозможности репликации стволовых клеток костного мозга. В случае приобретенной анемии под влиянием этиофакторов наблюдается активация Т-клеток, которые начинают продуцировать цитокины (интерферон-гамма, ФНО), поражающие клетки-предшественники гемопоэза. В стволовых клетках костного мозга повышается экспрессия генов, отвечающих за апоптоз и активизацию клеточной гибели. Основные клинические проявления обусловлены пангемоцитопенией – снижением в составе крови всех ее форменных элементов (эритроцитов, лейкоцитов, тромбоцитов).
Классификация
Кроме различных этиологических вариантов (лекарственного, постгепатитного, идиопатического), различают острую (до 1 мес. течения), подострую (от 1 до 6 мес.) и хроническую (более 6 мес.) форму заболевания. Анемию, протекающую с избирательным угнетением эритропоэза, называют парциальной красноклеточной аплазией. На основании выраженности тромбо- и гранулоцитопении данная форма анемии подразделяется на 3 степени тяжести:
- очень тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,2х109/л)
- тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,5х109/л), по данным трепанобиопсии – низкая клеточность костного мозга (менее 30% от нормы)
- умеренную (тромбоцитов более 20,0х109/л; гранулоцитов более 0,5х109/л)
Симптомы апластической анемии
Поражение трех гемопоэтических ростков (эритро-, тромбоцито- и лейкопоэза) обусловливает развитие анемического и геморрагического синдромов, инфекционных осложнений. Дебют апластической анемии обычно происходит остро. Анемический синдром сопровождается общей слабостью и утомляемостью, бледностью кожи и видимых слизистых, шумом в ушах, головокружением, покалыванием в груди, одышкой при нагрузке.
Основным проявлением тромбоцитопении выступает геморрагический синдром. Больные отмечают появление петехий и экхимозов на коже, повышенную кровоточивость десен, спонтанные носовые кровотечения, меноррагии. Возможно возникновение гематурии, маточных и желудочно-кишечных кровотечений. Следствием лейкопении и агранулоцитоза служит частое развитие инфекционных процессов – стоматитов, пневмоний, инфекций кожи и мочевыводящих путей. Для апластической анемий нехарактерны похудание, лимфаденопатия, гепато- и спленомегалия – при этих признаках следует искать другую причину пангемоцитопении.
Врожденная апластическая анемия (синдром Фанкони) обычно развивается у детей в возрасте до 10 лет и кроме аплазии костного мозга характеризуется другими нарушениями: микроцефалией, гипоплазией почек, низкорослостью, аномалиями развития верхних конечностей (гипоплазией первой пястной и лучевой кости), гипоспадией, гиперпигментацией кожи, крайней степенью тугоухости и др. При наследственной анемии Эстрена-Дамешека отмечается тотальное поражение кроветворения и панцитопения при отсутствии врожденных аномалий развития. Для анемии Даймонда-Блекфена или парциальной красноклеточной аплазии характерно только снижение количества эритроцитов.

Экхимозы на коже при апластической анемии
Осложнения
Летальный исход может быть обусловлен кровоизлияниями во внутренние органы, массивными кровотечениями, инфекционными осложнениями, анемической комой. Наиболее грозное из геморрагических осложнений – кровоизлияние в головной мозг (геморрагический инсульт). Больные склонны к частым и тяжело протекающим вирусным и бактериальным инфекциям респираторного тракта. Значительное или стремительное снижение уровня красных кровяных телец может привести к анемической коме. При молниеносной форме крайне быстро развиваются тяжелейшая анемия, иммунодефицит, коагулопатии, имеющие фатальные последствия.
Диагностика
Оценка гематологического статуса включает внимательный клинический осмотр и проведение тщательной лабораторной диагностики. При физикальном обследовании выявляется выраженная бледность или желтушность кожи, артериальная гипотония, тахикардия. Основу диагностического алгоритма составляет проведение общего и биохимического анализа крови, стернальной пункции, трепанобиопсии:
- Исследования крови. Для гемограммы при гипопластической анемии типичны эритро-, лейкоцито- и тромбоцитопения, нейтропения и относительный лимфоцитоз. Оценка биохимических показателей (печеночных проб, нефрологического комплекса, сывороточного железа, билирубина) информативна для исключения других анемий.
- Исследование пунктата костного мозга. В миелограмме обнаруживается уменьшение количества миелокариоцитов и мегакариоцитов, снижение клеточности. В трепанобиоптате определяется замещение красного костного мозга жировым (желтым).
В рамках диагностического поиска апластическую анемию необходимо дифференцировать с мегабластными (В12-дефицитными, фолиеводефицитными) анемиями, идиопатической тромбоцитопенической пурпурой, пароксизмальной ночной гемоглобинурией, острым лейкозом.

Миелограмма: слева – апластическая анемия, справа – нормальный костный мозг
Лечение апластической анемии
Больные с апластической анемией госпитализируются в специализированные отделения. Им обеспечиваются полная изоляция и асептические условия для предупреждения возможных инфекционных осложнений. Проведение эффективного лечения является сложной проблемой практической гематологии. В зависимости от уровня цитопении используются следующие лечебные подходы:
- Иммуносупрессиная терапия. При умеренной цитопении назначается фармакотерапия, включающая комбинацию антитимоцитарного иммуноглобулина и циклоспорина А. Поддерживающая терапия проводится анаболическими стероидами или их сочетанием с циклоспоринами.
- Гемотрансфузии. В комплексе с курсом иммуносупрессивной терапии при низких показателях красной крови показано проведение заместительной гемотрансфузионной терапии (переливание тромбоцитов и эритроцитарной массы), плазмафереза. Данная мера не оказывает воздействия на патогенетическое звено заболевания, но позволяет восполнить дефицит кровяных телец, не вырабатываемых костным мозгом.
- Трансплантация КМ и СК. Наиболее благоприятные прогнозы на долгосрочную выживаемость оказывает выполнение аллогенной трансплантации костного мозга. Однако ввиду сложности подбора иммунологически совместимого донора процедура используется ограниченно. В качестве экспериментальных подходов рассматриваются аутологичные трансплантации, пересадка стволовых клеток периферической крови. Больным с нетяжелой формой анемии может быть показано проведение спленэктомии, эндоваскулярной окклюзии селезеночной артерии.
Прогноз и профилактика
Прогноз определяется этиологической формой, тяжестью и остротой течения анемии. Критериями неблагоприятного исхода служат быстрое прогрессирование заболевания, тяжелый геморрагический синдром и инфекционные осложнения. После трансплантации костного мозга ремиссии удается достичь у 75–90% пациентов. Первичная профилактика данной разновидности анемии предполагает исключение влияния неблагоприятных внешнесредовых факторов, необоснованного применения лекарственных препаратов, предупреждение инфекционной заболеваемости и др. Пациентам с уже развившимся заболеванием требуется диспансерное наблюдение гематолога, систематическое обследование и длительная поддерживающая терапия.
