Компенсаторно приспособительные реакции при анемии
Все
анемии сопровождаются развитием
гемической гипоксии. Срочная
адаптация:
5. Приспособительные
реакции системы внешнего дыхания:
увеличение
альвеолярной вентиляции за счет
углубления и учащения дыхания и
мобилизации резервных альвеол (вызывает
развитие дыхательного алкалоза, кривая
диссоциации НЬОг сдвигается влево и
оксигенация крови улучшается);увеличение
легочного кровотока и повышение
перфузионного давления в капиллярах
легких;возрастание
проницаемости альвео-калиллярных
мембран для газов.
6.Приспособительные
реакции в системе кровообращения:
развитие
тахикардии, увеличение ударного и
минутного объемов сердца;увеличение
массы циркулирующей крови за счет
выброса из кровяного депо;увеличение
системного артериального давления и
скорости кровотока;расширение
сосудов (под влиянием СО2, рН, аденозина).
7. Приспособительные
реакции системы крови:
усиление
диссоциации оксиНЬ за счет ацидоза;повышение
кислородной емкости крови за счет
усиления вымывания эритроцитов
из костного мозга;
8.Тканевые
приспособительные реакции:
ограничение
функциональной активности органов и
тканей, непосредственно
не участвующих в обеспечении транспорта
кислорода;увеличение
сопряжения окисления и фосфорилирования
и активности ферментов
дыхательной цепи;усиление
анаэробного синтеза АТФ за счет активации
гликолиза (накапливается
лактат, рН смещается в кислую сторону,
а кривая Баркрофта – вправо, НЪС>2
легче диссоциирует, отдавая кислород).
Долговременная
адаптация:
увеличение
силы дыхательных мышц и дыхательной
поверхности легких;гипертрофия
миокарда;активация
эритропоэза за счет усиления образования
эритропоэтинов в почках и,
возможно, других органах;увеличение
массы митохондрий.
163
3.2. Лейкоцитозы и лейкопении. Лейкозы.
Лейкоциты
–
это гетерогенная группа клеток, которые
являются основой антимикробной
защиты организма (рис. 3.2Л.)
В
клинической практике лейкоциты обычно
группируют в соответствии с морфологией
клеточного ядра (полиморфно-ядерные
и мононуклеарные) или по наличию
цито-плазматических включений (гранулоциты
и агранулоциты). Базофилы,
эозинофилы и ней-трофилы –
полиморфно-ядерные гранулоциты; лимфоциты
и моноциты –
мононуклеарные агранулоцитарные
лейкоциты.
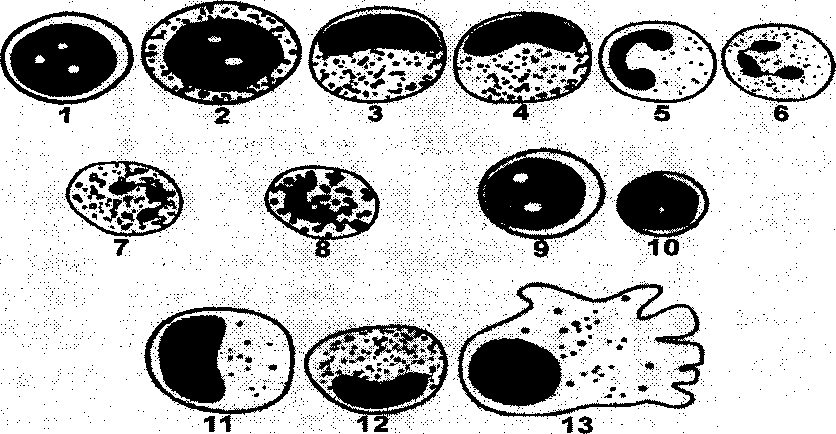
Рис.
3.2.1. Схематическое изображение различных
видов лейкоцитов. 1 – миелобласт*, 2 –
промие-лоцит,
3 – миелоцит, 4 – метамиелоцит, 5 – «юный»
или палочко-ядерный нейтрофил, 6 –
сегменто-ядерный нейтрофил,
7 – эозинофил, 8 – базофил, 9 – лимфобласт*,
10 – «зрелый» лимфоцит, 11 – промоноцит*,
12 -моноцит,
13 -макрофаг*.
*
– У
здоровых людей эти клетки локализуются
в костном мозге и обычно в мазках
периферической крови не встречаются.
Нейтрофилы
(молодые
формы – миелоциты, метамиелоцит («юные),
палочко-ядерные; зрелые формы –
сегментоядерные) представляют собой
самую большую группу циркулирующих
лейкоцитов. В крови нейтрофилы находятся
около 6-8 ч?
а затем мигрируют во внесосудистое
пространство. В очагах инфекции они
распознают, захватывают и уничтожают
бактерии.
Эозинофилы
играют
особую роль в борьбе с паразитами и
контроле аллергии; способны к хемотаксису,
фагоцитозу и обладают бактерицидной
активностью.
Базофилы
–
самая малочисленная группа циркулирующих
гранулоцитов; опосредуют аллергические
реакции, особенно 1§Е-зависимые.
Моноциты
проводят
в кровотоке всего около 20 ч, далее
мигрируют в периваску-лярные пространства,
где трансформируются в макрофаги
ретикулоэндотелиальной системы
(РЭС). Моноциты и макрофаги – долгоживущие
клетки, функциональные особенности
которых во многом схожи с таковыми у
гранулоцитов. Они более эффективно
захватывают и поглощают микобактерии,
грибки и макромолекулы; менее значима
их роль в фагоцитозе пиогенных бактерий.
В селезенке макрофаги ответственны за
утилизацию сенсибилизированных и
стареющих эритроцитов. Макрофаги играют
важную роль в про-цессинге и представлении
антигенов лимфоцитам в ходе клеточных
и гуморальных иммунных реакций.
Лимфоциты
–
небольшие мононуклеарные клетки,
осуществляющие иммунный. Лимфоциты
подразделяются на В-, Т-клетки и
клетки-киллеры. Подгруппы лимфоцитов
164
отличаются
по месту их образования и эффекторным
молекулам, но имеют общее свойство
– способность опосредовать высокоспецифический
антигенный ответ.
В
1 л крови здорового человека содержится
4-
9*109
лейкоцитов. Увеличение
концентрации лейкоцитов – лейкоцитоз,
снижение.—
лейкопения.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Анемия – это
патологическое состояние, характеризующееся
уменьшением содержания эритроцитов и
гемоглобина или каждого из них в
отдельности в единице объёма крови. Это
может наблюдаться в силу следующих
причин: кровопотерь (постгеморрагические
анемии), нарушений кроветворения
(дисгемопоэтические анемии),
усиленного гемолиза эритроцитов
(гемолитические анемии). Различают
острую и хроническую постгеморрагические
анемии. Гемолитические анемии бывают
приобретёнными и наследственными (рис.
15.1).
Основным звеном
в патогенезе анемий является развитие
гемической и тканевой гипоксии.
Потребность организма в кислороде в
этих условиях возмещается
компенсаторно-приспособительными
реакциями (КПР): дыхательными,
гемодинамическими, гемическими, тканевыми
и гематогенными.
Дыхательные КПР
заключаются в усилении лёгочной
вентиляции. Эффекты гемодинамических
КПР проявляются в учащении сердечного
ритма (тахикардии), возрастании ударного
и минутного объёмов сердца, повышении
тонуса кровеносных сосудов, мобилизации
крови из естественных депо. Тканевая
жидкость переходит в сосудистое русло
(гемодилюция), увеличивая объём
плазмы. Кровь перераспределяется в
пользу головного мозга, сердца, лёгких,
почек.
К гемическим КПР
относятся понижение вязкости крови
вследствие гемодилюции, и увеличение
диссоциации оксигемоглобина, что
облегчает отдачу кислорода тканями. В
клетках возрастает активность
митохондриальных ферментов
(цитохромоксидаз). Одновременно
интенсифицируется гликолиз.
Своевременное и
полноценное развитие гематогенных
КПР при анемиях зависит от регенераторных
возможностей костного мозга. Анемии по
состоянию костномозгового кроветворения
подразделяют на регенераторные,
гипорегенераторные, гипо- и апластические.
При регенераторной
анемии в красном костном мозге
увеличивается количество эритроидных
островков. Их число возрастает также в
жёлтом костном мозге. Экстрамедуллярные
островки гемопоэза обнаруживаются в
печени, лимфоидной и соединительной
ткани. В периферической крови появляются
эритробласты, нормобласты,
ретикулоциты. Их называют клетками
физиологической регенерации эритроцитов.
К регенераторным анемиям относят
острую постгеморрагическую анемию и
большинство приобретённых гемолитических
анемий.
Гипорегенераторное
состояние эритропоэза характеризуется
его неэффективностью, что обусловливает
выход в периферическую кровь клеток
патологической регенерации эритроцитов.
К ним относятся эритроциты с зернистостью
цитоплазмы, остатками ядер или ядерных
оболочек. Дегенеративные формы эритроцитов
– это клетки различных размеров (анизоциты)
и формы (пойкилоциты), эритроциты с
изменённым содержанием гемоглобина
(гипо- или гиперхромные).
Причиной развития
гипо- и аплазии костного мозга является
действие факторов, подавляющих
костномозговое кроветворение
(миелотоксические факторы). К ним
относятся: ионизирующая радиация,
бензол, противоопухолевые препараты,
нерациональный приём некоторых
лекарственных веществ, например,
сульфаниламидов, производных пиразолона,
антибиотиков (особенно левомицетина).
Угнетение гемопоэза проявляется в
недостаточном образовании всех форменных
элементов крови – панцитопении.
Гипорегенераторными
анемиями являются хроническая
постгеморрагическая анемия,
дисгемопоэтические и наследственные
гемолитические анемии. Они часто
осложняются гипо- и апластическими
кризами.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
1. Регенерация Регенерация – восстановление структурных элементов ткани взамен погибших.
В биологическом смысле регенерация представляет собой приспособительный процесс, выработанный в ходе эволюции и присущий всему живому.
Различают три вида регенерации:
– физиологическую (образующиеся клетки дифференцируются и заменяют потерянные в процессе нормальной жизнедеятельности клетки);
– репаративную (восстановление клеток и тканей взамен погибших в результате различных патологических процессов);
– патологическую (извращение регенераторного процесса, нарушение смены фаз пролиферации и дифференцировки).
Морфогенез регенераторного процесса складывается из двух фаз – пролиферации и дифференцировки. В фазу пролиферации размножаются молодые, недифференцированные клетки. Эти клетки называются камбиальными, стволовыми клетками или клетками-предшественниками. В фазу дифференцировки молодые клетки созревают, происходит их структурно-функциональная специализация.
Клетки организма на основании их регенераторной способности делятся на три группы:
– лабильные (делятся активно в течение всей жизни, являясь источником для восстановления клеток, которые непрерывно погибают);
– относительно стабильные (имеют длительный срок существования и поэтому характеризуются низкой митотической активностью);
– постоянные (не имеют никакой способности митотического деления в постнатальной жизни).
Регенерация кровеносных сосудов протекает неоднозначно в зависимости от калибра. Регенерация сосудов микроциркуляторного русла – капилляров, венул, артериол – может происходить путем почкования или аутогенно. Крупные сосуды не обладают достаточными пластическими свойствами. Поэтому при повреждении их стенки восстанавливаются лишь структуры внутренней оболочки, ее эндотелиальная выстилка. Элементы средней и наружной оболочек восстанавливаются за счет рубцевания.
Регенерация соединительной ткани. Процесс заживления дефекта ткани путем формирования рубца делится на несколько стадий:
– подготовка (удаление некротического детрита);
– разрастание грануляционной ткани (фаза пролиферации клеток – грануляционная ткань заполняет поврежденную область, по мере того как некротический детрит удаляется);
– синтез фибронектина;
– созревание (содержание коллагена прогрессивно увеличивается со временем);
– сокращение и уплотнение (заключительная стадия заживления путем формирования рубца).
Регенерация эпителия осуществляется полностью, так как он обладает высокой регенераторной способностью. Осуществляется по типу регенерационной гипертрофии: в участках повреждения ткань замещается рубцом, а по периферии его происходит гиперплазия и гипертрофия клеток паренхимы. В железах внутренней секреции восстановительные процессы представлены неполной регенерацией.
Заживление ран кожи
Типы повреждений кожи: ссадина, разрез и разрыв; раны с дефектами эпидермиса.
Заживление первичным натяжением (чистые резаные и рваные раны, в которых края раны находятся на близком расстоянии друг от друга).
Заживление вторичным натяжением (в рваных ранах, когда невозможно добиться сопоставления краев раны; когда в ране присутствует чужеродный материал; когда произошел обширный некроз тканей; когда рана инфицирована).
Факторы, нарушающие процесс регенерации:
– нарушение синтеза коллагена;
– наличие чужеродных частиц, некротической ткани;
– инфекция;
– нарушение кровотока;
– уменьшение жизнеспособности клеток; сахарный диабет; чрезмерный уровень;
– группа редких наследственных нарушений, в основе которых лежит нарушение формирования коллагена.
Регенерация костной ткани при переломе костей может происходить двумя путями в виде:
– первичного костного сращения (при неосложненном костном переломе, когда костные отломки хорошо сопоставлены и неподвижны, отсутствует инфекция);
– вторичного костного сращения (при нарушении местных условий регенерации кости – расстройства кровообращения, обширные оскольчатые диафизарные переломы, подвижность отломков).
Регенерация ЦНС. В головном мозге новообразования нейроцитов не происходит.
Регенерация периферического нерва происходит за счет центрального отрезка, сохранившего связь с клеткой.
Регенерация мышечной ткани. Гладкие мышцы при небольших дефектах могут регенерировать достаточно полно. При больших повреждениях гладких мышц происходит рубцевание (неполная регенерация). Поперечнополосатые мышцы регенерируют лишь при сохранении сарколеммы путем почкования.
2. Организация Организация – это процесс замещения соединительной тканью нежизнеспособных тканей и инородных тел, когда массы подвергаются рассасыванию и одновременно в них врастает молодая соединительная ткань, превращающаяся затем в рубцовую.
3. Метаплазия Метаплазия – это переход одного вида ткани в другой в пределах одного зародышевого листка. Метаплазия возникает из-за неправильной дифференцировки стволовых клеток. “Новая” метапластическая ткань структурно нормальна, так как имеется четкая клеточная организация. Метаплазия обратима.
Чтобы организм мог полноценно функционировать, он должен постоянно адаптироваться к изменениям, которые происходят в окружающем мире и внутри него. Этот процесс получил название компенсаторно-приспособительных реакций. Подробнее о его разновидностях, этапах, стадиях и особенностях нарушения далее в статье.
Понятие компенсации, реакции и механизма
Чтобы свободно ориентироваться и понимать данную проблему, следует различать понятия компенсации в целом, компенсаторно-приспособительных реакций и компенсаторных механизмов.
В широком смысле “компенсация” – физиологическое свойство организма, основной целью которого является восстановление его внутреннего постоянства для дальнейшего осуществления своих обычных функций. Вне зависимости от особенностей внешних раздражителей (болевых, температурных и прочих) механизмы компенсации универсальны. Есть лишь незначительные отличия в скорости включения компенсации, степени включения в работу высших нервных центров (коры головного мозга) и так далее.
Компенсаторно-приспособительные реакции организма – это первичные сдвиги в его работе, которые направлены на полное устранение или ослабление нарушенных функций вследствие воздействия экстремальных условий окружающей среды.
Компенсаторные механизмы – это последовательность изменений в организме, которые возникают быстро и динамично сменяют друг друга. Они развиваются на различных уровнях – от молекулы до целого организма.
Основные разновидности
В зависимости от уровня развития соответствующих изменений выделяют такие виды компенсаторно-приспособительных реакций:
- Внутриклеточные – изменения возникают внутри клетки вследствие напряжения функции ее элементов (митохондрий, лизосом, аппарата Гольджи и прочее).
- Тканевые – развитие изменений на уровне ткани.
- Органные – изменение функции отдельного органа.
- Системные – возникновение приспособительных реакций на уровне нескольких органов, которые входят в одну систему (дыхательную, сердечно-сосудистую, пищеварительную и прочее).
- Межсистемные – изменения сразу ряда систем органов вплоть до всего организма.
Наибольшее распространение в клинической практике получили виды компенсаторно-приспособительных реакций в зависимости от характера изменений, которые происходят в определенных структурах:
- регенерация;
- атрофия;
- гипертрофия;
- гиперплазия;
- метаплазия;
- перестройка тканей;
- организация;
- дисплазия.
Подробнее о некоторых видах рассказано в соответствующих разделах.
Стадии развития
Выделяют три стадии развития компенсаторно-приспособительных реакций:
- становления;
- относительно устойчивого компенсирования функций;
- декомпенсации.
На первой стадии происходит максимальная активация процессов организма. При этом изменения наблюдаются на всех уровнях: от клетки до систем органов. Но с ростом функциональной активности органа происходит его истощение и распад элементов. Поэтому необходима максимальная мобилизация всех резервных структур в организме.
На этапе относительно устойчивой компенсации наблюдается перестройка структуры органа. Он меняется таким образом, чтобы иметь возможность обеспечить устойчивую компенсацию на протяжении как можно более длительного времени. Орган при этом пропитывается сосудами, число клеток растет, как и их размеры.
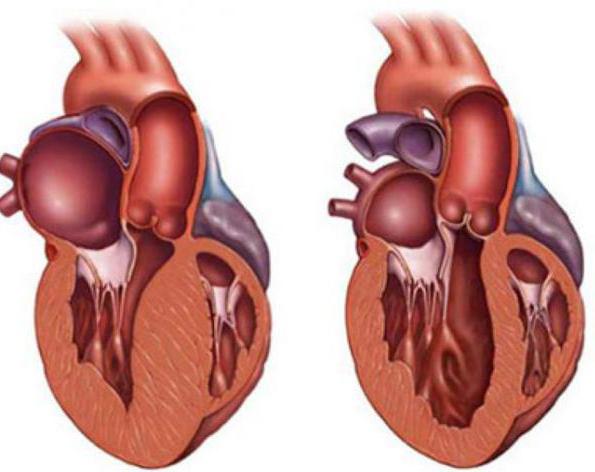
Вследствие этого орган увеличивается, что получило название гипертрофии. Примером может быть гипертрофическое сердце у спортсменов. Необходимость перекачать больше крови, чтобы снабдить ею активно работающие мышцы, приводит к увеличению размеров сердечной мышцы.

Последняя стадия компенсаторно-приспособительных реакций – декомпенсации – получила такое название, так как проявляется нарушением функции. Она возникает, когда причина компенсации не была устранена вовремя. Резерв организма постепенно истощается. Энергии, которая вырабатывается в нем, становится недостаточно для гипертрофированного органа. В итоге постепенно нарушается обмен веществ, пораженный орган перестает функционировать, а за ним начинают страдать и другие органы и системы.
Особенности регенерации
Теперь пришло время разобрать особенности отдельных видов компенсаторно-приспособительных реакций. Гипертрофия – одна из самых распространенных разновидностей. Она заключается в возобновлении структурных элементов ткани и органа. Это происходит вследствие роста новых элементов на месте поврежденных. Существует три вида гипертрофии:
- физиологическая;
- патологическая;
- репаративная.
Физиологическая регенерация – это нормальный процесс в человеческом организме. Клетки не бессмертны, каждая из них имеет определенный срок жизни. Например, эритроциты (красные клетки крови) живут до 120 дней. На месте погибших постоянно образовываются новые клетки, которые дифференцируются из стволовых клеток в костном мозге.
Репаративная регенерация
Суть репаративной регенерации соответствует таковой при физиологической. Но репаративная характерна только для патологических процессов. Она характеризуется более быстрой активацией механизмов адаптации, мобилизацией резервов организма. То есть, по сути своей, репаративная регенерация – это более быстрая и мощная версия физиологической.
Существует два вида репаративной регенерации: полная и неполная. Полная еще получила название реституции. Она характеризуется тем, что погибшая ткань замещается абсолютно идентичной ей структурой. Это свойственно в первую очередь регенерации на клеточном уровне. Неполная регенерация, или субституция, заключается в замещении погибшей структуры на соединительную ткань. Клинически это выглядит как рубец.
Патологическая регенерация, соответственно своему названию, является одним из вариантов патологии компенсаторно-приспособительных реакций. Она возникает вследствие нарушения механизмов регенерации. Примером может служить развитие келоидных рубцов, невромы при травме – чрезмерные разрастания поврежденных нервов, слишком большие костные мозоли при переломе.

Особенности гипертрофии
Еще один достаточно распространенный вариант компенсаторно-приспособительной реакции организма при патологии и в норме – это гипертрофия. Она заключается в увеличении размера ткани или всего органа из-за роста размеров клеток. Выделяют несколько разновидностей гипертрофий:
- рабочая;
- викарная;
- гормональная;
- гипертрофические разрастания.
Рабочая разновидность гипертрофии встречается как у здоровых людей, так и при патологии. Примером физиологической гипертрофии может быть увеличение сердца у спортсменов, о котором уже упоминалось ранее. Так как этот орган выполняет повышенную функцию у спортивных людей и лиц, которые занимаются тяжелым физическим трудом, его клетки постепенно увеличиваются в размерах, что приводит к утолщению миокарда (сердечной мышцы).
Рабочая гипертрофия сердца возникает при патологии, причем причины могут быть как интракраниальные (внутри сердца), так и экстракраниальные (вне его). К первой группе относят воспаления сердечной стенки, врожденные и приобретенные пороки клапанов сердца. Функция органа при этих патологиях страдает. Поэтому, чтобы хоть как-то обеспечить внутренние органы необходимым количеством крови, развивается гипертрофия.
Ярким примером экстракраниальных причин является артериальная гипертензия. Это состояние, которое характеризуется повышенным артериальным давлением. высокое давление создает сопротивление выталкиваемой крови из сердца. Органу приходится прикладывать больше усилий, чтобы вытолкнуть ее наружу, что и вызывает гипертрофию.
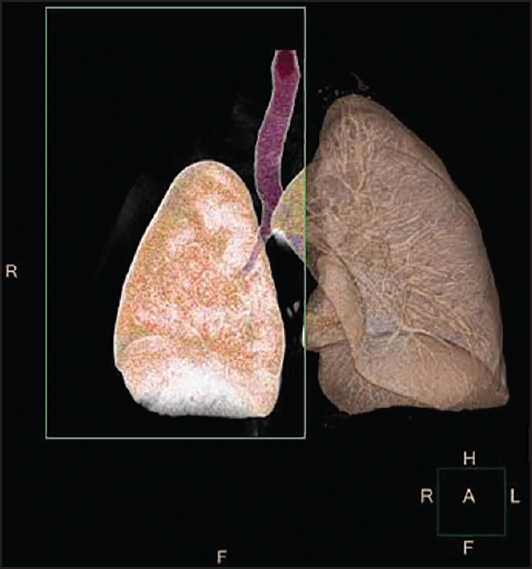
Викарная и гормональная гипертрофии
Викарная разновидность гипертрофии развивается при удалении одного из парных органов. Например, у человека, которому удалили одного легкое, оставшееся постепенно вырастает до очень больших размеров. Это необходимая мера, чтобы обеспечить организм достаточным количеством кислорода.
Гормональная гипертрофия также может быть в норме и при патологии. В ее развитии принимают участие биологически активные вещества (гормоны). Один из примеров – гипертрофия матки во время беременности. Это происходит под влиянием гормона прогестерона.
Патологическая гипертрофия развивается при нарушении функции желез внутренней секреции. Например, при повышенной выработке соматотропного гормона гипофизом развивается акромегалия. При этом акральные (конечные) части туловища увеличиваются в размерах. Чаще всего вырастает непропорционально большая рука или нога.
Особенности гиперплазии
Если гипертрофия – это увеличение размеров органа за счет роста отдельной клетки, то гиперплазия возникает вследствие увеличения количества клеток. Механизм развития компенсаторно-приспособительной реакции по типу гиперплазии заключается в увеличении частоты делений клеток (митозов). Это приводит к прогрессирующему росту их числа.
Различают три вида гиперплазии:
- реактивная, или защитная;
- гормональная;
- заместительная.
Первый вид гиперплазии развивается в органах, которые принимают участие в иммунном ответе организма при попадании чужеродных агентов – вилочковой железе, лимфатических узлах, селезенке, костном мозге и прочее. Например, при гемолизах (разрушении эритроцитов) или хронической гипоксии у людей, которые живут высоко в горах, наблюдается гиперплазия эритроцитарного ростка в костном мозге. Вследствие этого у них вырабатывается больше эритроцитов, чем у других людей.
Гормональная гиперплазия возникает под воздействием биологически активных веществ. Например, у женщин при беременности увеличивается грудь именно по такому принципу. Еще один пример – гиперплазия эндометрия (внутреннего слоя матки) перед менструацией.
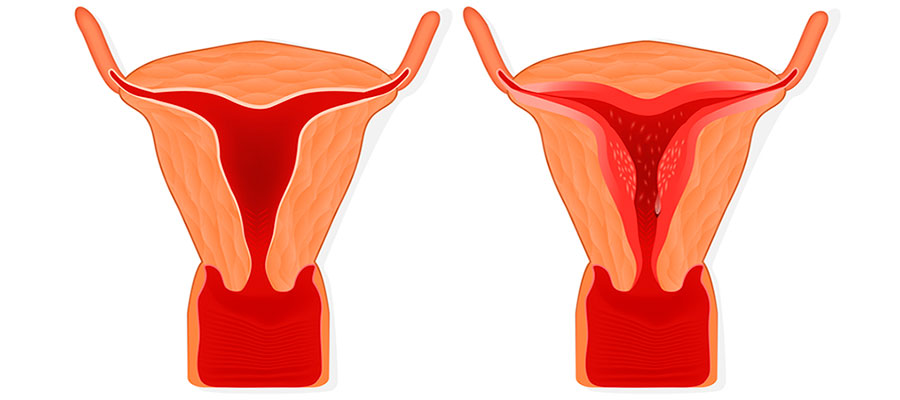
Гиперплазия может быть и патологической. При гиперплазии желез внутренней секреции они начинают слишком активно синтезировать гормоны, что приводит к развитию различных заболеваний. Например, при гиперплазии надпочечников возникает болезнь Иценко-Кушинга, щитовидной железы – тиреотоксический зоб.
Особенности изменений в организме при гипоксии
Гипоксия (снижение концентрации кислорода в тканях) – одно из наиболее шоковых состояний для организма. Головной мозг может функционировать без кислорода в среднем 6 минут, после чего наступает его смерть. Поэтому во время гипоксии организм тут же мобилизуется, чтобы обеспечить внутренние органы максимально возможным количеством кислорода.
Основной механизм компенсаторно-приспособительной реакции организма при гипоксии – активация симпато-адреналовой системы. Она характеризуется выбросом адреналина и норадреналина надпочечниками в кровяное русло. Это приводит к развитию нескольких процессов:
- увеличению частоты сердечных сокращений (тахикардии);
- спазму периферических сосудов;
- повышению артериального давления.
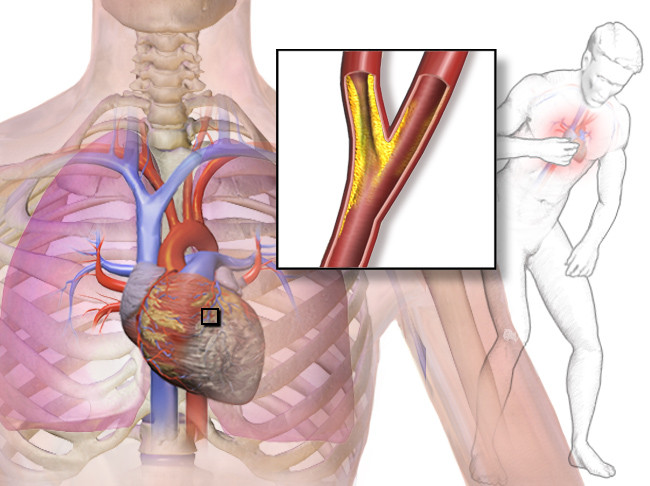
За счет спазма периферических сосудов возникает феномен централизации кровообращения. Благодаря этой компенсаторно-приспособительной реакции при гипоксии кровь поступает к наиболее важным для жизни органам: головному мозгу, сердцу и надпочечникам.
Но длительное время компенсация происходить не может. Если не устранить причину гипоксии вовремя, сердцебиение замедляется, а давление падает.
Принципы компенсации
Компенсаторно-приспособительные реакции организма не развиваются хаотично. Как уже было отмечено выше, они универсальны вне зависимости от вида раздражителя. Поэтому ученые выделили ряд правил, согласно которым организм приспосабливается к этим условиям.
| Правило | Краткое пояснение |
| Наличие исходного фона | Особенности механизмов компенсаторно-приспособительных реакций напрямую зависят от исходного состояния регуляторных систем и метаболизма конкретного индивидуума |
| Компенсаторной регенерации клеток и увеличения ткани в размерах (гиперплазии) | Способность ткани к восстановлению и росту зависит от концентрации и соотношения гормонов, которые стимулируют, и биологически активных веществ, которые ингибируют этот процесс |
| Избыточности | В организме человека находится гораздо большее количество элементов, чем необходимо для реализации компенсаторной реакции |
| Дублирования | В человеческом организме находится множество парных структур (почки, легкие, глаза, надпочечники) и структур, которые выполняют идентичные функции (гепатоциты в печени, нейроны в нервной системе и прочее). Таким образом организм “подстраховывает себя” |
| Резервирования функций | Существуют структуры, которые находятся в “спящем режиме” во время спокойствия организма. Но при воздействии экстремальных условий они активируются. Например, депо крови находится в печени. Она выходит оттуда в общее кровяное русло во время кровопотери |
| Периодичности функционирования | В состоянии покоя структуры организма периодически меняют свою работу для осуществления определенной функции. К примеру, альвеолы в легких открываются при поступлении воздуха (вдохе) и закрываются при его выходе |
| Возможности замены одной функции на другую | Нарушение одной функции в организме может замениться другой вследствие осуществления компенсаторных механизмов |
| Усиления | За счет особых механизмов в организме минимальные усилия его структур приводят к развитию мощной компенсации |
Повышения чувствительности | Структуры, которые лишены иннервации, то есть поступления импульсов от нервных волокон, становятся более чувствительны |
Основные из них представлены в этой таблице.
