Компенсаторные явления при анемиях

Все
анемии сопровождаются развитием
гемической гипоксии. Срочная
адаптация:
5. Приспособительные
реакции системы внешнего дыхания:
увеличение
альвеолярной вентиляции за счет
углубления и учащения дыхания и
мобилизации резервных альвеол (вызывает
развитие дыхательного алкалоза, кривая
диссоциации НЬОг сдвигается влево и
оксигенация крови улучшается);увеличение
легочного кровотока и повышение
перфузионного давления в капиллярах
легких;возрастание
проницаемости альвео-калиллярных
мембран для газов.
6.Приспособительные
реакции в системе кровообращения:
развитие
тахикардии, увеличение ударного и
минутного объемов сердца;увеличение
массы циркулирующей крови за счет
выброса из кровяного депо;увеличение
системного артериального давления и
скорости кровотока;расширение
сосудов (под влиянием СО2, рН, аденозина).
7. Приспособительные
реакции системы крови:
усиление
диссоциации оксиНЬ за счет ацидоза;повышение
кислородной емкости крови за счет
усиления вымывания эритроцитов
из костного мозга;
8.Тканевые
приспособительные реакции:
ограничение
функциональной активности органов и
тканей, непосредственно
не участвующих в обеспечении транспорта
кислорода;увеличение
сопряжения окисления и фосфорилирования
и активности ферментов
дыхательной цепи;усиление
анаэробного синтеза АТФ за счет активации
гликолиза (накапливается
лактат, рН смещается в кислую сторону,
а кривая Баркрофта – вправо, НЪС>2
легче диссоциирует, отдавая кислород).
Долговременная
адаптация:
увеличение
силы дыхательных мышц и дыхательной
поверхности легких;гипертрофия
миокарда;активация
эритропоэза за счет усиления образования
эритропоэтинов в почках и,
возможно, других органах;увеличение
массы митохондрий.
163
3.2. Лейкоцитозы и лейкопении. Лейкозы.
Лейкоциты
–
это гетерогенная группа клеток, которые
являются основой антимикробной
защиты организма (рис. 3.2Л.)
В
клинической практике лейкоциты обычно
группируют в соответствии с морфологией
клеточного ядра (полиморфно-ядерные
и мононуклеарные) или по наличию
цито-плазматических включений (гранулоциты
и агранулоциты). Базофилы,
эозинофилы и ней-трофилы –
полиморфно-ядерные гранулоциты; лимфоциты
и моноциты –
мононуклеарные агранулоцитарные
лейкоциты.
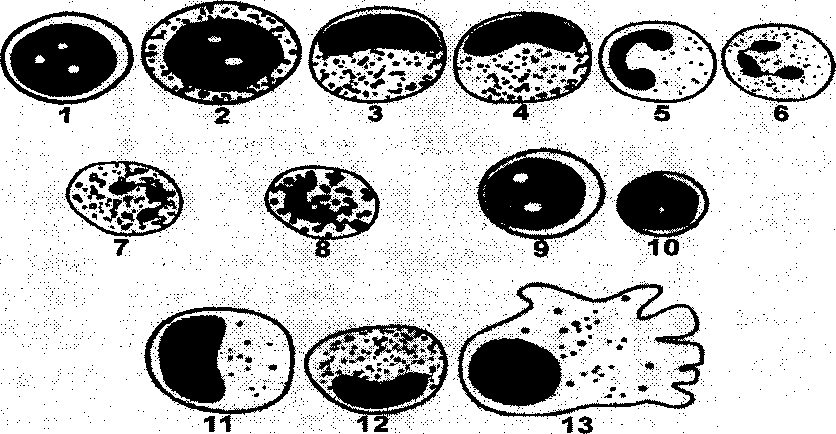
Рис.
3.2.1. Схематическое изображение различных
видов лейкоцитов. 1 – миелобласт*, 2 –
промие-лоцит,
3 – миелоцит, 4 – метамиелоцит, 5 – «юный»
или палочко-ядерный нейтрофил, 6 –
сегменто-ядерный нейтрофил,
7 – эозинофил, 8 – базофил, 9 – лимфобласт*,
10 – «зрелый» лимфоцит, 11 – промоноцит*,
12 -моноцит,
13 -макрофаг*.
*
– У
здоровых людей эти клетки локализуются
в костном мозге и обычно в мазках
периферической крови не встречаются.
Нейтрофилы
(молодые
формы – миелоциты, метамиелоцит («юные),
палочко-ядерные; зрелые формы –
сегментоядерные) представляют собой
самую большую группу циркулирующих
лейкоцитов. В крови нейтрофилы находятся
около 6-8 ч?
а затем мигрируют во внесосудистое
пространство. В очагах инфекции они
распознают, захватывают и уничтожают
бактерии.
Эозинофилы
играют
особую роль в борьбе с паразитами и
контроле аллергии; способны к хемотаксису,
фагоцитозу и обладают бактерицидной
активностью.
Базофилы
–
самая малочисленная группа циркулирующих
гранулоцитов; опосредуют аллергические
реакции, особенно 1§Е-зависимые.
Моноциты
проводят
в кровотоке всего около 20 ч, далее
мигрируют в периваску-лярные пространства,
где трансформируются в макрофаги
ретикулоэндотелиальной системы
(РЭС). Моноциты и макрофаги – долгоживущие
клетки, функциональные особенности
которых во многом схожи с таковыми у
гранулоцитов. Они более эффективно
захватывают и поглощают микобактерии,
грибки и макромолекулы; менее значима
их роль в фагоцитозе пиогенных бактерий.
В селезенке макрофаги ответственны за
утилизацию сенсибилизированных и
стареющих эритроцитов. Макрофаги играют
важную роль в про-цессинге и представлении
антигенов лимфоцитам в ходе клеточных
и гуморальных иммунных реакций.
Лимфоциты
–
небольшие мононуклеарные клетки,
осуществляющие иммунный. Лимфоциты
подразделяются на В-, Т-клетки и
клетки-киллеры. Подгруппы лимфоцитов
164
отличаются
по месту их образования и эффекторным
молекулам, но имеют общее свойство
– способность опосредовать высокоспецифический
антигенный ответ.
В
1 л крови здорового человека содержится
4-
9*109
лейкоцитов. Увеличение
концентрации лейкоцитов – лейкоцитоз,
снижение.—
лейкопения.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Анемия (малокровие) – уменьшение в крови общего количества гемоглобина, которое, за исключением острых кровопотерь, характеризуется снижением уровня гемоглобина в единице объема крови. В большинстве случаев при анемии падает и уровень эритроцитов в крови. Однако при железодефицитных состояниях, анемиях, связанных с нарушением синтеза порфиринов, талассемии содержание эритроцитов в крови может оставаться нормальным (при талассемии – нередко повышенным) при низком уровне гемоглобина. При острых кровопотерях (массивное кровотечение или острый гемолиз) в первые часы уровень гемоглобина и эритроцитов в крови остается нормальным, хотя есть очевидные признаки малокровия – бледность кожных покровов, конъюнктив, славшиеся вены, сердцебиение и одышка при небольшой нагрузке, а в тяжелых случаях и падение артериального давления.
Анемии всегда вторичны, т. е. являются одним из симптомов какого-то общего заболевания. Наряду с часто встречающимися и легко диагностируемыми формами анемии имеются и очень редкие анемические синдромы, требующие для диагностики сложных методических приемов. Некоторые формы анемии можно диагностировать лишь в специализированных учреждениях.
Классификация. Из многочисленных классификаций, строившихся по этиологи-ческому, патогенетическому и клиническому принципу, наиболее удачными оказались патогенетические.
I. Дефицитные анемии
Преимущественно белково-дефицитные
Преимущественно витамино-дефицитные
Преимущественно железодефицитные
II. Постгеморрагические анемии
Анемии вследствие острых кровопотерь
Анемии вследствие хронических кровопотерь
III. Гипо-и апластические анемии
А. Врожденные формы
1. С поражением эритро-, лейко- и тромбоцитопоэза:
а) с врожденными аномалиями развития (тип Фанкони);
б) без врожденных аномалий развития (тип Эстрена-Дамешека)
2. С парциальным поражением гемопоэза:
а) избирательная эритроидная аплазия (тип Блекфена-Даймонда)
Б. Приобретенные формы
1.С поражением эритро-, лейко- и тромбоцитопоэза: а) острая апластическая;
б) подострая гипопластическая; в) хроническая гипопластическая;
г) хроническая гипопластическая с гемолитическим компонентом на почве аутоиммунизации
2.Парциальная гипопластическая анемия с избирательным поражением эритропоэза
IV. Гемолитические анемии
А. Наследственные
1.Мембранопатии (микросфероцитоз, элиптоцитоз, пиропойкилоцитоз, стоматоцитоз, ксероцитоз, пароксизмальная ночная гемоглобинурия и др.);
2.Ферментопатии (дефекты цикла Эмбдена – Мейергофа, пентозофосфатного цикла, обмена нуклетотидов, метгемоглобинемия)
3.Дефекты структуры и синтеза гемоглобина (серповидноклеточная болезнь и другие гемоглобинозы с аномальными гемоглобинами; талассемии, эритропорфирии).
Б. Приобретенные
1.Иммунные и иммунопатологические (изоиммунные – переливание несовместимой крови, гемолитическая болезнь новорожденных; утоиммунные, гаптеновые медикаментозные и др.);
2.Инфекционные (цитомегаловирусная и другие вирусные инфекции, бактериальные инфекции – менингококковая и др.);
3.Витаминодефицитные (Е-витаминодефицитная анемия недоношенных) и анемии, обуслов-ленные отравлениями тяжелыми металлами, ядом змей.
4.ДВС-синдром разной этиологии.
Анемией или малокровием называется уменьшение содержания эритроцитов и (или) гемоглобина в единице объема крови, часто сочетающееся с их качественными изменениями.
Основной функцией эритроцитов является перенос кислорода и углекислого газа. Эта функция становится недостаточной вследствие:
уменьшения количества эритроцитов в крови;
падения содержания гемоглобина;
появления в крови незрелых или патологически измененных эритроцитов;
наличия эритроцитов с наследственным дефектом;
потери способности гемоглобина связывать кислород и других причин.
Чаше всего в клинической практике недостаточность функции эритроцитов отмечается при анемиях.
Анемии возникают на почве:
различных заболеваний и интоксикаций;
недостатка факторов, участвующих в кроветворении;
гипоплазии костного мозга;
гемолиза эритроцитов;
кровопотерь и т. д.
При анемиях нарушается дыхательная функция крови – доставка кислорода к тканям. Потребность организма в кислороде в какой-то степени компенсируется мобилизацией защитно-приспособительных реакций, которые обычно возникают при гипоксических состояниях. В случае прогрессирующей анемии наступает тяжелая кислородная недостаточность, которая может стать причиной смерти.
Для различных видов анемий характерны не только уменьшение количества эритроцитов и гемоглобина, но и качественные изменения эритроцитов крови, степени их зрелости, размеров, формы, окраски, структуры и биохимических свойств.
Анемия – это синдром, либо самостоятельное заболевание, характеризующееся понижением содержания в крови гемоглобина, которое как правило сопровождается понижением содержания эритроцитов. Клиническая симптоматика характеризуется общими признаками для всех видов анемий: головокружение, шум в ушах, слабость, обмороки. Классификация анемий: 1. По типу эритропоэза выделяет нормобластические и мегалобластические анемии. 2. По диаметру эритроцитов выделяют нормоцитарные анемии (7,5-8,5 мкм); макроцитарные анемии (более 8,5 мкм); микроцитарные анемии (менее 7,5 мкм). 3. По цветовому показателю выделяют нормохромные анемии (0,85-1,05), гипохромные (менее 0,85) и гиперхромные (более 1,05). Цветовой показатель рассчитывается по формуле: . 4. По регенераторной способности красного костного мозга выделяют: регенераторные анемии – 0,8-10% ретикулоцитов, гиперрегенаторные – более 10% ретикулоцитов и гипорегенераторные – менее 10% ретикулоцитов. В норме содержание ретикулоцитов составляет от 0,2 до 1%. 5. По этиопатогенезу выделяют анемии: а) в следствии кровопотери. К ним относятся острая постгеморрагическая и хроническая постгеморрагическая анемии. б) в следствии нарушенного кровообразования: железодефицитная, В12 и фолиеводефицитная, гипо- и апластическая анемии. в) в следствии избыточного кроворазрушения: наследственные и приобретенные гемолитические анемии. Практически при всех видах анемий имеет место качественное изменение со стороны эритроцитов. К ним относятся: анизоцитоз, пойкилоцитоз, анизохромия, наличие патологических включений в эритроцитах (тельца Жолли и кольца Кебота), базофильная пунктация, в следствии коагуляции белков цитоплазмы, сидероциты и сидеробласты.
Источник
Компенсация железа осуществляется за счет расхода запасов (ретикулоэндотелиальных), которые хранятся в виде ферритиновых гранул в МФ костного мозга, селезенки и печени и в сидеробластах- эритробластических клетках костного мозга. Железо вновь может сохраняться в МФ при гемолизе ЭЦ при участии гемопексина путем аутофагоцитоза и эндоцитоза. Гемосидерин- малорастворимый комплекс кристаллов железа- мобилизируется медленно.
Насчет уровня запаса железа судят по уровню ферритина.
Нарушения обмена железа в организме (депо железа, суточная потребность, его транспорт). Расстройства в организме, связанные с нарушением обмена железа. Железодефицит. Этиология, патогенез, стадии. Сидеробластические анемии. Гемохроматоз, этиология, патогенез, виды
Железо не подпадает под формальный критерий микроэлементов. Выполняет свои функции в связанной с белками форме.
Важнейшие железосодержащие белки:
1. Гемопротеины (гемоглобин, миоглобин, цмтохромы, цитохромоксидаза, миелопероксидаза и т.д.)
2. Железофлавопротеины (цитохром-C-редуктаза, сукцинатдегидрогеназа, НАДФ-дегидрогеназа, ацил-КоА-дегидрогеназа, ксантиноксидаза)
3. Белки, содержащие железо различных молекулярных конфигураций, – трансферрин, ферритин, феррин, гемосидерин, мобил-феррин, лактоферрин и др.)
Функции железа:
1) Участие в энергетическом метаболизме (половина ферментов и КоФакторов цикла Кребса содержат этот железо/нуждаются в его присутствии)
2) Формирование в мозге дофаминовых рецепторов (недостаток нарушает нормальное функционирование и развитие D-рецепторов)
3) Низкий уровень железа мешает деградации ГАМК/нарушает функционирование нейронов, производящих дофамин
Потребность взрослого человека в железе – 15 мг/сутки
Всасывание и транспорт (адская хрень впереди!)
Способность организма выводить железо строго ограничена. В целом, только малая часть железа, содержащегося в продуктах, абсорбируется. Количество всосавшегося железа определяется меж- и внутри индивидуальными различиями.
Всасывание железа в основном идет в верхней части тонкого кишечника. Соляная кислота желудка и витамин С способствуют переходу железа во всасываемую, некомплексную Ферро-форму.
Железо всасывается как в виде гема (10% поглощаемого железа), так и в негемовой (9%) форме с помощью ворсинок верхней части тонкого кишечника. (рис. 1). Железо присутствует в пищевых продуктах в формах: окисной (Fe3+) и закисной (Fe2+).
Лучше всего усваивается окисное железо в составе гемина из животных продуктов.
Геминовое железо. Содержится лишь в небольшой части пищевого рациона (мясные продукты). Оно очень хорошо всасывается (на 20-30%) и на его усвоение не влияют другие компоненты пищи:
· Железо гемина свободно проходит через клетки интестинальной слизистой,
· Внутри энтероцитов гем деградирует под действием ферментов, а железо присоединяется к пулу внутриклеточного белка ферритина.
Большая часть пищевого железа – негемовое (оно содержится в основном в листовых овощах). Степень его усвоения определяется рядом факторов, которые могут, как мешать, так и способствовать абсорбции железа.
Негеминовое железо: а)
1) Всасывание негеминового ферри-железа требует связывания с кишечным муцином
a. Сначала комплекс железо-муцин фиксируется на β3-интегрине люменальной мембраны энтероцитов
b. Затем комплекс связывается с мобилферрином – цитоплазматическим белком энтероцитов (гомологом кальретикулина)
2) Белок DMT-I – обеспечивает транспорт закисного железа Fe2+ в энтероциты. Состоит из 2-x компонентов: Ферроредуктазы щеточной каймы энтероцитов, которая восстанавливает ферри-железо в ферро-форму, и лиганд ферро-железа.
a. Белок SFT – стимултор транспорта железа – обеспечивает индукцию DMT-I и секрецию мобилферрина при недостатке железа в организме
В итоге все процессы всасывания железа передают его далее на апоферритин.
В кровь из энетероцитов железо попадает через образования комплекса с базолатеральным транспортером железа – гефестином.
Схема поступления экзогенного железа в ткани.
1) В полости кишечника железо освобождается из белков и солей органических кислот пищи. (Усвоению железа способствует аскорбиновая кислота, восстанавливающая железо в ферро-Fe2+ форму)
2) В клетках слизистой оболочки кишечника избыток поступившего железа соединяется с белком апоферритином с образованием ферритина (при этом ферритин окисляет ферро Fe2+ в ферри Fe3+)
3) Поступление железа из клеток слизистой оболочки кишечника в кровь сопровождается окислением железа ферментом сыворотки крови ферроксидазой. В крови Fe3+ транспортирует белок сыворотки крови трансферрин.
4) В тканях Fe2+ используется для синтеза железосодержащих белков или депонируется в ферритине.
Трансферрин переносит железо во многие ткани:
1) В основном в костный мозг, где больше всего экспрессируется трансферриновый рецептор 1-го типа (может отрываться от поверхности клетки и циркулировать, связывая трансферрин в крови, эритропоэтин усиливает его экспрессию)
2) В печени низкоаффинный трансферриновый рецептор 2-го типа (важен для обратной связи в системе гепцидина)
В эритроидных клетках железо делится между а) митохондриями (где включается в гем) и б) белком ферритином. В миелоидных клетках часть попадает в защитный белок лактоферрин. В макрофагах включается в ферритин (в макрофаги идет железо гемолизнувших эритроцитов при участии гаптоглобина и механизмов аутофагоцитоза).
Ферритин – депо железа
При избытке железа и усилении свободно-радикальных процессов ферритин превращается в гемосидерин. Избыток гемосидерина наблюдается при усиленном разрушении эритроцитов.
Источник
Введение
Клинико-гематологический симптом, характеризующийся эритроцитопенией или снижением количества гемоглобина, получил название анемии.
Зачастую, анемический симптом проявляется при многочисленных заболеваниях, однако может быть так, что анемия это самостоятельная нозологическая единица. Большое значение в диагностике анемий играет сбор анамнеза у пациента и тщательное комплексное обследование.
Давайте рассмотрим, каковы ее основные клинические признаки, методы диагностики и основные принципы лечения.
Вернуться к оглавлению
Клинические симптомы анемии
Все симптомы, развивающиеся при анемии, подразделяется на неспецифические и специфические (симптомы, обусловленные нарушением функционирования отдельных органов и систем). Существуют пять основополагающих факторов, влияющих на клинические симптомы и течение анемии:
- изменение объема крови (вариации процентного соотношения между плазмой и форменными элементами);
- изменение кислородной емкости крови;
- время развития изменений;
- компенсаторные реакции организма;
- манифестирование основного заболевания.
Неспецифические симптомы анемии
Неспецифические симптомы наиболее часто у пациентов представлены в виде появления общей слабости, недомогания, повышенной усталости, снижения настроения. При первичном осмотре отмечается бледность или покраснение кожных покровов, шелушение кожи, наличие на ее поверхности мелкоточечной сыпи, петехий, язвенных дефектов и гнойничковых поражений, которые имеют генерализованный характер. Такие признаки обусловлены сниижением доставки кислорода к тканям.

На слизистой полости рта возможно появление язв, покрытие ее налетом, а так же изменения состояния десен и зубов. Характерным признаком является т.н. «лакированный язык». При обследовании брюшной полости возможно увеличение размеров печени и селезенки.
Специфические симптомы
При длительном и хроническом течении заболевания со стороны дыхательной системы симптомы анемии могут не проявляться вовсе или ограничиваться незначительной одышкой. Причины данного явления кроются в мощных компенсаторных реакциях и особенностях физиологии крови. Исключением является острая постгеморрагическая анемия, при которой за счет обширной кровопотери появляется резкая одышка и слабость.
Со стороны сердца при легких формах анемий появляются симптомы в виде слабого шума в области проекции легочного ствола, возникающего в период систолы. При более тяжелых формах систолический шум может выслушиваться над областью проекций двух- и трехстворчатых клапанов.
Очень важно помнить, что возникающие при анемии шумы необходимо дифференцировать от шумов органического генеза. Со стороны центральной нервной системы преобладает неспецифическая симптоматика, связанная с возникающей гипоксией: головокружение, слабость, периодически возникающие головные боли, а так же снижение концентрации, что может косвенно свидетельствовать о гипоксии головного мозга. Кроме этого, при В12-фолиеводефицитной анемии характерно появление парестезий, которые сопровождаются появлением симптомов периферической нейропатии.
Наиболее часто у пациентов с анемиями встречается симптоматика со стороны желудочно-кишечного тракта, которая проявляется атрофией сосочков языка, глосситом, болезненностью и изъязвлением слизистых. Со стороны системы выделения возможно появление протеинурии (наиболее отчетливо данный симптом проявляется при тяжелых формах заболевания).
Вклад анамнеза в диагностику заболевания
При диагностике анемии особое внимание следует уделить сбору анамнеза заболевания у пациента. Для исключения наследственного характера заболевания, необходимо уточнить наличие заболевания по линии близких родственников (дедушки, бабушки, братья, сестры). С целью исключения влияния лекарственных препаратов или химических веществ на систему крови, необходимо уточнить, какие медикаменты принимал пациент в недалеком прошлом.
Так же необходимо уделить внимание профессиональной ориентации: работа с вредными химическими веществами на производстве, контакт с потенциальными отравляющими или токсическими химическими веществами. Особого внимания заслуживает мониторинг постоянной массы тела пациента, так как ее резкое уменьшение может говорить о развитии злокачественного новообразования и, как следствие, появление анемии.
Вернуться к оглавлению
Лабораторная диагностика
Несмотря на разнообразные симптомы анемии и причины, способные ее вызвать, основными методами в постановке окончательного диагноза является физикальное обследование и адекватные лабораторные тесты.

Среди гематологических тестов наиболее часто используются такие как:
- определение гематокрита;
- определение уровня гемоглобина;
- подсчет количества эритроцитов;
- подсчет количества лейкоцитов;
- подсчет количества ретикулоцитов;
- подсчет количества тромбоцитов;
- определение параметров эритроцитарного распределения;
- определение СОЭ;
- развернутая лейкоцитарная формула.
Наряду с определением количественного содержания форменных элементов крови, особое внимание уделяется их морфологическому исследованию. При помощи световой микроскопии производят исследование формы эритроцитов с оценкой анизоцитоза, пойкилоцитоза, полихромазии, патологических включений. При помощи автоматизированных тестеров производят оценку показателей эритроцитарного распределения, которые отражают вариабельность размеров эритроцитов.
При анализе плазмы крови наиболее распространенными тестами являются:
- определение мочевины;
- определение креатинина;
- определение биллирубина;
- определение белкового состава (альбумины, глобулины);
- определение уровня ферритина и железосвязывающей способности плазмы.
При анализе мочи определяют:
- цвет, кислотность, удельный вес и прозрачность;
- белок, в т.ч. белок Бен-Джонса;
- уровень биллирубина;
- эритроциты;
- производят микроскопию осадка.
Вернуться к оглавлению
Классификация анемий
Анемии принято классифицировать в зависимости от этиологических факторов и патогенетических механизмов развития заболевания. В связи с этим, выделяют основные этиологические группы, внутри которых происходит более детальная систематизация.
Так, в первой группе анемий, связанных с кровопотерей, выделяют острую и хроническую формы. Такая градация обусловлена объемом и длительностью возникших кровотечений.
Вторая группа представлена заболеваниями, связанными с нарушением процессов гемопоэза. Внутри данной группы выделяют анемии, возникающие при недостатке в организме железа, нарушением его перераспределения между органами и тканями, а так же обусловленные нарушениями процессов синтеза составляющих гемоглобина. Сюда относятся заболевания, возникающие в результате нарушения синтеза ДНК и РНК, связанные с нарушением процесса деления при созревании эритроцитов, угнетением пролиферации клеток костного мозга, понижением потребности тканей в кислороде и повышенной доставкой кислорода к тканям и др.
Третью группу представляют анемии, причины возникновения которых связаны с повышенными процессами кроворазрушения. Внутри данной группы выделяют:
- наследственные гемолитические анемии;
- приобретенные гемолитические анемии.
Отдельную группу представляют собой анемии новорожденных и анемии подросткового возраста, которые, как правило, не являются патологическим состоянием, а отражают собой физиологические процессы, происходящие в организме.

Кроме представленной классификации, диагностика анемий должна базироваться на морфологической и кинетической классификациях.
Вернуться к оглавлению
Основные принципы лечения
Основные принципы лечения будут зависеть от этиологических факторов и патогенетических механизмов, которые задействованы в развитии заболевания, а так же от того, насколько ярко проявляются клинические признаки и симптомы.
Для лечения острых постгеморрагических анемий необходимо как можно более быстрое восполнение объема циркулирующей крови, восстановление онкотического и осмотического давления, предупреждение явлений внутрисосудистой агрегации форменных элементов, а так же сохранение водно-электролитного и кислотно-щелочного равновесия. В зависимости от объема кровопотери лечение может быть проведено в объеме трансфузии плазмозамещающих растворов, или же при помощи переливания компонентов крови.
При хронических постгеморрагических анемиях симптоматическое лечение будет зависеть от уровня гемоглобина и эритроцитов. Однако основное внимание при лечении данного типа анемий должно быть направлено на устранение причины, вызывающей кровотечение.
Лечение железодефицитных анемий должно быть направлено на восстановление запасов железа в организме железосодержащими препаратами, а при выявлении причины – лечение должно быть направлено на ее устранение. Предпочтительно назначение комплексных железосодержащих препаратов, содержащих вещества, усиливающие всасывания железа.
Следует помнить, что восстановление уровня гемоглобина и цветного показателя наблюдается спустя 2-3 недели после начала терапии, а длительность приема лекарственных средств должна составлять минимум 12 месяцев для восстановления запасов железа в организме. Парентеральная терапия данного вида анемий применяется редко и только в тяжелых случаях.
Совместно с назначением железосодержащих препаратов, пациенты должны получать разнообразное и полноценное питание. Для лечения В12-дефицитных анемий применяется парентеральное введение гидроксикабаламина (цианокабаламина) в дозе, обеспечивающей суточную потребность. При легких формах заболевания хорошие результаты могут быть получены при помощи пивных дрожжей: такое их применение обусловлено высоким содержанием в них витаминов группы В.

С целью лечения порфирий применяется гипертрансфузии эритроцитарной массы для супрессии костного мозга, а так же снижение травматизации и воздействия солнечных лучей на кожные покровы (целесообразно применение солнцезащитных кремов). Для терапии анемии, связанной с нарушением синтеза цепей гема применяется трансфузия отмытых или размороженных эритроцитов с назначением деффероксамина.
Успех ее лечения во многом будет зависеть от раннего начала терапии. Специфического лечения для дизэритропоэтическиой анемии нет. Для ее терапии применяется симптоматическая терапия, кровопускания и назначение хелатирующих лекарственных препаратов.
Вернуться к оглавлению
Профилактические рекомендации
Среди основных мер, направленных на профилактику заболевания и анемия лечение, необходимо отметить рациональное и полноценное питание, здоровый образ жизни, своевременное обращение за помощью к врачам не только для ее лечения, но и для лечения сопутствующих заболеваний. При планировании семьи в обязательном порядке необходимо пройти медико-генетическое консультирование, так как предупреждение развития наследственной анемии у ребенка — лучший способ ее профилактики.
Источник
