Компенсаторные механизмы при анемии
Все
анемии сопровождаются развитием
гемической гипоксии. Срочная
адаптация:
5. Приспособительные
реакции системы внешнего дыхания:
увеличение
альвеолярной вентиляции за счет
углубления и учащения дыхания и
мобилизации резервных альвеол (вызывает
развитие дыхательного алкалоза, кривая
диссоциации НЬОг сдвигается влево и
оксигенация крови улучшается);увеличение
легочного кровотока и повышение
перфузионного давления в капиллярах
легких;возрастание
проницаемости альвео-калиллярных
мембран для газов.
6.Приспособительные
реакции в системе кровообращения:
развитие
тахикардии, увеличение ударного и
минутного объемов сердца;увеличение
массы циркулирующей крови за счет
выброса из кровяного депо;увеличение
системного артериального давления и
скорости кровотока;расширение
сосудов (под влиянием СО2, рН, аденозина).
7. Приспособительные
реакции системы крови:
усиление
диссоциации оксиНЬ за счет ацидоза;повышение
кислородной емкости крови за счет
усиления вымывания эритроцитов
из костного мозга;
8.Тканевые
приспособительные реакции:
ограничение
функциональной активности органов и
тканей, непосредственно
не участвующих в обеспечении транспорта
кислорода;увеличение
сопряжения окисления и фосфорилирования
и активности ферментов
дыхательной цепи;усиление
анаэробного синтеза АТФ за счет активации
гликолиза (накапливается
лактат, рН смещается в кислую сторону,
а кривая Баркрофта – вправо, НЪС>2
легче диссоциирует, отдавая кислород).
Долговременная
адаптация:
увеличение
силы дыхательных мышц и дыхательной
поверхности легких;гипертрофия
миокарда;активация
эритропоэза за счет усиления образования
эритропоэтинов в почках и,
возможно, других органах;увеличение
массы митохондрий.
163
3.2. Лейкоцитозы и лейкопении. Лейкозы.
Лейкоциты
–
это гетерогенная группа клеток, которые
являются основой антимикробной
защиты организма (рис. 3.2Л.)
В
клинической практике лейкоциты обычно
группируют в соответствии с морфологией
клеточного ядра (полиморфно-ядерные
и мононуклеарные) или по наличию
цито-плазматических включений (гранулоциты
и агранулоциты). Базофилы,
эозинофилы и ней-трофилы –
полиморфно-ядерные гранулоциты; лимфоциты
и моноциты –
мононуклеарные агранулоцитарные
лейкоциты.

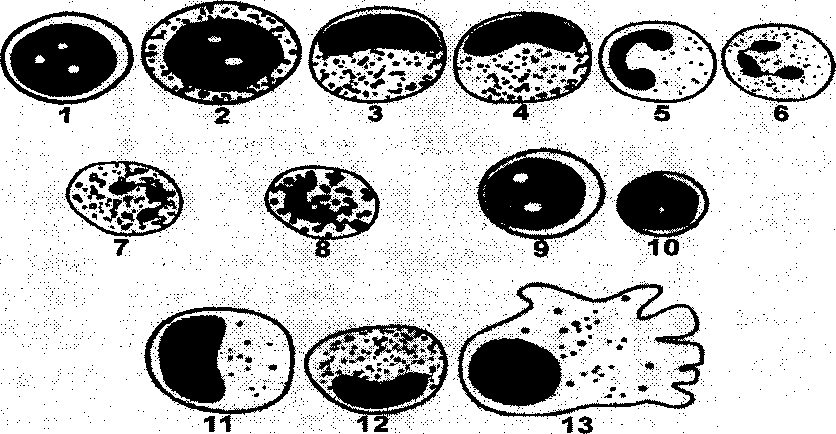
Рис.
3.2.1. Схематическое изображение различных
видов лейкоцитов. 1 – миелобласт*, 2 –
промие-лоцит,
3 – миелоцит, 4 – метамиелоцит, 5 – «юный»
или палочко-ядерный нейтрофил, 6 –
сегменто-ядерный нейтрофил,
7 – эозинофил, 8 – базофил, 9 – лимфобласт*,
10 – «зрелый» лимфоцит, 11 – промоноцит*,
12 -моноцит,
13 -макрофаг*.
*
– У
здоровых людей эти клетки локализуются
в костном мозге и обычно в мазках
периферической крови не встречаются.
Нейтрофилы
(молодые
формы – миелоциты, метамиелоцит («юные),
палочко-ядерные; зрелые формы –
сегментоядерные) представляют собой
самую большую группу циркулирующих
лейкоцитов. В крови нейтрофилы находятся
около 6-8 ч?
а затем мигрируют во внесосудистое
пространство. В очагах инфекции они
распознают, захватывают и уничтожают
бактерии.
Эозинофилы
играют
особую роль в борьбе с паразитами и
контроле аллергии; способны к хемотаксису,
фагоцитозу и обладают бактерицидной
активностью.
Базофилы
–
самая малочисленная группа циркулирующих
гранулоцитов; опосредуют аллергические
реакции, особенно 1§Е-зависимые.
Моноциты
проводят
в кровотоке всего около 20 ч, далее
мигрируют в периваску-лярные пространства,
где трансформируются в макрофаги
ретикулоэндотелиальной системы
(РЭС). Моноциты и макрофаги – долгоживущие
клетки, функциональные особенности
которых во многом схожи с таковыми у
гранулоцитов. Они более эффективно
захватывают и поглощают микобактерии,
грибки и макромолекулы; менее значима
их роль в фагоцитозе пиогенных бактерий.
В селезенке макрофаги ответственны за
утилизацию сенсибилизированных и
стареющих эритроцитов. Макрофаги играют
важную роль в про-цессинге и представлении
антигенов лимфоцитам в ходе клеточных
и гуморальных иммунных реакций.
Лимфоциты
–
небольшие мононуклеарные клетки,
осуществляющие иммунный. Лимфоциты
подразделяются на В-, Т-клетки и
клетки-киллеры. Подгруппы лимфоцитов
164
отличаются
по месту их образования и эффекторным
молекулам, но имеют общее свойство
– способность опосредовать высокоспецифический
антигенный ответ.
В
1 л крови здорового человека содержится
4-
9*109
лейкоцитов. Увеличение
концентрации лейкоцитов – лейкоцитоз,
снижение.—
лейкопения.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Одни и те же симптомы могут быть признаками разных заболеваний, а болезнь может протекать не по учебнику. Не пытайтесь лечиться сами — посоветуйтесь с врачом.
Терапия железодефицитной анемии должна проводиться препаратами железа. Цель лечения препаратами железа – устранение дефицита железа в организме, а не просто нормализация уровня гемоглобина, поэтому срок лечения длительный (не менее 3 месяцев).
Очень важно ориентироваться не на содержание железа в продуктах питания, а на его форму. Именно форма железа определяет процент его всасывания и усвоения и, следовательно, эффективность терапии.
Из различных форм железа легче всего усваивается гемовое железо – сложное органическое соединение, в котором железо находится в составе гемоглобина. Железо из злаков, овощей, фруктов всасывается значительно хуже из-за присутствия в них ингибиторов, таких как оксалаты, фосфаты, танин и другие. Сравните: коэффициент усвояемости железа из говядины (гемовое железо) составляет 17–22 %, из фруктов – не более 3 %. Таким образом, рацион питания должен быть максимально богат продуктами, в которых железо содержится в виде гема (язык говяжий, мясо кролика, говядина). Необходимо отметить также, что мясо, печень и рыба улучшают всасывание железа из фруктов и овощей при одновременном их употреблении.
Всасываемость железа из злаковых, бобовых, клубневых, овощей, фруктов значительно ниже. Усиливают всасывание растительного железа аскорбиновая кислота, продукты из мяса, птицы, рыбы, а также вещества, понижающие кислотность пищи (например, молочная кислота). Снижают усвоение железа соевый белок, чай, кофе, орехи и бобовые.
Необходимо учитывать, что всасывание железа может уменьшаться при одновременном применении ряда медикаментов (тетрациклины, альмагель, соли магния). Для лучшей переносимости препараты железа следует принимать во время еды. Для детей препаратами выбора являются жидкие формы препаратов железа (актиферрин, мальтофер).
Суточная терапевтическая доза препаратов железа должна быть достаточной для нормализации уровня гемоглобина и восполнения запасов железа в костном мозге, что составляет для солевых препаратов железа 3–6 мг/кг/сутки элементарного железа в два-три приема. Учитывая, что при развитии железодефицитной анемии всасывание железа увеличивается по сравнению с нормой и составляет 25–30 % (при нормальных запасах железа – всего 3–7 %), необходимо применять от 100 до 300 мг двухвалентного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. Таким образом, минимальная эффективная доза составляет 100 мг, а максимальная – 300 мг двухвалентного железа в сутки.
Таблица: содержание железа в основных продуктах питания
| Продукты животного происхождения | Продукты растительного происхождения | |||
| Наименование | Содержание (мг/100г) | Наименование | Содержание (мг/100г) | |
| Сыр из обезж.молока | 37 | Фасоль | 72 | |
| Печень свинная | 29,7 | Орехи лесные | 51 | |
| Сыр швейц. | 19 | Халва тахинная | 50,1 | |
| Пивные дрожжи | 18 | Овсяные хлопья | 45 | |
| Печень говяжья | 9 | Грибы свежие | 35 | |
| Почки говяжьи | 7 | Халва подсолнечная | 33,2 | |
| Сердце | 6,3 | Крупа пшенная | 31 | |
| Желток | 6 | Мак | 24 | |
| Язык говяжий | 5 | Горох | 20 | |
| Кролик(мясо) | 4,5 | Капуста морская | 16 | |
| Мясо индейки | 4 | Яблоки сушеные | 15 | |
| Баранина | 3,1 | Груша сушеная | 13 | |
| Телятина | 2,9 | Чернослив | 13 | |
| Говядина | 2,8 | Курага | 12 | |
| Мясо куриное | 2,5 | Какао | 11 | |
| Скумбрия | 2,5 | Урюк | 11 | |
| Яйцо куриное | 2,5 | Шиповник | 11 | |
| Сазан | 2,2 | Гречка | 8 | |
| Сосиски | 1,9 | Черника | 8 | |
| Икра кетовая | 1,8 | Толокно | 6 | |
| Колбаса | 1,7 | Грибы сушеные | 5,5 | |
| Курица | 1,6 | Миндаль | 5 | |
| Свинина | 1,6 | Крупа овсяная | 4,3 | |
| Налим | 1,4 | Кизил | 4,1 | |
| Макароны | 1,2 | Персик | 4,1 | |
| Рыба морская | 1,2 | Абрикосы | 4 | |
| Мед | 1,1 | Нектарин | 4 | |
| Сельдь атлант. | 1 | Крупа пшеничная | 3,9 | |
| Грудное молоко | 0,7 | Пшеничная мука | 3,3 | |
| Треска | 0,6 | Шпинат | 3,3 | |
| Творог | 0,4 | Мука гречневая | 3,2 | |
| Белок яичный | 0,2 | Изюм | 3 | |
| Коровье молоко | 0,1 | Cушеные абрикосы | 2,6 | |
| Сливки | 0,1 | Яблоки с красной кожурой | 2,5 | |
| Сливочное масло | 0,1 | Груша | 2,3 | |
| Слива | 2,3 | |||
| Чернослив | 2,1 | |||
| Смородина черная | 2,1 | |||
| Яблоки свеж. | 2 | |||
| Алыча | 1,9 | |||
| Малина | 1,8 | |||
| петрушка | 1,8 | |||
| Черешня | 1,8 | |||
| Крупа манная | 1,6 | |||
| Крыжовник | 1,6 | |||
| Малина | 1,6 | |||
| Белый хлеб | 1,5 | |||
| Капуста цветная | 1,5 | |||
| Вишня | 1,4 | |||
| Свекла | 1,4 | |||
| Рис | 1,3 | |||
| Капуста | 1,2 | |||
| Картофель жареный | 1,2 | |||
| Морковь | 1,1 | |||
| Дыня | 1 | |||
| Кукуруза | 1 | |||
| Огурцы | 0,9 | |||
| Гранаты | 0,8 | |||
| Картофель вареный | 0,8 | |||
| Морковь | 0,8 | |||
| Тыква | 0,8 | |||
| Клубника | 0,7 | |||
| Банан | 0,6 | |||
| Виноград | 0,6 | |||
| Клюква | 0,6 | |||
| Лимон | 0,6 | |||
| Помидоры | 0,6 | |||
| Ревень | 0,6 | |||
| Салат | 0,6 | |||
| Апельсин | 0,4 | |||
| Брусника | 0,4 | |||
| Кабачки | 0,4 | |||
| Мандарин | 0,4 | |||
| Ананас | 0,3 |
Дополнительно о питании при железодефицитной анемии можно прочесть в нашей отдельной статье.
Индивидуальные колебания в количестве необходимого железа обусловлены степенью дефицита железа в организме, истощения запасов, скоростью кроветворения, всасываемостью, переносимостью и некоторыми другими факторами. С учетом этого при выборе лекарственного препарата следует ориентироваться не только на содержание в нем общего количества, но главным образом на количество двухвалентного железа, которое только и всасывается в кишечнике. Так, например, при назначении препарата с низким содержанием двухвалентного железа (ферроплекс) количество принимаемых таблеток должно быть не менее 8–10 в сутки, в то время как препараты с высоким содержанием двухвалентного железа (ферроградумент, сорбифер дурулес и др.) можно принимать в количестве 1–2 таблетки в сутки.
- Авторы
- Файлы
- Литература
Чеснокова Н.П.
1
Невважай Т.А.
1
Моррисон В.В.
1
Бизенкова М.Н.
1
1 ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского Минздрава России»
1. Абдулкадыров К.М. Гематология. – М.: ЭКСМО, СПб.: Сова, 2004. – 928 с.
2. Воробьев А.И. Городецкий В.М., Шулутко Е.М., Васильев С.А. Острая массивная кровопотеря. – М.: ГЭОТАР-МЕД, 2001. – 175 с.
3. Воробьев П.А. Анемический синдром в клинической практике. – М.:«Ньюдиамед», 2001. – 165 с.
4. Гематология /Рукавицын О.А., Павлов А.Д., Моршакова Е.Ф. [и др.] /под ред. О.А.Рукавицына. – СПб.: ООО «ДП», 2007. – 912 с.
5. Литвицкий П.Ф. Патофизиология: учебник. – 4-е изд. – М.:ГЭОТАР- Медиа, 2008. – 496 с.
6. Наглядная гематология / Перевод с англ. Под редакцией проф. В.И. Ершова. – 2-е изд. – М.: ГЭОТАР-Медиа, 2008. – 116 с.: ил.
7. Кардиология. Гематология / под ред. Н.А. Буна, Н.Р. Колледжа и др. – М.: ООО «Рид Элсивер», 2009. – 288 с.
8. Папаян А.В., Жукова Л.Ю. Анемии у детей: руководство для врачей. – СПб.: ПИТЕР. – 2001 год – 384 с.
9. Патофизиология: учебник: в 2 т./под ред. В.В. Новицкого, Е.Д. Гольдберга, О.И. Уразовой. – 4-е изд. – ГЭОТАР-Медиа, 2010. – Т.2. – 848 с.: ил.
10. Патофизиология: учебник, в 3 т.: [А.И. Воложин и др.]; под ред. А.И. Воложина, Г.В. Порядина. – М.: Издательский центр «Академия», 2006.- Т.2 – 256 с.: ил.
11. Патофизиология: курс лекций/ [Порядин Г. В. и др.]; под ред. Г. В. Порядина. – М. : ГЭОТАР-Медиа, 2012. – 592 с.
12. Руководство по гематологии. В 2 т. / Под ред. А.И. Воробьева. – М.: Ньюдиамед, 2002. – 280 с.
13. Руководство по гематологии /Под ред. А.И Воробьева. – М.: Ньюдиамед, 2007. – 1275 с.
14. Садчиков Д.В., Хоженко А.О., Черная А.В. Количественные и качественные изменения клеточных элементов системы крови при тяжелой постгеморрагической анемии (обзор). – Саратовский научнор-медицинский журнал, 2011. – Т.4. – №4. – С.809-813.
15. Третьякова О.С. Постгеморрагические анемии в педиатрической практике. – Здоровье Украины. – 2012. – №8. – С.37-44.
16. Шиффман Ф.Дж. Патофизиология крови. – М.: Изд-во БИНОМ, 2009. – 448 с.
Анемии – состояния, характеризующиеся уменьшением содержания гемоглобина в общем объеме крови, а также как правило, и в единице объема крови.
Анемии следует отличать от гидремии, при которой абсолютное содержание гемоглобина в общем объеме крови не изменяется.
В большинстве случаев патологии анемии характеризуются и эритропенией, в связи с чем анемия может проявляться одновременным уменьшением содержания в единице объема крови и гемоглобина, и эритроцитов.
Анемии в ряде случаев могут быть отнесены к самостоятельным нозологическим формам патологии, в других – являются лишь симптомом какого-то заболевания.
Касаясь механизмов развития и происхождения анемий, следует отметить, что они могут носить наследственный, врожденный характер, однако в большинстве случаев анемии являются вторичными, или приобретенными.
В зависимости от патогенеза выделяют три основные группы анемий:
1. Постгеморрагические (острые и хронические).
2. Гемолитические (врожденные и приобретенные).
3. Дизэритропоэтические, обусловленные нарушением костномозгового кроветворения.
В процессе установления патогенеза и проведения дифференциальной диагностики анемий используют нередко следующие показатели состояния периферической крови:
– цветовой показатель;
– размер и форму эритроцитов;
– наличие регенераторных форм.
В связи с этим принято различать следующие виды анемий:
1. Нормохромные (цветовой показатель 0,85-1,05).
2. Гиперхромные (цветовой показатель больше 1,05).
3. Гипохромные (цветовой показатель меньше 0,85).
Следует отметить, что в ряде случаев цветовой показатель дает возможность дать ориентировочную оценку происхождения анемии. Так, к числу гиперхромных анемий относятся В12-дефицитные, фолиеводефицитные анемии. Железодефицитные анемии, в частности постгеморрагические,- гипохромные. В то же время метапластические, гемолитические анемии могут носить нормохромный характер.
В зависимости от регенераторной активности костного мозга выделяют следующие виды анемий:
1. Гиперрегенераторные.
2. Регенераторные.
3. Гипорегенераторные.
4. Арегенераторные (гипо-, апластические анемии).
Для гиперрегенераторных анемий характерно наличие ретакулоцитарных кризов, когда содержание ретикулоцитов в периферической крови может достигать нескольких процентов. При этом отмечается появление в периферической крови эритрокариоцитов. К категории гиперрегенераторных анемий относят некоторые формы гемолитических анемий, к числу гипорегенераторных – В12-дефицитные, фолиеводефицитные, железодефицитные анемии.
При гипо- и арегенераторных формах анемий количество ретикулоцитов может быть сниженным или вообще не определяться в крови, одновременно возрастает уровень дегенеративных форм эритроцитов.
В зависимости от размеров эритроцитов выделяют следующие формы анемий:
1. Нормоцитарные (7,2-8,3мкм).
2. Микроцитарные (меньше 7,2 мкм).
3. Макроцитарные (9-12 мкм).
4. Мегалоцитарные (12-15 мкм).
Макроцитоз, мегалоцитоз отмечаются при В12-, фолиеводефицитных анемиях; микроцитоз – при врожденных гемолитических анемиях; нормоцитарные анемии могут быть различного происхождения.
В зависимости от характера кроветворения анемии делят на две группы:
1. С нормобластическим типом кроветворения, для которого характерна последовательность дифференцировки элементов эритроцитарного ряда, включающая следующие этапы: эритробласт – пронормоцит – базофильный нормоцит – полихроматофильный нормоцит – оксифильный нормоцит, ретикулоцит – эритроцит;
2. С мегалобластическим типом кроветворения, включающим следующие этапы дифференцировки: промегалобласт – базофильный мегалобласт – полихроматофильный мегалобласт – оксифильный мегалобласт – мегалоцит.
Использование приведенных выше классификаций анемий в клинической практике, безусловно, облегчит правильную постановку диагноза, а также даст возможность объективной оценки тяжести течения заболевания и его прогноза.
Постгеморрагические анемии. Различают острую и хроническую постгеморрагическую анемию.
Причины кровопотерь весьма разнообразны: травмы, оперативные вмешательства, поражение сосудистой стенки при язвенной болезни, опухолевом и туберкулезном процессе, метро- и меноррагии, спонтанные кровотечения или слегка индуцированные при врожденной или приобретенной недостаточности коагуляционного, тромбоцитарного звеньев системы гемостаза и т.д.
У новорожденных причинами кровопотерь могут быть родовая травма., трансплацентарная кровопотеря, кровотечение из сосудов пуповины, наследственные геморрагические диатезы, коагулопатии, тромбоцитопении. У девочек возможны ювенильные кровотечения. Чем младше ребенок, тем чувствительнее он к кровопотере.
Реакция взрослого человека на кровопотерю определяется двумя основными факторами: объемом и скоростью кровопотери.
Одномоментная кровопотеря у взрослого человека в объеме 10-15 % всей массы крови не вызывает обычно развития шокового синдрома и соответственно тяжелых нарушений гемодинамикн. Между тем быстрая потеря крови новорожденным в таком же объеме может привести к развитию шока.
Для оценки степени кровопотери рекомендуют использовать следующую формулу:
П = К+44 1g ШИ,
где П – кровопотеря, в %; К – коэффициент, равный 27 при желудочно-кишечной кровопотере; 33 – при полостных кровотечениях; 24 – при ранениях конечностей; 22 – при поражении грудной клетки; ШИ – шоковый индекс, равный отношению частоты пульса к систолическому давлению.
Касаясь значимости объема кровопотери, необходимо отметить, что выход из сосудистого русла до 20-25 % объема циркулирующей крови мало опасен и хорошо компенсируется за счет включения экстренных механизмов адаптации, при чем в случае потери до 500 мл крови, что составляет в среднем 10 % ОЦК, клинические проявления могут отсутствовать, иногда возникает умеренная тахикардия.
При кровопотере объемом от 500 до 1200 мл (10-20 % ОЦК) возникает прогрессирующая тахикардия, снижается артериальное давление, появляются признаки вазоконстрикции.
Потеря 25-35 % циркулирующей крови (1200-1800 мл) сопровождается выраженными расстройствами центральной, органно-тканевой и микрогемоциркуляцин. При этом отмечаются выраженная тахикардия (пульс свыше 120/мин), нарастающая гипотензия, потливость, бледность кожных покровов, беспокойство, слабость, олигурия.
При потере более 40 % объема циркулирующей крови возникает выраженная гипотензия, артериальное давление падает ниже 70 мм рт. ст., прогрессирующая тахикардия (пульс свыше 150/мин), бледность кожных покровов, холодный пот, беспокойство, слабость, олигурия.
Быстрая потеря 50 % крови от общего объема является, как правило, летальной. Потеря такого же объема крови в течение нескольких дней при маточном, желудочном, кишечном кровотечении, как правило, компенсируется при хорошей корригирующей терапии.
Следует отметить высокую чувствительность детского организма к потере крови. Уменьшение объема циркулирующей крови у ребенка на 15-20 % может привести к развитию шока с потерей сознания. У взрослого же человека уменьшение объема циркулирующей крови на 25 % может протекать в ряде случаев без выраженной гипотензии.
В развитии постгеморрагической анемии следует выделить три стадии: начальную, компенсаторную и терминальную. Причем, характер изменений со стороны периферической крови при постгеморрагической анемии определяется не только тяжестью кровопотери, но и стадией развития постгеморрагической анемии.
Начальная стадия характеризуется уменьшением объема циркулирующей крови – гиповолемией, при этом в единице объема крови не возникает существенных изменений содержания гемоглобина, количества эритроцитов. Однако снижение объема циркулирующей крови сопровождается уменьшением венозного возврата в сердце, снижением ударного и минутного объема крови, что приводит к развитию циркуляторной гипоксии. Таким образом, гемическая гипоксия при кровопотере всегда сочетается и с циркуляторной.
Возникновение гипоксии, гиповолемии, метаболического ацидоза инициирует развитие механизмов срочной адаптации. Одним из мобильных звеньев адаптации является активация симпатоадреналовой системы, что приводит к развитию комплекса защитно-приспособительных реакций. Во-первых, возникает рефлекторный спазм периферических сосудов, или рефлекторно-сосудистая компенсация постгеморрагической анемии, направленная на адаптацию емкости сосудистого русла к объему циркулирующей крови и предотвращение развития шокового синдрома. Однако даже при максимальном спазме сосудов емкость сосудистого русла может уменьшиться лишь на 15-20 %. Активация симпатоадреналовой системы в этот период анемии приводит к рефлекторному учащению сердечных сокращений.
Изучение гематологических показателей в период рефлекторно-сосудистой компенсации может выявить лишь незначительное снижение уровня гемоглобина и эритроцитов, отсутствие выраженных изменений гематокрита.
В условиях гипоксии, гиповолемии активируется ренин-ангиотензиновая система, усиливается освобождение минералокортикоидов, что приводит к усилению реабсорбции натрия в почечных канальцах, повышению осмотического давления в плазме крови, стимуляции выброса антидиуретического гормона и усилению факультативной реабсорбции воды в дистальных почечных канальцах. Жидкость поступает в кровеносные капилляры по градиенту осмотического давления. Развивается так называемая гидремическая компенсация спустя 1-3 суток после кровопотери. для этого периода характерно уменьшение количества эритроцитов и гемоглобина в единице объема крови и во всем объеме крови. Анемия носит нормохромный характер.
Возникновение гипоксии при постгеморрагической анемии стимулирует продукцию эритропоэтина. по физико-химическим свойствам эритропоэтин представляет собой кислый термостабильный гликопротеин. Мономерная форма белка эритропоэтина имеет ММ от 23000 Д до 32000 Д. Однако в натуральном виде гормон представляет собой димер с ММ от 46000 Д до 60000 Д; содержание белка в нем составляет около 65,5 °/о; углеводов – около 30 %. Считают, что эритропоэтин образуется в различных клетках нефрона, а также в печени и селезенке.
Существует точка зрения, что эритропоэтин почечного происхождения неактивен, его именуют эритрогенином. В процессе взаимодействия почечного эритрогенина со специализированными белками плазмы крови α2-глобулиновой фракции, вырабатываемыми в печени, образуется активная форма эритропоэтина.
Под влиянием эритропоэтина эритропоэтинчувствительные клетки дифференцируются в эритробласты и далее – до зрелых эритроцитов, которые выходят в сосудистое русло и компенсируют утраченные при кровопотере клетки. Возникает период костномозговой компенсации, выраженный обычно уже спустя 45 дней после кровопотери. При этом в периферической крови появляются молодые, недонасыщенные гемоглобином формы эритроцитов – ретикулоциты, оксифильные, полихроматофильные, базофильные нормоциты, т. е. клетки, характеризующие регенераторную активность костного мозга. Анемия приобретает гипохромный характер. Одновременно в периферическую кровь из костного мозга поступают и другие клеточные элементы. Признаком достаточно выраженной регенераторной способности костного мозга является возникновение нейтрофильного лейкоцитоза со сдвигом влево.
Стимуляторами костномозговой компенсации после кровопотери являются и такие гормоны адаптации, как катехоламины, глюкокортикоиды. Однако их стимулирующий эффект на кроветворение опосредуется, по-видимому, за счет первичной активации синтеза под влиянием этих гормонов эритропоэтина.
Параллельно с костномозговой компенсацией развертывается белковая компенсация за счет активации синтеза в печени различных плазменных белков, в частности, плазменных белковых факторов свертывания крови. Следует отметить, что активация протеосинтеза наблюдается уже через несколько часов после кровотечения и регистрируется в течение последующих 1,5-3 недель и более в зависимости от объема кровопотери и состояния реактивности организма.
Вышеописанная стадийность развития свойственна острым постгеморрагическим анемиям. Все постгеморрагические анемии – острые и хронические – являются железодефицитными, поэтому характеризуются комплексом метаболических и функциональных расстройств, обусловленных недостаточностью железа.
Библиографическая ссылка
Чеснокова Н.П., Невважай Т.А., Моррисон В.В., Бизенкова М.Н. ЛЕКЦИЯ 2. АНЕМИИ: КЛАССИФИКАЦИЯ, ОБЩАЯ ХАРАКТЕРИСТИКА ГЕМАТОЛОГИЧЕСКИХ СДВИГОВ. ПОСТГЕМОРРАГИЧЕСКИЕ АНЕМИИ // Международный журнал прикладных и фундаментальных исследований. – 2015. – № 6-1. – С. 152-155;
URL: https://applied-research.ru/ru/article/view?id=6864 (дата обращения: 12.09.2020).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
