Контрольные карты на гемоглобин
КУПИТЬ
Инструкция для печати (в формате pdf)

УТВЕРЖДАЮ
Руководитель Департамента государственного контроля качества, эффективности, безопасности лекарственных средств и медицинской техники МЗ РФ Р.У. Хабриев 17.03.2000 г.
Рекомендована к утверждению Комиссией по лабораторным реагентам Комитета по новой медицинской технике МЗ РФ (протокол № 8 от 25.10.1999 г.) ИНСТРУКЦИЯ по применению набора контрольных растворов гемоглобина
НАЗНАЧЕНИЕ
Набор контрольных растворов гемоглобина предназначен для контроля правильности и воспроизводимости определения гемоглобина в крови унифицированным гемиглобинцианидным методом. Набор может быть также использован для контроля правильности и воспроизводимости других методов определения гемоглобина, основанных на принципе трансформирования, то есть на переводе всех форм гемоглобина в одну: пиридин-гемхромогеновый, гемихромный (под действием поверхностно-активных веществ), метод с образованием щелочного гематина D-575 и других. Набор предназначен для использования в клинико-диагностических и биохимических лабораториях. Содержимое набора «Гемоглобин-Контроль» должно обеспечить проведение 250 определений по контролю качества.
ПРИНЦИП МЕТОДА
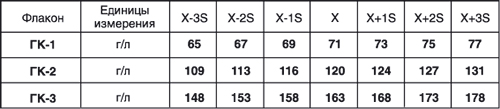
Принцип действия набора «Гемоглобин-Контроль» основан на выявлении погрешности в результатах определения концентрации гемоглобина путем сравнения полученных опытных результатов с приведенными в паспорте значениями. В паспорте для каждого диапазона концентраций указаны: — точные средние значения концентрации гемоглобина; — 95% доверительные интервалы; — параметры для построения контрольной карты.
ХАРАКТЕРИСТИКА НАБОРА
Набор контрольных растворов гемоглобина поставляется в двух вариантах комплектации: Комплектация № 1 состоит из трех флаконов, содержащих по 5,0 мл контрольного раствора гемоглобина каждый: Флакон 1 — с содержанием гемоглобина 65–75 г/л (ГК-1); Флакон 2 — с содержанием гемоглобина 110–130 г/л (ГК-2); Флакон 3 — с содержанием гемоглобина 145–175 г/л (ГК-3).
Комплектация № 2 состоит из 3 флаконов, содержащих по 5,0 мл контрольного раствора гемоглобина с содержанием гемоглобина 110–130 г/л (ГК-2).
АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
Диапазон определяемых концентраций гемоглобина — от 65 до 175 г/л. Коэффициент вариации результатов определения концентрации гемоглобина в одной и той же пробе — не более 2%. Отклонение концентрации контрольного раствора гемоглобина от паспортной величины — не более 2%.
МЕРЫ ПРЕДОСТОРОЖНОСТИ
Контрольные растворы гемоглобина «Гемоглобин-Контроль» изготовлены на основе крови доноров, прошедшей медицинское освидетельствование согласно приказу МЗ СССР № 408 от 12.07.89 г., в том числе на отсутствие антител к возбудителям гепатита и СПИДа. В качестве консерванта контрольный раствор гемоглобина содержит этиленгликоль. Применяется только «ин витро». При работе с данным набором необходимо соблюдать правила техники безопасности, рекомендуемые при работе с кровью в соответствии с «Инструкцией по мерам профилактики распространения инфекционных заболеваний при работе в клинико-диагностических лабораториях лечебных и профилактических учреждений» утвержденной Минздравом СССР 17.01.91 г. При работе с набором следует надевать одноразовые резиновые или пластиковые перчатки, так как образцы крови человека следует рассматривать как потенциально инфицированные, способные длительное время сохранять или передавать ВИЧ, вирус гепатита или любой другой возбудитель вирусной инфекции.
ОБОРУДОВАНИЕ
Спектрофотометр, фотоэлектроколориметр или гемоглобинометр.
ПРОВЕДЕНИЕ КОНТРОЛЯ
1. Контроль правильности определения гемоглобина крови. Определение концентрации гемоглобина в контрольном растворе проводят так же, как и анализ проб крови. Если полученный результат по контрольным растворам входит в указанный в паспорте 95% доверительный интервал, то результаты исследования проб считаются правильными.
2. Контроль воспроизводимости определения гемоглобина крови методом контрольных карт. Карты контроля качества (для каждого диапазона концентраций) строят, откладывая на оси абсцисс дни исследования, а на оси ординат — концентрацию гемоглобина в г/л. Параллельно абсциссе проводят прямые, соответствующие среднему значению (Х) и отклонениям (-3SD, −2SD, −1SD, +1SD, +2SD, +3SD), величины которых приведены в паспорте. Ежедневно проводят по одному определению для каждого диапазона концентраций, и результаты наносятся на графики в виде точек. Интерпретация результатов контрольных исследований производится в соответствии с Приказом Минздрава № 545 от 23.04.85 г и соответствующими методическими рекомендациями.
УСЛОВИЯ ХРАНЕНИЯ И ЭКСПЛУАТАЦИИ НАБОРА
Набор следует хранить в упаковке предприятия-изготовителя при температуре +2–8° С в течение всего срока годности. Допускается хранение наборов при температуре до +25° С не более 5 суток. Срок годности — 2 года. После вскрытия контрольные растворы устойчивы в течение 6 месяцев, но не более указанного срока годности набора при хранении в укупоренном виде при температуре +2–8° С.
По вопросам, касающимся приобретения наборов и их качества, просим обращаться по адресу: 105173, г. Москва, ул. Западная, д. 2, стр. 1, ООО «Агат—Мед». Телефон для справок: (495) 777-41-92.
Инструкция составлена: к.б.н. И.В. Смирновым — ст.н.с. Гематологического научного центра РАМН, к.б.н. Н.Н. Контугановым, В.В. Майоровой — сотрудниками ООО «Агат—Мед».
ПРИМЕР АТТЕСТАТА
набора контрольных растворов гемоглобина
Сер. Годен до

Регистрационные удостоверения
Назад к списку инструкций
1. Проводим 20 измерений:
1. 117
2. 118
3. 119
4. 120
5. 115
6. 120
7. 125
8. 117
9. 113
10. 116
11. 123
12. 124
13. 121
14. 119
15. 125
16. 115
17. 110
18. 115
19. 117
20. 119
2. Рассчитываем среднее арифметическое по формуле:
Складываем все значения (2368) и делим на 20 (количество измерений). Получаем 118.
3. Рассчитываем среднее квадратичное отклонение по формуле:
Сумма квадратов — 298,8. Делим на 19 (количество измерений минус один). Берем квадратный корень из этого числа. Получаем 4.
4. Рассчитываем коэффициент вариации по формуле:
Делим 4 на 118 и умножаем на 100%. Получаем 3,35.
5. Находим границы карты:
Среднее арифметическое плюс среднее квадратичное отклонение (122)
Среднее арифметическое минус среднее квадратичное отклонение (114)
Среднее арифметическое плюс удвоенное среднее квадратичное отклонение (126)
Среднее арифметическое минус удвоенное среднее квадратичное отклонение (110)
Среднее арифметическое плюс утроенное среднее квадратичное отклонение (130)
Среднее арифметическое минус утроенное среднее квадратичное отклонение (106)
6. Строим график
Задача
Вам поручено организовать контроль качества подсчета лейкоцитарной формулы.
1. Как готовятся контрольные мазки для подсчета лейкоцитарной формулы?
2. Какие требования предъявляются к правильному приготовления мазков?
3. Почему не подходит неравномерно (волнообразно) сделанный мазок?
4. Какова методика ведения контроля качества подсчета лейкоцитарной формулы?
1. Контрольные мазки готовятся из капиллярной крови доноров и больных обычным способом не предметных стеклах, выполняя требования к правильному приготовлению мазков, фиксируются и окрашиваются.
2. Хорошо сделанный мазок крови должен отвечать следующим условием:
2.1. Он начинается на 1-1,5 см от узкого края предметного стекла и кончаться в 2-3 см от его другого края.
2.2. Мазок должен быть равномерной толщины, а не волнообразным.
2.3. Мазок должен быть «свободным с края». Другими словами, слой крови не должен достигать длинного края стекла, а между ним к краем должно остаться расстояние в несколько миллиметров.
3. Распределение клеток неудовлетворительно: толстые участки содержат больше лимфоцитов, тонкие — больше моноцитов и сегментоядерных клеток.
4. Контрольные мазки готовятся из капиллярной крови доноров и больных обычным способом не предметных стеклах, выполняя требования к правильному приготовлению мазков, фиксируются и окрашиваются. Затем контрольные мазки многократно просчитываются (не менее 20 раз) по 200 клеток. Из полученных данных статистически рассчитываются критерии определения правильности подсчета мазка путем расчета среднего арифметического.
Моноциты — самые большие, без зернистости
Лимфоциты — самые маленькие
Базофилы — зернистость, почти черные
Эозинофилы — круглые ядра, кирпично-красная зернистость
Нейтофилы — палочкоядерные и сегментоядерные, фиолетовая зеернистость, цельное или сигментированное ядро.
Подсчет клеток крови в мазке, практическая работа
Моноциты — 13
Палочкоядерные — 36+10
Сегментоядерные — 47
Базофил — 1
Лимфоцит — 3
Эозинофил — 0
Номер результат X-X (X-X)2
пробы Исследовали гемоглобин
1 142 2,6 6,76 11 раз в одной пробе,
2 141 3,6 12,96 получили 11 результатов
3 146 1,4 1,96
4 144 0,6 0,36 1) находим ср.арифметич:
5 143 1,6 2,56
6 140 4,6 21,16 X = 1591 = 144,6
7 146 1,4 1,96 11
8 150 5,4 29,16
9 150 5,4 29,16 2) находим отклонение от
10 143 1,6 2,56 среднего:
11 146 1,4 1,96 X – X
——– 3) квадрат отклонения от
1591 среднего
4) находим сумму отклонений от среднего: (X – X)2 = 110,56
5) находим среднеквадратичное отклонение:
6) коэфициент вариации (CV):
Допустимый CV по гемоглобину равен 2%, значит воспроизводимость низкая (так как превышает допустимую погрешность)
Построим контрольную карту:
Находим:
X + 1S = 144,6+3,32=147.92
X + 2S = 144,6+(3,32*2)=151.24
X + 3S = 144,6+(3,32*3)=154.56
X – 1S = 144,6-3,32=141.28
X – 2S = 144,6-(3,32*2)=137.96
X – 3S = 144,6-(3,32*3)=134.64
¦
¦
X+3S¦154,5
¦
X+2S¦151,2
¦
X+1S¦147,9
¦
X¦144,6
¦
X-1S ¦141,3
¦
X-2S¦138
¦
X-3S¦134,7
—————————————————————-
¦ 1 2 3 4 5 6 7 8 9 10 11
ВЫВОД: Хотя имелась большая разница между низким и высоким уровнем гемоглобина (10 г/л) и незначительно повышался коэффициент вариации (2%-2,3%),в целом исследование гемоглобина выполнено на должном уровне для клинических целей.
Контрольная карта показала, что тест имеет один предупредительный критерий (3 результата за пределами 1 среднеквадратичного отклонения)
В этом случае результаты анализов можно выдавать, но необходимо проверить стандартные растворы, пипетки, улучшить работу персонала. По результатам контрольной карты можно установить, что ошибки скорее всего случайные и нет систематических погрешностей.
Контрольная карта оценивается по правилам Вестгарда:
1.12S используются как предупредительный критерий. Если один из результатов анализа выходит за пределы X ± 2S,то проверяется последовательно наличие всех последующих правил. Аналитическая серия признаётся неудовлетворительной, если присутствует хотя бы один из них.
2.13S одно из контрольных измерений выходит за пределы Х ±3S.
3.22S два последовательных контрольных измерений выходят за пределы X ± 2S.
4.R4S два контрольных измерения расположены по разные стороны от коридора Х ± 2S.
5.41S четыре последовательных измерения выходят за пределы X ± 1S.
6.10 Хср десять последовательных контрольных исследований располагаются по одну сторону от линии Хср.
2.МЕТОД КУМУЛЯТИВНЫХ СУММ.
Контрольная карта выявляет явные изменения в воспроизводимости и в правильности. Контрольная карта не позволяет обнаружить небольшие изменения в правильности. Когда очень высокий коэффициент вариации можно использовать метод кумулятивных сумм.
X X-K C
1 120 0 0
2 119 -1 -1 К = 120 ммоль/л-кол-во
3 122 +2 +1 гемоглобина в контроль-
4 125 +5 +6 ной сыворотке.
5 121 +1 +7 К – референтная величина
6 118 -2 +5 (известная)
7 119 -1 +4 С – кумулятивная сумма
8 120 0 +4 (накопление)
9 121 +1 +5 X – ежедневные результаты
10 116 -4 +1 контроля
11 119 -1 0
12 121 +1 +1
13 121 +1 +2
14 120 0 +2
15 121 +1 +3
16 121 +1 +4
17 119 -1 -3
18 117 -3 0
19 116 -4 -4
20 121 +1 -3
¦
+6 ¦
+4 ¦
+2 ¦
0 +——————————————————–
-2 ¦
-4 ¦
-6 ¦
——+———————————————————
¦ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
¦
¦
Внеконтрольная ситуация:
1. Шесть последовательных точек вверх или вниз от нуля.
2. Общий наклон графика не должен превышать 60.
Недостатки методов, использующих контрольные материалы:
1. Требуют определенных расходов.
2. Контрольные материалы могут быть нестабильными.
3. Контролируется только этап анализа, игнорируются преаналитические и послеаналитические факторы.
МЕТОДЫ КОНТРОЛЯ КАЧЕСТВА, ИСПОЛЬЗУЮЩИЕ ПРОБЫ ПАЦИЕНТА
1.Метод параллельных проб – позволяет определить случайные ошибки.
Пример подсчета лейкоцитов – берут 10 проб и исследуют дважды.
1 подсчет 2 подсчет d d2
5,4 5,8 0,4 0,16
8,3 10,5 2,2 4,34
17,2 18,0 0,8 0,64
5,4 5,4 0 0
12,2 11,8 0,4 0,16
14,3 13,8 0,5 0,25
6,2 6,4 0,2 0,04
8,2 8,6 0,4 0,16
7,3 7,5 0,2 0,04
5,4 5,9 0,5 0,25
d – разница между результатами параллельных проб
d2- квадрат разницы.
n – число параллельных проб
d2 – (сумма) = 6,54
S – среднеквадратическое отклонение
2S = 1,14
Ни один из результатов исследования параллельных проб не должен превышать
2S, в нашем случае исследование неудовлетворительное.
КОНТРОЛЬ КАЧЕСТВА РАБОТЫ ЛАБОРАНТА
1. Результаты внешней оценки качества.
2. Метод дублирования анализа- проба исследуется дважды под другим номером
3. Метод случайных проб.
4. Метод разведения проб.
МЕЖЛАБОРАТОРНЫЙ КОНТРОЛЬ КАЧЕСТВА(ФСВОК):
Федеральная система внешней оценки качества(Внешняя оценка качества) – контроль сравнимости результатов, полученных в нескольких лабораториях на одном и том же контрольном материале одними и теми же методами.
Самая простая форма внешней оценки качества – рассылка одного или нескольких образцов для исследования в каждую лабораторию.
Блок контроля и самоконтроля
Вопросы для самоконтроля
Понятие контроля качества.
Нормативные документы по контролю качества.
Виды контроля качества.
Виды и причины лабораторных ошибок.
Особенности проведения контроля качества гематологических исследований.
Контрольные материалы при проведении гематологических исследований.
Методы проведения контроля качества гематологических исследований.
Проведение контроля воспроизводимости и правильности гематологических исследований.
Ведение и оформление документации по контролю качества гематологических исследований.
Подготовка рабочего места для проведения контроля качества гематологических исследований.
Лист регистрационных изменений
| № измене-ния | Номера листов (страниц) | Всего листов (страниц) в документе | Вход. № сопроводительного документа и дата | Подпись ответствен-ного за внесение | Дата |
| Изменен-ных | Новых | Аннули-рованных | |||
Руководитель Департамента государственного контроля
качества, эффективности, безопасности лекарственных
средств и медицинской техники МЗ РФ
Р.У. Хабриев
17.06.2000 г.
Рекомендована к утверждению
Комиссией по лабораторным реагентам
Комитета по новой медицинской технике МЗ РФ
(протокол № 1 от 31.01.2000 г.)
ИНСТРУКЦИЯ
по применению набора реагентов для определения
гемоглобина в крови гемиглобинцианидным методом
НАЗНАЧЕНИЕ
Набор предназначен для количественного определения содержания гемоглобина в крови гемиглобинцианидным методом (метод Drabkin) в клинико-диагностических и биохимических лабораториях.
Набор рассчитан на проведение 600 определений при расходе 5,0 мл рабочего раствора на один анализ.
ПРИНЦИП МЕТОДА
Гемоглобин крови при взаимодействии с железосинеродистым калием (красная кровяная соль) окисляется в метгемоглобин (гемиглобин), образующий с ацетонциангидрином гемиглобинцианид (цианметгемоглобин), интенсивность окраски которого пропорциональна концентрации гемоглобина в крови и измеряется фотометрически при длине волны 540 (500–560) нм.
СОСТАВ НАБОРА
1. Трансформирующий реагент – сухая смесь (натрий углекислый кислый, 1,0 г; калий железосинеродистый, 200 мг) – 3 упаковки.
2. Ацетонциангидрин – 3 ампулы (по 0,5 мл).
3. Калибровочный раствор гемоглобина с концентрацией 120 г/л – 1 флакон (2 мл).
АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
Линейная область определения концентрации гемоглобина – в диапазоне от 20 до 200 г/л, отклонение от линейности – не более 2%.
Чувствительность определения – не более 10 г/л.
Воспроизводимость: коэффициент вариации не более 2%.
Нормальные величины концентрации гемоглобина в крови составляют:
– у мужчин 130–160 г/л;
– у женщин 120–140 г/л.
Качество набора можно оценивать с использованием контрольных растворов гемоглобина отечественного или зарубежного производства.
Рекомендуется в каждой лаборатории уточнить диапазон нормальных величин у обследуемого контингента.
МЕРЫ ПРЕДОСТОРОЖНОСТИ
При работе с данным набором необходимо соблюдать правила техники безопасности, рекомендуемые при работе с кровью в соответствии с Инструкцией по мерам профилактики распространения инфекционных заболеваний при работе в клинико-диагностических лабораториях лечебных и профилактических учреждений, утвержденной Минздравом СССР от 17.01.91 г., и «Правила устройства, техники безопасности, производственной санитарии, противоэпидемического режима и личной гигиены при работе в лабораториях (отделениях, отделах) санитарно-эпидемиологических учреждений системы Министерства здравоохранения СССР».
При работе с набором следует надевать одноразовые резиновые или пластиковые перчатки, так как образцы крови человека следует рассматривать как потенциально инфицированные, способные длительное время сохранять или передавать ВИЧ, вирус гепатита или любой другой возбудитель вирусной инфекции.
В состав трансформирующего раствора входит ацетонциангидрин, ядовитое вещество. В случае попадания раствора на кожу и слизистые необходимо сразу же промыть пораженное место большим количеством проточной воды. Пипетирование per os категорически запрещается. При попадании внутрь следует немедленно выпить 0,5 л теплой воды и вызвать рвоту.
Другие компоненты набора в используемых концентрациях являются нетоксичными.
ОБОРУДОВАНИЕ И РЕАГЕНТЫ
– Спектрофотометр, длина волны 540 нм, или фотоэлектроколориметр, длина волны 500–560 нм (зеленый светофильтр), кювета с толщиной поглощающего свет слоя 10 мм;
– пипетки, позволяющие отбирать объемы жидкости 0,02 и 5,0 мл;
– колба мерная вместимостью 1,0 л;
– пробирки вместимостью 5–10 мл;
– секундомер;
– вода дистиллированная;
– перчатки резиновые или пластиковые.
ПОДГОТОВКА РЕАГЕНТОВ ДЛЯ АНАЛИЗА
Трансформирующий раствор. Один пакет трансформирующего реагента и одну ампулу ацетонциангидрина количественно перенести в мерную колбу вместимостью 1,0 л, растворить в небольшом количестве дистиллированной воды и довести объем дистиллированной водой до метки.
Калибровочный раствор гемоглобина готов к применению.
ПРОВЕДЕНИЕ АНАЛИЗА
В пробирки внести по 5,0 мл трансформирующего раствора, добавить по 0,02 мл крови (разведение в 251 раз), тщательно перемешать и инкубировать при комнатной температуре (+18–25° С) в течение 20 минут, после чего измерить величину оптической плотности опытных проб против холостой пробы (трансформирующего раствора) при длине волны 540 (500–560) нм в кювете с толщиной поглощающего свет слоя 10 мм.
Калибровочный раствор гемоглобина обрабатывать так же, как и пробу цельной крови.
Окраска устойчива в течение 1 часа.
Концентрацию гемоглобина в крови рассчитать по формуле:
Eо
С = ——— х 120 ,
Eк
где: С – концентрация гемоглобина в опытной пробе, г/л;
Eо – оптическая плотность опытной пробы, ед.опт.плотн.;
Eк – оптическая плотность калибровочной пробы, ед.опт.плотн.;
120 – концентрация гемоглобина в калибровочном растворе, г/л.
УСЛОВИЯ ХРАНЕНИЯ И ЭКСПЛУАТАЦИИ НАБОРА
Набор должен храниться в упаковке предприятия-изготовителя при температуре +2–8° С в течение всего срока годности. Допускается хранение наборов при температуре до +25° С не более 5 суток.
Срок годности набора – 2 года.
Трансформирующий раствор должен быть прозрачным, желтого цвета и может храниться в посуде из темного стекла при комнатной температуре не более 6 месяцев. При появлении осадка или при обесцвечивании раствор непригоден для употребления. Не замораживать!
Калибровочный раствор гемоглобина после вскрытия флакона может храниться в течение 6 месяцев, но не более срока годности набора, при хранении в укупоренном виде при температуре +2–8° С.
По вопросам, касающимся приобретения наборов и их качества, просим обращаться по адресу: 105173, г. Москва, ул. Западная, д. 2, стр. 1, ООО «Агат–Мед». Телефон для справок (495) 777-41-92.
Инструкция составлена: к.б.н. И.В. Смирновым – ст.н.с. Гематологического научного центра РАМН, к.б.н. Н.Н. Контугановым, В.В. Майоровой – сотрудниками ООО «Агат–Мед».
