Нарушение углеводного обмена при анемии

- Анемия вследствие нарушений гликолитических ферментов
- Гемолитическая анемия вследствие дефицита гексокиназы, пируваткиназы и триозофосфатизомеразы
- Наследственная гемолитическая анемия 2-го типа
- Нарушение метаболизма нуклеотидов
Анемия вследствие нарушений гликолитических ферментов
Гликолиз в организме человека представляет собой универсальный путь получения энергии из поступающих углеводов, прокариот и эукариот, аэробных и анаэробных микроорганизмов. В анаэробных условиях гликолиз является единственным значимым источником получения энергии из углеводов. Гликолиз производит энергию в виде АТФ и НАДН (Никотинамидадениндинуклеотид). Последний представляет собой кофермент, который присутствует во всех живых клетках человека и других живых существ.
Гликолитический путь состоит из 10 стадий, в каждой из которых принимают участие специфические ферменты. Каждая молекула глюкозы метаболизируется, в результате чего производится две молекулы АТФ (аденозинтрифосфорной кислоты) и две молекулы НАДН.
Гликолиз проходит не изолировано от других метаболических путей. Молекулы глюкозы могут вступить в этот процесс не только в самом его начале. Например, продукт распада гликогена — глюкоза-6-фосфат, может войти в гликолитический путь на втором этапе. Глицеральдегида-3-фосфат, который получают путем фотосинтеза, так же представляет собой гликолитически промежуточное соединение, поэтому может быть направлен по анаболическому пути в гликолиз только тогда, когда необходима энергия.
Кроме того, промежуточные продукты могут быть произведены во время гликолиза даже при высоких энергетических уровнях — для использования в биосинтетических путях. Например, в период активного производства пирувата — продукта гликолиза, входящего в цикл лимонной кислоты, пируват служит в качестве субстрата в синтезе аминокислоты.
Любые нарушения в производстве ферментов довольно быстро (в течение нескольких недель) сказываются на самочувствии человека, составе его крови, состоянии эритроцитов. Передача и синтез энергии в организме должны проходить непрерывно, и если по каким-либо причинам эти процессы нарушаются, развивается анемия и другие сопутствующие симптомы и состояние. Нарушения углеводного обмена приводят к нарушению функции скелетных мышц, слабости, апатии, проблемам с суставами, пищеварением, ростом волос.
Врожденные нарушения ферментов приводят к рождению детей с различными дефектами или умственной отсталостью. Приобретенные же заболевания такого типа чаще всего развиваются в подростковом возрасте, оказывая прямое воздействие на силу мышц, их тонус, энергообеспечение. Такие больные не могут адекватно переносить нагрузку, быстро утомляются, испытывают боль в мышцах и другие симптомы.
Лечение гемолитической анемии
Поскольку любая анемия, в том числе и гемолитическая, связана с другим, более серьезным заболеванием, для определения лечения необходима точная диагностика. Основные методы лечения гемолитической анемии независимо от причины:
- прием глюкокортикостероидов;
- спленэктомия (удаление селезенки);
- прием иммунодепрессантов;
- отмывание (трансфузия) эритроцитов, проводится при гемолитических кризах;
- коррекция уровня железа (при избыточном уровне проводят десфераловый тест — определение уровня железа, выводящегося с мочой).
Гемолитическая анемия вследствие дефицита гексокиназы, пируваткиназы и триозофосфатизомеразы
Основные ферменты, ответственные за процесс гликолиза – это гексокиназа (или глюкокиназа), фосфофруктокиназа и пируваткиназа. Концентрация этих трех ферментов в клетке регулируется гормонами, которые влияют на темпы их функционирования. Пептидный гормон инсулин, секретируемый поджелудочной, дает ответ на увеличение уровня аминокислот в крови, а также стимулирует ответ ЖКТ на этот процесс. Общий эффект инсулина заключается в поддержании соответствующего уровня энергии, когда пища поступает в достаточном количестве.
Глюкагон — еще один пептидный гормон, секретируемый клетками поджелудочной железы. Его секреция стимулируется низким уровнем глюкозы в крови, а общий эффект противоположен действию инсулина. Инсулин активирует выработку глюкокиназы, фосфофруктокиназы и пируваткиназы, в то время как глюкагон подавляет их производство. Такие процессы могут проходить как в течение нескольких часов, так и в течение нескольких дней и обычно отражают, сыт человек или голоден.
Что делает фосфофруктокиназа?
Фосфофруктокиназа (ФФК) является важным ферментом практически всех живых клеток. Он выполняет определенную функцию в процессе гликолиза, а именно — превращение фруктозы-6-фосфата во фруктозу-1, 6-бисфосфат. Глюкоза поддерживает устойчивое количество АТФ, основного носителя энергии в живых клетках.
Фосфофруктокиназа является мультисубъединичным белком. В таких белках субъединицы могут вести себя кооперативно; то есть, активность одной субъединицы влияет на активность всех других субъединиц. Белки, которые демонстрируют такое поведение, известны под названием аллостерических белков. Особенно известным примером аллостерического белка является гемоглобин, который скорее является белком, транспортирующим кислород, чем ферментом.
Активность такого аллостерического фермента как ФФК может регулироваться связыванием с малой молекулой, которая действует как активатор или ингибитор. Поскольку субъединицы действуют совместно, активация одной субъединицы приводит к активации всех субъединиц, и ингибирование одной субъединицы приводит к ингибированию всех субъединиц.
Что делает гексокиназа?
Гексокиназа нужна для выполнения первого этапа гликолиза в большинстве тканей, в том числе в мышцах и мозге. Она имеет низкую толерантность к глюкозе, поэтому позволяет инициирование гликолиза даже когда уровень глюкозы в крови являются относительно низким. Гексокиназа важна для предотвращения потребления слишком большого количества клеточного АТФ, когда глюкоза поступает в организм в больших количествах.
Глюкокиназа, содержащаяся в печени и поджелудочной железе, требует гораздо более высокой концентрации глюкозы для максимальной активности.
Таким образом, эти органы становятся наиболее активными сразу после употребления пищи, богатой углеводами. Гексокиназа позволяет печени эффективно удалить избыток глюкозы и свести к минимуму уровень гипергликемии после приема пищи.
В печени действие глюкокиназы противостоит воздействию глюкозо-6-фосфатазы, которая гидролитически удаляет фосфат из цикла. Такие реакции требуют большого количества АТФ, но помогают печени нормально функционировать.
Что делает пируваткиназа?
Пируваткиназа — это третий фермент, принимающий участие в гликолизе. Пируваткиназа также связана с уровнем сахара в крови. Она необходима для гормональной регуляции гликолиза, обеспечения активного роста тканей и работы внутренних органов. Гормоны и ферменты, которые регулируют скорость гликолиза, определяют и метаболизм гликогена — вещества, которое накапливается в печени и расходуется во время физических нагрузок.
Что делает триозофосфатизомераза?
Триозофосфатизомераза (ТФИ или TIM) является ферментом, который катализирует процессы превращения различных фосфатсодержащих соединений. Этот фермент также важен для гликолиза эффективного производства энергии. ТФИ был найден практически в каждом живом организме, не только у млекопитающих, но и у насекомых, грибов, растений и бактерий. Тем не менее, некоторые бактерии, которые не принимают участие в гликолизе, например, уреаплазма, не имеет в составе достаточного количества ТФИ.
У человека недостаток ТФИ связаны с прогрессивными, тяжелыми неврологическими расстройствами. Это расстройство называется дефицитом изомеразного триозофасфата.
Состояние приводит к хронической гемолитической анемии, которая может быть и врожденной. И хотя существуют различные мутации, вызывающие это заболевание, наиболее задействована в этом мутация глутаминовой кислоты.
Триозофосфатизомераза является высокоэффективным ферментом, благодаря которому проведение реакции в организме проходит в миллиарды раз быстрее, чем это имело бы место в природе. Реакция происходит настолько быстро, что ТФИ часто называют идеальным катализатором.
Наследственная гемолитическая анемия 2-го типа
Гемолитическая анемия возникает, когда костный мозг не в состоянии заменить разрушающиеся красные кровяные клетки новыми.
Иммунная гемолитическая анемия возникает, когда иммунная система ошибочно воспринимает свои собственные красные кровяные клетки, как чужеродные вещества. Антитела затем начинают действовать против красных кровяных клеток. Эти антитела атакуют эритроциты и заставляют их разрушаться раньше положенного срока.
Эритроциты при гемолитической анемии разрушаются из-за:
- генетических дефектов (например, серповидно-клеточной анемии, талассемии и дефиците G6PD);
- воздействия некоторых химических веществ, наркотиков и токсинов;
- инфекций.
Другие причины:
- сгустки крови в мелких кровеносных сосудах;
- переливание крови от донора с типом крови, не соответствующим типу крови пациента.
Симптомы наследственной гемолитической анемии
При легкой форме симптомы отсутствуют. При наследственной форме недомогание начинается появляться уже в первые месяцы жизни или же в подростковом возрасте.
Основные симптомы:
- чувство слабости, усталости, вялость;
- новорожденные плохо едят, постоянно спят или много кричат;
- бледный цвет кожи;
- дыхательные нарушения;
- болезненность языка;
- синие ногти;
- сонливость, беспокойство, раздражительность.
Нарушение метаболизма нуклеотидов
Чем опасно нарушение метаболизма нуклеотидов и как оно проявляется? По сути это то же самое нарушение процесса выработки или взаимодействия ферментов между собой, которое влечет последствия в виде различных нарушений работы внутренних органов, состава крови, процессов метаболизма, усвоения питательных веществ и обеспечения клеток энергией.
Соединение АТФ, обеспечивающее клетки энергией, это тоже нуклеотид. Без нормального синтеза АТФ и других нуклеотидов организм человека не может нормально существовать и полноценно усваивать питательные вещества. Клетки не получают нужных соединений, следовательно, не справляются со своими функциями. Нарушение метаболизма нуклеотидов прежде всего сказывается на состоянии крови, поэтому любой вид анемии должен стать поводом для визита к доктору.
Как известно, анемия лишь сигнализирует о нарушении, а не является первопричиной серьезного заболевания.
Источники статьи:
https://www.ncbi.nlm.nih.gov/
https://cmgm.stanford.edu/
https://library.med.utah.edu/
https://www.nlm.nih.gov/
https://www.quora.com/
https://www.wiley.com/
https://www.wiley.com/
https://www.proteopedia.org/
По материалам:
U.S. Department of Health and Human Services, National Institutes of Health
https://library.med.utah.edu
National Center for Biotechnology Information, U.S. National Library of Medicine
https://cmgm.stanford.edu
https://www.wiley.com
https://www.proteopedia.org
Dr. Shashank Rai
Смотрите также:
У нас также читают:
При некоторых
состояниях можно наблюдать повышение содержания глюкозы в крови –
гипергликемию, а также понижение концентрации глюкозы – гипогликемию.
Гипергликемия является довольно частым симптомом различных заболеваний, прежде
всего связанных с поражением эндокринной системы.
Сахарный диабет. В регуляции гликолиза и глюконеогенеза
большую роль играет инсулин. При недостаточности содержания инсулина возникает
заболевание, которое носит название «сахарный диабет»: повышается концентрация
глюкозы в крови (гипергликемия), появляется глюкоза в моче (глюкозурия) и
уменьшается содержание гликогена в печени. Мышечная ткань при этом утрачивает
способность утилизировать глюкозу крови. В печени при общем снижении
интенсивности биосинтетических процессов: биосинтеза белков, синтеза жирных
кислот из продуктов распада глюкозы – наблюдается усиленный синтез ферментов
глюконеогенеза. При введении инсулина больным диабетом происходит коррекция
метаболических сдвигов: нормализуется проницаемость мембран мышечных клеток для
глюкозы, восстанавливается соотношение между гликолизом и глюко-неогенезом.
Инсулин контролирует эти процессы на генетическом уровне как индуктор синтеза
ключевых ферментов гликолиза: гексокиназы, фос-фофруктокиназы и пируваткиназы.
Инсулин также индуцирует синтез гли-когенсинтазы. Одновременно инсулин
действует как репрессор синтеза ключевых ферментов глюконеогенеза. Следует
отметить, что индукторами синтеза
ферментов глюконеогенеза служат глюкокортикоиды. В связи с этим при инсулярной
недостаточности и сохранении или даже повышении секреции кортикостероидов (в
частности, при диабете) устранение влияния инсулина приводит к резкому
повышению синтеза и концентрации ферментов глюконеогенеза, особенно
фосфоенолпируват-карбоксикиназы, определяющей возможность и скорость
глюконеогенеза в печени и почках.
Развитие
гипергликемии при диабете можно рассматривать также как результат возбуждения
метаболических центров в ЦНС импульсами с хе-морецепторов клеток, испытывающих
энергетический голод в связи с недостаточным поступлением глюкозы в клетки ряда
тканей. Роль системы фруктозо-2,6-бисфосфата в регуляции метаболизма углеводов,
а также нарушения ее функционирования при сахарном диабете см. главу 16.
Гипергликемия
может возникнуть не только при заболевании поджелудочной железы, но и в
результате расстройства функции других эндокринных желез, участвующих в
регуляции углеводного обмена. Так, гипергликемия может наблюдаться при
гипофизарных заболеваниях, опухолях коркового вещества надпочечников,
гиперфункции щитовидной железы. Иногда гипергликемия появляется во время
беременности. Наконец, гипергликемия возможна при органических поражениях ЦНС,
расстройствах мозгового кровообращения, болезнях печени воспалительного или
дегенеративного характера. Поддержание постоянства уровня глюкозы в крови, как
отмечалось,– важнейшая функция печени, резервные возможности которой в этом
отношении весьма велики. Поэтому гипергликемия, обусловленная нарушением
функции печени, выявляется обычно при тяжелых ее поражениях.
Большой
клинический интерес представляет изучение реактивности организма на сахарную
нагрузку у здорового и больного человека. В связи с этим в клинике довольно
часто исследуют изменения во времени уровня глюкозы в крови, обычно после
приема per os 50 г или 100 г глюкозы, растворенной в
теплой воде,– так называемая сахарная нагрузка. При оценке построенных
гликемических кривых обращают внимание на время максимального подъема, высоту
этого подъема и время возврата концентрации глюкозы к исходному уровню. Для
оценки гликемических кривых введено несколько показателей, из которых наиболее
важное значение имеет коэффициент Бодуэна:
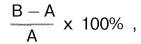
где А –
уровень глюкозы в крови натощак; В – максимальное содержание глюкозы в крови
после нагрузки глюкозой. В норме этот коэффициент составляет около 50%.
Значения, превышающие 80%, свидетельствуют о серьезном нарушении обмена
углеводов.
Гипогликемия.
Нередко гипогликемия связана с понижением функций тех эндокринных желез,
повышение функций которых приводит, как отмечалось, к гипергликемии. В
частности, гипогликемию можно наблюдать при гипофизарной кахексии, аддисоновой
болезни, гипотиреозе. Резкое снижение уровня глюкозы в крови отмечается при
аденомах поджелудочной железы вследствие повышенной продукции инсулина β-клетками
панкреатических островков. Кроме того, гипогликемия может быть вызвана
голоданием, продолжительной физической работой, приемом
β-ганглиоблока-торов. Низкий уровень глюкозы в крови иногда отмечается при
беременности, лактации.
Гипогликемия
может возникнуть при введении больным сахарным диабетом больших доз инсулина.
Как правило, она сопровождает почечную глюкозурию, возникающую вследствие
снижения «почечного порога» для глюкозы.
Глюкозурия.
Обычно присутствие глюкозы в моче (глюкозурия) является результатом нарушения
углеводного обмена вследствие патологических изменений в поджелудочной железе
(сахарный диабет, острый панкреатит и т.д.). Реже встречается глюкозурия
почечного происхождения, связанная с недостаточностью резорбции глюкозы в
почечных канальцах. Как временное явление глюкозурия может возникнуть при
некоторых острых инфекционных и нервных заболеваниях, после приступов
эпилепсии, сотрясения мозга.
Отравления
морфином, стрихнином, хлороформом, фосфором также обычно сопровождаются
глюкозурией. Наконец, необходимо помнить о глюкозурии алиментарного
происхождения, глюкозурии беременных
и глюкозурии
при нервных стрессовых состояниях (эмоциональная глюкозурия).

Изменение углеводного обмена при гипоксических состояниях. Отставание скорости окисления пирувата
от интенсивности гликолиза наблюдается чаще всего при гипоксических состояниях,
обусловленных различными нарушениями кровообращения или дыхания, высотной
болезнью, анемией, понижением активности системы тканевых окислительных
ферментов при некоторых инфекциях и интоксикациях, гипо- и авитаминозах, а
также в результате относительной гипоксии при чрезмерной мышечной работе.
При усилении
гликолиза происходит накопление пирувата и лактата в крови, что сопровождается
обычно изменением кислотно-основного равновесия, уменьшением щелочных резервов
крови. Увеличение содержания лактата и пирувата в крови может наблюдаться также
при поражениях паренхимы печени (поздние стадии гепатита, цирроз печени и т.п.)
в результате торможения процессов глюконеогенеза в печени.
Гликогенозы.
Ряд наследственных болезней связан с нарушением обмена гликогена. Эти болезни
получили название гликогенозов. Они возникают в связи с дефицитом или полным
отсутствием ферментов, катализирующих процессы распада или синтеза гликогена, и
характеризуются избыточным его накоплением в различных органах и тканях (табл.
10.2).
Гликогеноз I типа
(болезнь Гирке) встречается наиболее часто, обусловлен наследственным дефектом
синтеза фермента глюкозо-6-фосфатазы в печени и почках. Болезнь наследуется по
аутосомно-рецессивному типу. Патологические симптомы появляются уже на первом
году жизни ребенка: увеличена печень, нередко увеличены почки. В результате
гипогликемии появляются судороги, задержка роста, возможен ацидоз. В крови –
повышенное количество лактата и пирувата. Введение адреналина или глюка-гона
вызывает значительную гиперлактатацидемию, но не гипергликемию, так как
глюкозо-6-фосфатаза в печени отсутствует и образования свободной глюкозы не
происходит.
