Наследственная микросфероцитарная анемия симптомы

В статье приведен обзор литературы, касающийся клинических и лабораторных проявлений, диагностики, лечения и прогноза наследственной микросфероцитарной анемии. Описаны результаты собственных наблюдений двоих пациентов, находящихся на лечении в онкогематологическом отделении Йошкар-Олинской детской городской больницы.
Hereditary microspherocytosis (Minkowsky — Shauffard disease)
The paper presents a literature review of clinical and laboratory manifestations, diagnosis, treatment and prognosis of hereditary microspherocytic anemia. It is describes the results of his own observations of two patients treated in oncohematological office in Yoshkar-Ola City Children’s Hospital.
Наследственный микросфероцитоз был впервые описан в 1900 году Минковским, а в дальнейшем более подробно — Шоффаром. Распространенность данного заболевания — 1:5000 населения, наиболее часто встречается у жителей Северной Европы [1, 2].
Патогенез. Врожденная микросфероцитарная гемолитическая анемия представляет собой семейное заболевание, наследуемое по аутосомно-доминантному типу. В основе заболевания лежит генетический дефект белка мембраны эритроцитов, в результате чего повышается ее проницаемость для ионов натрия, что приводит к набуханию эритроцитов, нарушению способности эритроцитов деформироваться, отщеплению в селезенке части их поверхности, укорочению продолжительности их жизни и разрушению макрофагами селезенки [3, 4]. Патология эритроцитов проявляется морфологической аномалией — микросфероцитозом. Продолжительность пребывания микросфероцитов в циркулирующей крови резко уменьшена, средний срок их пребывания в кровеносном русле может составлять 12-14 дней (вместо нормальных 120-125 дней) [5].
Клиническая картина. Центральное место в клинической картине принадлежит гемолитическому синдрому, который проявляется тремя кардинальными признаками: желтухой, спленомегалией и анемией [5]. Могут наблюдаться признаки замедленного развития, а также нарушение лицевого скелета в виде «башенного черепа», седловидного носа, высокого стояния неба, нарушение расположения зубов, узких глазниц [6]. Выраженность анемического синдрома различна. Часто наблюдается умеренное снижение гемоглобина. У некоторых больных анемия вообще отсутствует. Наиболее резкая анемизация наблюдается в период гемолитического криза. Микросфероцитарная гемолитическая анемия имеет хроническое течение и сопровождается периодическими кризами и ремиссиями. Гемолитический криз возникает под влиянием провоцирующих факторов (инфекция, переохлаждение, переутомление, беременность и другие) и проявляется резким усилением симптомов на фоне непрерывно текущего гемолиза [6]. При этом повышается температура в связи с массовым распадом эритроцитов, увеличивается интенсивность желтухи, выражена гепатомегалия, селезенка плотная и гладкая, нередко болезненная в результате напряжения капсулы при кровенаполнении или перисплените. Гемолитическая болезнь нередко осложняется приступами печеночной колики, вследствие образования пигментных камней в желчном пузыре и в желчных протоках. В связи с приступами печеночной колики и застоем желчи в печени у больных могут наблюдаться симптомы ангиохолецистита и паренхиматозного гепатита с появлением прямого билирубина в крови. При обострении болезни наблюдается наклонность к носовым кровотечениям [3, 7]. Несмотря на врожденный характер, болезнь лишь в редких случаях проявляется в первые дни после рождения, обычно симптомы проявляются в детском, чаще в 3-10 лет, или зрелом возрасте [8].
Лабораторная диагностика. При микроскопическом исследовании препаратов периферической крови выявляются сфероциты, характеризующиеся уменьшением значений среднего диаметра (меньше 7,2-7,0 мкм) на фоне нормального среднего объема МСV и увеличенного значения МСНС. Кривая распределения эритроцитов по размеру (кривая Прайс-Джонса) на графике смещена влево. Анемия носит нормохромный характер. Величина RDW превышает 12% (анизоцитоз). Ретикулоцитоз — 15%-30% [1, 10]. Число лейкоцитов обычно нормальное. При гемолитических кризах отмечается нейтрофильный лейкоцитоз со сдвигом влево. Количество тромбоцитов варьирует в пределах нормы. Содержание непрямого билирубина в крови повышено умеренно и, как правило, не превышает 50-70 мкмоль/л [6, 7]. Аутоантитела на мембране эритроцитов не выявляются, прямая проба Кумбса — отрицательная. Характерным лабораторным признаком является снижение осмотической резистентности эритроцитов по отношению к гипотоническим растворам хлорида натрия. Начало гемолиза при наследственном микросфероцитозе соответствует 0,6-0,7%, а конец — 0,4% вместо 0,48-0,22% в норме [1, 9]. Снижение осмотической резистентности свидетельствует о преобладании в крови эритроцитов сферической формы — сфероцитов, которые менее стойки к осмотическому гемолизу, чем нормальные макропланоциты (рис. 1).
Рисунок 1. Морфология микросфероцитов в мазках периферической крови больного (слева), здорового (справа)
 Дифференциальная диагностика наследственного микросфероцитоза сводится к диагностике гемолитической анемии вообще. Многим больным ошибочно ставят диагноз синдрома Жильбера, хронического гепатита или даже цирроза печени, а анемию считают следствием этих заболеваний. Во всех случаях желтухи необходимо тщательное обследование больного независимо от содержания гемоглобина.Преимущественное увеличение содержания непрямого билирубина, ретикулоцитов, выявляемый при просмотре мазка микросфероцитоздают основание для правильного диагноза. Затем необходима дифференциальная диагностика аутоиммунной гемолитической анемии и микросфероцитоза, так как аутоиммунные гемолитические анемии часто дают симптоматический микросфероцитоз [3]. В этой ситуации помогают тщательное выяснение анамнеза, давности заболевания, наличие подобного заболевания у родственников, выявление изменений скелета, постановка проб, позволяющих выявить аутоантитела (прямая проба Кумбса).
Дифференциальная диагностика наследственного микросфероцитоза сводится к диагностике гемолитической анемии вообще. Многим больным ошибочно ставят диагноз синдрома Жильбера, хронического гепатита или даже цирроза печени, а анемию считают следствием этих заболеваний. Во всех случаях желтухи необходимо тщательное обследование больного независимо от содержания гемоглобина.Преимущественное увеличение содержания непрямого билирубина, ретикулоцитов, выявляемый при просмотре мазка микросфероцитоздают основание для правильного диагноза. Затем необходима дифференциальная диагностика аутоиммунной гемолитической анемии и микросфероцитоза, так как аутоиммунные гемолитические анемии часто дают симптоматический микросфероцитоз [3]. В этой ситуации помогают тщательное выяснение анамнеза, давности заболевания, наличие подобного заболевания у родственников, выявление изменений скелета, постановка проб, позволяющих выявить аутоантитела (прямая проба Кумбса).
Лечение и прогноз. Лечение во время гемолитического криза направлено на ликвидацию анемии, гипоксии, гипербилирубинемии. Методом выбора при лечении наследственного сфероцитоза является спленэктомия, оптимальная в возрасте 4-5 лет. Спленэктомия обеспечивает практическое выздоровление, несмотря на сохранность сфероцитоза. Показанием к спленэктомии при микросфероцитозе являются постоянная или возникающая в виде кризов анемия, значительная гипербилирубинемия, даже без анемии, появление болей в правом подреберье, отставание в развитии у детей [3]. Переливания крови (эритроцитарной массы) показаны в случае тяжелого гемолитического криза [5]. Прогноз при наследственном микросфероцитозе благоприятный. Вероятность развития заболевания у детей, если один из супругов болен микросфероцитозом, несколько ниже 50% [9].
Клинический случай № 1. Больной С., 1 год 10 мес., с 01.06.09 г. по 09.06.09 г. находился на стационарном обследовании в онкогематологическом отделении Йошкар-Олинской детской городской больницы. Из анамнеза известно, что ребенок от первой беременности, родился недоношенным, с массой тела 900 грамм. Выхаживался в отделении второго этапа выхаживания недоношенных. Наследственность неизвестна, так как в четырехмесячном возрасте был усыновлен. С рождения отмечались снижение уровня гемоглобина в анализе крови, иктеричность кожных покровов. С декабря 2008 года наблюдается гематологом по поводу анемии недоношенных, принимал препараты железа. При поступлении жалобы на вялость, слабость, повышение температуры до фебрильных цифр, бледность и желтушное окрашивание кожных покровов. При пальпации печень выступает из-под края реберной дуги на 2,5 см, селезенка — на 2 см, мягкая, эластичная.
Общий анализ крови от 01.06.09 г.: HGB — 106 g/l, RBC — 3,9×10¹²/l, WBC — 11,6×109/l, Ht — 26%, MCV — 68,8 fl, MCH — 25,8 pg, МСНС — 375 g/l, RDW — 20,5%, PLT — 434×109/l, СОЭ — 6 мм/ч, в лейкоцитарной формуле: эозинофилы — 10%, с/я нейтрофилы — 34%, лимфоциты — 47%, моноциты — 9%.
Анемия носит нормохромный характер. В мазках крови преобладают микросфероциты, отличающиеся отсутствием характерного для нормальных эритроцитов центрального просветления, что подтверждается графически на кривой Прайс-Джонса, отражающей количественные соотношения эритроцитов различных диаметров. Вершина кривой Прайс-Джонса растянута и сдвинута влево в сторону микроцитов. Кроме того, в мазках крови просматриваются нормоциты и единичные макроциты, это подтверждает увеличение индекса RDW — 20,5%. Во многих эритроцитах определяется базофильная пунктация и полихроматофилия. Ретикулоцитоз — 27%. Осмотическая резистентность эритроцитов: min — 0,52%, max — 0,34% (при норме 0,48-0,22%) — определяется понижение резистентности по отношению к гипотоническим растворам поваренной соли. Биохимический анализ от 02.06.09 г.: концентрация непрямого билирубина — 29,9 мкмоль/л, АЛТ — 15 Е/л, АСТ — 26 Е/л, щел. фосфатаза — 415 Е/л, ЛДГ — 273 Е/л, показатели метаболизма железа в пределах нормы: сывороточное Fe — 14,4 мкм/л, ОЖСС — 69,9 мкм/л. Отрицательный результат прямой пробы Кумбса позволил исключить аутоиммунную гемолитическую анемию.
При наследственном микросфероцитозе картина крови характеризуется патологической триадой со стороны эритроцитов: 1) микросфероцитозом; 2) ретикулоцитозом; 3) пониженной осматической резистентностью. В нашем случае все три фактора хорошо выражены. Больному был выставлен диагноз «наследственная микросфероцитарная гемолитическая анемия».
Ребенок выписан в стабильном состоянии 09.06.09 г. с рекомендациями: наблюдение гематолога и педиатра, общий и биохимический анализы крови 1 раз в 3 месяца.
24.06.09 г. больной С. повторно поступает в онкогематологическое отделение. При поступлении состояние тяжелое, жалобы на вялость, отсутствие аппетита, плохой сон, повышение температуры до 39,6°С, бледность, желтушность кожных покровов, темный цвет мочи. Зев гиперемирован, рыхлый. Увеличены лимфатические узлы шейной группы. Живот увеличен в объеме, печень выступает из-под края реберной дуги на 3,5 см, селезенка — на 5 см.
Общий анализ крови от 24.06.09 г.: HGB — 89 g/l, RBC — 3,4×10¹²/l, WBC — 27,7×109/l, Ht — 21%, MCV — 68,6 fl, MCH-25,5 pg, МСНС — 381 g/l, RDW — 20,8%, PLT — 260×109/l, СОЭ — 12 мм/ч, в формуле: эозинофилы — 4%, базофилы — 1%, п/я нейтрофилы — 4%, с/я нейтрофилы — 15%, лимфоциты — 20%, моноциты — 1%, атипичные мононуклеары — 55%. Ретикулоцитоз — 46,7%. В мазках крови до 50% микросфероцитов. Непрямой билирубин — 41 мкмоль/л, АЛТ — 19 Е/л, АСТ — 45 Е/л, щел. фосфатаза — 316 Е/л, ЛДГ — 295 Е/л. Определяется повышенное содержание стеркобилина в кале. В моче отмечается уробилинурия, выделение уратов и кристаллов мочевой кислоты, объясняемое повышенным распадом эритроцитов. ИФА на вирус Эпштейна — Барр (инфекционный мононуклеоз) — положительный.
Учитывая у ребенка наличие интоксикации, лихорадки, увеличение шейных групп лимфоузлов, в крови высокий лейкоцитоз, мононуклеары до 55%, положительный ИФА, был диагностирован инфекционный мононуклеоз, который в свою очередь явился пусковым моментом для развития у мальчика гемолитического криза.
Проведено лечение: диета, постельный режим, инфузионная и противовирусная терапия. В результате терапии лихорадка купирована, уменьшились размеры печени, селезенки и лимфатических узлов. Общий анализ крови от 06.07.09 г.: HGB — 104g/l, RBC — 3,9×10¹²/l, WBC — 10,7×109/l, Ht — 28%, MCV — 73,3 fl, MCH — 26,4 pg, МСНС — 360 g/l, RDW — 21,8%, PLT — 452×109/l, СОЭ — 2 мм/ч, в лейкоцитарной формуле: эозинофилы — 5%, п/я нейтрофилы — 5%, с/я нейтрофилы — 25%, лимфоциты — 47%, моноциты — 8%, атипичные момонуклеары — 10%. Ретикулоцитоз — 9,3%. Количество микросфероцитов снизилось до 23%. Непрямой билирубин — 18,8 мкмоль/л. Нормализовались аппетит и сон. В стабильном состоянии 09.07.09 г. ребенок выписан домой с рекомендациями: наблюдение гематолога 1 раз в 3 месяца, общий анализ крови с ретикулоцитами и биохимический анализ крови 1 раз в 3 месяца, контроль УЗИ брюшной полости 1 раз в год.
Клинический случай № 2. Больная Г., 12 лет, 22.09.09 г. переведена в онкогематологическое отделение Йошкар-Олинской детской городской больницы из инфекционного стационара. При поступлении жалобы на заложенность носа, боль в горле, общую слабость, увеличение шейных и затылочных лимфоузлов, лихорадка до 39,2°С, иктеричность кожных покровов, гепатоспленомегалия с выраженной плотностью паренхиматозных органов. Из анамнеза известно, что отец девочки страдает синдромом Жильбера и у девочки с рождения на фоне повышения температуры, ОРВИ — появляется желтушность кожи, склер.
Общий анализ крови от 23.09.09 г.: HGB — 61g/l, RBC — 1,8×10¹²/l, WBC — 10,7×109/l, Ht — 16%, MCV — 85 fl, MCH — 32,5 pg, МСНС — 382g/l, RDW — 20,3%, PLT — 162×109/l, СОЭ — 48 мм/ч, в лейкоцитарной формуле: миелоциты — 1%, метамиелоциты — 2%, п/я нейтрофилы — 29%, с/я нейтрофилы — 9%, лимфоциты — 24%, моноциты — 4%, атипичные мононуклеары — 31%. Ретикулоцитоз — 82,5%. В мазках крови значительное количество микросфероцитов. Осмотическая резистентность эритроцитов: min — 0,72%, max — 0,42%, определяется резкое понижение резистентности по отношению к гипотоническим растворам поваренной соли. Повышено содержание уробилина в моче и стеркобилина в кале. Биохимический анализ крови от 23.09.09 г.: АЛТ — 71 Е/л, АСТ — 78 Е/л, ЛДГ 1234 Е/л, билирубин прямой — 5,68 мкмоль/л, непрямой — 54,8 мкмоль/л. Прямая проба Кумбса — отрицательная.
Тяжелая нормохромная анемия, обнаружение значительного количества микросфероцитов в препаратах крови, выраженный ретикулоцитарный криз, резкое понижение осмотической резистентности эритроцитов, гипербилирубинемия, а также наличие сходной симптоматики у отца дали основание диагностировать у девочки гемолитический криз наследственной микросфероцитарной анемии, спровоцированный инфекционным мононуклеозом (ИФА на вирус Эпштейна — Барр — положительный). Осмотр инфекциониста подтверждает диагноз инфекционного мононуклеоза.
Больной были назначены инфузионная, антибактериальная и противовирусная терапия, витамины. На фоне лечения состояние пациентки стабилизировалось. Общий анализ крови от 12.10.09 г. : HGB — 106g/l, RBC — 3,5×10¹²/l, WBC — 3,9×109/l, Ht — 29,3%, MCV — 83,8 fl, MCH — 30,4 pg, МСНС — 362 g/l, RDW — 217,8%, PLT — 170×109/l, СОЭ — 8 мм/ч, в формуле: базофилы — 1%, п/я нейтрофилы — 4%, с/я нейтрофилы — 62%, лимфоциты — 20%, моноциты — 4%, атипичные мононуклеары — 9%. Ретикулоцитоз — 13,1%. Биохимический анализ крови: АЛТ — 41 Е/л, АСТ — 32 Е/л, билирубин прямой — 2,75 мкмоль/л, непрямой — 24,35 мкмоль/л. По данным УЗИ брюшной полости отмечается положительная динамика в виде уменьшения размеров печени и селезенки. Девочка выписана домой 13.10.09 г. с рекомендациями: наблюдение гематолога, инфекциониста и педиатра, общий анализ крови с ретикулоцитами 1 раз в 3 месяца, контроль УЗИ брюшной полости.
Оба пациента находятся на диспансерном учете у врача-гематолога.
Диагноз врожденного микросфероцитоза представляет порой известные трудности. Наиболее типичные проявления гемолиза — желтушность склер и кожных покровов — не всегда бывают правильно расценены врачом. Описанные нами клинические случаи являются прямым подтверждением этого. У обоих пациентов с рождения определялись иктеричность склер и кожных покровов, но подробного обследования, до развития гемолитического криза, больным не проводилось. Наличие сходной симптоматики у отца девочки (синдром Жильбера?) дает возможность предположить, что пациентка Г. заболевание унаследовала от отца. Наследственность больного С. неизвестна.
В обоих случаях провоцирующим фактором развития гемолитического криза явился вирус Эпштейна — Барр. Дети и раньше болели вирусными инфекциями, но развития гемолитического криза они не вызывали. Возможно, не всякая, а лишь определенная группа вирусов может вызывать кризы. Этот вопрос остается открытым, так как на примере двух случаев нельзя утверждать, что вирус Эпштейна — Барр всегда провоцирует развитие гемолитического криза у больных наследственным микросфероцитозом.
Е.В. Ширданина, З.С. Гордеева
Йошкар-Олинская детская городская больница, г. Йошкар-Ола
Ширданина Екатерина Валерьевна — врач клинико-диагностической лаборатории
Литература:
1. Погорелов В.М., Козинец Г.И., Ковалева Л.Г. Лабораторно-клиническая диагностика анемий. — Москва. Медицинское информационное агентство, 2004. — C. 136-137.
2. Коколина В.Ф., Румянцев А.Г. Практическое руководство по детским болезням. Гематология/Онкология детского возраста. — Том 4. — М.: Медпрактика-М, 2004. — C. 169-172.
3. Воробьев А.И. Руководство по гематологии. — Том 2. — М.: Медицина, 1985. — C. 46-54.
4. Кишкун А.А. Руководство по лабораторным методам диагностики. М.: ГЭОТАР-Медиа, 2007. — C. 468-680.
5. Кассирский И.А., Алексеев Г.А. Клиническая гематология. — М.: Медицина, 1970. — C. 235-242.
6. Луговская С.А, Почтарь М.Е. Гематологический атлас. — М.: Триада, 2004. — 227 с.
7. Колоколов Г.Р., Герасина Е.В., Ананьев О.Л и др. Анализы. Полный справочник. — М.: Эксмо, 2008. — C. 497-499.
8. Максимов В.А., Дамидович К.К., Федорчук А.Н. и др. Редкие болезни, клинические синдромы и симптомы заболеваний органов пищеварения. — М.: АдамантЪ, 2007. — C. 128-129.
9. Рукавицин О.А., Скворцов С.В., Зенина М.Н. Гематология. Атлас-справочник. СПб: Детство-Пресс, 2009. — C. 219-220.
10. Погорелов В.М., Козинец Г.И., Дягилева О.А. и др. Цветной атлас клеток системы крови. — М.: Практическая медицина, 2007. — C. 98-99.
Наследственный сфероцитоз (микросфероцитоз или болезнь Минковского-Шоффара) – эпидемиология, причины, клиника
Наследственный сфероцитоз (микросфероцитоз или болезнь Минковского-Шоффара) характеризуется гемолитической анемией внутриэритроцитного вида, ахолурической желтухой, высоким показателем ретикулоцитоза и спленомегалией.
К тому же отмечаются характерные эритроцитные признаки, в том числе микросфероцитоз, ослабление устойчивости эритроцита к гипотонному солевому раствору, повышение показателя самопроизвольного гемолиза (который выравнивается после назначения глюкозы), секвестрация эритроцитов в селезенке и положительный результат после удаления последней.
История изучения наследственного сфероцитоза – микросфероцитоза
Болезнь была описана Минковским в 1900 г., который, на сессии Общества врачей в Висбадене, сделал сообщение о 8 случаях, наблюдаемых на 3 поколениях с выявлением характерной для этого заболевания симптоматологии. Десятками лет раньше была описана, в определенных видах, одинаковая симптоматология.
Ценный вклад внес Шоффар, который, в 1907 г., определил наследственный характер гематологического расстройства, при котором развивается микроцитоз эритроцитов и понижение их устойчивости.
В 1911 г., по совету Micheli, Банти, Эпингер и др. провели первые операции по удалению селезенки. В последующие годы число сообщений увеличилось. Однако и в настоящее время продолжается описание болезни под различными, более или менее новыми аспектами.
Географическое распространение и частота наследственного сфероцитоза – микросфероцитоза
Распространение болезни носит повсеместный характер — встречается на всех материках, среди всех рас и лиц обоего пола. Наблюдаются некоторое преобладание среди белой расы, в частности у северноевропейских народов и относительная редкость случаев заболевания среди негров Африки и Америки. У нас в стране представляется как гемолитическая болезнь внутриэритроцитного вида наибольшого распространения.
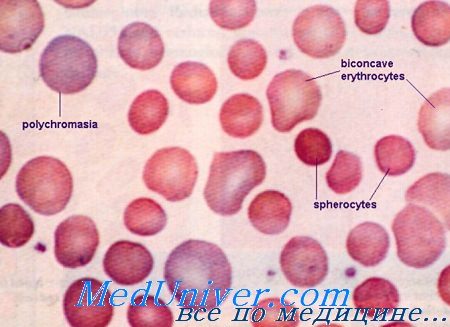
Мазок крови при наследственном сфероцитозе
Этиология наследственного сфероцитоза – микросфероцитоза
Болезнь передается преобладающим аутосомальным менделеевским способом (переходит по наследтсву от одного из родителей, независимо от пола, причем поражаемые лица гетерозиготные в отношении отягчений, болезнь выявляется у 50% потомства). Описаны и отдельные случаи, объяснение которых следует искать в мутациях, рождении незаконных детей или невысокой проницаемости отягчений у предшественников.
Наличие гомозиготных форм еще не доказано; видимо подобный продукт зачатия нежизнеспособный (Израель).
Клинические признаки наследственного сфероцитоза – микросфероцитоза
Начало наследственного сфероцитоза – микросфероцитоза. Несмотря на наследственный характер болезни лишь в редких случаях она выявляется вскоре после рождения или в раннем детстве. Чаще заболевание обнаруживается в условиях соматических преобразований на втором периоде детского возраста (7—8 лет) или у подростков. В отдельных случаях, при купании матерями обнаруживалось наличие отягчения уже на первый месяцах жизни ребенка, когда нашупывалась увеличенная селезенка (личные неопубликованные случаи).
Однако описаны и случаи проявления характерной картины заболевания лишь в возрасте 75 или даже 80 лет, что говорит о различном проникновении отягчения и хорошей компенсации на весьма продолжительный период времени. Конечно, болезнь выявима и раньше, но при условии проведения семейного исследования в попытке обнаружения скрытых случаев.
Формы проявления мало убедительны, в основном это признаки строения и общего характера (задержка физического развития с заниженной сосредоточенностью у детей школьного возраста, а у взрослых — неуспеваемость в работе коллектива; также описаны нехарактерные явления диспепсии). Вот почему период начала следует рассматривать больше как период отождествления наличия болезни.
Период разгара наследственного сфероцитоза – микросфероцитоза определяется по следующим характерным признакам:
а) Нарушения соматопсихического развития — отмечающиеся в большинстве случаев. У больных нередко coxpai яется детский аспект, в наступлении половой зрелости отмечается задержка (недоразвитие роста и веса и слабое половое развитие); при этом инфантилизм сопровождается и другими эндокринными растройствами ((Wintrobe).
б) Аспект покровов и слизистых оболочек. Бледность и желтушная окраска два элемента, которые, нередко, чередуются или проявляются одновременно. Тем не менее бледность покровов не чрезмерно резкая, поскольку костный мозг располагает большой способностью компенсации. Составляют исключение тяжелые анемии, при которых продолжительность жизни эритроцитов сокращается до менее 18—20 дней и процесс кроветворения не покрывает высокую степень разрушения красных кровяных клеток.
Желтуха наблюдается в 2/3 случаев, причем она локализуется на белковых оболочках, либо принимает характер общего распространения. Больные хорошо переносят эту желтуху, которая, в отдельных случаях, не проходит всю жизнь; тем не менее они проявляют физическую трудоспособность («больше желтушные, чем больные»). Интенсивность желтухи зависит не только от разрушения красных кровяных клеток, но и от работоспособности печени. В отличие от печеночной желтухи, при наследственном сфероцитозе в любом случае отсутствуют зуд, брадикардия, поскольку желтуха носит исключительно пигментный характер и отсутствует явление задержки желчных солей (ахолируческая желтуха).
в) Спленомегалия. Кроме бледности и желтухи спленомегалия составляет третий основной признак заболевания. Ее размеры колеблятся от едва ли прощупываемой селезенки до занимающей всю левую часть брюшной полости. В принципе она не чувствительна при прощупывании и хотя может быть обнаружена уже на первом году жизни, она постепенно увеличивается, достигая максимальной величины у взрослого человека. Вопреки тому факту, что спленомегалия последствие гемолитической гиперактивности, не установлена какая-либо взаимосвязь ее размера и клинического состояния.
Гигантская спленомегалия обусловливает нарушения, связанные с компрессией, а иногда болезненный периспленит, способствующий образованию распространенной спайки с прилегающими зонами, (Heilmeyer L., Busch D.).
г) Хроническое изъязвление голеней отмечается примерно в 1/3 случаев. В основном оно локализуется в дистальной части, возможно одной или обеих голенях. Изъязвление длится месяцы и даже годы, после выздоровления остаются зоны гиперпигментации, которые перемежаются с перламутровыми участками. Травма, будь она и небольшая, способствует развитию изъязвления. Наличие этого трофического нарушения составляет ценное доказательство внутриэритроцитной гемолитической анемии.
Поздний период наследственного сфероцитоза – микросфероцитоза. Поскольку болезнь наследственного характера ее течение отличается чередованием периодов улучшения и обострения болезни. Существенным элементом для течения болезни представляется сохранение или нарушение равновесия между повышенным расплавлением крови и высоким показателем восстановления красных кровяных клеток. В результате этих колебаний анемия и желтуха исчезают или обостряются. Когда оба явления клинически исчезают, лишь спленомегалия свидетельствует о наличии болезни и трофические расстройства голеней, естественно когда в прошлом бывали изъязвления.
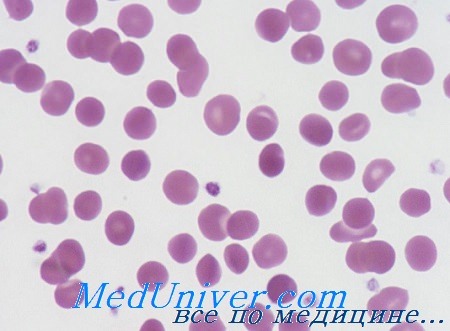
Мазок крови при наследственном сфероцитозе
Осложнения наследственного сфероцитоза гематологические или желчнопеченочные
а) Гематологические осложнения наследственного сфероцитоза — приступообразное усугубление анемии (деглобулизация) весьма важное событие в эволюции наследственного сфероцитоза. Они развиваются в результате нарушения равновесия между образованием и разрушением эритроцитов. У большинства больных, с явными клиническими явлениями наблюдается приступоподобное ухудшение анемии, явление, получившее, частично несоответствующее название «приступа деглобулизации». Патогенетический механизм явления подсказывает термин «апластический приступ».
Наступление приступа обусловливают весьма разнообразные причины, в том числе, инфекция, чрезмерное потребление спиртных напитков, физическое усилие, беременность, послеродовой период, менструация. В отдельных случаях диспептическое состояние, психическая травма или даже метеорологическое влияние благоприятствуют подобным приступам, а иногда и переливание совместимой крови. Однако нередко отсутствует какая-либо видимая причина, за счет которой можно отнести развитие приступа.
В принципе больные жалуются на общее плохое состояние, к которому относятся слабость (вплоть до прострации), сердцебиение, головная боль, тошнота, боль в животе и даже рвота, озноба и лихорадочное состояние (с повышением температуры до 39—40°С). Иногда наблюдается быстрое увеличение объема селезенки. В тяжелых случаях отмечаются коллапс и кома, требующих срочное определение в больницу, массивные переливания крови, за отсутствием которых может наступить летальный исход. Однако, помимо тяжелых форм, значительно чаще развиваются умеренные приступы, проявляющиеся усилением анемии и желтухи, которым сопутствуют слабость, явления диспепсии, гиперхромная моча и пр.
Длительность регенеративной фазы также колеблется. Так, при легких формах она составляет 3—4 дня, в то время как в тяжелых — 10—15 дней. С клинической точки зрения состояние больных возвращается к исходному — предприступному.
б) Желчно-печеночные осложнения наследственного сфероцитоза наблюдаются, в основном, у лиц в возрасте, отнюдь не составляя исключение даже у детей. У взрослых поражение желчного пузыря составляет 1/2 случаев, оно проявляется простым воспалением желчного пузыря, но наиболее часто желчнокаменным пигментным заболеванием (причем камни образованы из билирубината кальция). В некоторых случаях каменная болезнь осложняется резью в печени и явлениями ангиоколита.
В результате чрезмерной нагрузки печени в связи с необходимостью сопряжения косвенного билирубина на протяжении десятилетий, печень «ослабевает» развивается печеночная желтуха (помимо желтухи, за счет задержки) и осуществляется смешанная желтуха.
– Также рекомендуем “Лабораторная диагностика наследственного сфероцитоза – анализы при микросфероцитозе”
– Вернуться в раздел “гематология”
Оглавление темы “Гемолитические анемии”:
- Копропорфирия: причины, диагностика, лечение
- Классификация анемий: этиологическая, патогенетическая
- Клиническая диагностика анемии – признаки малокровия
- Лабораторная диагностика анемии в гематологии – методы исследования
- Причины гемолитических анемий – этиология, патогенез
- Классификация гемолитических анемий – этиологическая, патогенетическая
- Клиника гемолитической анемии – гемолитическая желтуха
- Лабораторная диагностика общего гемолитического синдрома – анализы
- Дифференциация причины гемолитической анемии – лабораторные методы
- Наследственный сфероцитоз (микросфероцитоз или болезнь Минковского-Шоффара) – эпидемиология, причины, клиника
