Наследственный сфероцитоз при гемолитической анемии
Медицина / Патология / Патология (статья)
Гемолитическая анемия: Классификация и Формы
Статья |
7-11-2018, 21:34
|
 АнемияПод определение «гемолитическая анемия» подпадает любая анемия, характеризующаяся преобладанием гемолиза (процессом распада эритроцитов) над эритропоэзом (процессом образования эритроцитов). Гемолиз может быть иммунный и неиммунный. Гемолитическая анемия бывает наследственные и приобретенные.
АнемияПод определение «гемолитическая анемия» подпадает любая анемия, характеризующаяся преобладанием гемолиза (процессом распада эритроцитов) над эритропоэзом (процессом образования эритроцитов). Гемолиз может быть иммунный и неиммунный. Гемолитическая анемия бывает наследственные и приобретенные.
Наследственная гемолитическая анемия
- Наследственная форма гемолитической анемии, обусловленная нарушением мембраны эритроцитов
- Наследственная форма гемолитической анемии, обусловленная нарушением активности ферментов эритроцитов
- Наследственная форма гемолитической анемии, обусловленная нарушением синтеза или структуры гемоглобина
Приобретенная гемолитическая анемия
- Анемия, обусловленная влиянием антител
- Анемия, обусловленная изменением структуры мембраны, вызванной соматической мутацией
- Анемия, обусловленная механическим повреждением оболочки эритроцитов
- Анемия, вызванная химическим повреждением эритроцитов
- Анемия, вызванная дефицитом витаминов (фолиевой кислоты и цианокобаламина)
- Анемия, вызванная разрушением эритроцитов паразитами
Отдельные формы наследственной гемолитической анемии
Наследственный микросфероцитоз
Болезнь Минковского-Шоффара (наследственный микросфероцитоз) – группа наследственных гемолитических анемий, характеризующихся образованием микросфероцитов (шаровидных эритроцитов) и обусловленных дефектом протеинов цитоскелета эритроцитов. При этом эритроциты теряют часть мембраны, уменьшается соотношение площади поверхности к объему, в результате чего эритроцит превращается в микросфероцит. Как правило, патология наследуется по аутосомно-доминантному признаку. Распространенность наследственного микросфероцитоза составляет примерно 1 случай на 1000-4500 человек.
При наследственном микросфероцитозе генетические нарушения влияют на протеины цитоскелета, преимущественно на те, которые объединяют цитоскелет с мембраной эритроцита. У большинства больных отмечается значительный дефицит спектрина, и только в некоторых случаях этот дефицит обусловлен генетическими дефектами самого спектрина.
Главные признаки наследственного микросфероцитоза – анемия, желтуха, спленомегалия (увеличенная селезенка). Анемия возникает из-за внутриклеточного распада эритроцитов. Желтуха развивается посредством непрямой гипербилирубинемии, может быть непостоянной и, как правило, слабо выражена у детей раннего возраста. Повышенное содержание билирубина в желчи часто является причиной образования пигментных желчных камней (даже у детей). Увеличение селезенки (спленомегалия) отмечается практически во всех случаях. При системных инфекционных патологиях интенсивность гемолиза может увеличиваться, в результате чего развивается спленомегалия.
Тяжелые формы наследственного микросфероцитоза характеризуются деформацией скелета: изменение расположения зубов, акрокефалия (башенный череп), высокое верхнее небо, микрофтальмия (уменьшение глазного яблока). В некоторых случаях отмечаются укороченные мизинцы. Могут образовываться трофические язвы на ногах.
Наследственный микросфероцитоз сопровождается апластическими кризами, которые провоцируются инфекцией (особенно парвовирусной).
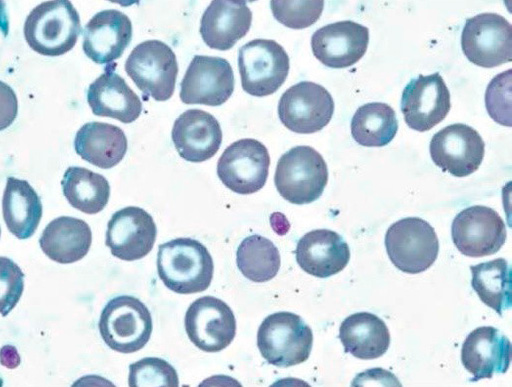
Микросфероцитоз – характерное изменение формы эритроцитов при этой патологии. При анализе мазка крови в биологическом материале наблюдаются микросфероциты в виде мелких клеток без центрального просветления (см рисунок 1). Отметим, что обнаружение микросфероцитов в мазках не всегда является признаком наследственного сфероцитоза.
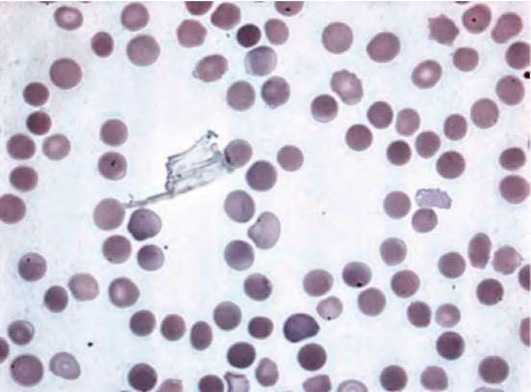
Рисунок 1. Наследственный микросфероцитоз. Микросфероциты в мазке периферической крови (окр. по Романовскому-Гимзе, ув. ×100)
Такой признак обнаруживается при аутоиммунной гемолитической анемии с неполными тепловыми агглютинами, при наследственных дизэритропоэтической анемии. Средний объем эритроцитов, как правило, остается в норме или незначительно снижен. Показатель среднего содержания гемоглобина в эритроцитах в норме или незначительно повышен. Средняя концентрация гемоглобина в эритроцитах повышена почти у 50% пациентов.
Количественным показателем сферичности эритроцитов является осмотическая устойчивость (она снижена). Уровень ретикулоцитов в крови при гемолитическом кризе может значительно повышаться. Миелограмма показывает резкое раздражение красного ростка. Дифференциальный диагноз проводят с аутоиммунной гемолитической анемией, для которой характерна положительная проба Кумбса, отсутствие этой патологии среди родственников пациента и отсутствие данных о начале заболевания в детском возрасте.
Основной метод лечения анемии при наследственном микросфероцитозе – спленэктомия, с помощью которой устраняется анемия; при этом нельзя устранить морфологический дефект эритроцитов.
Наследственная гемолитическая анемия при дефиците глюкозо-6-фосфат дегидрогеназы эритроцитов
Наследственная гемолитическая анемия, обусловленная дефицитом глюкозо-6-фосфат дегидрогеназы эритроцитов – наиболее распространенная ферментопатия эритроцитов из группы ферментопатий пентозофосфатного пути метаболизма глюкозы. Глюкозо-6-фосфатдегидрогеназа эритроцитов – олигомер (в зависимости от условий может быть димер или тетрамер), который состоит из субъединиц с молекулярной массой 56 000 D. По данным ВОЗ (Всемирной организации здравоохранения) во всем мире количество людей, страдающих этой патологией, составляет более 200 млн. Наиболее широкое распространение этого заболевания характерно для Средиземноморского региона (Сицилия, Греция, Сардиния), негроидной расы, жителей Ближнего и Дальнего востока.
Клиническая картина при наследственной форме гемолитической анемии полиморфна: степень тяжести патологии может колебаться от гемолитической анемии, возникающей спонтанно после рождения, до гемолитических кризов. Гемолитический криз, который может провоцироваться метаболическим ацидозом или гипогликемией, развивается за несколько часов. В тяжелых случаях у больного развивается гемоглобинурия и шок. Также наблюдаются желтуха, моча приобретает бурый или черный цвет, одышка, диарея, рвота, снижение артериального давления, развивается тяжелая анемия, увеличиваются печень (гепатомегалия) и селезенка (спленомегалия).
Тяжелый гемолитический криз может спровоцировать развитие ДВС-синдрома (диссеминированного внутрисосудистого свертывания крови). Некоторые пациенты не переносят конские бобы (Viciafaba), после употребления которых происходит молниеносное развитие гемолитического криза (это явление также известно, как фовизм или примахиновая анемия).
Дефицит глюкозо-6-фосфат дегидрогеназы эритроцитов необходимо подозревать во всех случаях острого гемолиза, особенно у лиц негроидной расы и жителей средиземноморского региона. Диагноз подтверждается путем проведения лабораторных анализов. Острый гемолиз характеризуется быстрым снижением гематокрита с одновременным повышением уровня гемоглобина и непрямого гемоглобина, а также снижением уровня гаптоглобина. Анализ мазка крови показывает наличие фрагментов эритроцитов. Основой диагностики считается качественное (при необходимости – количественное) определение активности глюкозо-6-фосфат дегидрогеназы эритроцитов. У пациентов с вариантом «А-» явление аномального гемолиза проходит, как правило, самостоятельно – такие больные не нуждаются в специальном лечении. В случае развития тяжелого гемолитического криза необходимо проводить форсированный диурез, профилактику ДВС-синдрома, плазмаферез (с целью удаления продуктов гемолиза).
Гемоглобинопатия
В случае возникновения качественной гемоглобинопатии происходит изменение аминокислотной последовательности цепей глобина. Талассемия (количественная гемоглобинопатия) характеризуется снижением образования цепей глобина без изменения их цепей. Нужно отметить, что разница между качественной и количественной гемоглобинопатиями не абсолютна.
Талассемия (анемия Кули) – группа патологий, обусловленных генетическим нарушением синтеза одной из цепей глобина. В норме процесс синтеза глобиновых цепей сбалансирован, поэтому свободных цепей глобина нет. В случае нарушения синтеза одной из цепей глобина баланс нарушается, образуются лишние цепи, которые агрегируют и откладываются в эритрокариоцитах. Среди жителей Средиземноморья наиболее распространена β-талассемия.
«Большая талассемия» (болезнь Кули, β-талассемия) – наследственная гемолитическая анемия, впервые описанная американскими педиатрами-гематологами Томасом Бентоном Кули (Thomas Benton Cooley) и Ли (P. Lee) в статье «Серия случаев спленомегалии у детей с анемией и необычными изменениями костей» («A Series of Cases of Splenomegaly in Children, with Anemia and Peculiar Bone Changes»), где были приведены случаи у выходцев из стран Средиземноморья. Для анемии Кули характерна тяжелая степень течения с самого детства, задержка роста и изменения костей в результате увеличения объема костного мозга, возникающие в случае отсутствия соответствующего лечения). Также при этой патологии у больного наблюдаются гепатомегалия, спленомегалия, гиперспленизм, деформации черепа (монголоидное лицо, башенный череп); желтуха, бледность и отложение меланина придают коже особый медный оттенок. Кроме этого, наблюдается перегрузка железом сердца, легких, печени, поджелудочной железы и других органов эндокринной системы, переломы костей, сдавления периферических нервов, разного рода инфекционные осложнения.
Результаты лабораторных исследований периферической крови показывают гипохромную анемию, ретикулоцитоз, мишеневидные эритроциты (см рис 2-4).
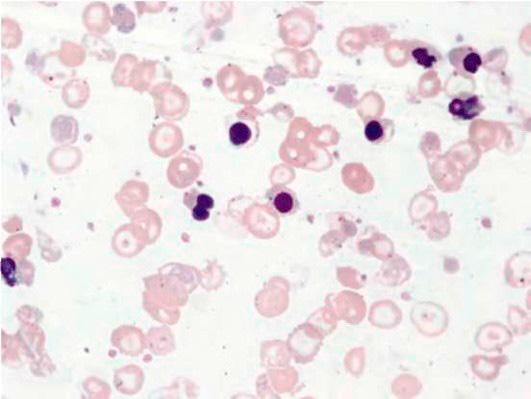
Рисунок 02. Анемия Кули (большая талассемия). Периферическая кровь. Микроцитоз, выраженная гипохромия, мишеневидные нормобласты и эритроциты (окр. по Романовскому-Гимзе, ув. ×100)
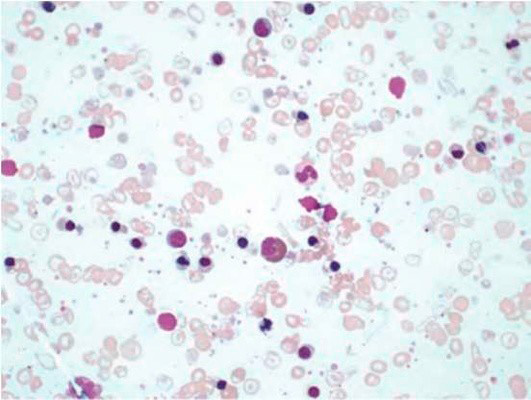
Рисунок 03. Анемия Кули (большая талассемия). Периферическая кровь (окр. по Романовскому-Гимзе, ув. ×50)

Рисунок 04. Анемия Кули (большая талассемия). Периферическая кровь. Множественные мишеневидные эритроциты (окр. по Романовскому-Гимзе, ув. ×100)
Миелограмма демонстрирует раздражение «красного ростка» и повышение количества сидеробластов. Также наблюдается повышение осмотической резистентности эритроцитов и количества билирубина за счет непрямой фракции. В крови повышается содержание железа и ферритина, развивается гемосидероз (чрезмерное отложение гемосидерина в тканях) внутренних органов. При гомозиготной β-талассемии необходимо проводить пренатальную диагностику – забор клеток плода из амниотической жидкости на предмет выявления мутации генов, отвечающих за кодирование β-цепи глобина, с применением метода полимеразной цепной реакции.
Без соответствующего лечения больные анемией Кули умирают в детском возрасте. Продлить жизнь, предупредить деформации костей и задержку роста можно путем регулярных трансфузий эритроцитарной массы (лучше переливать отмытые или размороженные эритроциты) при условии поддержания достаточно высокого уровня гемоглобина. В случае значительной спленомегалии и явлениях гиперспленизма больному показана спленэктомия (удаление селезенки). С целью предотвращения развития гемосидероза пациентам периодически назначают Деферазирокс (Эксиджад) или Дефероксамин (Десферал). Излечение возможно при аллогенной трансплантации костного мозга.
Серповидноклеточная анемия
Серповидноклеточная анемия обусловлена носительством гемоглобина, который меняет свою структуру в условиях гипоксии. Самой распространенной аномалией структуры гемоглобина является гемоглобинопатия Sα2β26 глу+вал. При гомозиготном носительстве можно говорить о серповидноклеточной анемии; при гетерозиготном носительстве – серповидноклеточная аномалия. Патология наследуется по аутосомно-доминантному признаку. При серповидноклеточной анемии наблюдается мутация, в результате которой в цепи глобина глутаминовая кислота заменяется валином. В результате растворимость гемоглобина S при отдаче кислорода снижается, что приводит к образованию геля.
Серповидноклеточная анемия наиболее распространена среди населения Центральной Африки, Турции, Индии, Кубы. У больных диагностируется анемия, тромботические осложнения, поражения костей и суставов (отмечаются некрозы плечевой и бедренной костей). Кроме этого, тромбозы осложняются инфарктами (сердца, легких, почек, селезенки, головного мозга), приступами сильной боли в области живота. У детей отмечаются нарушения физического (отставание в росте) и полового развития, ночное недержание мочи, нарушение зрения (тромбозы сосудов сетчатки). Также могут развиваться гемолитический, апластический и секвестрационные кризы, при этом в селезенке происходит резкое накопление эритроцитов, что вызывает гиповолемический шок и резкое снижение уровня гемоглобина.
Для анализов крови при апластической анемии характерны низкий уровень гемоглобина, наличие серповидных эритроцитов (рисунок 5), базофильная пунктация эритроцитов, их мишеневидность, повышение уровня ретикулоцитов и непрямого билирубина. Миелограмма демонстрирует раздражение «красного ростка».
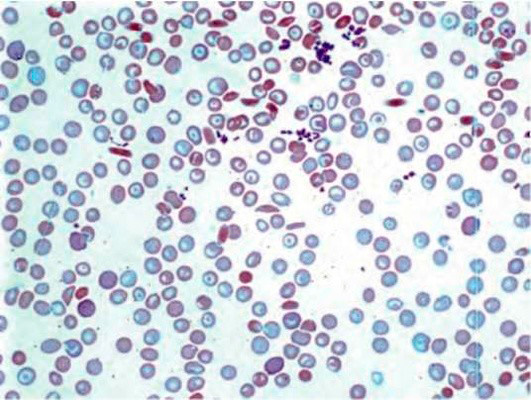
Рисунок 5. Серповидноклеточная анемия. Периферическая кровь. Серповидные и мишеневидные эритроциты. выраженная гипохромия эритроцитов (окр. по Романовскому-Гимзе, ув. ×100)
В качестве лечения применяют адекватную инфузионную терапию, переливания эритроцитарной массы, оксигенотерапии.
Приобретенная гемолитическая анемия
К приобретенным гемолитическим анемиям относится группа заболеваний разного патогенеза, которые объединяет внутрисосудистый гемолиз (гемолиз эритроцитов в периферической крови). В зависимости от механизма эритролиза приобретенная гемолитическая анемия может носить иммунный и неиммунный характер. Но, несмотря на разные патогенетические механизмы, клинические признаки этих анемий часто совпадают.
Гемолитическая анемия при механическом повреждении эритроцитов в средних и крупных сосудах
Гемолитическая анемия у пациентов с протезированными клапанами сердца и сосудами развивается примерно в 10% случаев при протезированном аортальном клапане. При использовании стеллитовых запирательных элементов частота гемолиза незначительно увеличивается (по сравнению с селиконовыми). Также некоторое увеличение частоты гемолиза отмечается при наличии околоклапанной регургитации и при малом диаметре клапана. Биопротезы (свиные клапаны) в редких случаях являются причиной механического гемолиза. Гораздо реже причиной гемолиза может быть также протезированный митральный клапан, так как трансклапанный градиент давления в этом случае ниже.
Гемолиз протезированными клапанами происходит в результате одновременного действия сразу нескольких факторов:
- Значительная сила сдвига, которая при турбулентном токе крови действует на мембрану эритроцитов, особенно когда под высоким давлением кровь проходит через маленькое отверстие (например, при околоклапанной регургитации)
- Отложения фибрина на участках неплотного прилегания кольца клапана к тканям сердца
- Прямое механическое повреждение эритроцитов при закрытии запирательного элемента
Значительное разрушение эритроцитов может наблюдаться после закрытия дефекта межпредсердной перегородки типа ostium primum заплатой из синтетического материала. Умеренное сокращение жизни эритроцитов с легкой анемией или без нее может наблюдаться при значительном обызвествлении аортального клапана. Механический гемолиз обнаруживается также у пациентов, перенесших аортокоронарное и аортобедренное шунтирование.
Тяжелые случаи механического гемолиза сопровождаются тяжелой анемией, ретикулоцитозом, обнаруживаются фрагментированные эритроциты (шизоциты), гемоглобинемия и гемоглобинурия, повышается активность лактатдегидрогеназы, снижается уровень гаптоглобина. Выведение железа из организма с мочой в виде гемосидерина или гемоглобина может вызвать дефицит железа в организме. В случае развития дефицита железа пациенту назначается пероральный прием препаратов железа. Терапия препаратами железа способствует повышению уровня гемоглобина и способствует снижению сердечного выброса и снижению интенсивности гемолиза. Отметим, что ограничение физической активности также способствуют снижению интенсивности распада эритроцитов. Если предпринимаемые меры не приводят к желаемому результату, нужно полностью устранить околоклапанную регургитацию или заменить протез.
Что такое наследственный сфероцитоз?
Наследственный сфероцитоз (сокр. НС, синдром/анемия Минковского-Шоффара) — наследственное заболевание, поражающее эритроциты. Характерными симптомами наследственного сфероцитоза являются разрушение эритроцитов в селезенке и их удаление из кровотока (гемолитическая анемия), пожелтение кожи (желтуха) и увеличение селезенки (спленомегалия).
Анемия Минковского-Шоффара поражает примерно 1 из 2000 человек. НС возникает в результате генетических изменений в пяти разных генах; ANK1, SLC4A1, SPTA1, SPTB и EPB42. Возраст начала варьируется, но часто встречается в возрасте от 3 до 7 лет. Симптомы могут развиться в младенчестве, но у некоторых людей с наследственным сфероцитозом нет никаких симптомов или симптомы незначительны, и они диагностируются в более позднем возрасте.
Подозрение на анемию Минковского-Шоффара основано на клинических особенностях и семейном анамнезе сфероцитоза или связанных с ним симптомов. Диагноз подтверждается на основании анализа крови. В качестве лечения анемии Минковского-Шоффара при тяжелой анемии используется хирургическое удаление селезенки (спленэктомия). Другие методы лечения включают в себя прием фолиевой кислоты (витамина B9) и переливание крови.
Признаки и симптомы
Наследственный сфероцитоз подразделяется на легкие, средние и тяжелые формы заболевания. Классификация основана на количестве гемоглобина, ретикулоцитов и билирубина и количестве спектрина в эритроцитах. Гемоглобин транспортирует кислород в крови. Ретикулоциты — незрелые эритроциты. Билирубин образуется в печени при разрушении гемоглобина. Спектрин — белок, который помогает сохранить форму клетки. Снижение гемоглобина и спектрина и увеличение ретикулоцитов и билирубина связаны с более тяжелым НС. Люди с тяжелой формой заболевания обычно диагностируются в более молодом возрасте, чем люди с умеренной или легкой формой анемией Минковского-Шоффара. Те, у кого мягкая форма НС, могут иметь компенсированный гемолиз. Это означает, что эритроциты создаются с той же скоростью, что и разрушаются. Эти люди не имеют заметных симптомов, и, следовательно, диагностируются в более позднем возрасте.

У людей с наследственный сфероцитозом эритроциты имеют круглую форму, похожую на шарик (сфероциты), а не на типичную форму пончика. Эти клетки чаще разрушаются при стрессе, чем нормальные эритроциты (осмотическая хрупкость). Наиболее часто у больных с НС возникают следующие признаки:
- анемия;
- увеличение селезенки (спленомегалия);
- пожелтение кожи или глаз (желтуха).
Анемия может вызвать крайнюю усталость и бледность кожи. Спленомегалия может вызвать боль в животе. Люди с НС часто обращаются за лечением с недавней или продолжающейся лихорадкой или инфекцией. Другие признаки у людей с синдромом Минковского-Шоффара встречаются реже. К ним относятся увеличение печени (гепатомегалия), нарушение роста и аллергические заболевания. Некоторым людям с НС, у которых заболевание диагностируется еще младенческом возрасте, может потребоваться регулярное переливание крови (зависимость от трансфузии). Однако, как правило, с возрастом потребность в переливании крови уменьшается.
Наиболее распространенная проблема, наблюдаемая у людей с наследственным сфероцитозом, — это развитие камней в желчном пузыре (желчнокаменная болезнь). Желчные камни могут быть обнаружены с помощью ультразвука, что позволяет ранней диагностику и лечение. Люди с НС также могут иметь гемолитический, апластический и мегалобластный кризы. Гемолитические кризисы часто вызываются вирусными заболеваниями и вызывают большее разрушение эритроцитов. Может потребоваться переливание крови, но гемолитический криз обычно протекает мягко. Апластические кризы встречаются реже и тяжелее, чем гемолитические, но также вызываются вирусными заболеваниями, особенно паровирусом B19. После того, как человек был заражен паровирусом B19, он остается невосприимчивым до конца жизни. Мегалобластные кризисы вызваны нехваткой витамина B9 (фолата). Детям, беременным женщинам и людям, восстанавливающимся после апластических кризисов, нужно больше фолата, поэтому они более восприимчивы. Применение фолатных добавок может также предотвратить мегалобластные кризисы.
У людей с НС ткань, которая создает клетки крови, может расти вне костного мозга, где она обычно находится (экстрамедуллярный гемопоэз). Также были сообщения о язвах ног, раке крови и небольших трещинах в слое сетчатки в задней части глаза (ангиоидные полосы). Тем не менее, эти проблемы не считаются общими и были зарегистрированы только у нескольких людей с синдромом/анемией Минковского-Шоффара.
Причины
Наследственный сфероцитоз вызывается изменениями (мутациями) в пяти различных генах, кодирующих белки, которые являются частью мембраны эритроцитов. Этими генами являются ANK1, SLC4A1, SPTA1, SPTB и EPB42. НС наследуется по аутосомно-доминантному типу в 75% случаев, а в 25% случаев — по аутосомно-рецессивному типу.
У всех нас есть две копии всех наших генов. Одна копия передается от мамы, а другая — от папы.
Рецессивные генетические нарушения возникают, когда человек наследует ненормальный ген от каждого родителя. Если человек получает один нормальный ген и один ненормальный ген заболевания, человек будет носителем заболевания, но обычно бессимптомным. Риск того, что двое родителей-носителей оба передадут аномальный ген и, следовательно, заразят ребенка, составляет 25% при каждой беременности. Риск родить ребенка, который будет носителем, как и родители, составляет 50% при каждой беременности. Вероятность для ребенка получить нормальные гены от обоих родителей составляет 25%. Все вероятности одинаковы для мужчин и женщин.
Доминантные генетические расстройства возникают, когда только одна копия ненормального гена необходима для того, чтобы вызвать конкретное заболевание. Аномальный ген может быть унаследован от любого из родителей или быть результатом мутации (изменения) гена у пострадавшего человека. Риск передачи ненормального гена от пораженного родителя потомству составляет 50% при каждой беременности. Риск одинаков для мужчин и женщин.
Вызывающие заболевание изменения в генах, связанных с НС, вызывают дефекты мембранных белков эритроцитов. Это уменьшает площадь поверхности клеток и оставляет клетки неспособными изменить форму под давлением. Это округлые сфероциты. Сфероциты попадают в селезенку. В селезенке сфероциты дополнительно повреждаются, и многие разрушаются. Те, что ускользнули от селезенки, возвращаются в кровообращение.
Затронутые группы населения
Наследственный сфероцитоз приблизительно поражает 1 из 2000 человек. О генетических изменениях, которые чаще встречаются у определенных групп людей (мутации основателей), не сообщалось. НС затрагивает мужчин и женщин в равной степени. Возраст при постановке диагноза НС часто находится в пределах 3-7 лет, но может проявляться и сразу в младенческом возрасте с тяжелым течением или во взрослом возрасте с легким течением.
Диагностика
Наследственный сфероцитоз впервые подозревается на основании клинической картины. Люди с анемией Минковского-Шоффара часто имеют одну или несколько характерных признаков; анемия, спленомегалия или желтуха. Желтуха является наиболее распространенной особенностью, которая развивается у маленьких детей. Другими распространенными причинами, по которым люди с НС обращаются к специалисту, являются анемия с неизвестной причиной или анемия, устойчивая к употреблению пищевых добавок, содержащих железо. Данные семейного анамнеза позволяют предположить, существуют ли родственники с диагнозом наследственный сфероцитоз, какими-либо характерными признаками или анамнезом хирургического удаления селезенки (спленэктомия) или желчного пузыря (холецистэктомия).
Для поиска сфероцитов проводится общий анализ крови для определения количества незрелых эритроцитов (ретикулоцитов) и формы эритроцитов. Также важно исключить аутоиммунную гемолитическую анемию. Это можно сделать с помощью прямого теста на антиглобулин. Этот тест может определить, вызвано ли разрушение эритроцитов неправильной иммунной реакцией.
Если диагноз неясен после клинического обследования и лабораторных испытаний, описанных выше, могут потребоваться дополнительные лабораторные исследования. Тест на связывание эозин-5 малеимида (э5м) является наиболее точным анализом. Тест на связывание э5м ищет мембранные белки, участвующие при болезни в образце эритроцитов. Если эти белки отсутствуют, результат предполагает НС.
Если необходимо подтвердить диагноз НС, с помощью гель-электрофореза могут провести анализ мембран эритроцитов. Это исследование может сказать, насколько повреждены эритроциты, но это исследование может и не выявить повреждения при очень легких случаях болезни.
Стандартные методы лечения
Для людей с умеренным или тяжелым НС, а также для всех беременных женщин с НС рекомендуется добавки фолиевой кислоты. Добавки, вероятно, не потребуются для людей с легкой формой наследственного сфероцитоза. Некоторым больным необходимо переливание крови. Больные должны получать кровь, соответствующую их группе крови, из которой удалены белые кровяные клетки (лейкоциты).
В основном, хирургическое удаление селезенки (спленэктомия) позволяет излечить НС. Однако, после операции повышается риск тяжелой инфекции. Поэтому рекомендации по спленэктомии отличаются в зависимости от тяжести. Больным с тяжелым НС рекомендовано провести спленэктомию. Больным с умеренным заболеванием решение о проведении спленэктомии должно основываться на размере селезенки и качестве жизни. Спленэктомия не рекомендуется пациентам с наследственным сфероцитозом легкой степени тяжести. По возможности спленэктомию следует отложить до 6 лет или старше. Для таких пациентов рекомендуется минимально инвазивная (лапароскопическая) спленэктомия, при условии наличия квалифицированного хирурга и соответствующего оборудования. После спленэктомии людям часто делают прививки и назначают профилактику антибиотиками для снижения риска заражения.
Прогноз
Пациенты с очень легкой формой НС могут оставаться незатронутыми своим расстройством, если оно не вызвано стрессовым фактором окружающей среды. У пациентов, перенесших спленэктомию, выживаемость эритроцитов резко улучшается, и большинство из них способны поддерживать нормальный уровень гемоглобина.
Голландское исследование 132 детей и подростков с наследственным сфероцитозом, из которых 48 перенесли спленэктомию, пришло к выводу, что в целом эти пациенты обладают сильной способностью справляться с болезнью.
Считается, что пациенты с НС, не перенесшие спленэктомию, имеют повышенный риск получения тупого повреждения селезенки от травмы из-за спленомегалии.
