Норма содержания фенилаланина в крови


«Помню, когда ей было три месяца, она лежала в своей маленькой корзинке на прогулочной палубе корабля. Пока мы путешествовали, я приносила ее сюда, чтобы она дышала утренним воздухом. Люди, прогуливающиеся по палубе, останавливались взглянуть на нее, и меня одолевала гордость, когда они говорили о ее необычной красоте и о разуме в ее глубоких голубых глазах», — так писала о своей первой дочери Кэрол — американская писательница Перл Бак (“The Child Who Never Grew”, 1950). Автор длительно вынашивала идею написать это произведение не только для того, чтобы выразить свою боль, но и помочь другим родителям, находящимся в подобной ситуации. Но можно сказать, что эта новелла стала, вероятно, первым описанием ребенка с далеко не редкой болезнью: в 1960 году Кэрол, сильно отстающей в развитии и обучающейся в специальной школе, поставили диагноз «фенилкетонурия».
Хотя все началось несколько раньше…
В 1934 году физиолог Асбьерн Феллинг, изучавший метаболические расстройства, определил причину необычного запаха мочи у двух норвежских детей с умственной отсталостью: виной тому был избыточный уровень одного из метаболитов фенилаланина — фенилпировиноградной кислоты. Год спустя британцем Пенроузом был предложен термин «фенилкетонурия», а также определен аутосомно-рецессивный тип передачи заболевания. Помимо этого, Пенроуз предложил лечебную диету, но она не была принята. Аналогичная идея, озвученная Джервисом и Бикелем несколько позже, уже в 50-х, стала и остается до сих пор краеугольным камнем в лечении ФКУ. В 60-х микробиолог Роберт Гатри предложил диагностический тест для определения гиперфенилаланинемии: в качестве индикатора он использовал колонии Bacillus subtilis, которым для роста необходим фенилаланин. В наши дни многие страны по всему миру включили тест Гатри (либо более новые тестовые системы, основанные на тандемной масс-спектрометрии) в программы неонатального скрининга, что позволило сразу же приступить к лечению новорожденных и избежать серьезных нарушений интеллекта. Последние 20 лет прошлого века пролили свет на генетическую природу ФКУ, а в конце первого десятилетия 21-го века была сформирована база данных мутаций гена фермента фенилаланингидроксилазы, являющихся причиной развития заболевания. Примерно в это же время были установлены генетические причины нарушения метаболизма тетрагидробиоптерина.
Итак…
Фенилкетонурия (ФКУ) — врожденное нарушение метаболизма фенилаланина, приводящее к избыточному накоплению в биологических жидкостях фенилаланина (гиперфенилаланинемии, ГФА) и его дериватов.
Наиболее часто (~ 97–98 %) развитие ФКУ обусловлено мутацией гена фенилаланингидроксилазы (ФАГ), локализованного на длинном плече 12 хромосомы, участке 12q22–q24.1, которая наследуется аутосомно-рецессивно. Данный фермент лимитирует реакцию превращения фенилаланина в тирозин, и уровень ГФА, и, соответственно, тяжесть заболевания напрямую зависят от его активности, которая определяется особенностями мутации гена.
В остальных ~ 2–3 % случаев ФКУ вызвана недостаточностью тетрагидробиоптерина, которая развивается из-за мутацией гена одного или нескольких ферментов, регулирующих его обмен (BH4-дефицитная ФКУ). BH4 является коферментом ФАГ, а также некоторых других энзимов, опосредующих синтез дофамина и серотонина (см. рис.1).
В МКБ-10 выделяют «классическую ФКУ» и «другие гиперфенилаланинемии».
«Классический» вариант заболевания дифференцируется по степени тяжести согласно уровню фенилаланина в крови (см. табл.1)
Таблица 1 | Классификация классической ФКУ по степени тяжести
| Форма ФКУ* | Уровень фенилаланина в крови, мкмоль/л | Уровень фенилаланина в крови, мг/дл |
| Легкая ГФА** (не ФКУ) | 120–600 | 2–10 |
| Умеренная (мягкая, средняя) | 600–1200 | 10–20 |
| Классическая (тяжелая) | >1200 | >20 |
ФКУ* — фенилкетонурия; ГФА** — гиперфенилаланинемия
Благодаря результатам генетических исследований была создана классификация, отражающая этиопатогенез ГФА и ФКУ (см. табл.2)
Таблица 2 | Этиопатогенетическая классификация фенилкетонурии и гиперфенилаланинемии
| Название | Причинный фермент |
| ФАГ*-зависимая ФКУ** | Фенилаланин-4-гидроксилаза |
| ГФА***, BH4****-дефицит, тип А (ФКУ, 3 типа) | 6-пирувоил-тетрагидроптерин синтаза |
| ГФА, BH4-дефицит, тип B | Гуанозинтрифосфат-циклогидролаза |
| ГФА, BH4-дефицит, тип C (ФКУ, 2 типа) | Дигидроптеридинредуктаза |
| ГФА, BH4-дефицит, тип D | Птерин-4-альфа-карбиноламиндегидратаза |
| ГФА, BH4-дефицит | Сепиаптеринредуктаза |
ФАГ* — фенилаланингидроксилаза; ФКУ** — фенилкетонурия; ГФА*** — гиперфенилаланинемия; BH4**** — тетрагидробиоптерин
Другие ГФА встречаются как при физиологических, так и при патологических состояниях. У новорожденных может быть транзиторное повышение уровня фенилаланина в крови до патологических значений ввиду незрелости ферментных систем печени или избыточного белкового питания матери, но, как правило, состояние это не длительно, а клинические проявление незначительны либо вовсе отсутствуют. Патологическая ГФА может сопровождать поражения печени различной этиологии и в этом случае будет имеет вторичный характер.
Патогенез
Фенилаланин является незаменимой аминокислотой, поступающей в организм человека преимущественно в составе белковых продуктов животного происхождения. Большая часть этой аминокислоты расходуется на синтез собственных белков организма, а оставшаяся часть — на синтез тирозина, что является главным путем катаболизма фенилаланина. Эта реакция регулируется ферментом ФАГ при участии кофермента BH4 (см. рис 1). Отсутствие данного энзима либо его малое количество (при ФКУ от 0 до 50 % нормальной активности фермента) приводит к накоплению фенилаланина и развитию клинической картины ФКУ различной степени тяжести. Не утилизированный фенилаланин катаболизируется по минорному пути с образованием токсичных продуктов (фенилацетата, фенилпирувата,фениллактата), а сниженное образование тирозина влечет за собой нарушение синтеза гормонов щитовидной железы, нейротрансмиттеров и пигментов меланоцитов (меланинов). Помимо участия в синтезе тирозина, BH4 является коферментом в реакциях образования ДОФА и серотонина.
Также на количество медиаторов ЦНС влияет и само количество фенилаланина. Дело в том, что в норме фенилаланин, а также тирозин (как уже было обозначено выше — предшественник дофамина, норадреналина и адреналина) и триптофан (предшественник серотонина) преодолевают гематоэнцефалический барьер при помощи переносчика больших нейтральных аминокислот LAT1. Возросший при ФКУ уровень фенилаланина может ингибировать LAT1, препятствуя поступлению иных субстратов в нейроны.
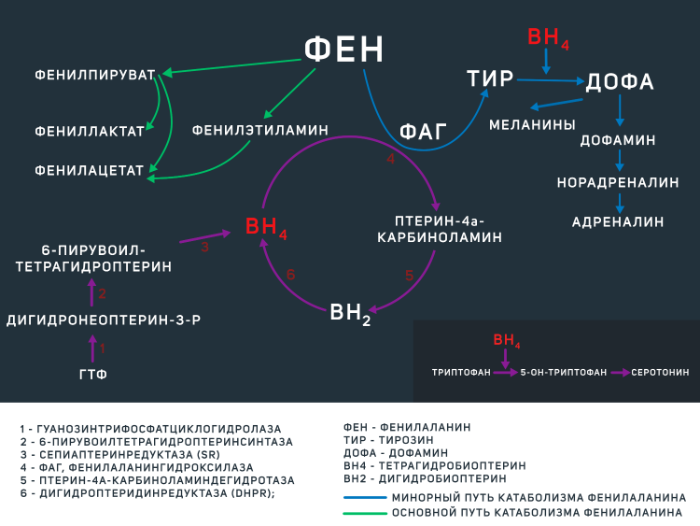
Рисунок 1 | метаболизм фенилаланина
Клиническая картина
Первые симптомы нелеченной ФАГ-зависимой ФКУ появляются, как правило, на первом году жизни ребенка, достигая максимума ко второму полугодию. Сперва обращает на себя внимание вялость ребенка либо, напротив, его беспокойство, возбужденность и срыгивания, нарушение мышечного тонуса, судороги, а также специфический затхлый запах мочи, названный «мышиным». Кроме того, нередко ФКУ проявляется эпилептическими приступами в виде абсансов, кивков, генерализованных судорог. Несколько позже, по мере роста ребенка, становится очевидным его задержка в моторном и нервно-психическом развитии. Болезнь, при отсутствии лечения, прогрессирует медленно, но неуклонно, приводя к глубокой олигофрении, несформированности речи, отсутствию игровой и предметной деятельности. Фенотипически для детей и взрослых, больных ФКУ, характерна гипопигментации кожи, волос и радужки.
При BH4-дефицитной ФКУ, помимо вышеобозначенных признаков, из-за большей недостаточности нейротрансмиттеров ЦНС выявляются атаксия, тремор, нарушения мышечного тонуса, гипокинезия, нарушения терморегуляции, затруднение глотания и поперхивания.
Диагностика
Первый этап лабораторной диагностики проводится на 3–7-й день жизни (но не ранее, чем через 2 дня от начала энтерального питания) новорожденного в рамках неонатального скрининга путем определения уровня фенилаланина на сухом пятне крови с помощью флюориметрии или тандемной масс-спектрометрии. При ГФА (фенилаланин > 120 мкмоль/л или > 2 мг/дл) проводится ретест. Если при повторном исследовании были получены подобные результаты, переходят ко второму этапу — определению отношения фенилаланин/тирозин. Этот косвенный метод позволяет провести дифференциальную диагностику между ФАГ-зависимой и BH4-зависимой ФКУ, что важно для назначения правильного лечения. Кроме лабораторных методов с целью уточнения типа заболевания используют молекулярно-генетические методы.
При отсутствие возможности провести неонатальный скрининг, в постановке диагноза опираются на клиническую картину, биохимические показатели, генеалогический анамнез, молекулярно-генетическую диагностику.
При выявлении легкой ГФА необходимо дальнейшее наблюдение и повторная диагностика.
Лечение
Основная цель терапии ФКУ — снижение уровня фенилаланина в крови для избежания нарушения моторного и нервно-психического развития ребенка — , достигается следующими методами:
- Гипофенилаланиновая диета — основной способ лечения уже более 60 лет. Для уменьшения поступления фенилаланина больным следует ограничивать прием высокобелковой пищи (мясо, рыба, яйца, молочные продукты, орехи, бобовые и др.) и вводить в рацион растительные продукты с высоким содержанием тирозина. Строгость диеты напрямую зависит от степени ГФА, меню должно составляться с опорой на факт «1 г белка = ~ 50 мг фенилаланина», возрастные физиологические нормы потребности в фенилаланине, тирозине и соотношение Б/Ж/У. У детей первого года жизни возможно употребление женского молока или молочных смесей при соответствующем расчете рациона и строгом контроле уровня фенилаланина в крови. Для восполнения недостающего белка используются аминокислотные смеси с низким содержанием фенилаланина и высоким содержанием тирозина, у детей старшего возраста компенсация происходит за счет растительных продуктов. Большой недостаток данного способа лечения — низкий комплаенс, особенно у детей подросткового возраста. Но при хорошей приверженности пациентов к диете снижение IQ можно свести к минимуму.
Некоторыми исследователями были получены данные об эффективности применения гликомакропептидов в диете. Гликомакропептиды (GLP, glycomacropeptides) — белки, получаемые из молочной сыворотки, которая богата валином, изолейцином, треонином и при этом содержит низкий уровень фенилаланина. Их использование позволило бы сделать гипофенилаланиновую диету более физиологичной, но для широкого применения необходимы дальнейшие исследования и подтверждение безопасности применения GLP в течение длительного срока. - Заместительная терапия BH4. Из-за участия BH4 в нескольких важных реакциях у больных BH4-зависимой формой ФКУ даже при хорошем соблюдении гипофенилаланиновой диеты остается симптоматика заболевания. В таком случае, как только на втором этапе лабораторной диагностики и/или на этапе медико-генетической диагностики подтверждается диагноз BH4-зависимой ФКУ, больным проводится тест на потенциальную чувствительность к сапроптерину дигидрохлориду — синтетическому аналогу BH4.
Иные методы лечения, имеющие потенциал:
- Большие нейтральные аминокислоты (The LNAAs, large neutral amino acids). Как было указано выше, фенилаланин способен конкурировать с другими аминокислотами (тирозин, триптофан) при взаимодействии с переносчиком LAT1. Некоторыми авторами было предположено, что в слизистой кишечника имеется подобный механизм, и при увеличении концентрации LNAAs всасывание фенилаланина будет уменьшаться.
- Генная терапия. Этот метод лечения мог бы стать идеальным решением, но в данный момент был тестирован лишь на мышах и требует дальнейшей серьезной разработки.
- Энзимотерапия фенилаланинамиаклиазой (PAL, phenylalanine ammonia-lyase). PAL — это фермент растений и дрожжевых грибков, осуществляющий катаболизм фенилаланина по альтернативному пути с образованием транс-циннамата и аммиака. За три последних десятилетия на мышах изучалось влияние PAL, внедренного в организм животного различными путями, начиная от оральных и инъекционных препаратов вплоть до помещения в кишечник генномодифицированных амеб, но, как и в случае с генной терапией, этот способ лечения требует дальнейшего изучения и разработки.
Источники:
- Blau N. et al. Phenylketonuria. // Lancet. Vol 376 October 23, 2010: pp 1417-1427.
- Blau N. Genetics of Phenylketonuria: Then and Now. // Human mutation, Vol 37, No. 6, 2016: pp 508-515.
- Hafid N.A., Christodoulou J. Phenylketonuria: a review of current and future treatments. // Translational Pediatrics 2015, 4(4): 304-317.
- Skirlou E., Lichter-Konecki U. Inborn Errors of Metabolism with Cognitive Impairment Metabolism Defects of Phenylalanine, Homocysteine and Methionine, Purine and Pyrimidine, and Creatine. // Pediatric Clinics of North America, Vol 65, 2018: pp 267-277.
- Руководство по педиатрии / [под ред. А.А. Баранова и др.] – Т: Врожденные и наследственные заболевания / [под ред. П.В.Новикова] – М.: “Династия”, 2007.
- Е.С. Северин и др.. Биологическая химия — М.: ООО «Медицинское информационное агентство», 2008.
- Клинические рекомендации “Фенилкетонурия и нарушения обмена тетрагидробиоптерина у детей”, 2017. https://www.pediatr-russia.ru/news/recomend
По материалам форума Вместе со всеми Тема SOS!!! Слишком высокий уровень ФА
Эту статью нам любезно предоставила Medina Стиль и орфография автора перевода сохранены.

![]()
Высокий анализ Фа – что делать?
Название: Высокий анализ Фа – что теперь? (Hoher Phe-Wert -was nun?).
Автор: Agnes van Teeffelen-Heithoff, (Университетская детская клиника Мюнстера).
Фенилаланин – определение
Уровень фенилаланина
Итак, по-порядку.
Очевидно, что уровень ФА в крови Вашего ребенка намного превысил идеальное значение, и Вы сильно напуганы. Очень велик страх повреждения головного мозга ребенка. Но наиболее опасно не отдельное повышение уровня ФА, а продолжительно существующий высокий уровень.
Также у молодого человека или взрослого длительно повышенный уровень ФА в крови может приводить к проблемам концентрации, нервозности, раздражению или даже к психическим или нейрологическим проблемам.
Это руководство должно помочь Вам своевременно регулировать высокие значения ФА, чтобы сохранить уровень ФА в норме и успешно справиться с ФКУ без большого стресса.
Слишком высокий уровень ФА
Когда говорят о слишком высоком уровне ФА в крови?
Для начала нужно знать допустимый уровень ФА в крови. Он обозначается как нормативный показатель и находится в большинстве случаев между 1 и 2 мг / дл. На протяжении многих лет и даже десятилетий в течение срока лечения публиковались все новые директивы и показатели желательного уровня ФА в крови. Большое федеративное исследование ФКУ, а также изучения в Америке и Англии привели к середине 90-ых годов к некоторой ясности в большой массе цифр. Был более уверенно определен максимальный уровень ФА в крови, желательный для пациентов больных ФКУ вплоть до юношеского возраста.
Для взрослых больных ФКУ в настоящее время еще нет никаких твердых установок. В немногих крупных университетских больницах проводятся исследования. Однако, уже достоверно известно, что взрослые больные должны поддерживать по возможности более низкий уровень ФА в крови. Стало известно, что основная масса взрослых совершенно обычных пациентов с показателем ФА в крови между 15 и 20, при показателе свыше 20 мг/дл начинают с течением времени испытывать физические и психические проблемы, которые необходимо устранять, как правило, снова длительным и устойчивым показателем крови.
| Возраст | Минимальный уровень ФА в крови | Максимальный уровень ФА в крови |
|---|---|---|
| 0 – 10 лет | 0,7 мг/дл | 4,0 мг/дл |
| 11 – 16 лет | 0,7 мг/дл | 15 мг/дл |
| Больше 16 лет | 0,7 мг/дл | 20 мг/дл |
Основная масса взрослых должна также соблюдать диету. Однако у них допускается более высокие показатели ФА в крови (см. выше). Таким образом, дополнительно к диете могут приобщаться в малых количествах некоторые обычные продукты. Однако достаточное количество минеральных веществ, витаминов и аминокислот должно поступать с аминокислотной смесью.
На особом положении находятся женщины с ФКУ, желающие иметь детей, быть беременными или уже беременные. Они должны соблюдать строгую диету и иметь низкие значения ФА в крови.
► Если упомянутые нормы превышают рекомендованные на 3-5 мг/дл, говорят о повышении уровня ФА до высокого.
Тот, кто знает о нормах ФА в крови, может контролировать его уровень. К сожалению, нельзя чувствовать повышенный уровень ФА – он не причиняет боль и не делает каждого ребенка тотчас дурно настроенным или даже агрессивным. Уровень ФА в крови можно контролировать только регулярным забором крови на анализ.
Как часто должны делаться эти проверки, можно увидеть из таблицы:
| Возраст | Периодичность контроля крови |
|---|---|
| Меньше 1 годика | Каждые 1 – 2 недели |
| От 1 до 9 лет | Каждые 2 – 4 недели |
| От 10 до 15 лет | Каждые 4 недели |
| Старше 15 лет | Каждые 2 – 3 месяца |
Когда нужно реагировать на более высокий уровень ФА в крови?
Собственно, этот вопрос уже отвечает уже сам за себя – всегда! Регулярные проверки необходимы, чтобы прореагировать на соответствующие значения. При этом необходимо выяснить причины повышенного уровня ФА (об этом в следующих главах) с тем, чтобы в течение максимально короткого срока, в течение несколько дней снова взять под контроль уровень ФА в крови.
Слишком высокий уровень ФА – причины
Вследствие чего уровень ФА в крови может подниматься?
Как только в организм поступает больше фенилаланина с питанием, чем требует организм и способен переработать, излишний фенилаланин накапливается в крови;
► Съедено слишком много содержащих белок продуктов!
Всегда, когда организм нездоров и реагирует, например, на инфекции, фенилаланин, наряду с другими аминокислотами, освобождается распадом и преобразованием собственного белка организма, попадая в кровообращение и вызывая повышенный уровень ФА.
► Болезнь, например, простуда и температура, грипп, инфекции ЖКТ, детские болезни – ветряная оспа и так далее.
Если количество потребляемой энергии меньше, чем нуждается организм для своей ежедневной работы, белки наряду с жирами резервируются из клеток тела. Вследствие этого уровень ФА в крови также повышается. Это очень быстро происходит у грудных и маленьких детей, а также у спортсменов-разрядников и взрослых, которые пытаются достигнуть идеального веса голоданием.
► Продолжительное недоедание с потерей веса.
Нельзя недооценить как причину высокого уровня ФА в крови, недостаточное снабжение организма белком. Чтобы иметь в достаточном количестве аминокислоты для важных функций, организм реагирует распадом своего собственного белка. При этом повышается фенилаланин в крови. Это происходит всегда, когда наряду с правильно рассчитанным и контролируемым поступлением ФА, аминокислотная смесь принималась нерегулярно или не принималась совсем. Большинство детей с ФКУ нуждаются в получении 80 % необходимой массы белка из аминокислотной смеси!
► Если нет гарантированного регулярного приема аминокислотной смеси, распределенного на 3-4 приема в день.
► Примечание: Елена : – Я несколько раз читала у девчат, что рост уровня ФА в крови возможен из-за стрессовой ситуации у ребенка, например, когда малыша отдают в детский сад, не проведя достаточную адаптацию к этому. И поэтому наших деток надо приучать очень осторожно и постепенно…
Слишком высокий уровень фенилаланина – мероприятия
Теперь речь пойдет о повышенном уровне ФА в крови – Что нужно делать?
В первую очередь необходимо сократить избыток фенилаланина в крови. Этого можно добиться, только принимая меньшее количество фенилаланина с пищей, чем обычно.
► Сократить ежедневный прием ФА.
Принимают только половину или на 1/3 меньше суточной потребности в ФА. В зависимости от уровня ФА это должно продолжаться в течение 1-7 дней и постоянно контролироваться.
Нужно не допускать наряду с сокращением фенилаланина также сокращения поступления энергоносителей – жиров и углеводов, включая в рацион достаточное количество малобелковых или безбелковых продуктов.
► Активно употреблять в пищу такие бедные белком продукты, как специальную выпечку, макаронные изделия, блинчики, картофельное пюре, вафли и хлеб, а также продукты, содержащие глюкозу, сахар, мальтодекстрин, богатые сахаром продукты – конфеты, сладкие минеральные газированные воды и напитки (кроме какао).
► Обогащать рацион жирами – маргарин, смалец, топленое масло, масло, а также употреблять в пищу богатые жирами и сахаром малобелковые продукты.
► Одновременно необходимо обеспечить достаточное снабжение организма смесью аминокислот (непродолжительный период возможно применение увеличенного на 10-15% количества смеси по сравнению с рекомендованным объемом). Объем делится обязательно на 3-4 приема и принимается с калорийной жидкостью или компотом. Нужно получать достаточное количество аминокислотной смеси, распределенной в течение дня.
Что необходимо делать во время болезни?
Во время болезни не всегда возможно поступать вышеописанными способами. Часто при болезни невозможен достаточный прием пищи и нужно предпринимать нижеописанные действия:
Помощь при рвоте:
► До тех пор, пока рвота не прекратилась, ребенок не может принимать никакую твердую пищу. Если желудок опорожнен полностью, начните сначала с маленьких глоточков воды, обогащенной по возможности Elektrolyten*. Если рвота не возобновляется, объем принимаемой жидкости должен постепенно увеличиваться и в течение 24 часов должен составить 1-3 литра (в зависимости от возраста ребенка).
- (например, Humana-Elektrolyte, Milupa-GSD 60 из аптеки) – электролиты для приема внутрь.
► В течение последующих 2-4 часов после прекращения рвоты вводят совсем малую порцию более твердой пищи – малобелковый крекер, белый хлеб, сухарь, печенье, кусочек банана, делают это постепенно, через короткие промежутки времени, чтобы желудок не оставался пустым.
► Прием аминокислотной смеси допустим только после того, как начат прием твердой пищи. Первоначально это может быть примерно 1/3 дневной массы, разведенной в чае с лимоном или в ранее употребляемом приготовлении, разбавленном водой. Можно перелить в бутылку, либо пить через соломинку, чтобы не раздражал запах.
► Если тошнота, рвота, водянистый стул продолжаются (у грудных детей свыше 8 часов, старших детей, молодых людей и взрослых через 12-24 часа), если недостаточен прием жидкости и невозможен прием пищи, Вам срочно должна быть оказана врачебная помощь, особенно грудным и маленьким детям.
Мероприятия при лихорадочных инфекциях, детских болезнях:
► При инфекциях, детских болезнях срочно обратитесь к Вашему педиатру или домашнему врачу для оказания обычной медицинской помощи (в большинстве случаев медикаментозно).
► Одновременно необходимо сократить суточный прием фенилаланина примерно на 25-50% (предпочтительным является прием половины суточной нормы ФА). Эти мероприятия в большинстве случаев проходят успешно, т.к. у многих детей проблемы с аппетитом возникают незадолго до начала болезни и продолжаются во время нее.
► Следует обеспечить рацион достаточным количеством калорийных малобелковых продуктов, богатых жирами и сахаром.
При затяжных болезнях дополните рацион глюкозой и мальтодекстрином(SHS), чтобы повышение уровня ФА не затягивалось надолго.
► Соблюдать прием достаточного количества аминокислотной смеси небольшими порциями несколько раз в течение дня.
► После перенесенной инфекции делают забор крови на определение ФА. О перенесенной инфекции необходимо известить врача звонком или приложив к анализу информационную этикетку.
►Если уровень ФА находится в допустимой области, ежедневная масса ФА может далее увеличиваться до обыкновенной дневной массы. Если уровень ФА в крови еще слишком высок, сокращенную массу ФА оставляют и далее, через 4-6 дней снова производят контроль.
Что необходимо делать, если повышенный уровень ФА не снижается, несмотря на все усилия?
Мероприятия при более длительном (или по неизвестной причине) повышенном уровне ФА:
► Необходимо установить, не употребляется ли в течение суток ФА в большем количестве, чем необходимо. Нужно снова начать ежедневно записывать расчеты по продуктам и контролировать.
► Не поддерживалось ли длительно слишком сильно сниженное поступление ФА?
- ПОПРАВКА Medina: – предложение означает, что не занижалось ли потребление фа?! При нехватке гидролизата или калорий, человек ошибочно будет занижать норму потребления Фа, что тоже негативно скажется на его анализе!-
Вследствие этого организм имеет слишком мало ФА для роста и сохранения своих функций и вынужден расходовать свой собственный белок. Необходимо осторожно увеличивать поступление ФА, одновременно употребляя достаточное количество энергии и аминокислотной смеси.
► В порядке ли весы?
Возможно, необходимо поменять батарею, а может быть и приобрести новые весы? Если не взвешивается, а оценивается лишь «на глазок», то фенилаланинсодержащие продукты должны взвешиваться и контролироваться в течение как минимум недели.
► Повторно оцените последние дни или недели перед анализом:
- возможно, в рацион были включены рассчитанные ошибочно новые продукты.
- был съеден продукт, не относящийся к низкобелковой диете, например, обычный хлеб от других детей, сладости, содержащие желатин и много фенилаланина, много шоколада, картошки фри…
- возможно ли, что разрешенная масса фенилаланина была превзойдена в более богатых белком продуктах (как жирная колбаса или свежий сыр)?
► Просмотрите еще раз все использованные специальные продукты (наименования) и точно удостоверьтесь, что по недоразумению Вы не получили продукты без глютена вместо предназначенных для больных ФКУ малобелковых продуктов. Это также отражается на анализах, количество ФА должно быть указано для каждого продукта!
► Перепроверьте продукты, которые почти ежедневно ест или пьет Ваш ребенок.
Может так случиться, что, например, часто используемые сладости или лимонады стали использовать синтетическое подслащивающее средство Аспартам (Aspartam/Nutrasweet), или в их составе появились новые компоненты, содержащие белок – молоко, молочный белок, сыворотка, желатин, яйцо или соя, или использовались чаи для грудных детей, содержащие фенилаланин.
► Получал Ваш ребенок недостаточное количество аминокислотной смеси?
Не давалось ли ежедневно предписанное количество сразу, а не порционно в течение дня? Возможно, прием забывался в последние дни или смесь принималась только в половинном объеме?
► В рационе Вашего ребенка было недостаточное количество энергии?
Не употреблялись ли в пищу сначала преимущественно высокобелковые продукты с большим количеством ФА, а затем — слишком мало малобелковых продуктов, таких как хлеб, печенья или макароны? Затем давали еще большее количество этих богатых ФА продуктов?
Не принималась ли слишком малокалорийная пища, чтобы потерять вес? Не было ли пропусков в приеме пищи в школе, детском саду? Оставалось ли время на обед?
Если причина повышенного фенилаланина в крови найдена, вы должны сразу же устранить ее!
Начните, кроме того, с сокращения ежедневного поступления ФА на 25-50% (в зависимости от уровня ФА в крови) на 3-5 дней, соблюдая все упомянутые указания.
Через 1-2 недели сдайте контрольный анализ крови, чтобы Вы знали, необходимо ли более длительное сокращение ФА.
Позвоните в генетическую консультацию и сообщите предположение или причину высокого ФА в крови, чтобы врач так же получил информацию об этом.
Если повышенный уровень фенилаланина в крови все же не снижается?
Уровень ФА в крови не спал существенно вопреки соответствующим мероприятиям?
Это может быть потому, что эти мероприятия проводились не достаточно долго. Необходимо еще в течение 3-5 дней принимать сокращенную суточную массу ФА.
При этом всегда необходимо употреблять достаточное количество энергии в форме малобелковых продуктов, жиров, сахара и принятие аминокислотной смеси порционно в течение дня!
Если высокий уровень ФА все же совсем не снижается, и Вы не можете установить причины, почему это происходит, Вы должны составить изменения в контакте с генетическим центром.
Недельный продовольственный протокол, который Вы должны были вести добросовестно и точно, может быть очень полезен Вашей диетсестре, чтобы найти ошибку вместе с Вами.
Незамедлительно просите помощи в генетической консультации. Диетсестра или врач смогут помочь Вам, если Вы опишите Ваши проблемы.
Как часто должен контролироваться уровень ФА и когда я оканчиваю сокращение суточного потребление ФА?
Уровень ФА в крови должен контролироваться в зависимости от возраста ребенка через 1-2 недели, у молодых людей не реже 1 раза в 4 недели. Если уровень ФА в крови упал до желательного значения, то диета может расшириться до старого значения ФА.
Что предпринимать, если диета прерывается и возобновляется снова, например, у молодых людей или взрослых, и точная суточная масса ФА не известна?
Здесь очень может помочь обращение в генетический центр. В большинстве случаев у диетсестр и врачей есть информация о том, как высок был уровень ФА в крови в детстве. Кроме того, пищевой дневник в течение 3-5 дней поможет выяснить, сколько ФА употребляется в пищу в настоящее время. В сочетании с контролируемым уровнем ФА в крови, диетолог может рассмотреть необходимость перехода к дальнейшему расчету ФА или необходимого количества белка в питании.
Чтобы достигнуть достаточно низкого уровня ФА в крови, сначала необходимо выполнять все описанные в этом руководстве предложения по сокращению.
Далее, прежде всего, увеличивают на 10-50 мг ФА и на 2-5 гр. белка в день.
ПРИМЕЧАНИЕ Прохожий Я так думаю, что увеличивается как объем ОБЩЕГО белка (на 2 г) так и количество фенилаланина (на 50 мг), то есть нужно добавить общего белка в два раза больше, чем натурального До тех пор, пока соответствующая дневная масса ФА не достигнута, при которой уровень ФА может считаться нормальным, необходим контроль уровня ФА в крови каждые 1-2 недели!
Должна ли даваться при приспособленном к белку питании дополнительно аминокислотная смесь или смесь минеральных веществ?
- Руководствуются исходя из массы естественного белка, которая может быть позволена диетой.
- Если допускаемая масса природного белка не достаточна для получения физической дееспособности, необходимо восполнять недостающий белок аминокислотной смесью.
- В противном случае недостающие минеральные вещества ежедневно дополняются соответствующими смесями или отдельными препаратами. Совсем без дополнительного снабжения при ограниченной белком диете, организм в большинстве случаев нуждается в таких витаминах и минеральных веществах, как кальций, железо, цинк, витамин В12 и фолиевая кислота.
О причинах повышения уровня фенилаланина в крови в результате каких либо стрессовых ситуаций, соматических заболеваний, рассказано в статье Е. В. Денисенковой и Е. П Клыковой “Нутритивная терапия фенилкетонурии в стрессовых ситуациях”. Читать статью полностью >>
