Оксигемоглобин венозной крови норма
О чем говорят анализы
5. Газы крови
5.1. Кислород
5.2. Двуокись углерода (углекислый газ)
* * *
5.1. Кислород
Важнейшая функция крови — дыхательная. Поглощенный в легких кислород переносится кровью к органам и тканям, а углекислый газ транспортируется в обратном направлении. Основная (ключевая) роль в переносе дыхательных газов принадлежит гемоглобину, содержащемуся в эритроцитах крови.
Гемоглобин относится к классу сложных белков — хромопротеинов. Он состоит из небелковой части, относящейся к железопорфиринам, — гема и белковой части — глобина. Гемоглобин выполняет функцию переносчика кислорода благодаря наличию в молекуле гема двухвалентного железа. Железо гемоглобина, присоединяя молекулу кислорода, не окисляется, то есть не переходит из двух- в трехвалентное состояние, а образует обратимую связь, которая сравнительно легко разрушается при соответствующих изменениях концентрации кислорода в среде.
Гемоглобин (Нb), присоединивший кислород, становится оксигемоглобином (Нb0 2 )
• Реакцию связывания кислорода гемоглобином называют оксигенацией, обратный процесс — дезоксигенацией. Не связанный с кислородом гемоглобин носит название дезоксигемоглобина.
В условиях организма 1 г гемоглобина способен связать 1,34 мл кислорода. Если известно содержание гемоглобина крови, можно рассчитать кислородную емкость крови — максимальное количество кислорода, которое может связать гемоглобин при его полном насыщении 02. При содержании 150 г/л количество кислорода в 1 л крови составит 1,34 х 150 = 201 мл; в 100 мл крови — 20,1 мл или 20,1 об. % (объемных %).
Процентное отношение количества О2, реально связанного с гемоглобином, к кислородной емкости крови называется насыщением (saturation — сатурация) гемоглобина кислородом (SO2 или НBО2). Другими словами, S0 2 — это отношение оксигемоглобина к общему количеству гемоглобина крови.
В норме насыщение артериальной крови кислородом (SO2 или НВО2) составляет 96-98% . Небольшое «недонасыщение» (2-4%) объясняется некоторой неравномерностью легочной вентиляции и незначительной примесью венозной крови, которые имеют место и у здоровых людей.
Насыщение гемоглобина кислородом зависит от напряжения О2 в крови (в соответствии с физическим законом действующих масс). Графически эту зависимость отражает кривая диссоциации оксигемоглобина, имеющая S-образную форму.
Напряжение кислорода в артериальной крови (Ра02) в норме колеблется в пределах 95-100 мм рт. ст. С возрастом газовый состав крови претерпевает некоторые изменения. Напряжение 02 в артериальной крови здоровых молодых людей в среднем составляет 95-100 мм рт. ст.; к 40 годам оно снижается примерно до 80 мм рт. ст., а к 70 годам — до 70 мм рт. ст. Эти изменения связаны с тем, что с возрастом увеличивается неравномерность функционирования различных участков легких.
Таким образом, степень оксигенации крови может быть охарактеризована двумя показателями: напряжением кислорода (РаО2) и насыщением крови кислородом (SO2 или НВО2).
Снижение этих показателей в артериальной крови (венозная кровь для исследования газового состава непригодна) называется артериальной гипоксемией. Умеренная гипоксемия характеризуется прежде всего снижением РаО2, величина S02 (НВО2) более устойчива.
5.2. Двуокись углерода (углекислый газ)
Двуокись углерода — конечный продукт обменно-окислительных процессов в клетках и тканях организма — переносится кровью к легким и удаляется через них во внешнюю среду (99,5% С02 покидает организм через легкие и только незначительная часть выделяется почками).
Двуокись углерода может переноситься как в физически растворенном виде, так и в составе обратимых химических соединений. Химические реакции связывания С02 сложнее и многообразнее, чем реакции присоединения кислорода. Это обусловлено тем, что механизмы, отвечающие за транспорт углекислого газа, должны обеспечивать и постоянство кислотно-основного состояния крови.
Двуокись углерода находится в крови в следующих формах:
• в растворенном виде в плазме — 5%;
• в связи с аминогруппами гемоглобина — 15%;
• в виде угольной кислоты (Н2СО3) — незначительное количество;
• в виде бикарбонатионов (НСО3), обеспечивающих постоянство активной реакции крови (рН), — более 80%.
В нормальных условиях в артериальной крови напряжение С02 (РаС02) составляет около 40 мм рт. ст. (с колебаниями от 35 до 45 мм рт. ст.). Повышение РаС02 называется артериальной гиперкапнией, снижение — артериальной гипокапнией.
Нарушения газового состава крови выявляются при большинстве заболеваний легких. По показателям газового состава артериальной крови можно судить о функции легких в целом.
Идеальным объектом изучения газового состава крови является артериальная кровь, полученная пункцией локтевой или бедренной артерии. Газовый состав венозной крови не может быть использован как показатель функции аппарата внешнего дыхания, так как содержание в ней 0 2 и С0 2 зависит еще и от уровня обмена веществ и скорости кровотока в тканях.
Забор крови и ее доставка к аппарату должны осуществляться без доступа воздуха (в шприце, закрытом капилляре, сосуде под вазелиновым маслом). Шприц и иглу для пункции необходимо промыть гепарином.
Необходимость получения крови из артерии исключает возможность повторных исследований на протяжении короткого периода времени, поэтому широкое распространение получило исследование малых порций капиллярной крови, полученных из кончика пальца или мочки уха.
Еще Холденом было показано, что если руку человека держать в течение 20 мин в водяной бане с температурой воды 38 °С, то в этих условиях газовый состав крови из подкожной вены руки станет идентичным газовому составу артериальной крови. Еще более близок к артериальной газовый состав капиллярной крови.
Используемая в настоящее время измерительная аппаратура предусматривает исследование минимальных порций крови (0,1 мл), которые можно получить из кончика разогретого пальца или мочки уха, предварительно добившись того, чтобы кровоток в ней был максимален (растирание).
Для определения газового состава крови могут быть использованы различные методы.
В настоящее время наиболее доступным и широко распространенным способом изучения оксигенации крови являются оксиметрические методы. Они основаны на различии оптических свойств (спектров поглощения) гемоглобина и оксигемоглобина.
Алый цвет артериальной крови обусловлен тем, что оксигемоглобин достаточно интенсивно поглощает коротковолновые лучи, соответствующие синей части спектра, но пропускает большую часть длинноволновых («красных») лучей. Дезоксигемоглобин более интенсивно поглощает длинноволновые лучи и менее интенсивно — коротковолновые. В связи с этим венозная кровь выглядит темнее и имеет красный цвет с синеватым оттенком.
Для определения насыщения крови кислородом (SO 2 или Нb0 2 ) используются спектрофотометры — приборы, в которых видимый свет при помощи призмы или дифракционной решетки разлагается в спектр. Затем из спектра выделяется узкая полоса лучей с определенной длиной волны (монохроматический свет) и пропускается через исследуемый раствор (порцию крови).
Поглощение света зависит от оптических свойств крови. Для определения соотношения между интенсивностью падающего и прошедшего через раствор света используется фотоэлемент.
Напряжение кислорода и углекислого газа крови можно измерить с помощью специальных электродов.
Для определения напряжения кислорода применяют полярографический метод. Он предусматривает использование двух электродов: измеряющего, изготовленного из благородных (не окисляющихся) металлов (платины или золота), и референтного. Электроды отделены от крови мембраной, проницаемой для газов, и включены в замкнутую цепь, где создается небольшое напряжение.
Молекулы кислорода, диффундирующие через мембрану, восстанавливаются на поверхности измеряющего электрода. В результате возникает электрический ток, величина которого пропорциональна напряжению 0 2 в крови.
Электрод для определения напряжения углекислого газа представляет собой рН-метр, в котором измеряющий и референтный электроды окружены раствором бикарбонатного буфера и отделены от крови тонкой мембраной, проницаемой для газов и непроницаемой для ионов НСО 3 -. Углекислый газ диффундирует из крови через мембрану, вследствие чего меняется рН бикарбонатного буфера. Чем выше напряжение углекислого газа крови, тем большее количество молекул СО 2 проникает через мембрану. Изменения рН электролитного раствора регистрируются амперметром.
Источник
Несмотря на то, что исследование кислотно-основного состояния, строго говоря, подразумевает исследование только величины pH (концентрации ионов H+), в реальности в него также включается исследование физиологически важных газов, присутствующих в крови – O2 и CO2. Анализ газов показывает эффективность газообмена по величинам парциальных давлений – pO2 и pCO2.
Через альвеолярную мембрану молекулы любых газов перемещаются диффузно по градиенту концентрации. Молекулы O2 атмосферного воздуха поступают из альвеол в кровь, а молекулы CO2 из крови в альвеолы до тех пор пока их парциальные давления не выровняются.
Величина парциального давления – это процентная доля газа в общем объеме.
Углекислый газ
Концентрация СО2 в альволярном воздухе столь низка, а в крови столь высока, что диффузия этого газа в альвеолы чрезвычайно эффективна и скорость его удаления зависит только от альвеолярной вентиляции – общего объема воздуха, транспортируемого в минуту между альвеолами и атмосферой (“скорости выдувания”).
Следовательно,
- при усиленной вентиляции легких углекислый газ быстро выводится, и показатель pCO2в крови снижается. Это означает потерю организмом угольной кислоты (ионов H+), что является причиной защелачивания крови – алкалоза, называемого дыхательным или респираторным.
- при недостаточной альвеолярной вентиляции величина рСО2 повышается, что свидетельствует о недостаточном его удалении и накоплении H2CO3. Иными словами, повышение в крови показателя рСО2 является причиной дыхательного ацидоза.
Увеличенное pCO2 (гиперкапния) всегда свидетельствует о снижении альвеолярной вентиляции.
Кислород
Вопросы, связанные с оксигенацией крови и транспортом кислорода более сложны. Связано это с тем, что в виде свободных (растворенных) молекул O2 находится лишь небольшая доля общего кислорода крови. Основная часть кислорода связана с гемоглобином (оксигемоглобин) и истинное содержание кислорода зависит от двух дополнительных параметров – концентрации Hb и насыщения (сатурации) гемоглобина кислородом.
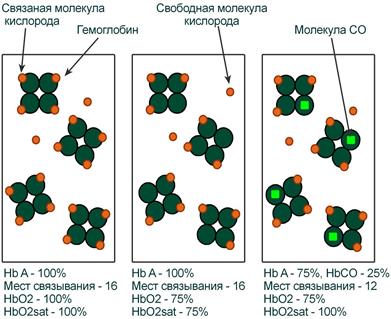
Оксигемоглобин
Оксигемоглобин (HbО2) – процентное содержание в крови, является отношением фракции оксигемоглобина (HbО2) к сумме всех фракций (общему гемоглобину).
Насыщение гемоглобина кислородом
Насыщение гемоглобина кислородом (HbOSAT, SО2), представляет собой отношение фракции оксигенированного гемоглобина к тому количеству гемоглобина в крови, который способен транспортировать О2.
Отличия между двумя показателями HbО2 и HbOSAT заключаются в том, что у пациентов возможно наличие в крови такой формы гемоглобина, которая не способна акцептировать О2 (Hb‑CO, metHb, сульфоHb). Но так как большинство больных не имеют в крови повышенного содержания этих форм гемоглобина, значения HbО2 и SО2 обычно очень близки.
Например, если при отравлении нитритами количество metHb составляет 15%, тогда величина HbО2 никогда не сможет превысить 85%, но насыщение (HbOsat) может быть различно – от максимума (HbOsat=95-98%) при полном насыщении до низких величин при отсутствии кислорода.
Показатель насыщения кислородом показывает процент доступных мест связывания на гемоглобине.

Иллюстрация понятий оксигемоглобина (HbO2) и насыщения гемоглобина (HbO2sat)
Парциальное давление кислорода (pO2)
Парциальное давление O2 выступает как движущая сила, приводящая к насыщению гемоглобина кислородом. И хотя, как правило, чем выше pO2 тем выше HbOsat, эта зависимость не является линейной.
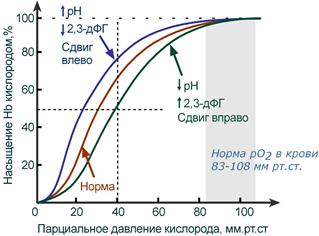
Кривая диссоциации гемоглобина в норме и
при изменении pH и концентрации 2,3-дифосфоглицерата
В центральной части кривой насыщения (или кривой диссоциации) гемоглобина малейшие сдвиги pO2 приводят к резким изменениям насыщения гемоглобина. И наоборот, при высоком pO2 (80-90-100 мм рт.ст) кривая становится плоской, насыщение гемоглобина мало зависит от колебаний кислорода в плазме.
Сдвиг влево происходит при защелачивании и снижении концентрации 2,3-дифосфоглицерата и сигнализирует об увеличении сродства кислорода к гемоглобину (в легких). Сдвиг вправо – это снижение сродства кислорода к гемоглобину (в тканях), обеспечивается закислением среды и накоплением 2,3-дифосфоглицерата.
Показатель pO2 не отражает содержание кислорода в цельной крови! Но хотя pO2 и не показывает общее количество кислорода в крови, но это общее количество зависит от pO2 через показатель сатурации гемоглобина.
В свою очередь имеются факторы, влияющие на величину pO2:
1. Альвеолярная вентиляция. Хотя она влияет как на pO2 так и на pCO2, но доля кислорода в альвеолах при гипервентиляции может лишь слегка увеличиться, приближаясь к pO2 атмосферного воздуха, при гиповентиляции – стремительно падает, вытесняясь поступающим из крови CO2. В то же время доля CO2 в альвеолах быстро снижается при усиленной вентиляции.
2. Вентиляционно-перфузионное соотношение, определяется тем, что
- не вся кровь, притекающая к легким, соприкасается с хорошо вентилируемыми альвеолами (спадение альвеол, уплотнение стенки).
- не все хорошо вентилируемые альвеолы получают достаточно крови (правожелудочковая сердечная недостаточность).
3. Концентрация кислорода во вдыхаемом воздухе (FiO2, fraction of inspired oxygen).
В таблице приведены сравнительные величины концентрации кислорода и углекислого газа в воздухе, крови и тканях.
Необходимо обратить внимание на перепады концентраций кислорода и углекислого газа в крови и альвеолярном воздухе. Важной особенностью является то, что pO2 в альвеолярном воздухе и артериальной крови очень близки, т.е. в обычных условиях глубоким и/или частым дыханием невозможно повысить потребление кислорода и насыщение им гемоглобина. В то же время разность концентраций pCO2 в венозной крови и альвеолярном воздухе позволяет эффективно его удалять при частом дыхании.
| pO2, мм рт.ст. | pCO2, мм рт.ст | |
| Вдыхаемый воздух | 159 | 0,23 |
| Альвеолярный воздух | 105-110 | 40 |
| Артериальная кровь | 83-108 | 35-45 |
| Ткани | 10-20 | 50-60 |
| Венозная кровь | 35-49 | 46-51 |
| Выдыхаемый воздух | 116 | 32 |
Источник
Дыхательная (легочная) гипоксияразвивается при различных видах дыхательной недостаточности, когда по тем или другим причинам затруднено проникновение кислорода из альвеол в кровь. Это может быть связано: 1) с гиповентиляцией альвеол, вследствие чего в них падает парциальное давление кислорода; 2) их спадением из-за недостатка сурфактанта; 3) уменьшением дыхательной поверхности легких вследствие понижения количества функционирующих альвеол; 4) затруднением диффузии кислорода через альвеолярно-капиллярную мембрану; 5) нарушением кровоснабжения ткани легких, развитием в них отека; 6) появлением большого количества перфузируемых, но не вентилируемых альвеол; 7) усилением шунтирования венозной крови в артериальную на уровне легких (пневмония, отек, эмболия a. pulmonalis) или сердца (при незаращении боталлова протока, овального отверстия и др.). Из-за этих нарушений снижается рО2 в артериальной крови, уменьшается содержание оксигемоглобина, т.е. возникает состояние гипоксемии.При гиповентиляции альвеол развивается гиперкапния,понижающая сродство гемоглобина к кислороду, сдвигающая кри-
вую диссоциации оксигемоглобина вправо и затрудняющая еще больше процесс оксигенации гемоглобина в легких. Вместе с тем в крови возрастает содержание восстановленного гемоглобина, что способствует появлению цианоза.
Скорость кровотока и кислородная емкость при дыхательном типе гипоксии нормальны или повышены (в качестве компенсации).
Циркуляторная (сердечно-сосудистая) гипоксияразвивается при нарушениях кровообращения и может иметь генерализованный (системный) или местный характер.
Причиной развития генерализованной циркуляторной гипоксии могут являться: 1) недостаточность функции сердца; 2) снижение сосудистого тонуса (шок, коллапс); 3) уменьшение общей массы крови в организме (гиповолемия) после острой кровопотери и при обезвоживании; 4) усиленное депонирование крови (например, в органах брюшной полости при портальной гипертензии и др.); 5) нарушение текучести крови в случаях сладжа эритроцитов и при синдроме диссеминированного внутрисосудистого свертывания крови (ДВС-синдроме); 6) централизация кровообращения, что имеет место при различных видах шока. Циркуляторная гипоксия местного характера, захватывающая какой-либо орган или область тела, может развиться при таких местных нарушениях кровообращения, как венозная гиперемия и ишемия.
Для всех перечисленных состояний характерно уменьшение объемной скорости кровотока. Общее количество крови, притекающей к органам и участкам тела, снижается, соответственно уменьшается и объем доставляемого кислорода, хотя его напряжение (рО2) в артериальной крови, процент оксигемоглобина и кислородная емкость могут быть нормальными. При этом виде гипоксии обнаруживается нарастание коэффициента утилизации кислорода тканями вследствие увеличения времени контакта между ними и кровью при замедлении скорости кровотока, кроме того, замедление скорости кровотока способствует накоплению в тканях и капиллярах углекислоты, которая ускоряет процесс диссоциации оксигемоглобина. Содержание оксигемоглобина в венозной крови в этом случае понижается. Артериовенозная разница по кислороду возрастает. У больных отмечается акроцианоз.
Повышение утилизации кислорода тканями не происходит при усиленном шунтировании крови по артериоло-венулярным анастомозам вследствие спазма прекапиллярных сфинктеров или на-
рушения проходимости капилляров при сладже эритроцитов или развитии ДВС-синдрома. В этих условиях содержание оксигемоглобина в венозной крови может оказаться повышенным. То же происходит, когда транспорт кислорода замедлен на отрезке пути от капилляров до митохондрий, что имеет место при интерстициальном и внутриклеточном отеках, снижении проницаемости стенок капилляров и клеточных мембран. Из этого следует, что для правильной оценки количества кислорода, потребленного тканями, большое значение имеет определение содержания оксигемоглобина в венозной крови.
Гемическая (кровяная) гипоксияразвивается при уменьшении кислородной емкости кровииз-за снижения содержания гемоглобина и эритроцитов (так называемая анемическая гипоксия)или вследствие образования разновидностей гемоглобина, не способных транспортировать кислород, таких, как карбоксигемоглобин и метгемоглобин.
Снижение содержания гемоглобина и эритроцитов имеет место при различных видах анемий и при гидремии, возникающей в связи с избыточной задержкой воды в организме. При анемияхрО2 в артериальной крови и процент оксигенации гемоглобина не отклоняются от нормы, но снижается общее количество кислорода, связанного с гемоглобином, и поступление его в ткани является недостаточным. При этом виде гипоксии общее содержание оксигемоглобина в венозной крови по сравнению с нормой понижено, но артериовенозная разница по кислороду нормальная.
Образование карбоксигемоглобинапроисходит при отравлении окисью углерода (СО, угарный газ), которая присоединяется к молекуле гемоглобина в том же месте, что и кислород, при этом сродство гемоглобина к СО в 250-350 раз (по данным различных авторов) превышает сродство к кислороду. Поэтому в артериальной крови процент оксигенации гемоглобина снижен. При содержании в воздухе 0,1% угарного газа более половины гемоглобина быстро превращается в карбоксигемоглобин. Как известно, СО образуется при неполном сгорании топлива, работе двигателей внутреннего сгорания, может накапливаться в шахтах. Важным источником СО является курение. Содержание карбоксигемоглобина в крови курильщиков может достигать 10-15%, у некурящих оно составляет 1-3%. Отравление СО происходит также при вдыхании большого количества дыма при пожарах. Частым источником СО является метиленхлорид – распространенный компонент растворителей
красок. Он проникает в организм в виде паров через дыхательные пути и через кожу, поступает с кровью в печень, где расщепляется с образованием угарного газа.
Карбоксигемоглобин не может участвовать в транспорте кислорода. Образование карбоксигемоглобина уменьшает количество оксигемоглобина, способное переносить кислород, а также затрудняет диссоциацию оставшегося оксигемоглобина и отдачу кислорода тканям. В связи с этим уменьшается артериовенозная разница по содержанию кислорода. Кривая диссоциации оксигемоглобина в этом случае сдвигается влево. Поэтому инактивация 50% гемоглобина при превращении его в карбоксигемоглобин сопровождается более тяжелой гипоксией, чем недостаток 50% гемоглобина при анемии. Утяжеляющим является и то обстоятельство, что при отравлении СО не происходит рефлекторной стимуляции дыхания, так как парциальное давление кислорода в крови остается неизменным. Токсическое действие угарного газа на организм обеспечивается не только образованием карбоксигемоглобина. Малая фракция растворенной в плазме крови окиси углерода играет очень важную роль, так как она проникает в клетки и повышает образование в них активных радикалов кислорода и перекисное окисление ненасыщенных жирных кислот. Это ведет к нарушению структуры и функции клеток, в первую очередь в ЦНС, с развитием осложнений: угнетением дыхания, падением кровяного давления. В случаях тяжелых отравлений быстро возникает состояние комы и наступает смерть. Наиболее эффективными мерами помощи при отравлении СО являются нормо- и гипербарическая оксигенация. Сродство окиси углерода к гемоглобину снижается при повышении температуры тела и под действием света, а также при гиперкапнии, что послужило поводом для использования карбогена при лечении людей, отравленных угарным газом.
Карбоксигемоглобин, формирующийся при отравлении угарным газом, имеет яркий вишнево-красный цвет, и его присутствие нельзя визуально определить по цвету крови. Для определения содержания СО в крови используют спектрофотометрический анализ крови, цветовые химические пробы с веществами, придающими СО-содержащей крови малиновый цвет (формалин, дистиллированная вода) или коричневато-красный оттенок (КОН) (см. раздел 14.4.5).
Метгемоглобинотличается от оксигемоглобина наличием в составе гема трехвалентного железа и так же, как карбоксигемогло-
бин, имеет большее сродство к гемоглобину, чем кислород, и не способен к переносу кислорода. В артериальной крови при метгемоглобинообразовании процент оксигенации гемоглобина снижен.
Существует большое количество веществ – метгемоглобинообразователей.К их числу относятся: 1) нитросоединения (окислы азота, неорганические нитриты и нитраты, селитра, органические нитросоединения); 2) аминосоединения – анилин и его производные в составе чернил, гидроксиламин, фенилгидразин и др.; 3) различные красители, например метиленовая синь; 4) окислители – бертолетова соль, перманганат калия, нафталин, хиноны, красная кровяная соль и др.; 5) лекарственные препараты – новокаин, аспирин, фенацитин, сульфаниламиды, ПАСК, викасол, цитрамон, анестезин и др. Вещества, вызывающие превращение гемоглобина в метгемоглобин, образуются при ряде производственных процессов: при производстве силоса, работе с ацетиленовыми сварочно-режущими аппаратами, гербицидами, дефолиантами и др. Контакт с нитритами и нитратами происходит также при изготовлении взрывчатых веществ, консервировании пищевых продуктов, при сельскохозяйственных работах; нитраты часто присутствуют в питьевой воде. Существуют наследственные формы метгемоглобинемии, обусловленные дефицитом ферментных систем, участвующих в превращении (редукции) постоянно образующегося в малых количествах метгемоглобина в гемоглобин.
Образование метгемоглобина не только снижает кислородную емкость крови, но и резко уменьшает способность оставшегося оксигемоглобина отдавать кислород тканям вследствие сдвига кривой диссоциации оксигемоглобина влево. В связи с этим уменьшается артериовенозная разница по содержанию кислорода.
Метгемоглобинообразователи могут оказывать и непосредственное угнетающее действие на тканевое дыхание, разобщать окисление и фосфорилирование. Таким образом, имеется значительное сходство в механизме развития гипоксии при отравлении СО и метгемоглобинообразователями. Признаки гипоксии выявляются при превращении в метгемоглобин 20-50% гемоглобина. Превращение в метгемоглобин 75% гемоглобина является смертельным. Присутствие в крови метгемоглобина свыше 15% придает крови коричневый цвет («шоколадная кровь») (см. раздел 14.4.5).
При метгемоглобинемии происходит спонтанная деметгемоглобинизация благодаря активации редуктазной системы эритроцитов
и накоплению недоокисленных продуктов. Этот процесс ускоряется под действием аскорбиновой кислоты и глутатиона. При тяжелом отравлении метгемоглобинообразователями лечебный эффект могут оказать обменное переливание крови, гипербарическая оксигенация и вдыхание чистого кислорода.
Тканевая (гистотоксическая) гипоксияхарактеризуется нарушением способности тканей поглощать в нормальном объеме доставленный им кислород из-за нарушения системы клеточных ферментов в цепи транспорта электронов.
В этиологии данного вида гипоксии играют роль: 1) инактивация дыхательных ферментов: цитохромоксидазы под действием цианидов; клеточных дегидраз – под действием эфира, уретана, алкоголя, барбитуратов и других веществ; ингибирование дыхательных ферментов происходит также под действием ионов Cu, Hg и Ag; 2) нарушение синтеза дыхательных ферментов при дефиците витаминов B1, B2, PP, пантотеновой кислоты; 3) ослабление сопряженности процессов окисления и фосфорилирования при действии разобщающих факторов (отравление нитритами, микробными токсинами, тиреоидными гормонами и др.); 4) повреждение митохондрий ионизирующей радиацией, продуктами перекисного окисления липидов, токсически действующими метаболитами при уремии, кахексии, тяжелых инфекциях. Гистотоксическая гипоксия может развиться также при отравлении эндотоксинами.
При тканевой гипоксии, обусловленной разобщением процессов окисления и фосфорилирования, потребление кислорода тканями может возрастать, однако превалирующее количество образующейся энергии рассеивается в виде тепла и не может использоваться для нужд клетки. Синтез макроэргических соединений снижен и не покрывает потребностей тканей, они находятся в таком же состоянии, как при недостатке кислорода.
Подобное состояние возникает и при отсутствии в клетках субстратов для окисления, что имеет место при тяжелой форме голодания. На этом основании выделяют субстратную гипоксию.
При гистотоксической и субстратной формах гипоксии напряжение кислорода и процент оксигемоглобина в артериальной крови нормальны, а в венозной крови – повышены. Артериовенозная разница в содержании кислорода падает вследствие снижения утилизации кислорода тканями. Цианоз при данных видах гипоксии не развивается (табл. 16-2).
Таблица 16-2.Основные показатели, характеризующие различные виды гипоксии
Смешанные формы гипоксииявляются наиболее частыми. Они характеризуются сочетанием двух основных типов гипоксии или более: 1) при травматическом шоке наряду с циркуляторной может развиться дыхательная форма гипоксии в связи с нарушением микроциркуляции в легких («шоковое легкое»); 2) при тяжелой анемии или массивном образовании карбоксиили метгемоглобина развивается гипоксия миокарда, что ведет к снижению его функции, падению кровяного давления – в результате на анемическую гипоксию наслаивается циркуляторная; 3) отравление нитратами вызывает гемическую и тканевые формы гипоксии, так как под действием этих ядов происходит не только образование метгемоглобина, но и разобщение процессов окисления и фосфолирирования. Разумеется, смешанные формы гипоксии могут оказать более выраженное повреждающее действие, чем какой-либо один вид гипоксии, так как приводят к срыву ряда компенсаторноприспособительных реакций.
Развитию гипоксии способствуют состояния, при которых возрастает потребность в кислороде, – лихорадка, стресс, высокая физическая нагрузка и др.
Перегрузочная форма гипоксии (физиологическая)развивается у здоровых людей при тяжелой физической работе, когда поступление в ткани кислорода может стать недостаточным из-за высокой потребности в нем. При этом коэффициент потребления кислорода тканями становится очень высоким и может достигать 90% (вместо 25% в норме). Повышенной отдаче кислорода тканям способствует развивающийся при тяжелой физической работе метаболический ацидоз, который снижает прочность связи гемоглобина с кислородом. Парциальное давление кислорода в артериальной крови нормально, так же как и содержание оксигемоглобина, а в венозной крови эти показатели резко снижены. Артериовенозная разница по кислороду в этом случае повышается вследствие возрастания утилизации кислорода тканями.
Источник
