Осмотическое давление крови человека в норме равно
Осмотическое давление крови — это давление, которое способствует проникновению водного растворителя через полупроницаемую мембрану в сторону более концентрированного состава.
Благодаря этому в организме человека происходит водный обмен между тканями и кровью. Измерять его можно с помощью осмометра или криоскопически.
От чего зависит осмотическая величина
На этот показатель оказывает влияние количество электролитов и неэлектролитов, растворенных в плазме крови. Не менее 60% составляет ионизированный хлорид натрия. Растворы, осмотическое давление которых приближается к плазменному, называют изотоническими.
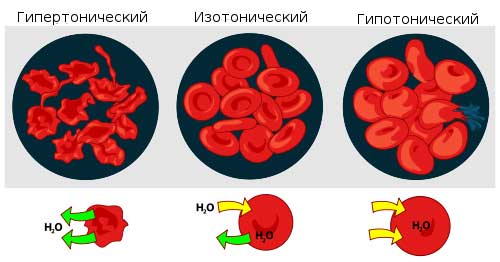
Если эта величина снижена, то такой состав зовется гипотоническим, а в случае ее превышения — гипертоническим.

При изменении нормального уровня раствора в тканях клетки повреждаются. Для нормализации состояния жидкости могут вводиться извне, причем состав будет зависеть от характера болезни:
- Гипертонический раствор способствует выведению воды в сосуды.
- Если давление в норме, то препараты разводят в изотоническом растворе, обычно это натрий хлорида.
- Гипотонический концентрированный раствор способен привести к разрыву клетки. Вода, проникая в клетку крови, стремительно наполняет ее. Но при правильной дозировке это способствует очистке ран от гноя, уменьшению аллергического отека.
Почки и потовые железы заботятся о том, чтобы этот показатель был неизменным. Они создают защитный барьер, который не допускает влияния продуктов обмена на организм.
Поэтому осмотическое давление у человека практически всегда имеет постоянную величину, резкий скачек может произойти лишь после интенсивной физической нагрузки. Но организм все равно сам быстро нормализует этот показатель.
Как влияет питание
Правильное питание — залог здоровья всего человеческого тела. Изменение давления происходит в случае:
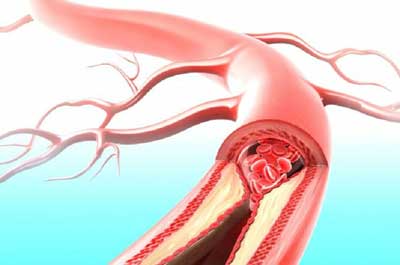
- Употребления большого количества соли. Это приводит к отложению натрия, из-за чего стенки сосудов становятся плотными, соответственно, уменьшается просвет. В таком состоянии организм не справляется с выведением жидкости, что приводит к увеличению циркуляции крови и повышению артериального давления, появлению отеков.
- Недостаточного употребления жидкости. Когда организму не хватает воды, нарушается водный баланс, кровь сгущается, так как уменьшается количество растворителя, то есть воды. Человек ощущает сильную жажду, утолив которую, запускает процесс возобновления работы механизма.
- Употребления вредной пищи или нарушения работы внутренних органов (печени и почек).
Как измеряется, и о чем говорят показатели
Величина осмотического давления плазмы крови измеряется при замерзании последней. В среднем эта величина в норме составляет 7,5–8,0 атм. При повышении показателя температура замерзания раствора будет выше.
Часть осмотической величины создает онкотическое давление, его образуют белки плазмы. Оно отвечает за регуляцию водного обмена. Онкотическое давление крови в норме составляет 26–30 мм рт. ст. Если показатель изменяется в меньшую сторону, то появляется отечность, так как организм плохо справляется с выведением жидкости, и она скапливается в тканях.
Это может происходить при заболеваниях почек, длительном голодании, когда состав крови содержит мало белков, или при проблемах с печенью, в этом случае за сбой отвечают альбумины.
Влияние на человеческий организм
Бесспорно, осмос и осмотическое давление — это основные факторы, влияющие на упругость тканей и способность организма сохранять форму клеток и внутренних органов. Они обеспечивают ткани нутриентами.
Чтобы понять, что это такое, следует эритроцит поместить в дистиллированную воду. Со временем вся клетка наполнится водой, оболочка эритроцита разрушится. Этот процесс получил название «гемолиз».

Если клетку окунуть в концентрированный солевой раствор, она потеряет свою форму и упругость, произойдет ее сморщивание. Плазмолиз приводит к потере эритроцитом воды. В изотоническом же растворе сохранятся первоначальные свойства.
Осмотическое давление обеспечивает нормальное движение воды в организме.
Мы настоятельно рекомендуем не заниматься самолечением, лучше обратитесь к своему лечащему доктору. Все материалы на сайте носят ознакомительный характер!
Осмотическое давление — давление на раствор, отделенный от чистого растворителя полупроницаемой мембраной, при к-ром прекращается осмос, т. е. переход молекул растворителя в раствор через разделяющую их полупроницаемую мембрану или переход молекул растворителя через полупроницаемую мембрану от раствора, менее концентрированного, к раствору, более концентрированному. Полупроницаемые мембраны представляют собой естественные или искусственные пленки, проницаемые только для молекул растворителя (напр., воды) и не проницаемые для молекул растворенного вещества. Осмос и Осмотическое давление играют большую роль в поддержании концентрации веществ, растворенных в жидкостях организма, на определенном, физиологически необходимом уровне, и, следовательно, в распределении воды между тканями и клетками. При изучении изолированных клеток и тканей важно, чтобы искусственная культуральная среда была изотонична естественной среде. При введении в организм различного рода жидкостей наименьшие нарушения вызывают р-ры с Осмотическим давлением, равным Осмотическому давлению жидкостей организма.

Рис. Схема простейшего осмометра: 1— внешний сосуд, наполненный чистой водой; 2— внутренний сосуд из необожженной глины, в порах которого осаждена железосинеродистая медь, образующая полупроницаемую мембрану, наполнен исследуемым раствором; h — высота столба жидкости, гидростатическое давление которого равно избыточному давлению чистой воды на раствор, т. е. осмотическому давлению раствора.
Измерение О. д. (осмометрия) находит широкое применение для определения мол. веса (массы) биологически активных высокомолекулярных веществ, таких, как белки, углеводы, нуклеиновые к-ты и др. Измерение величины О. д. производят с помощью приборов, называемых осмометрами (рис.). Число молекул воды, сталкивающихся со стороны воды с полупроницаемой мембраной, образованной железосинеродистой медью, больше числа молекул воды, сталкивающихся с этой мембраной со стороны р-ра, т. к. концентрация молекул воды в р-ре ниже, чем в чистой воде. В результате этого происходит осмос и возникает избыточное гидростатическое давление на р-р, под действием к-рого скорость перехода молекул воды через мембрану в чистую воду возрастает. Если избыточное давление на р-р достигает величины, равной О. д. р-ра, то число молекул воды, проходящих сквозь мембрану в обоих направлениях, становится одинаковым, осмос прекращается, и между р-ром и растворителем, находящимися по обе стороны полупроницаемой мембраны, устанавливается осмотическое равновесие. Т. о., осмотическое давление возникает лишь в том случае, когда р-р и растворитель отделены друг от друга полупроницаемой мембраной.
Осмотическое давление изолированных клеток или тканей наиболее просто измерить методом плазмолиза. Для этого исследуемые объекты помещают в р-ры с разными концентрациями какого-нибудь вещества, по отношению к к-рому клеточная мембрана непроницаема. Растворы с О. д. более высоким, чем О. д. содержимого клеток (гипертонические р-ры), вызывают сморщивание клеток — плазмолиз вследствие перехода воды из клетки в р-р. Растворы с О. д. более низким, чем О. д. содержимого клеток (гипотонические р-ры), вызывают увеличение объема клеток в результате перехода воды из р-ра в клетку. Р-ры с О. д., равным О. д. содержимого клеток (изотонические р-ры), не вызывают изменения объема клеток. Зная концентрацию такого р-ра, вычисляют его О. д.; такова же будет величина О. д. и содержимого клеток. Важным фактором, определяющим прохождение воды через клеточную мембрану, особенно в начальной стадии процесса, могут быть мембранные потенциалы, к-рые вызывают электроосмотическое перемещение воды через оболочку клетки, так наз. аномальный осмос (см. Электроосмос). В подобных случаях измерение О. д. методом плазмолиза является неточным.
Определение Осмотического давления р-ров, содержащих низкомолекулярные вещества, для к-рых трудно приготовить непроницаемую мембрану, производят косвенными методами, обычно посредством измерения понижения температуры замерзания р-ра (см. Криометрия).
Я. Вант-Гофф показал, что Осмотическое давление разбавленных р-ров неэлектролитов подчиняется законам, установленным для давления газов (см.), и может быть вычислено по уравнению, аналогичному уравнению Клапейрона—Менделеева для газов:
π•v = n • RT, (1)
где π — осмотическое давление, v — объем раствора в л, n — число молей растворенного вещества-не-электролита, T — температура по абсолютной шкале, R — постоянная, численное значение к-рой таково же, как и для газов (R для газов равна 82,05*10-3 л-атм/град-моль).
Приведенное уравнение является математическим выражением закона Вант-Гоффа: О. д. разбавленного р-ра равно давлению, к-рое производило бы растворенное вещество, находясь в газообразном состоянии и занимая объем, равный объему р-ра при той же температуре. Введя в уравнение молярную концентрацию — с = nv получим π = c*RT.
О. д. р-ра электролита больше О. д. р-ра неэлектролита той же молярной концентрации. Это объясняется диссоциацией молекул электролита в р-ре на ионы, вследствие чего возрастает концентрация кинетически активных частиц, к-рой определяется величина О. д.
Число i, показывающее, во сколько раз О. д. (дэ) р-ра электролита больше О. д. (л) р-ра неэлектролита той же молярной концентрации, называют изотоническим коэффициентом Вант-Гоффа:
i = πэ/π
Численная величина i зависит от природы электролита и его концентрации в р-ре. Для слабых электролитов величина i может быть вычислена по формуле:
i = a*(N — 1) + 1,
где а — степень диссоциации электролита, а N — число ионов, на к-рые распадается одна молекула электролита. Для разбавленных р-ров сильных электролитов i можно принять равным N.
Из сказанного следует, что О. д. р-ра электролита можно вычислить по уравнению:
πэ = i • с • RT,
где с — молярная концентрация.
Если в р-ре, кроме низкомолекулярных растворенных веществ, содержатся высокомолекулярные вещества (коллоиды), то О. д., обусловленное высокомолекулярными веществами, называют, по предложению Шаде (H. Schade), онкотическим, или коллоидно-осмотическим давлением.
Общее Осмотическое давление плазмы крови человека в норме равно 7,6 атм, онкотическое давление, обусловленное в основном белками плазмы, составляет только 0,03—0,04 атм. Онкотическое давление, несмотря на малую величину по сравнению с общим О. д. плазмы крови, играет большую роль в распределении воды между кровью и тканями организма.
Многие биополимеры, напр, белки, нуклеиновые к-ты и др., являясь полиэлектролитами, при диссоциации в р-ре образуют многозарядные ионы (полиионы) большого мол. веса (массы), для к-рых мембрана осмометра непроницаема, и обычные ионы малых размеров, проходящие сквозь полупроницаемую мембрану. Если в р-ре, заполняющем осмометр, содержится полиэлектролит, то низкомолекулярные ионы, диффундирующие сквозь мембрану, неравномерно распределяются по обе стороны мембраны (см. Мембранное равновесие). Наблюдаемое при этом избыточное гидростатическое давление в осмометре будет равно πБ = πБ + π1 — π2, где πБ — О. д., обусловленное биополимером, а π1 и π2 — О. д. низкомолекулярного электролита, находящегося в осмотической ячейке и во внешнем р-ре соответственно. При измерении О. д. р-ров биополимеров необходимо учитывать возможность неравномерного распределения низкомолекулярных электролитов по обе стороны полупроницаемой мембраны осмометра или проводить измерения при достаточном избытке низкомолекулярного электролита, специально вводимого в р-р биополимера. В этом случае низкомолекулярный электролит распределяется по обе стороны полупроницаемой мембраны практически равномерно, при этом = π1 = π2 и πБ = πН.
Осморегуляция
Совокупность механизмов, обеспечивающих поддержание О. д. в жидких средах организма на оптимальном для обмена веществ уровне, называют осморегуляцией. Получая информацию от рецепторных зон об изменении О. д. крови, ц. н. с. включает ряд механизмов, возвращающих систему в оптимальное для организма состояние. Включение происходит двумя путями: нервным и гуморальным. Отклонение величины О. д. от оптимального уровня улавливается в организме осморецепторами (см.), среди к-рых ведущее место занимают центральные осморецепторы, расположенные в супраоптическом и паравентрикулярном ядрах гипоталамуса (см.).
Клетки супраоптического ядра гипоталамуса способны секретировать антидиуретический гормон (АДГ), по аксонам этих клеток он перемещается в нейрогипофиз, где происходит его накопление и выведение в общий кровоток (см. Вазопрессин). АДГ влияет на реабсорбцию воды в дистальных отделах нефрона и способен вызывать сужение просвета сосудов. Афферентные сигналы, регулирующие выделение АДГ, поступают в гипоталамус от объемных рецепторов (волюморецепторов) левого предсердия, от рецепторов дуги аорты, от осморецепторов внутренней сонной артерии, от баро рецепторов и хеморецепторов каротидного синуса. Увеличение О. д. внеклеточной жидкости вызывает возрастание секреции АДГ как за счет самого осмотического давления, так и за счет уменьшения объема внеклеточной жидкости при обезвоживании организма. Т. о., на выделение АДГ влияют две системы сигнализации: сигнализация от осморецепторов и сигнализация от барорецепторов и волюморецепторов. Однако ведущим звеном в регуляции секреции АДГ все же является О. д. плазмы крови, действующее на осморецепторы гипоталамуса.
Особая роль в поддержании физиологических величин Осмотического давления принадлежит ионам натрия (см.). Дегидратация возникает именно в связи с изменением содержания ионов Na+. При обезвоживании из-за изменения содержания ионов Na+ уменьшение объема артериальной крови и межклеточной жидкости регистрируется волюморецепторами, импульсы от к-рых по нервным путям достигают отделов ц. н. с., регулирующих выделение одного из минералокортикоидных гормонов — альдостерона (см.), к-рый повышает реабсорбцию натрия. Центральная регуляция секреции альдостерона осуществляется гипоталамусом, продуцирующим адренокортикотропин-рилизинг-фактор (АКТГ-рилизинг-фактор), к-рый регулирует секрецию адренокортикотропного гормона (АКТГ), образуемого передней долей гипофиза (см. Адренокортикотропный гормон). Существует мнение, что наряду с влиянием АКТГ на секрецию альдостерона, есть особый центр регуляции секреции альдостерона, расположенный в среднем мозге. Именно сюда и поступает афферентная импульсация при уменьшении объема межклеточной жидкости в результате изменения содержания ионов натрия. Клетки центра регуляции секреции альдостерона в среднем мозге способны к нейросекреции — образующийся гормон поступает в эпифиз, где накапливается и оттуда выделяется в кровь. Этот гормон получил название адреногломерулотропина (АГТГ).
Выделение АДГ и альдостерона может регулироваться и ангиотензином (см.), очевидно путем его действия на особые рецепторы гипоталамических нейронов. Ренин-ангиотензинная система почек может выступать как волюморецепторная зона, реагирующая на изменение почечного кровотока.
На нормализацию измененного О. д. влияют также мочевыделение (см. Диурез), транскапиллярный обмен жидкости и ионов (см. Водно-солевой обмен), потоотделение (см.), выделение жидкости через легкие (с выдыхаемым воздухом в сутки теряется 350—400 мл воды) и выделение жидкости через жел.-киш. тракт (100—200 мл воды теряется с калом).
Способностью к нормализации Осмотического давления обладает и сама кровь. Она может выполнять роль осмотического буфера при всевозможных сдвигах как в сторону осмотической гипертонии, так и гипотонии. По-видимому, эта функция крови связана, во-первых, с перераспределением ионов между плазмой и эритроцитами и, во-вторых, со способностью белков плазмы крови связывать или отдавать ионы.
При уменьшении водных ресурсов организма или нарушении нормального соотношения между водой и минеральными солями (гл. обр. хлористым натрием) возникает жажда (см.), удовлетворение к-рой способствует поддержанию физиологического уровня водного баланса и электролитного равновесия в организме (см. Гомеостаз).
Библиография: Бладергрён Н. В. Физическая химия в медицине и биологии, пер. с нем., с. 102 и др., М., 1951; Вагнер Р. Г. Определение осмотического давления, в кн.: Физич. методы органической химии, под ред. А. Вайсбергера, пер. с англ., т. 1, с. 270, М., 1950, библиогр.; Гинецинский А. Г. Физиологические механизмы водно-солевого равновесия, М.—Л., 1963; Губанов Н. И. и Утепбергенов А. А. Медицинская биофизика, с. 149, М., 1978; Наточин Ю. В. Ионорегулирующая функция почки, Д., 1976; Сатпаева X. К. Внепочечные механизмы осморегуляции, Алма-Ата, 1971, библиогр.; Уильямс В. и Уильямс X. Физическая химия для биологов, пер. с англ., с. 146, М., 1976; Физиология почки, под ред. Ю. В. Наточина, Л., 1972; Andersson В. Regulation of water intake, Physiol. Rev., v. 58, p. 582, 1978, bibliogr.
В. П. Мишин; С. А. Осиповский (физ.).
Объем крови – общее количество крови в организме взрослого человека составляет в среднем 6 – 8% от массы тела, что соответствует 5 – 6 л. Повышение общего объема крови называют гиперволемией, уменьшение – гиповолемией.Относительная плотность крови – 1,050 – 1.060 зависит в основном от количества эритроцитов. Относительная плотность плазмы крови – 1.025 – 1.034, определяется концентрацией белков.Вязкость крови – 5 усл.ед., плазмы – 1,7 – 2,2 усл.ед., если вязкость воды принять за 1. Обусловлена наличием в крови эритроцитов и в меньшей степени белков плазмы.
Осмотическое давление крови – сила, с которой растворитель переходит через полунепроницаемую мембрану из менее в более концентрированный раствор. Осмотическое давление крови вычисляют криоскопическим методом путем определения точки замерзания крови (депрессии), которая для нее равна 0,56 – 0,58 С. Осмотическое давление крови в среднем составляет 7,6 атм. Оно обусловлено растворенными в ней осмотически активными веществами, главным образом неорганическими электролитами, в значительно меньшей степени – белками. Около 60% осмотического давления создается солями натрия (NаСl).
Осмотическое давление определяет распределение воды между тканями и клетками. Функции клеток организма могут осуществляться лишь при относительной стабильности осмотического давления. Если эритроциты поместить в солевой раствор, имеющий осмотическое давление, одинаковое с кровью, они не изменяют свой объем. Такой раствор называют изотоническим, или физиологическим. Это может быть 0,85% раствор хлористого натрия. В растворе, осмотическое давление которого выше осмотического давления крови, эритроциты сморщиваются, так как вода выходит из них в раствор. В растворе с более низким осмотическим давлением, чем давление крови, эритроциты набухают в результате перехода воды из раствора в клетку. Растворы с более высоким осмотическим давлением, чем давление крови, называются гипертоническими, а имеющие более низкое давление – гипотоническими.
Онкотическое давление крови – часть осмотического давления, создаваемого белками плазмы. Оно равно 0,03 – 0,04 атм, или 25 – 30 мм рт.ст. Онкотическое давление в основном обусловлено альбуминами. Вследствие малых размеров и высокой гидрофильности они обладают выраженной способностью притягивать к себе воду, за счет чего она удерживается в сосудистом русле, При снижении онкотического давления крови происходит выход воды из сосудов в интерстициальное пространство, что приводит к отеку тканей.
Кислотно-основное состояние крови (КОС). Активная реакция крови обусловлена соотношением водородных и гидроксильных ионов. Для определения активной реакции крови используют водородный показатель рН – концентрацию водородных ионов, которая выражается отрицательным десятичным логарифмом молярной концентрации ионов водорода. В норме рН – 7,36 (реакция слабоосновная); артериальной крови – 7,4; венозной – 7,35. При различных физиологических состояниях рН крови может изменяться от 7,3 до 7,5. Активная реакция крови является жесткой константой, обеспечивающей ферментативную деятельность. Крайние пределы рН крови, совместимые с жизнью, равны 7,0 – 7,8. Сдвиг реакции в кислую сторону называется ацидозом, который обусловливается увеличением в крови водородных ионов. Сдвиг реакции крови в щелочную сторону называется алкалозом. Это связано с увеличением концентрации гидроксильных ионов ОН и уменьшением концентрации водородных ионов.
В крови имеется 4 буферных системы: бикарбонатная БС, фосфатная БС, гемоглобиновая БС, БС белков и плазмы. Все БС создают в крови щелочный резерв, который в организме относительно постоянен.
