Освободившиеся после распада гемоглобина соединения железа
Разрушение гемоглобина. Разновидности анемий
При разрыве эритроцитов их гемоглобин почти сразу же фагоцитируется макрофагами во многих частях тела, но особенно клетками Купфера печени и макрофагами селезенки и костного мозга. В течение нескольких следующих часов или дней макрофаги освобождают железо из гемоглобина, и оно возвращается в кровь и переносится трансферрином либо в костный мозг для формирования новых красных клеток крови, либо в печень и другие ткани для хранения в форме ферритина.
Порфириновая часть молекулы гемоглобина превращается макрофагами через ряд стадий в желчный пигмент билирубин, который выделяется в кровь и позднее удаляется из организма путем секреции печенью в желчь.
Анемия означает недостаток гемоглобина в крови, причиной может быть либо слишком малое число красных клеток крови, либо слишком малое количество гемоглобина в этих клетках. Далее представлены некоторые типы анемий и их физиологические причины.
Анемия, связанная с потерей крови. После острой кровопотери организм возмещает жидкую часть плазмы в течение 1-3 сут, но при этом концентрация красных клеток крови остается низкой. Концентрация эритроцитов обычно восстанавливается до нормы в течение 3-6 нед, если не происходит повторного кровотечения.
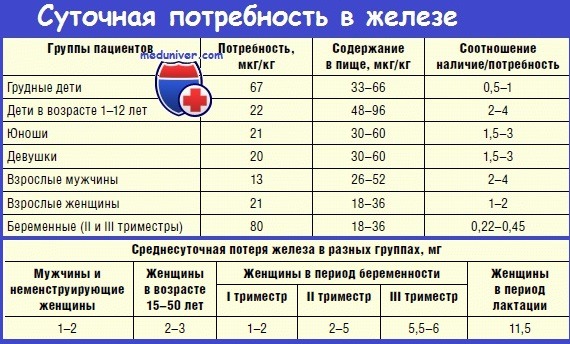
Часто при хронической кровопотере у человека железо из кишечника не может всасываться достаточно быстро, чтобы обеспечить адекватное возмещение теряемого с кровью гемоглобина. Формируемые в этом случае красные клетки крови гораздо мельче нормальных эритроцитов и содержат слишком мало гемоглобина, что характерно для микроцитарной гипохромной анемии; такие эритроциты показаны на рисунке.
Апластическая анемия. Аплазия костного мозга означает потерю функционирующего костного мозга. Например, у человека, подвергшегося облучению гамма-лучами при взрыве атомной бомбы, может произойти полное разрушение костного мозга с последующим развитием в течение нескольких недель летальной анемии. Тот же эффект могут вызвать избыточная рентгенотерапия, некоторые промышленные химикаты и даже лекарства, к которым у человека может быть повышенная чувствительность.
Мегалобластная анемия. На основании изложенного ранее обсуждения роли витамина B12, фолиевой кислоты и внутреннего фактора, секретируемого слизистой желудка, легко понять, что недостаток любого из этих веществ может привести к замедлению репродукции эритроцитов в костном мозге. В результате формируются слишком крупные красные клетки крови разнообразной формы, которые называют мегалобластами.
Следовательно, атрофия слизистой желудка, например при пернициозной анемии, или потеря всего желудка после хирургической тотальной гастрэктомии могут привести к мегалобластной анемии. Мегалобластная анемия часто развивается также у больных с кишечной спру, при которой плохо всасываются фолиевая кислота, витамин B12 и другие соединения витаминов группы В. Поскольку при этих состояниях эритробласты не могут пролиферировать достаточно быстро, чтобы формировать нормальное количество красных клеток крови, те эритроциты, которые формируются, по большей части увеличены в размерах, имеют неправильную форму и ломкие мембраны. Эти клетки легко рвутся, оставляя человека без необходимого количества красных клеток крови.
Гемолитическая анемия. Различные аномалии красных клеток крови, многие из которых — наследственные, делают клетки столь хрупкими, что они легко разрываются, проходя через капилляры, особенно в селезенке. Даже если количество формируемых красных клеток крови в норме или значительно ее превышает, как при некоторых гемолитических болезнях, срок жизни хрупкого эритроцита так короток, что клетки разрушаются быстрее, чем могут формироваться нормальные эритроциты; результатом этого является тяжелая анемия. Далее указаны некоторые из таких типов анемий.
При наследственном сфероцитозе красные клетки крови очень мелкие и сферические, а не двояковогнутые диски. Эти клетки не могут выдерживать сдавливания, поскольку не имеют нормальной свободной, мешкообразной клеточной мембраны, характерной для двояковогнутых дисков. При прохождении через пульпу селезенки и некоторые другие сосудистые ложа они легко ломаются даже при небольшом сдавливании.
При серповидно-клеточной анемии, которой болеют 0,3-1,0% коренных жителей Западной Африки, красные клетки крови содержат аномальный гемоглобин — гемоглобин S с поврежденными цепочками в его молекуле. Под действием низких концентраций кислорода такой гемоглобин осаждается в виде длинных кристаллов внутри эритроцита. Эти кристаллы удлиняют клетку и придают ей вид серпа, а не двояковогнутого диска.
Кроме того, осажденный гемоглобин повреждает клеточную мембрану, в результате клетка становится очень хрупкой, что сопровождается тяжелой анемией. Такие больные часто переживают порочный круг событий, называемый кризисом серповидно-клеточной болезни, при котором низкое напряжение кислорода в тканях вызывает образование серповидных форм эритроцитов, что ведет к разрушению красных клеток крови, а значит — к дальнейшему снижению напряжения кислорода, усилению образования серповидных форм и разрушению красных клеток крови. Сразу после начала процесс быстро прогрессирует, приводя в течение нескольких часов к резкому снижению числа красных клеток крови и часто — к смерти.
При гемолитической болезни новорожденных (эритробластозе) антитела от резус-отрицательной (Rh-) матери атакуют резус-положительные (Rh+) эритроциты плода. В результате резус-положительные клетки становятся ломкими, что ведет к их быстрому разрушению, способствуя развитию у новорожденного тяжелой анемии. Чрезвычайно быстрое формирование новых эритроцитов для возмещения разрушенных при гемолитической болезни новорожденных ведет к выделению в кровь из костного мозга большого количества молодых бластных форм красных клеток крови.
– Также рекомендуем “Влияние анемии на кровообращение. Полицитемия – эритремия”
Оглавление темы “Эритропоэз. Белые клетки крови”:
1. Влияние эритропоэтина на эритрогенез. Витамин В12 и фолиевая кислота в эритропоэзе
2. Пернициозная анемия. Образование гемоглобина
3. Связывание гемоглобина с кислородом. Обмен железа
4. Всасывание железа в кишечнике. Длительность жизни эритроцитов
5. Разрушение гемоглобина. Разновидности анемий
6. Влияние анемии на кровообращение. Полицитемия – эритремия
7. Влияние полицитемии на кровообращение. Лейкоциты – белые клетки крови
8. Типы белых клеток крови. Происхождение белых клеток крови
9. Длительность жизни белых клеток крови. Нейтрофилы и макрофаги
10. Фагоцитоз. Механизмы и значение фагоцитоза
Оглавление темы “Функции клеток крови. Эритроциты. Нейтрофилы. Базофилы.”: Железо. Железо в норме. Роль ионов железа в эритропоэзе. Трансферрин. Потребность организма в железе. Дефицит железа.В организме содержится 4—5 г железа в виде резервного (1/4) и функционально-активного железа (3/4). 62—70 % железа находится в гемоглобине эритроцитов, 5—10 % — в миоглобине, остальное — в тканях, где оно участвует во многих метаболических процессах: в составе металсодержащих энзимов—цитохромов обеспечивают митохондриальный транспорт электронов, синтез ДНК и деление клеток, метаболизм гормонов мозгового вещества надпочечников, детоксикационные механизмы, снижающие активность токсичных веществ под влиянием цитохрома Р450, в состав которого входит железо; поддерживают активность глицерол-3-фосфатдегидрогеназы в поперечно-полосатых мышцах, что сохраняет физическую работоспособность человека. Резервное железо постоянно переходит в функциональное и обратно. Так, за счет повторного использования костный мозг получает ежесуточно 20—25 мг железа. Ионы железа (Fe++) ежедневно всасываются в кишечнике из пищи. Fe2+ в кишечном содержимом вначале связывается с белком-рецептором на поверхности эпителия слизистой оболочки кишки (b3-интегрином), что необходимо для перехода его через мембрану клетки слизистой в цитозоль. Далее, образовав комплекс с цитозольным транспортным белком- мобилферрином, Fe2+ пересекает клетку эпителия слизистой кишечника оставаясь в этом комплексе вплоть до поступления Fe2+ в капиллярную сеть кишечника. С выходом в кровоток двухвалентное железо окисляется до трехвалентного белком плазмы крови церрулоплазмином и присоединяется к трансферрину, гликопротеину плазмы крови. Трансферрином Fe3+ доставляется к тканям и используется в митохондриях эритроб-ластов для синтеза гема, депонируется в макрофагах в виде резерва. Плазма содержит от 1,8 до 2,6 мг/л трансферрина, 1 мг которого связывает 1,25 мкг Fe. В общем объеме плазмы содержится около 3 мг Fe2+. В норме лишь ‘/з трансферрина плазмы насыщена железом. Количество железа, которое может быть связано трансферрином, называется общей железосвязывающей способностью крови и в норме составляет 250—400 мкг % (45— 72 мкмоль/л). Концентрация железа в сыворотке крови у взрослых людей обоего пола колеблется от 50 до 160 мкг % (9—29 мкмоль/л). С мочой выводится за сутки 60—100 мкг железа. Комплекс трансферрин — железо фиксируется на рецепторах мембран эритробластов. Количество этих рецепторов уменьшается за счет торможения их синтеза в ходе созревания эритроидных клеток и исчезает после созревания ретикулоцитов, поэтому в зрелые эритроциты железо не включается. Освобождение железа из комплекса трансферрин — железо обеспечивается энергией молекул АТФ, образуемых в эритробластах. Молекула трансферрина, отдавшая железо, смещается с мембранного участка молекулами трансферрина, связанными с железом, поскольку их сродство к рецепторам более сильное. Железо, поступившее в эритробласт, используется в митохондриях для синтеза гема и депонируется в эритробласте в виде резерва. В макрофагах печени и костного мозга резервное железо депонируется в молекуле ферритина. Внутри лизосом молекулы ферритина образуют большие аморфные нерастворимые агрегаты — гемосидерин. Таким образом, ферритин и гемосидерин — это формы резервного железа в клетках. Из клеточного резерва железо освобождается в двухвалентном состоянии (благодаря энзиму ксантиноксидазе, аскорбиновой кислоте и др.), затем церулоплазмин окисляет Fe2+ до трехвалентного состояния, Fe3+ соединяется с трансферрином и транспортируется с плазмой крови к эритробластам.
Абсорбции железа эпителиальными клетками желудочно-кишечного тракта способствуют сниженное насыщение трансферрина железом и повышенная эритропоэтическая активность крови. Абсорбция снижается при увеличении концентрации железа в клетках слизистой оболочки кишечника. В кишечнике более эффективна абсорбция Fe2+, чем Fe3+. Поэтому аскорбиновая кислота, фруктоза, аминокислоты (цистеин, метионин) поддерживают двухвалентную форму железа и ускоряют его абсорбцию. В кишечнике лучше абсорбируется биодоступное железо, входящее в состав гема (мясные продукты, кровяная колбаса), чем железо из пищи растительного происхождения. Абсорбция Fe2+ в желудочно-кишечном тракте зависит от возраста человека, функционального сотояния его организма. Она наиболее высокая у детей первых месяцев жизни и достигает 57 %, у 7— 10-летних —7,75—17,75 %, у взрослых мужчин и женщин — 1,1—11,2 % и у беременных женщин — 20 % от поступившего в желудочно-кишечный тракт железа. Отсюда ежедневная потребность в железе, абсорбируемом из пищи в организме человека, составляет: у детей от 0 до 4 мес жизни — 0,5 мг/день, от 1 года до 12 лет— 1,0 мг/день, женщины детородного периода — 2,8 мг/день (во время менструации потери железа составляют от 5 до 45 мг), молодые мужчины — 1 мг/день, старики — 0,9 мг/день, беременные женщины — 3—3,5 мг/день. В организм последних за время беременности должно поступать до 1 г железа (500 мг железа используется для синтеза дополнительного количества гемоглобина в организме беременной, 300 мг Fe2+ необходимо формирующемуся плоду и 200 мг Fe2+ компенсируют естественные потери металла организмом беременной женщины). Дефицит железа в организме человека приводит к развитию гипохромной анемии. – Также рекомендуем “Эритропоэз. Эритробластические островки. Анемия. Эритроцитоз.” |
За сутки у человека распадается около 9 г гемопротеинов, в основном это гемоглобин эритроцитов.
Эритроциты в норме живут 90-120 дней, после чего лизируются в клетках ретикулоэндотелиальной системы – макрофагах селезенки (главным образом), купферовских клетках печени и макрофагах костного мозга. При разрушении эритроцитов в кровеносном русле высвобождаемый гемоглобин образует комплекс с белком-переносчиком гаптоглобином (фракция α2-глобулинов крови) и также переносится в клетки РЭС селезенки, печени и костного мозга.
Синтез билирубина
В клетках РЭС гем в составе гемоглобина окисляется молекулярным кислородом. В реакциях последовательно происходит разрыв метинового мостика между 1-м и 2-м пиррольными кольцами гема с их восстановлением, отщеплением железа и белковой части и образованием оранжевого пигмента билирубина. Высвобождаемое железо может либо запасаться в клетке в комплексе с ферритином, либо выделяться наружу и связываться с трансферрином.
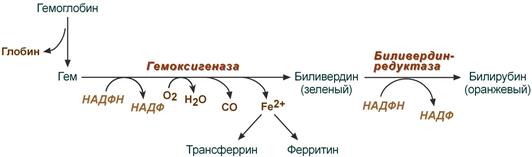
Реакции распада гемоглобина и образования билирубина
Билирубин – токсичное, жирорастворимое вещество, способное разобщать окислительное фосфорилирование в клетках. Особенно чувствительны к нему клетки нервной ткани.
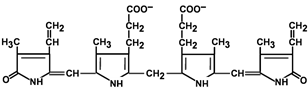
Строение билирубина
Выведение билирубина
Из клеток ретикуло-эндотелиальной системы билирубин попадает в кровь. Здесь он находится в комплексе с альбумином плазмы, в гораздо меньшем количестве – в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами. Образование таких комплексов не позволяет выделяться билирубину с мочой. Билирубин в комплексе с альбумином называется свободный (неконъюгированный) или непрямой билирубин.
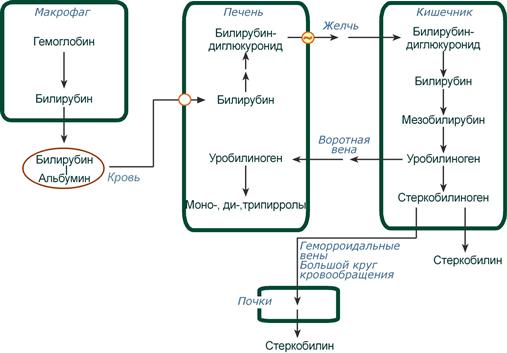
Этапы метаболизма билирубина в организме
Из сосудистого русла в гепатоциты билирубин попадает с помощью белка-переносчика (транспортный белок органических анионов) или по механизму флип-флоп. Далее при участии цитозольного связывающего белка лигандина (Y-протеин) билирубин транспортируется в ЭПР, где протекает реакция связывания билирубина с УДФ-глюкуроновой кислотой, при этом образуются моно- и диглюкурониды. Кроме глюкуроновой кислоты, в реакцию конъюгации могут вступать сульфаты, фосфаты, глюкозиды.
Билирубин-глюкуронид получил название связанный (конъюгированный) или прямой билирубин.
После образования билирубин-глюкурониды АТФ-зависимым переносчиком секретируются в желчные протоки и далее в кишечник, где при участии бактериальной β-глюкуронидазы превращаются в свободный билирубин. Одновременно, даже в норме (особенно у взрослых), некоторое количество билирубин-глюкуронидов может попадать из желчи в кровь по межклеточным щелям.
Таким образом, в плазме крови обычно присутствуют две формы билирубина: свободный (непрямой), попадающий сюда из клеток РЭС (80% и более всего количества), и связанный (прямой), попадающий из желчных протоков (в норме не более 20%).
Термины “связанный“, “конъюгированный“, “свободный“, “несвязанный” отражают взаимодействие билирубина и глюкуроновой кислоты (но не билирубина и альбумина!).
Термины “прямой” и “непрямой” введены, исходя из возможности химической реакции билирубина с диазореактивом Эрлиха. Связанный билирубин реагирует с реактивом напрямую, без добавления дополнительных реагентов, т.к. является водорастворимым. Несвязанный (жирорастворимый) билирубин требует добавочных реактивов, реагирует не прямо.
Превращение в кишечнике
В кишечнике билирубин подвергается восстановлению под действием микрофлоры до мезобилирубина и мезобилиногена (уробилиногена). Часть уробилиногена всасывается и с кровью портальной вены попадает в печень, где либо распадается до моно-, ди- и трипирролов, либо окисляется до билирубина и снова экскретируется. При этом при здоровой печени в общий круг кровообращения и в мочу мезобилирубин и уробилиноген не попадают, а полностью задерживаются гепатоцитами.
Оставшаяся в кишечнике часть пигментов ферментами бактериальной флоры толстого кишечника восстанавливается до стеркобилиногена. Далее
- малая часть стеркобилиногена может всасываться и катаболизировать в печени, подобно уробилиногену,
- незначительное количество стеркобилиногена через геморроидальные вены попадает в большой круг кровообращения, отсюда в почки и в мочу. После окисления на воздухе из стеркобилиногена образуется стеркобилин мочи,
- однако основное количество стеркобилиногена достигает нижних отделов толстого кишечника и выделяется. В прямой кишке и на воздухе стеркобилиноген окисляется в стеркобилин, окрашивая кал,
- аналогично уробилиноген, появляющийся в моче при патологии печени, окисляется в уробилин.
Очень часто стеркобилиноген, содержащийся в нормальной моче, называют уробилиногеном. И в клинической практике обычно не проводят различий между стеркобилиногеном и уробилиногеном мочи, их рассматривают как один пигмент – урохромы (уробилиноиды), что может создавать некоторую путаницу при оценке результатов анализа.
РАЗДЕЛ 13. МЕТАБОЛИЗМ ГЕМА И ОБМЕН ЖЕЛЕЗА
III. Катаболизм гемоглобина
Эритроциты имеют короткое время жизни (примерно 120 дней). При физиологических условиях в организме взрослого человека разрушается около 1 — 2 x 1011 эритроцитов в сутки. Их катаболизм происходит главным образом в ретикулоэндотелиальных клетках селезёнки, лимфатических; узлов, костного мозга и печени. При старении эритроцитов снижается содержание сиаловых кислот в составе гликопротеинов плазматической мембраны. Изменённые углеводные компоненты гликопротеинов мембран эритроцитов связываются рецепторами клеток РЭС, и эритроциты «погружаются» в них эндоцитозом. Распад эритроцитов в этих клетках начинается с распада гемоглобина на гем и глобин и последующего гидролиза ферментами лизосом белковой части гемоглобина.
А. Катаболизм гема
Первая реакция катаболизма гема происходит при участии NADPH-зaвиcимoгo ферментативного комплекса гемоксигеназы. Ферментная система локализована в мембране ЭР, в области электронтранспортных цепей микросомального окисления. Фермент катализирует расщепление связи между двумя пиррольными кольцами, содержащих винильные остатки, — таким образом, раскрывается структура кольца (рис. 13-11). В ходе реакции образуются линейный тетрапиррол — биливердин (пигмент жёлтого цвета) и монооксид углерода (СО), который получается из углерода метениловой группы. Гем индуцирует транскрипцию гена гемоксигеназы, абсолютно специфичной по отношению к гему.
Рис. 13-11. Распад гема. М — (-СН3) — метильная группа; В — (-СН = СН2) — винильная группа; П — (-СН2-СН2-СООН) — остаток пропионовой кислоты. В ходе реакции одна метильная группа превращается в окись углерода и, таким образом, раскрывается структура кольца. Образованный биливердин под действием биливердинредуктазы превращается в билирубин.
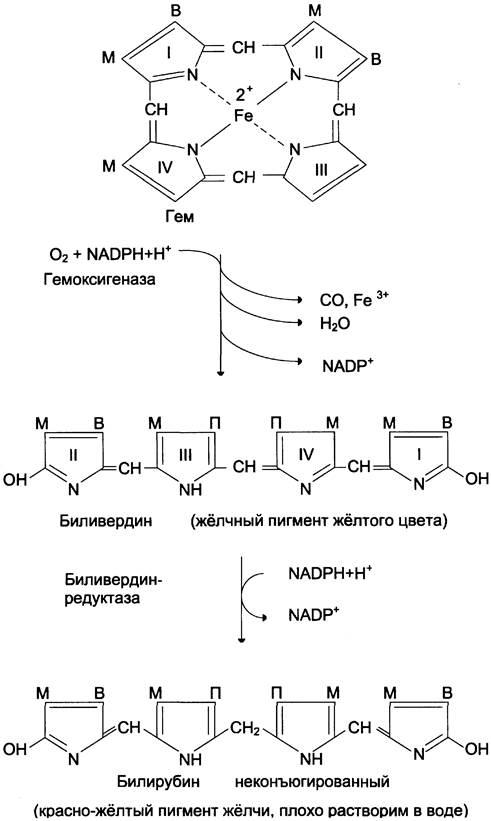
Ионы железа, освободившиеся при распаде гема, могут быть использованы для синтеза новых молекул гемоглобина или для синтеза других железосодержащих белков. Биливердин восстанавливается до билирубина NADPH-зависимым ферментом биливердинредуктазой. Билирубин образуется не только при распаде гемоглобина, но также при катаболизме других гемсодержащих белков, таких как цитохромы и миоглобин. При распаде 1 г гемоглобина образуется 35 мг билирубина, а в сутки у взрослого человека — примерно 250 — 350 мг билирубина. Дальнейший метаболизм билирубина происходит в печени.
Б. Метаболизм билирубина
Билирубин, образованный в клетках РЭС (селезёнки и костного мозга), плохо растворим в воде, по крови транспортируется в комплексе с белком плазмы крови альбумином. Эту форму билирубина называют неконъюгированным билирубином. Каждая молекула альбумина связывает 2 (или даже 3) молекулы билирубина, одна из которых связана с белком более прочно (более высокое сродство), чем другие. При сдвиге pH крови в кислую сторону (повышение концентрации кетоновых тел, лактата) изменяются заряд, конформация альбумина, снижается сродство к билирубину. Поэтому билирубин, связанный с альбумином непрочно, может вытесняться из центров связывания и образовывать комплексы с коллагеном межклеточного матрикса и липидами мембран. Ряд лекарственных соединений конкурирует с билирубином за высокоаффинный, имеющий высокое сродство центр альбумина.
Поглощение билирубина паренхиматозными клетками печени
Комплекс «альбумин — билирубин», доставляемый с током крови в печень, на поверхности плазматической мембраны гепатоцита диссоциирует. Высвобожденный билирубин образует временный комплекс с липидами плазматической мембраны. Облегчённая диффузия билирубина в гепатоциты осуществляется двумя типами белков-переносчиков: лигандина (он транспортирует основное количество билирубина) и протеина Z. Активность поглощения билирубина гепатоцитом зависит от скорости его метаболизма в клетке.
Лигандин и протеин Z обнаружены также в клетках почек и кишечника, поэтому при недостаточности функции печени они способны компенсировать ослабление процессов детоксикации в этом органе.
Конъюгация билирубина в гладком ЭР
В гладком ЭР гепатоцитов к билирубину присоединяются (реакция конъюгации) полярные группы, главным образом от глюкуроновой кислоты. Билирубин имеет 2 карбоксильные группы, поэтому может соединяться с 2 молекулами глюкуроновой кислоты, образуя хорошо растворимый в воде конъюгат — диглюкуронид билирубина (конъюгированный, или прямой, билирубин) (рис. 13-12).
Рис. 13-12. Структура билирубиндиглюкуронида (конъюгированный, «прямой» билирубин). Глюкуроновая кислота присоединяется эфирной связью к двум остаткам пропионовой кислоты с образованием ацилглюкуронида.
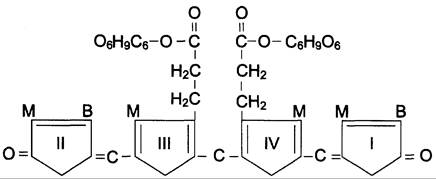
Донором глюкуроновой кислоты служит УДФ- глюкуронат. Специфические ферменты, УДФ-глюкуронилтрансферазы (уридиндифосфоглюкуронилтрансферазы) катализируют образование моно- и диглюкуронидов билирубина (рис. 13-13). Индукторами синтеза УДФ-глюкуронилтрансфераз служат некоторые лекарственные препараты, например, фенобарбитал (см. раздел 12).
Рис. 13-13. Образование билирубиндиглюкуронида.
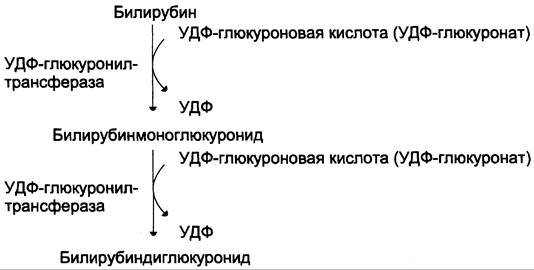
Секреция билирубина в жёлчь
Секреция конъюгированного билирубина в жёлчь идёт по механизму активного транспорта, т. е. против градиента концентрации. Активный транспорт является, вероятно, скорость-лимитирующей стадией всего процесса метаболизма билирубина в печени. В норме диглюкуронид билирубина — главная форма экскреции билирубина в жёлчь, однако не исключается присутствие небольшого количества моноглюкуронида. Транспорт конъюгированного билирубина из печени в жёлчь активируется теми же лекарствами, которые способны индуцировать конъюгацию билирубина. Таким образом, можно сказать, что скорость конъюгации билирубина и активный транспорт би- лирубинглюкуронида из гепатоцитов в жёлчь строго взаимосвязаны (рис. 13-14).
Рис. 13-14. Билирубин-уробилиногеновый цикл в печени. 1 — катаболизм Нb в ретикулоэндотелиальных клетках костного мозга, селезёнки, лимфатических узлов; 2 — образование транспортной формы комплекса билирубин-альбумин; 3 — поступление билирубина в печень; 4 — образование билирубинглюкуронидов; 5 — секреция билирубина в составе жёлчи в кишечник; 6 — катаболизм билирубина под действием кишечных бактерий; 7 — удаление уробилиногенов с фекалиями; 8 — всасывание уробилиногенов в кровь; 9 — усвоение уробилиногенов печенью; 10 — поступление части уробилиногенов в кровь и выделение почками с мочой; 11 — небольшая часть уробилиногенов секретируется в жёлчь.
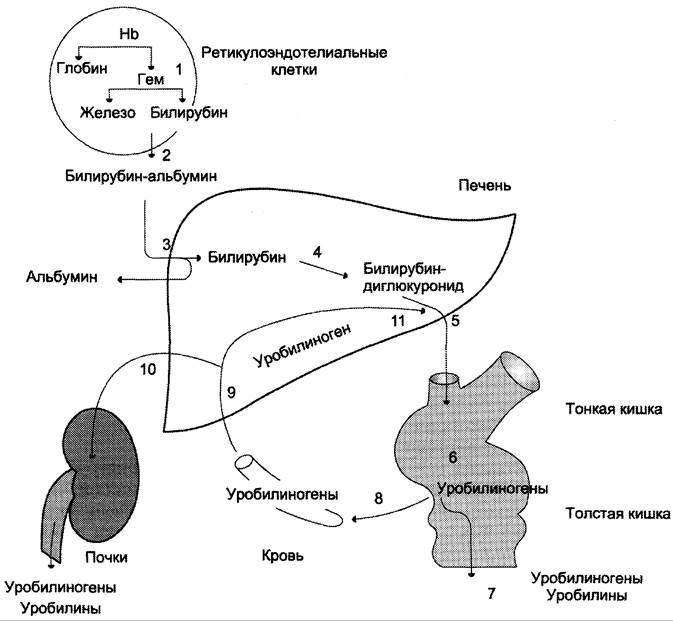
В. Катаболизм билирубиндиглюкуронида
В кишечнике поступившие билирубинглюкурониды гидролизуются специфическими бактериальными ферментами р-глюкуронидазами, которые гидролизуют связь между билирубином и остатком глюкуроновой кислоты. Освободившийся в ходе этой реакции билирубин под действием кишечной микрофлоры восстанавливается с образованием группы бесцветных тетрапиррольных соединений — уробилиногенов (рис. 13-15).
Рис. 13-15. Структура некоторых жёлчных пигментов. Мезобилиноген — промежуточный продукт катаболизма билирубина в кишечнике.
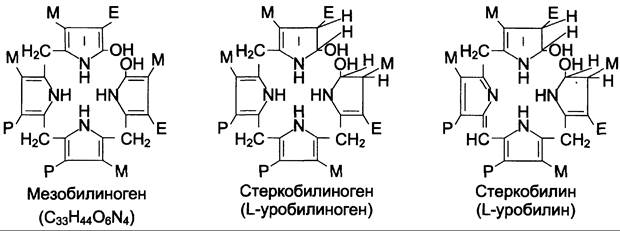
В подвздошной и толстой кишках небольшая часть уробилиногенов снова всасывается, попадает с кровью воротной вены в печень. Основная часть уробилиногена из печени в составе жёлчи выводится в кишечник и выделяется с фекалиями из организма, часть уробилиногена из печени поступает в кровь и удаляется с мочой в форме уробилина (рис. 13-14). В норме большая часть бесцветных уробилиногенов, образующихся в толстой кишке, под действием кишечной микрофлоры окисляется в прямой кишке до пигмента коричневого цвета уробилина и удаляется с фекалиями. Цвет фекалий обусловлен присутствием уробилина.
