Перенос кислорода гемоглобином от легких к тканям
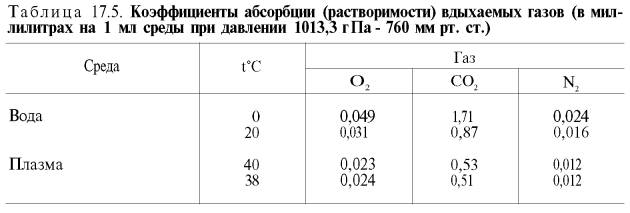
Сущность дыхательной функции крови состоит в доставке кислорода от легких к тканям и
углекислого газа от тканей к легким (табл. 17.4).
Кровь
осуществляет дыхательную функцию прежде всего благодаря наличию в ней
гемоглобина. Физиологическая функция гемоглобина как переносчика кислорода
основана на способности обратимо связывать кислород. Поэтому в легочных
капиллярах происходит насыщение крови кислородом, а в тканевых капиллярах, где
парциальное давление кислорода резко снижено, осуществляется отдача кислорода
тканям.
В состоянии
покоя ткани и органы человека потребляют около 200 мл кислорода в минуту. При
тяжелой физической работе количество потребляемого тканями кислорода возрастает
в 10 раз и более (до 2–3 л/мин). Доставка от легких к тканям такого количества
кислорода в виде газа, физически растворенного в плазме, невозможна вследствие
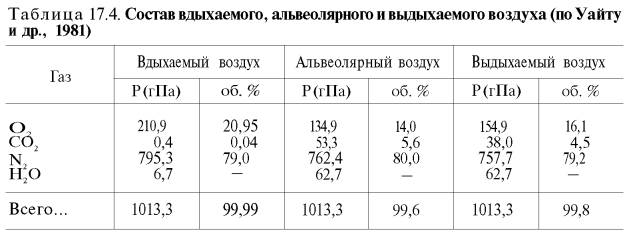
малой растворимости кислорода в воде и плазме крови (табл. 17.5).

Исходя из
приведенных в табл. 17.5 данных, а также зная РO2 в артериальной
крови – 107–120 гПа (80–90 мм рт. ст.), нетрудно видеть, что количество
физически растворенного кислорода в плазме крови не может превышать 0,3 об. %.
При расчете кислородной емкости крови этой величиной можно пренебречь.
Итак, функцию
переносчика кислорода в организме выполняет гемоглобин. Напомним, что молекула
гемоглобина построена из 4 субъединиц (полипептидных цепей), каждая из которых
связана с гемом (см. главу 2). Следовательно, молекула гемоглобина имеет 4
гема, к которым может присоединяться кислород, при этом гемоглобин переходит в
оксигемо-глобин.
Гемоглобин
человека содержит 0,335% железа. Каждый грамм-атом железа (55,84 г) в составе
гемоглобина при полном насыщении кислородом связывает 1 грамм-молекулу
кислорода (22400 мл). Таким образом, 100 г гемоглобина могут связывать

В венозной
крови в состоянии покоя РО2 = 53,3 гПа, и в этих условиях гемоглобин
насыщен кислородом лишь на 70–72%, т.е. содержание кислорода в 100 мл венозной
крови не превышает
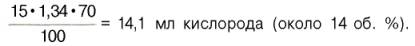
Артериовенозная
разница по кислороду будет около 6 об. %. Таким образом, за 1 мин ткани в
состоянии покоя получают 200–240 мл кислорода (при условии, что минутный объем
сердца в покое составляет 4 л).
Возрастание
интенсивности окислительных процессов в тканях, например при усиленной мышечной
работе всегда связано с более полным извлечением кислорода из крови. Кроме
того, при физической работе резко увеличивается скорость кровотока. Зависимость
между степенью насыщения гемоглобина кислородом и РО2, можно
выразить в виде кривой насыщения гемоглобина кислородом, или кривой диссоциации
оксигемоглобина, которая имеет S-образную форму и характеризует сродство
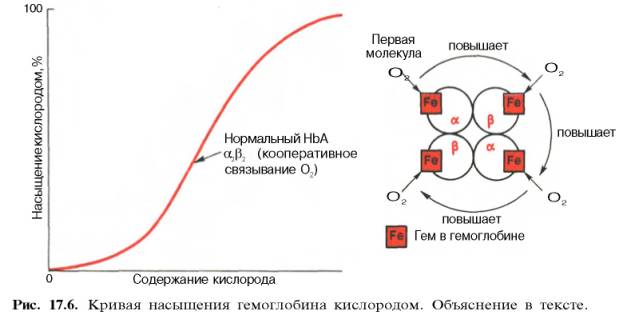
гемоглобина к кислороду (рис. 17.6).
Характерная
для гемоглобина S-образная кривая насыщения кислородом свидетельствует, что
связывание первой молекулы кислорода одним из
гемов
гемоглобина облегчает связывание последующих молекул кислорода тремя другими
оставшимися гемами. Долгое время механизм, лежащий в основе этого эффекта,
оставался загадкой, так как, по данным рентгено-структурного анализа, 4 гема в
молекуле гемоглобина довольно далеко отстоят друг от друга и вряд ли могут
оказывать взаимное влияние. В последнее время принято следующее объяснение
происхождения S-образ-ной кривой. Считают, что тетрамерная молекула гемоглобина
способна обратимо распадаться на две половинки, каждая из которых содержит одну
α-цепь и одну β-цепь:
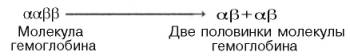
При
взаимодействии молекулы кислорода с одним из четырех гемов гемоглобина кислород
присоединяется к одной из половинок молекулы гемоглобина (допустим, к
α-цепи этой половинки). Как только такое присоединение произойдет,
α-полипептидная цепь претерпевает конформа-ционные изменения, которые
передаются на тесно связанную с ней β-цепь; последняя также подвергается
конформационным сдвигам. β-Цепь присоединяет кислород, имея уже большее
сродство к нему. Таким путем связывание одной молекулы кислорода
благоприятствует связыванию второй молекулы (так называемое кооперативное
взаимодействие).
После насыщения
кислородом одной половины молекулы гемоглобина возникает новое, внутреннее,
напряженное состояние молекулы гемоглобина, которое вынуждает и вторую половину
гемоглобина изменить конфор-мацию. Теперь еще две молекулы кислорода,
по-видимому, по очереди связываются со второй половинкой молекулы
гемоглобина, образуя оксигемоглобин.
S-образная
форма кривой насыщения гемоглобина кислородом имеет большое физиологическое
значение. При такой форме кривой обеспечивается возможность насыщения крови
кислородом при изменении РО2 в довольно широких пределах. Например,
дыхательная функция крови существенно не нарушается при снижении РО2
в альвеолярном воздухе со 133,3 до 80–93,3 гПа. Поэтому подъем на высоту до
3,0–3,5 км над уровнем моря не сопровождается развитием выраженной гипоксемии.
Численно
сродство гемоглобина к кислороду принято выражать величиной Р50 –
парциальное напряжение кислорода, при котором 50% гемоглобина связано с
кислородом (рН 7,4 температура 37°С). Нормальная величина Р50 около
34,67 гПа (см. рис. 17.6). Смещение кривой насыщения гемоглобина кислородом
вправо означает уменьшение способности гемоглобина связывать кислород и,
следовательно, сопровождается повышением Р50. Напротив, смещение
кривой влево свидетельствует о повышенном сродстве гемоглобина к кислороду,
величина Р50 снижена.
Ход кривой
насыщения гемоглобина кислородом или диссоциации оксигемоглобина зависит от
ряда факторов. Сродство гемоглобина к кислороду в первую очередь связано с рН.
Чем ниже рН, тем меньше способность гемоглобина связывать кислород и тем выше Р50.
В тканевых капиллярах рН ниже (поступает большое количество СО2), в
связи с чем гемоглобин легко отдает
кислород. В легких СО2 выделяется, рН повышается и гемоглобин
активно присоединяет кислород.
Способность
гемоглобина связывать кислород зависит также от температуры. Чем выше
температура (в тканях температура выше, чем в легких), тем меньше сродство
гемоглобина к кислороду. Напротив, снижение температуры вызывает обратные
явления.
Количество
гемоглобина в крови, а также в какой-то мере его способность связывать кислород
(характер кривой диссоциации оксигемоглобина) несколько меняются с возрастом.
Например, у новорожденных содержание гемоглобина доходит до 20–21% (вместо
обычных для взрослого 13–16%). У человека имеется несколько гемоглобинов,
которые образуются в различном количестве в разные стадии онтогенеза и
различаются по своему сродству к кислороду.
Рассмотрим
нарушения дыхательной функции крови при некоторых патологических состояниях.
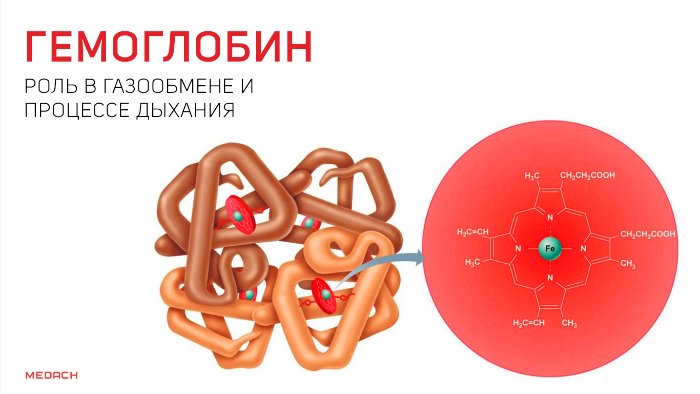
Одним из самых сложных процессов, что происходят в организме человека, несомненно, является дыхание. И сложность эта не только в танце легких, благодаря которому человек получает кислород, но и в процессах, с помощью которых этот кислород проникает дальше, в ткани, где превращается в углекислый газ, что отправляется в обратное путешествие. О данных процессах и пойдет речь далее.
Итак, приступим. Человек делает вдох, иии… Далеко не весь кислород поступает в легкие, а затем и в кровь. Часть вдыхаемого воздуха остается в так называемом мертвом пространстве. Мертвое пространство, в свою очередь, делится на анатомическое (дыхательные пути), в котором остается около 30 % вдыхаемого воздуха, и функциональное (вентилируемые, но по каким-то причинам не перфузируемые альвеолы).
Ухудшение альвеолярного газообмена может происходить при неглубоком и частом дыхании (причиной может стать перелом ребер, паралич дыхательной мускулатуры различного генеза и др.), а также при увеличении мертвого пространства, вызванном разнообразными причинами (нарушение перфузии альвеол в результате воспалительных заболеваний легких, удаление доли или целого легкого и др.), при снижении скорости кровотока по альвеолярным капиллярам (ТЭЛА, инфаркт легкого), при наличии диффузионного барьера (отек легких) и в результате ослабления альвеолярной вентиляции при обтурации просвета бронха. Газообмен между легкими и кровью происходит путем диффузии в соответствии с законом Фика. В легочных капиллярах она происходит за счет разности парциальных давлений в альвеолах и эритроцитах.
В альвеолах парциальное давление кислорода значительно превышает таковое для углекислого газа и составляет примерно 13,3 кПа (100 мм рт. ст.) и 5,3 кПа (40 мм рт. ст.) соответственно. Альвеолы омываются приносимой легочными артериями венозной кровью, в которой соотношение парциальных давлений этих двух газов обратно пропорционально и составляет приблизительно 5,3 кПа (40 мм рт. ст.) для кислорода и 6,1 кПа (46 мм рт. ст.) для углекислого газа. В среднем разница парциальных давлений составляет около 8 кПа (60 мм рт. ст.) для кислорода и около 0,8 кПа для углекислого газа.
Как уже было сказано выше, кислород путем диффузии проникает в кровь легочных капилляров. Диффузионное расстояние для кислорода при этом составляет 1–2 мкм, то есть именно на такое расстояние он проникает внутрь капилляра. Обмен крови в легочном капилляре происходит примерно за 0,75 секунды, но этого времени хватает на то, чтобы парциальные давления в альвеолах и в крови пришли в равновесие.
Кровь, в которой показатели парциального давления для кислорода и углекислого газа примерно равны таковым в альвеолах, называется артериализированной. Однако за счет наличия в легких артериовенозных шунтов и притока венозной крови из бронхиальных вен такой она остается недолго. В результате парциальное давление кислорода в аорте составляет примерно 12,0 кПа (как уже было сказано выше, парциальное давление в артериализированной крови равно таковому в альвеолах и составляет 13,3 кПа), а давление углекислого газа меняется незначительно и не приводит к затруднению его диффузии из крови в альвеолы.
Но кислород непосредственно в ткани попадает лишь в крайне незначительных количествах: для свободного перемещения по организму ему необходим транспортер. Эту функцию выполняет содержащийся в эритроцитах белок — гемоглобин. Гемоглобин существует в оксигенированной и неоксигенированной формах. В дезокси-гемоглобине железо находится на уровне порфиринового кольца и стабилизируется электростатическими силами, что обеспечивает поддержание всей структуры. Появившись, кислород начинает «тянуть» за железо, которое переносится на проксимальный гистидин на другом конце полипептидной цепи и меняет структуру всего протеина.
В результате гемоглобин переходит в оксигенированную форму, альфа- и бета-цепи при этом поворачиваются относительно друг друга на 15 градусов, облегчая присоединение остальных молекул кислорода. В итоге каждый из четырех содержащихся в нем атомов двухвалентного железа обратимо связывается с молекулой кислорода, что превращает молекулу гемоглобина в оксигемоглобин. По сравнению с миоглобином гемоглобин имеет низкое сродство к кислороду, однако оно не статично. Так, миоглобин может связывать кислород только одним участком, поэтому кривая его связывания — гипербола. Кривая связывания гемоглобина с кислородом имеет S-образную форму, демонстрируя, что при его связывании с первой молекулой кислорода гемоглобин имеет очень низкое сродство к кислороду, но при связывании последующих молекул кислорода сродство остальных его субъединиц к нему значительно увеличивается и в конечном счете повышается примерно в 500 раз.
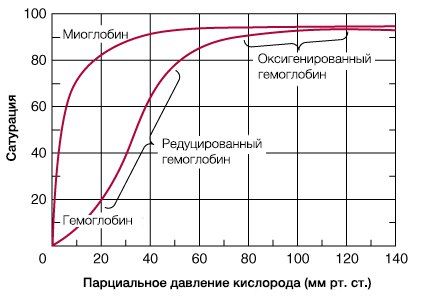
При этом альфа-цепи связывают кислород легче, чем бета-цепи. Этот процесс назван кооперативным взаимодействием. По мере снижения парциального давления кислорода в крови происходит его высвобождение из гемоглобина и поступление в ткани. Например, парциальное давление кислорода в работающих мышцах составляет всего 26 мм рт. ст, и при прохождении эритроцитов через капилляры, кровоснабжающие мышцы, происходит высвобождение и поступление в мышечные клетки примерно ⅓ всего переносимого гемоглобином кислорода. При повышении температуры тела также возрастает потребность в кислороде, что, в свою очередь, стимулирует высвобождение и поступление его в ткани. При снижении температуры, напротив, развивается гипоксия тканей, способствующая компенсаторному увеличению сродства гемоглобина к кислороду.
Гемоглобин также осуществляет перенос от тканей к легким продуктов тканевого дыхания — углекислого газа и ионов водорода. В ходе окислительных процессов в клетке выделяется углекислый газ, в результате гидратации которого образуются ионы водорода, что, в свою очередь, приводит к снижению рН. Давно известно, что снижение рН и повышение концентрации углекислого газа в крови оказывает сильное влияние на способность гемоглобина связывать кислород.
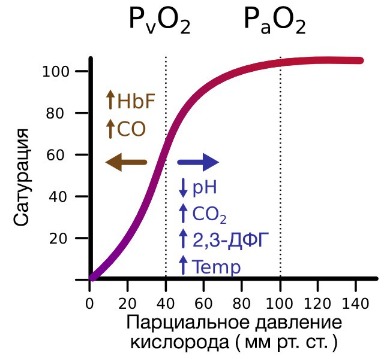
В периферических сосудах показатели рН низкие, и по мере связывания гемоглобина с ионами водорода и углекислым газом происходит снижение его сродства к кислороду. Это влияние величины рН и концентрации углекислого газа на способность гемоглобина связывать кислород называют эффектом Бора.
Обратная ситуация имеет место в альвеолярных капиллярах, где присоединение кислорода к гемоглобину превращает тот в более сильную кислоту.
При этом сродство гемоглобина к углекислому газу снижается, а повышение кислотности гемоглобина приводит к высвобождению излишка ионов водорода и образованию в крови из бикарбоната угольной кислоты, которая затем распадается на воду и углекислый газ. В обоих случаях углекислый газ из крови поступает в альвеолы, а затем в атмосферу. Данный процесс назван эффектом Холдейна. Стоит отметить, что важную роль в образовании углекислого газа в эритроцитах играет ион хлора, поступающий в плазму крови в обмен на бикарбонат при участии белка-переносчика АЕ1. Данный процесс в англоязычной литературе получил название «Chloride shift» или «перенос Хамбургера».
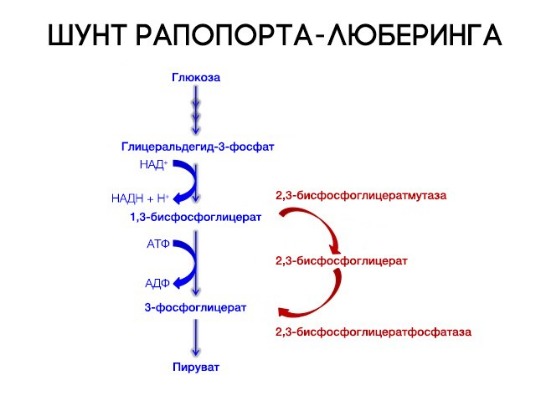
На сродство гемоглобина к кислороду оказывает влияние и присутствующее в эритроцитах вещество, получившее название 2,3-бисфосфоглицерат (БФГ). Его образование — своего рода побочная реакция анаэробного гликолиза, происходящего в эритроцитах в ходе ферментативного превращения глюкозы в пируват под действием фермента бифосфоглицератмутазы. БФГ способен самостоятельно связываться с неоксигенированной формой гемоглобина, образуя солевой мостик между двумя его бета-субъединицами и снижая сродство к кислороду.
При этом гемоглобин способен связать только одну молекулу БФГ, а при присоединении кислорода БФГ вытесняется из полости. В обычных условиях в эритроцитах крови содержится достаточно большое количество БФГ, которое может увеличиваться в условиях гипоксии (например, у дайверов при погружении на глубину), а также при восхождении на большую высоту. В первые часы подъема концентрация БФГ в эритроцитах будет возрастать, а сродство кислороду снижаться. Но на большой высоте парциальное давление будет значительно ниже такового на уровне моря, а значит, оно снизится и в тканях. При этом БФГ будет облегчать передачу кислорода от гемоглобина к тканям.
Некоторые вещества способны прочно связываться с гемоглобином или же вовсе менять его структуру. Одним из них является угарный газ, чье сродство к гемоглобину в 200 раз превышает таковое для кислорода. Отравления угарным газом часто происходят в помещениях с печным отоплением, при пожарах и авариях на производстве. Со временем кислород вытесняет угарный газ из гемоглобина, и в легких случаях пациенты помещаются под наблюдение и получают ингаляции с увлажненным кислородом. Необходимой мерой при тяжелых отравлениях угарным газом является переливание эритроцитарной массы.
К веществам, способным изменять структуру гемоглобина, относятся метгемоглобинобразователи — соединения, способные окислять двухвалентное железо в геме до трехвалентного. К ним относятся нитриты, нитраты, некоторые местные анестетики, аминофенолы, хлораты, примахин и некоторые сульфаниламиды. Состояние, характеризующееся появлением в крови окисленного гемоглобина, называют метгемоглобинемией. При высокой метгемоглобинемии капля крови, помещенная на фильтровальную бумагу, имеет характерный коричневый цвет, а при пропускании кислорода через пробирку с такой кровью ее цвет не меняется. Метгемоглобинемия выше 70 % от общего содержания гемоглобина часто приводит к гибели пациента еще до момента постановки диагноза.
Источники:
- Harrison’s hematology and oncology Longo, Dan L (Dan Louis), Third edition. New York : McGraw-Hill Education Medical, 2017.
- Наглядная физиология, С. Зильбернагль, А. Деспопулос, 2013.
- Ленинджер А. Основы биохимии: В 3-х т. Т. 1. /Д. Нельсон, М. Кокс ; Пер. с англ.-М.: БИНОМ: Лаборатория знаний, 2011.- 694 с.
Основная функция гемоглобина – транспорт кислорода, которую онвыполняет очень эффективно. Гемоглобин артериальной крови насыщен кислородом приблизительно на 96%, гемоглобин венозной крови – на 64% (White А. et al, 1981).
Уменьшение степени насыщения на 32 % соответствует количеству О2, потребляемому тканями. Принимая, что 100 мл крови содержат 15,0 г гемоглобина и что каждый грамм гемоглобина может связать 1,34 мл О2 (число Хюфнера) находим, что:
0,96 х 1,34 х 15 = 19,2 мл О2 –
транспортируется 100 мл артериальной крови (19,2 объемных %);
0,64 х 1,34 х 15 = 12,8 мл О2 –
транспортируется 100 мл венозной крови (12,8 объемных %);
19,2 – 12,8 = 6,4 мл О2 (6,4% объемных %)
или
0,32 х 1,34 х 15 = 6,4 мл О2 (6,4 % объемных %)
отдается тканям каждыми 100 мл артериальной крови, протекающими через капилляры.
Поскольку минутный объем крови (МОК) равен 5 литрам, в сутках 1440 минут, определяем, что в течение суток общий объем перекачиваемой сердцем крови составит:
5 х 1440 = 7200 литров
А так как один литр артериальной крови способен транспортировать 19,2 объемных % кислорода, из которых 6,4 объемных процента потребляются тканями, находим:
7200 х 19,2
———————– = 1382 литра – количество кислорода, транспортируемое
100 за сутки артериальной кровью
7200 х 6,4
———————– = 461 литр – количество кислорода, потребляемое тканями
100 за сутки из артериальной крови
В целом, за сутки кровь переносит от легких к тканям около 1400 л кислорода, из которых 450-600 л потребляются тканями. Причем, практически весь перенос кислорода обеспечивается гемоглобином, т.к. кислород плохо растворим в водных растворах. Ограниченная растворимость кислорода позволяет транспортировать его в растворенном состоянии в количестве, составляющем всего 0,3 мл О2 / 100 мл крови (White А. еt al, 1981) при РаО2 равном 12,7 кПа (95 мм рт ст). Это соотношение вытекает из закона Генри-Дальтона, в соответствии с которым «количество растворенного в жидкости газа пропорционально его напряжению». Важно отметить, что несмотря на малое количество растворенного кислорода, именно эта его фракция обусловливает РаО2.
Гемоглобин растворен в водном цитозоле эритроцитов в очень высокой концентрации, порядка 34%. Его синтез осуществляется в процессе созревания ретикулоцитов и перехода их в эритроциты. Гемоглобин состоит из белка – глобина и простетической группы – гема. Гем представляет собой соединение, в молекулу которого входят атом двухвалентного железа и 4 замещенных пиррольных кольца, связанных между собой метиновыми группами ( – СН = ). Скелетом молекулы гема служит порфирин. Fe2+ имеет в геме координационное число, равное 6, т.е. 6 пар электронов. Четыре из этих пар связаны с атомами азота, одна пара с белком (глобином) через гистидин. Оставшаяся пара электронов используется для образования донорско-акцепторной координационной связи (ковалентной химической связи) с кислородом (рис. 12).
Функциональные свойства гемоглобина, обусловленные его уникальной структурой, специфически соответствуют задачам обеспечения дыхательной функции. Каждая из четырех полипептидных цепей глобина содержит по одной молекуле гема. А поскольку атом железа в геме может обратимо связывать одну молекулу О2 понятно, что одна молекула полностью оксигенированного гемоглобина (НbО2) содержит четыре молекулы кислорода.Гемоглобин, отдавший кислород тканям, называется свободным (неоксигенированным) гемоглобином.
Рис. 12.Координационные связи железа в молекуле гема
(по A. Ленинджеру, 1985)
В процессе присоединения и отдачи кислорода железо в молекуле гемоглобина свою валентность не меняет, т.е. при присоединении кислорода или при его отдаче железо не окисляется и не восстанавливается. Следовательно, в этих случаях речь идет об оксигенированном (оксигемоглобин) и неоксигенированном (свободном) гемоглобине, но не об окисленном и восстановленном гемоглобине.
Окисленный гемоглобин – это метгемоглобин (MetHb), содержащий Fe3+. Он не способен присоединять кислород, однако Fe3+ в MetHb может взаимодействовать со многими анионами, например, при щелочном рН с ОН- и при кислом рН – с Cl-. В небольшом количестве, составляющем 0, 5% от всего гемоглобина, метгемоглобин образуется ежесуточно в условиях in vivo (White A. et al, 1981).
Кроме кислорода к атому железа в молекуле гемоглобина могут присоединяться и другие вещества (лиганды) : Н2О; СО; СN. Их сродство, проявляемое к атому железа, неодинаково. Оно наиболее выражено у цианидов, затем у окиси углерода, затем у кислорода и наименее выражено у воды.
Степень насыщения гемоглобина кислородом зависит от парциального давления кислорода (РО2). Это давление в легких ( 100 мм рт.столба) достаточно, чтобы практически полностью оксигенировать весь гемоглобин в эритроцитах. Уникальной особенностью связывания гемоглобином О2 является кооперативное взаимодействие между гемсвязывающими участками, получившее название гем-гем – взаимодействие. И хотя прямых физических контактов между четырьмя группами гема нет, кооперативность связывания О2 проявляется в том, что по мере протекания оксигенирования гемоглобина облегчается связывание последующих молекул кислорода. При физиологических условиях сродство к О2 у гемоглобина и у полностью оксигенированного гемоглобина отличается в 500 раз (A. White et al, 1981); это показывает, что после присоединения первых молекул О2 сродство частично насыщенного гемоглобина к кислороду увеличивается.Данное положение характеризуетсясигмовидной формой кривой диссоциации HbO2 (рис. 5).Такая формауказывает на то, что связывание О2 одной из гемовых групп гемоглобина влияет на константы диссоциации других гемовых групп этой же молекулы. Сигмовидный характер кривой диссоциации НbО2 имеет большое физиологическое значение. Как видно из рис. 5 парциальное давление О2 существенно влияет на насыщение гемоглобина в пределах от 20 до 60 мм рт. ст., когда показатель насыщения кислородом характеризуется наиболее крутым подъемом отрезка кривой. При больших значениях РО2 кривая насыщения приобретает пологий характер, увеличиваясь в диапазоне 60-90 мм рт. ст. всего на 7%.
Связывание гемоглобином кислорода зависит не только от РО2. Этот процесс тонко регулируется рядом соединений, подобно тому как это имеет место при действии на аллостерический фермент.Таким регуляторным действием обладают 2,3 – дифосфоглицерат, диоксид углерода (СО2) и ионы Н+.
Главной фракцией фосфатов в эритроцитах является 2,3 – дифосфоглицерат (ДФГ); его внутриклеточная концентрация составляет приблизительно 4-5 – ммоль, т.е. сопоставима с концентрацией гемоглобина. Дифосфоглицерат (ДФГ) связывается с тетрамерным гемоглобином при нейтральном рН, образуя комплекс с соотношением компонентов 1 : 1. Связывание с гемоглобином ДФГ обусловлено наличием в молекуле последнего отрицательно заряженных групп (рис. 13):
-О О
С
Н С О Р О-
Н С Н
О
О Р О
О-
Рис. 13. Структура молекулы ДФГ(по А. Ленинджеру, 1985).
Жирным выделены группы, взаимодействующие с β-цепями
Местом связывания служит центральная полость или канал в молекуле гемоглобина, выстланный многочисленными положительно заряженными R-группами β-цепей. В итоге образуется поперечная связь между двумя β-субъединицами. При связывании гемоглобина кислородом ДФГ вытесняется из этого канала.
Главным результатом образования комплекса ДФГ-гемоглобин является снижение сродства гемоглобина к кислороду:
НbO2 + ДФГ Нb • ДФГ + О2
Регулирующее влияние ДФГ на сродство гемоглобина к кислороду в эритроцитах зависит от величины парциального давления кислорода в легких. Чем ниже это давление (при подъеме на высоту), тем выше концентрация ДФГ в эритроцитах, тем легче будет освобождаться кислород от связи с гемоглобином в тканях.
Таким образом, при фиксированной концентрации оксигенированного гемоглобина, увеличение концентрации ДФГ повышает диссоциацию НbO2. При увеличении же РО2 и росте концентрации НbО2 будет усиливаться диссоциация комплекса Нb ДФГ.
Повышенное сродство крови плода к кислороду не является следствием различий сродства фетального (НbF) и постнатального (НbA) гемоглобинов к О2, поскольку кривые диссоциации изолированных НbАО2 и НbFO2 существенно не отличаются. Этот феномен повышенного сродства к кислороду крови плода является результатом менее эффективного связывания ДФГ фетальным гемоглобином, поскольку на ДФГ – связывающем участке НbF незаряженный Sery γ 143 заменяет His β 143.
В крови, консервированной в некоторых средах (цитрат-декстрозной) концентрация ДФГ снижается (в течение 10 дней с 4,5 до 0,5 мМ). Гемоглобин такой крови приобретает очень высокое сродство к кислороду, в связи с чем увеличивается риск развития гипоксии, обусловленной снижением отдачи им кислорода. Тем более, что восстановление содержания ДФГ самими эритроцитами происходит медленно (за 24 часа – до половины нормальной концентрации). Исправление ситуации путем добавления экзогенного ДФГ не эффективно, поскольку высокий отрицательный заряд его молекулы не позволяет ей проникать через мембрану эритроцитов. В связи с этим используются вещества, добавление которых к консервированной крови обеспечивает поддержание нормальной концентрации ДФГ (Волкова Н.П., 2005).
Способность гемоглобина взаимодействовать с СО2 и ионами Н+ определяется не наличием атома Fe2+ в гемах, а другими участками его молекулы, с которыми происходит связывание этих соединений. В частности, ионы водорода присоединяются к R – группам остатков гистидина в α и β – цепях глобина :
R CH COOH (общая формула аминокислоты)
NH2
R – группа, с которой связывается
ион водорода.
Что касается диоксида углерода, то он присоединяется к концевой α-аминогруппе каждой из четырех полипептидных цепей с образованием карбаминогемоглобина:
O O
R CH C + CO2 R CH C
OH OH
NH2 NHCOO- + H+
карбаминоконцевой остаток
( карбаминогемоглобин )
Важно подчеркнуть, что процессы связывания с гемоглобином О2, Н+ – ионов и СО2 (как и ДФГ) взаимозависимы. Эту взаимозависимость иногда называют кооперативным эффектом гемоглобина, который заключается в том, что изменение концентрации одного из этих веществ влияет на связывание гемоглобина с другими. В частности,связывание с гемоглобином СО2 и ионов водорода снижает его способность связывать кислороди наоборот:связывание с гемоглобином кислорода снижает его способность связывать СО2 и ионы Н+.Поэтому в периферических тканях с относительно низким значением рН и высокой концентрацией СО2 сродство Нb к кислороду падает по мере связывания СО2 и ионов водорода. И наоборот, в легочных капиллярах выделение СО2 и сопутствующее ему повышение рН крови приводят к увеличению сродства гемоглобина к кислороду. Это влияние величины рН и концентрации СО2 на связывание и освобождение кислорода гемоглобином называется эффектом Бора(в честь датского физиолога Христиана Бора, впервые открывшего его).
В основе данного эффекта лежит изменение четвертичной структуры (т.е. упаковки субьединиц молекулы белка) гемоглобина при его оксигенации. В результате молекула оксигенированного гемоглобина приобретает несколько более компактную структуру по сравнению с неоксигенированным. Вследствие этого аминокислотные остатки в α и β – цепях, связывающие ионы водорода, перемещаются из относительно гидрофильного окружения в более гидрофобное, что облегчает отщепление ионов водорода от протонированных групп. Иначе говоря, протонированные группы при оксигенации гемоглобина приобретают свойства более сильных кислот (как донаторов ионов водорода). Т.е. НbО2 более сильная кислота (в 70 раз – Войнов В.А., 1992), чем ННb. Можно сказать и так, что оксигенированный гемоглобин (НbO2) плохо присоединяет протоны, но зато легко их отдает. А неоксигенированный гемоглобин наоборот – плохо отдает протоны, но зато легко их присоединяет (ННb).
В легочной ткани вследствие уменьшения РСО2 и превращения гемоглобина в НbО2 освобождается также СО2, находящийся в виде карбаминогемоглобина..
Повышение или снижение сродства Hb к кислороду проявляется изменением кривой диссоциации оксигемоглобина (рис. 14).
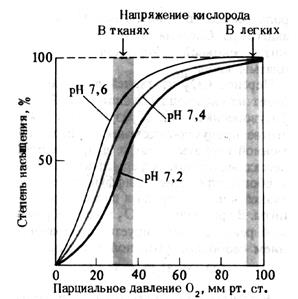
Рис. 14.Кривая диссоциации оксигемоглобина. Влияние рН(по A. Ленинджеру, 1985)
Эти изменения обозначаются понятием «сдвиг вправо» и «сдвиг влево». При сдвиге вправо, как это следует из рисунка, при снижении рН (рН = 7,2), 50% насыщение Hb кислородом, которое в норме происходит при значениях РаО2 ≈ 26,6 мм рт. ст, будет осуществляться уже при больших значениях РаО2, приближающихся к 40 мм рт. ст. Это означает, что сродство Hb к кислороду понизилось. Соответственно, при сдвиге влево (рН = 7,6) 50% насыщение Hb кислородом происходит при меньших, чем при нормальном рН значениях РаО2. Это означает, что сродство Hb к кислороду оказалось повышенным. Помимо кислотно-основного состояния на характер кривой диссоциации оксигемоглобина влияют и другие факторы (табл. 3).
Таблица 3.
