Почему анемия при раке желудка 4 степени

Анемия представляет собой патологическое состояние, для которого характерно снижение эритроцитов и/или концентрации гемоглобина в единице объема крови. Анемия не является самостоятельным заболеванием, это симптом, который характерен для самых разнообразных заболеваний, в том числе и для злокачественных опухолей.
Согласно статистике, данное состояние выявляется у каждого третьего онкологического пациента, а при прохождении химиотерапии — более чем в 90% случаев. Опасность анемии в онкологии заключается в том, что вместе с уменьшением уровня гемоглобина и эритроцитов, уменьшается и кислородная емкость крови. Этот фактор неблагоприятно сказывается на течении ракового процесса, снижает эффективность лечения и ухудшает дальнейший прогноз.
Основные причины развития анемии у онкологических пациентов
Снижение уровня эритроцитов и гемоглобина может развиваться вследствие снижения их образования, ускоренного разрушения или в результате потери. Каждой из этих причин способствуют собственные факторы, которые рассмотрим подробнее:
- Недостаточная выработка форменных элементов крови и гемоглобина может развиваться при поражении костного мозга, недостатке железа в организме или некоторых витаминов (фолиевая кислота, витамин В12). Данные состояния могут быть напрямую связаны с напрямую с онкологическим заболеванием. Например, потеря железа может развиваться в результате постоянной рвоты, отсутствия аппетита и нарушения его всасывания в кишечнике, который поражен опухолевым процессом. Некоторые виды препаратов, которые назначают при злокачественных опухолях, подавляют рост не только раковых клеток, но и клеток крови, которые активно делятся. Также анемия может развиваться при непосредственном поражении костного мозга опухолевым процессом.
- Ускоренное разрушение эритроцитов отмечается при воздействии различных лекарственных препаратов и при аномальной активности иммунной системы. Разрушение эритроцитов непосредственно в сосудах называется внутрисосудистым гемолизом. Этот процесс протекает в норме после завершения жизненного цикла эритроцитов, который составляет 120 дней. Однако при воздействии различных факторов (прием антибиотиков, цитостатиков, присоединение вторичной инфекции и др.), этот срок значительно уменьшается, что и приводит к развитию анемии.
- Кровопотеря у онкологических пациентов может быть как острой, так и хронической. Первый вариант встречается при проведении хирургического лечения рака, а также при развитии внутренних кровотечений, которые являются частым осложнением основного заболевания. Развитие анемии при хронической кровопотере отмечается в тех случаях, когда имеется скрытый источник незначительного кровотечения. Например, при колоректальном раке кровь может выделяться с калом незаметно для пациента.
Установление точной причины анемии играет решающее значение при выборе метода лечения. Кроме того, врач учитывает степень тяжести, тип анемии, общее состояние пациента и другие параметры. Получить эту информацию можно на диагностическом этапе.
Как выявить анемию
Обследование традиционно начинается с опроса пациента и сбора анамнеза. Врач должен помнить, что не всегда анемия развивается вследствие основного заболевания. Возможны наследственные или любые другие причины, которые не связаны с опухолевым процессом. Также необходимо установить вид предшествующего противоопухолевого лечения, продолжительность и количество курсов, наименование препаратов, которые применялись. На следующем этапе врач проводит общий осмотр. Анемия может проявляться бледностью кожных покровов, слабостью, потерей аппетита, головокружением и другими симптомами. Очень часто эти проявления отмечаются при различных видах рака, который протекает без анемии, поэтому поставить диагноз исходя только из жалоб пациента невозможно.
Объективную информацию можно получить только при помощи лабораторных исследований. Анемия диагностируется по следующим анализам:
- Количество ретикулоцитов.
- Уровень железа сыворотки крови.
- Уровень белка трансферрина и ферритина.
- Уровень витамина В12 и фолиевой кислоты.
Отдельное внимание уделяется общему анализу крови. В нем определяется уровень гемоглобина, количество эритроцитов и гематокрит (отношение форменных элементов к жидкой составляющей крови). Также определяют средний объем эритроцита, среднее содержание гемоглобина в эритроците и среднее содержание гемоглобина во всей эритроцитарной массе.
При необходимости в программу комплексного обследования при анемии могут включаться и другие лабораторные анализы или специальные методы.
Как классифицируется анемия
В зависимости от значения цветового показателя, степени тяжести и механизма развития, анемия разделяется на несколько категорий. Цветовой показатель крови отражает степень насыщения эритроцитов гемоглобином. Его значение в норме колеблется от 0,85 до 1,05 единиц. Снижение показателя отмечается при гипохромной анемии, а повышение — при гиперхромной. Если цветовой показатель в норме, но уровень гемоглобина все равно низкий, то говорят о нормохромной анемии.
По степени тяжести, анемия разделяется на три группы, в зависимости от концентрации гемоглобина:
- При легкой степени анемии уровень гемоглобина не опускается ниже отметки в 90 г/л.
- При средней степени анемии показатель колеблется в пределах 90-70 г/л.
- Тяжелая анемия характеризуется падением гемоглобина ниже 70 г/л.
Классификация анемии по механизму развития наиболее обширна. Среди распространенных форм отмечаются:
- Железодефицитная анемия. Развивается в результате нарушения всасывания, усиленной потери или недостаточного поступления железа в организм.
- Гемолитическая анемия. Характеризуется разрушением эритроцитов в сосудистом русле или за его пределами. Наиболее частые причины — недостаточность специфических ферментов, аутоиммунные заболевания, воздействие лекарственных препаратов.
- Постгеморрагическая анемия. Данное состояние характерно для острой или хронической кровопотери
- Апластическая анемия. Характеризуется снижением уровня клеток-предшественников эритроцитов в костном мозге. Обычно отмечается снижение и других форменных элементов — тромбоцитов и лейкоцитов.
- В12-дефицитная анемия. При недостатке витамина В12 нарушается процесс образования эритроцитов, снижается их продолжительность жизни. Дефицит витамина может быть связан как с нарушением его всасывания в кишечнике, так и с недостаточным поступлением в организм.
В большинстве случаев определить точный вид анемии можно после нескольких лабораторных тестов, но иногда приходится применять более сложные методы диагностики, например, генетическое исследование. Понимание механизма развития анемии и получение максимально полной информации об изменениях в показателях крови являются важным компонентом эффективной терапии данного симптома.
Методы лечения анемии
Устранить анемию у онкологических пациентов можно тремя способами: переливание эритроцитарной массы, введение эритропоэтина, назначение препаратов, содержащих железо. В отдельных случаях может применяться комбинация этих методов.
Переливание эритроцитарной массы при анемии
Переливание эритроцитарной массы является самым действенным методом, при помощи которого можно быстро восполнить дефицит эритроцитов, восстановить уровень гемоглобина и гематокрита. Однако без устранения причины анемии, этот способ даст лишь временный эффект. Поэтому переливание эритроцитарной массы не является альтернативой другим методикам и применяется только при наличии показаний. Одним из них является снижение уровня гемоглобина ниже 90 г/л. Переливание проводят при развитии у пациента характерных признаков анемии, среди которых отмечаются:
- Головокружение.
- Потеря сознания.
- Тахикардия.
- Быстрая утомляемость.
- Боль в груди.
- Одышка.
Данный метод лечения анемии также может применяться у пациентов, которые прошли курс химиотерапии или лучевой терапии и у которых отмечается быстрое снижение уровня гемоглобина или эритроцитов.
Применение стимуляторов эритропоэза
Стимуляторы эритропоэза при анемии увеличивают концентрацию гемоглобина и эритроцитов за счет усиления их образования в костном мозге. При сочетании с гемотрансфузиями, данный метод показывает очень хорошие результаты, но при этом имеет и ряд недостатков, которые касаются осложнений. В частности, применение стимуляторов эритропоэза для лечения анемии повышает риск развития тромботических осложнений, который и так является высоким у онкологических пациентов. По данным, полученным в ходе нескольких научных исследований, этот риск увеличивается в 1.4-1.7 раз.
В последнее время обсуждается вопрос о влиянии стимуляторов эритропоэза на выживаемость онкологических пациентов. В частности, специалисты установили, что применение препаратов данной группы при лечении анемии у пациентов с распространенным опухолевым процессом головы и шеи, шейки матки, молочной железы и других диагнозах снижает продолжительность жизни на 10-17%. В связи с этим специалисты предлагают придерживаться следующих правил:
- Если уровень гемоглобина составляет менее 100 г/л и пациент при этом проходит лечение химиопрепаратами, то стимуляторы эритропоэза могут назначаться с целью коррекции анемии и профилактики дальнейшего снижения показателей.
- Если уровень гемоглобина падает до 100 г/л и ниже, но химиотерапия при этом не проводится, то применять стимуляторы эритропоэза не рекомендуется ввиду повышенного риска развития осложнений и снижения продолжительности жизни.
- Во всех остальных случаях применять стимуляторы эритропоэза для лечения анемии у онкологических пациентов следует с осторожностью.
Также на протяжении всего времени лечения важно контролировать динамику лабораторных показателей и при увеличении уровня гемоглобина постепенно снижать дозировку стимуляторов эритропоэза.
Препараты железа при лечении анемии
Препараты железа применяются с целью лечения железодефицитных анемий, которые выявляются у 30-60% онкологический больных. При этом снижение уровня железа может быть связано как с самим опухолевым процессом или проводимым лечением, так и с другими факторами. Например, при назначении стимуляторов эритропоэза, существующего запаса железа в организме становится недостаточно для того, чтобы покрыть потребность, которая возникает в результате активного синтеза гемоглобина в костном мозге.

Для лечения анемии могут применяться как внутривенные, так и пероральные препараты. Второй вариант более удобен для пациента, так как таблетки проще принимать, но при этом данная форма действует медленнее и чаще приводит к осложнениям со стороны ЖКТ. Внутривенное введение позволяет добиться быстрого эффекта, что актуально при проведении химиотерапии.
Таким образом, для лечения анемии современная онкология может предложить различные методы, которые воздействуют на механизмы развития данного симптома. Точный план терапии подбирается индивидуально для каждого пациента, с учетом лабораторных показателей крови, особенностей лечения основного заболевания и других параметров.
Лечение анемии народными способами
Некоторые пациенты по разным причинам отказываются от приема описанных выше препаратов и обращаются к народной медицине. Безусловно, некоторые растения или продукты могут оказывать стимулирующее действие на систему кроветворения. Однако, учитывая основной диагноз и тяжесть анемии, этого действия крайне недостаточно для восстановления уровня гемоглобина и кислородной функции крови. В результате снижается эффективность противоопухолевого лечения, ухудшается прогноз и существенно повышается риск неблагоприятного исхода. Устранить выраженную анемию в домашних условиях при помощи народных методов невозможно. Этим должны заниматься врачи соответствующего профиля, в распоряжении которых имеются современные лекарственные препараты.
Источник
Стадию рака желудка определяют по трем показателям, которые обозначаются буквами латинского алфавита:
- T (tumor) — размер первичной опухоли, глубина ее прорастания в стенку желудка и распространение на соседние ткани.
- N (nodes) — распространение раковых клеток в ближайшие (регионарные) лимфатические узлы.
- M (metastasis) — наличие метастазов, вторичных очагов, которые возникли в результате распространения раковых клеток с током крови или лимфы из желудка в другие органы.
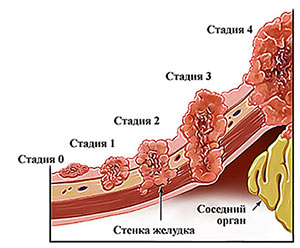
При раке желудка 4 стадии первичная опухоль может иметь любые размеры, прорастать в стенку желудка на любую глубину, распространяться или не распространяться в соседние органы, лимфатические узлы. Но всегда есть отдаленные метастазы. Это ключевой признак.
В какие органы чаще всего метастазирует рак желудка?
Опухолевые клетки могут распространяться из желудка в другие органы разными способами:
- Рак может непосредственно прорастать в соседние органы. Чаще всего — в поджелудочную железу, реже — в поперечную ободочную кишку, левую долю печени.
- Иногда раковые клетки распространяются по поверхности брюшины — тонкой пленки из соединительной ткани, которая выстилает изнутри стенки брюшной полости и покрывает внутренние органы. При этом у женщин нередко обнаруживаются метастазы в яичниках (опухоль Крукенберга).
- Гематогенным путем (с током крови) рак желудка 4 стадии чаще всего распространяется в печень, реже — в легкие и кости.
- Лимфогенное распространение раковых клеток происходит вдоль печеночно-дуоденальной связки, чревного ствола, сосудов селезенки.
При раке желудка могут возникать специфические метастазы. Для них существуют специальные названия:
- Метастаз Вирхова — в лимфатическом узле, расположенном над ключицей.
- Метастаз сестры Марии Джозеф — в пупок.
- Метастазы Шницлера — в лимфатические узлы, расположенные вокруг прямой кишки.
- Метастазы Айриша — в лимфатические узлы, расположенные в подмышечной области.
Согласно статистике, рак желудка 4 стадии чаще всего метастазирует в печень (у 48% пациентов), брюшину (32%), легкие (15%), кости (12%).
Симптомы
При раке желудка 4 стадии могут беспокоить такие неспецифические симптомы, как плохой аппетит и потеря веса, вплоть до сильного истощения (кахексии), дискомфорт, чувство тяжести, распирания и боль в животе, изжога, тошнота и рвота (иногда с кровью), запоры, примесь крови в стуле.
Специфические симптомы — это желудочное кровотечение при распаде опухоли и анемия из-за кровопотери. Поражение опухолевыми клетками брюшины приводит к асциту (скоплению жидкости в брюшной полости). Также характерны зловонный стул черного цвета и рвота массами, напоминающими кофейную гущу.
Рак желудка длительно не дает о себе знать. На ранних стадиях многие люди не испытывают симптомов и не знают, что больны. У четырех из пяти больных диагноз устанавливают, когда опухоль уже успевает распространиться на другие органы.

Люди, имеющие повышенный риск рака желудка, должны регулярно проходить скрининг — гастроскопию. Это помогает диагностировать опухоль на ранних стадиях.
Методы диагностики
При раке желудка 4 стадии применяют разные методы диагностики, они помогают выявить первичную опухоль и вторичные очаги в других органах:
- Эндоскопическое исследование (гастроскопия, ФГДС) помогает обнаружить патологические изменения на слизистой оболочке желудка.
- Эндоскопическое ультразвуковое исследование — по сути та же ФГДС, но на конце гастроскопа находится ультразвуковой датчик. Он может «просветить» соседние органы и лимфатические узлы через стенку желудка. Зачастую это намного информативнее, чем обычное УЗИ.
- Биопсия. Исследование, во время которого врач получает образец опухолевой ткани и отправляет на анализ в лабораторию. На данный момент биопсию можно назвать самым точным методом диагностики онкозаболеваний. Исследовать можно ткань желудка, лимфатических узлов, других органов.
- Рентгенография с контрастным усилением. Этот метод диагностики используется довольно редко, так как гастроскопия более информативна (к тому же, во время нее можно взять материал для биопсии). Но рентгенография — менее инвазивный метод, во время нее в желудок не вводят никаких инструментов. Иногда это преимущество важно. Суть метода в том, что пациенту дают выпить раствор непроницаемого для рентгеновских лучей сульфата бария, затем делают снимки.
- Компьютерная томография. Более «продвинутая» разновидность рентгенографии, позволяет получить послойные снимки-«срезы» всего тела, на которых будет видна опухоль желудка и очаги в других органах.
- МРТ — в каком-то смысле аналог компьютерной томографии, но во время этого исследования вместо рентгеновских лучей используют мощное магнитное поле. Это безопаснее. МРТ лучше «видит» мягкие ткани. Минус метода в том, что он более сложен, нужен дорогой аппарат, который есть далеко не во всех клиниках.
- Позитронно-эмиссионная томография (ПЭТ). Идеальна для поиска метастазов, которые не могут обнаружить другие методы диагностики. В организм вводят безопасный радиоактивный сахар. Он накапливается в раковых клетках, так как они активно потребляют энергию, и делает их видимыми на специальных снимках.
- Рентгенография грудной клетки. Применяется для поиска метастазов в легких.
Современные методы лечения
Лечение при раке желудка четвертой стадии преследует две цели:
- Сократить размеры опухоли, замедлить ее прогрессирование.
- Устранить симптомы: боль, анемию, нарушение проходимости желудка, асцит.
Хирургическое лечение
Хирургическое вмешательство при раке желудка, как правило, направлено на восстановление проходимости, если опухоль мешает движению пищи. Иногда удается выполнить субтотальную резекцию — удалить часть желудка. Чаще проводят шунтирование: создают сообщение между верхней частью желудка и тощей кишкой, в обход участка, перекрытого опухолью.
В случаях, когда операцию выполнить нельзя, можно провести стентирование желудка. В месте его соединения с пищеводом или двенадцатиперстной кишкой (в зависимости от локализации опухоли) с помощью эндоскопа устанавливают стент — полый каркас с металлической сетчатой стенкой. Иногда проводят эндоскопическую абляцию: через эндоскоп подают лазерный луч, который разрушает опухолевую ткань.
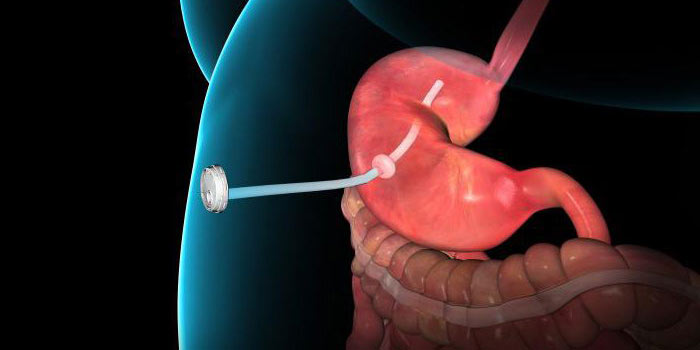
Если человек с раком желудка 4 стадии не может нормально есть, и хирургическое лечение не помогает это исправить, может быть наложена гастростома или еюностома. Желудок или тощую кишку подшивают к коже, формируют отверстие. Через него будет происходить питание.
Химиотерапия и лучевая терапия
При раке желудка с метастазами проводят паллиативную химиотерапию и лучевую терапию. Их главная задача — уменьшить размеры опухоли и продлить жизнь пациента. Применяют разные комбинации химиопрепаратов:
- Эпирубицин + цисплатин + 5-фторурацил.
- Доцетаксел + цисплатин + 5-фторурацил.
- Иринотекан + цисплатин.
- Иринотекан + 5-фторурацил.
- Иринотекан + капецитабин.
- Оксалиплатин + 5-фторурацил.
- Оксалиплатин + капецитабин.
Комбинации из трех препаратов, а также химиотерапия в сочетании с лучевой терапией (химиолучевая терапия) более эффективны, но хуже переносятся, несут более высокий риск побочных эффектов.
Таргетная терапия
Таргетные препараты могут быть эффективны в случаях, когда химиотерапия не помогает. Это современная группа противоопухолевых средств, они атакуют определенные молекулы-мишени, которые важны для роста опухолевой ткани. При раке желудка четвертой стадии применяют два таргетных препарата:
- Трастузумаб блокирует белок-рецептор HER2, который находится на поверхности раковых клеток и заставляет их размножаться. Активность этого белка повышена в каждой пятой злокачественной опухоли желудка (такой рак называют HER2-позитивным).
- Рамуцирумаб блокирует VEGF — белок, который вырабатывается раковыми клетками и стимулирует рост новых сосудов, снабжающих опухоль кислородом и питательными веществами.
Таргетные препараты применяют самостоятельно или в сочетании с химиопрепаратами. Они эффективны, когда раковые клетки обладают определенными молекулярно-генетическими особенностями, когда в них повышена активность соответствующего «вещества-мишени».
Иммунотерапия
Иммунитет человека устроен очень сложно. В нем есть множество звеньев и всевозможных механизмов регуляции. Например, для того чтобы сдерживать себя от атаки на собственные здоровые ткани, иммунная система использует особые вещества — контрольные точки. Иногда их используют злокачественные опухоли, чтобы защититься от иммунной атаки. С этим помогают бороться современные лекарства, которые относятся к классу иммунопрепаратов и называются ингибиторами контрольных точек.

При раке желудка 4 стадии иногда эффективен ингибитор контрольных точек под названием пембролизумаб (Кейтруда).
Лечение анемии
Кровотечение при раке желудка может привести к анемии — состоянию, при котором в крови снижается количество эритроцитов и гемоглобина. В результате ухудшается качество жизни, выживаемость. Приходится снижать дозы химиопрепаратов и сокращать продолжительность курсов химиотерапии, лечение становится менее эффективным.
С анемией при раке желудка 4 стадии борются с помощью препаратов железа, фолиевой кислоты, витамина B12, переливаний эритроцитарной массы. Существуют препараты-аналоги гормона эритропоэтина, который вырабатывается почками и активирует образование новых эритроцитов в красном костном мозге. Обеспечить организм дополнительным количеством железа помогают некоторые рекомендации относительно рациона питания.
Лечение асцита при раке желудка 4 стадии
Асцит — скопление жидкости в брюшной полости — одно из самых частых осложнений рака желудка четвертой стадии. Это состояние возникает по двум причинам:
- Из-за метастазов рака в брюшину. При этом увеличивается проницаемость стенок кровеносных сосудов, жидкость из них в большем количестве поступает в брюшную полость. Работа лимфатических сосудов нарушается, они не могут выводить жидкость.
- Из-за метастазов в лимфатических узлах. Нарушается отток лимфы, лимфатические сосуды, которые в норме должны выводить жидкость из брюшной полости, больше не могут выполнять свою функцию.
При асците проводят лапароцентез: в стенке брюшной полости делают прокол и выводят через него лишнюю жидкость. Для того чтобы обеспечить постепенное выведение жидкости в течение некоторого времени, применяют специальные перитонеальные порт-системы. Уничтожать метастазы в брюшине помогает внутрибрюшинная химиотерапия, когда химиопрепарат вводят в брюшную полость. При любом из видов лечения необходима специальная диета и приём ряда препаратов, уменьшающих тошноту.
Сколько живут с раком желудка 4 стадии?
Главный прогностический показатель при онкологических заболеваниях — пятилетняя выживаемость. Он обозначает процент пациентов, которые остались живы спустя 5 лет с момента диагностики и начала лечения злокачественной опухоли. Для IV стадии рака желудка этот показатель составляет 4%. В течение пяти лет 96 больных из 100 погибают, 4 остаются в живых. Но такая удручающая статистика — не повод сдаваться. Методы лечения совершенствуются, сегодня онкологи могут сделать намного больше, чем десятилетия назад. Пациенты, которым не помогают стандартные методы, могут принять участие в клинических испытаниях новых препаратов.
Источник
