Протезирование клапанов сердца анемия
Статья посвящена проблеме приобретенной механической гемолитической анемии, вызванной дисфункцией имплантированных сердечных клапанов. Показано, что в современных условиях наиболее часто выраженные признаки гемолиза наблюдаются при дисфункции протеза, например, вследствие образования параклапанной фистулы. Представлены клинические случаи.
В настоящее время благодаря современным возможностям сердечно-сосудистой хирургии операция протезирования клапанов сердца стала повседневной в работе специализированных кардиохирургических центров. В мире живут десятки тысяч пациентов с имплантированными сердечными протезами. В условиях хирургической коррекции клапанов становится актуальной проблема послеоперационной анемии, которая может носить различный характер. Вероятность развития у такого рода больных приобретенной механической гемолитической анемии во многом определяет течение послеоперационного периода. Большое значение в достижении хороших отдаленных результатов приобретают квалифицированный контроль и лечение этих пациентов у врача поликлиники по месту жительства [1].
Данные о воздействии протезов на эритроциты и на возникновение гемолиза противоречивы. По данным некоторых исследователей, гемолиз бывает клинически невыраженным, в других работах имеются указания на значительные клинические проявления гемолиза [1–4]. Степень клинических проявлений гемолиза зависит как от состояния самих эритроцитов, так и от механических свойств протезов [5, 6]. Несомненно, играют роль не только обработка протеза и материал, из которого он сделан, но и гемодинамические условия: скорость кровотока в области протеза, образование завихрений.
В связи с улучшением методологии оперативных вмешательств, а также с модернизацией искусственных клапанов сердца (ИКС) сердечно-сосудистый риск при операциях на сердце в течение последних десятилетий существенно снизился во всех возрастных группах. В 1960–1970-е гг. после введения в практику протезирования клапанов сердца гемолитическая анемия развивалась у 5–15% прооперированных пациентов, особенно после имплантирования механических шаровых протезов [2, 5]. Использование протезов нового поколения снизило частоту гемолитической анемии до 1% [2, 6]. Современные искусственные клапаны сердца разработаны на основе клинических данных использования нескольких поколений протезов. Они изготовлены из новейших материалов и имеют уникальную конструкцию [7, 8]. Однако компенсированный гемолиз может возникнуть при любом типе протеза. Наиболее часто выраженные признаки гемолиза наблюдаются при нарушении функции протеза, например, вследствие образования параклапанной фистулы. Разрушение эритроцитов с развитием гемолиза связано с нарушением кровотока через дефектный протез и увеличением повреждения эритроцитов его створками [3, 7]. Клинически гемолиз может проявляться симптомами сердечной недостаточности и анемии. Наблюдаются бледность кожных покровов, желтуха, моча может приобретать коричневый или черный цвет. Содержание билирубина повышено, особенно непрямая фракция, могут быть ретикулоцитоз, повышение активности лактатдегидрогеназы (ЛДГ) и уровня свободного гемоглобина в плазме крови. Синдром механического гемолиза подтверждается обнаружением в мазке крови больного фрагментов (обломков) эритроцитов (Fragmentes Red Cell (FRC)) или шистоцитов (син. — шизоциты). Наблюдаются анизопойкилоцитоз (изменение формы и размеров эритроцитов), полихромазия (способность окрашиваться как основными, так и кислыми красителями). При длительно протекающем гемолизе развивается дефицит железа.
В отечественной и зарубежной литературе описано очень мало случаев макроангиопатической гемолитической анемии, связанной с механическим повреждением эритроцитов у пациентов с ИКС. Мы приводим собственные наблюдения о гемолизе, вызванном дисфункцией механического двустворчатого протеза МедИнж (ЗАО НПП «МедИнж», Россия).
Пациентка, 65 лет.
Диагноз: сочетанный приобретенный порок митрального, аортального и трикуспидального клапанов. Проведено протезирование аортального (МедИнж 23) и митрального (МедИнж 29) клапанов, аннулопластика трикуспидального клапана по Де Вега-2.
До оперативного вмешательства у пациентки показатели красной крови не выходили за пределы соответствующих референтных интервалов: эритроциты — 4,16×1012/л; гемоглобин — 124 г/л; гематокрит — 36%; средний объем эритроцитов — 86,6 фл; среднее содержание гемоглобина в эритроците — 29,8 пг; средняя концентрация гемоглобина в эритроците — 344 г/л; ширина распределения эритроцитов по объему — 13,7%. На 10-е сут после операции у нее наблюдалась нормохромная анемия: эритроциты — 2,74×1012/л; гемоглобин — 83,2 г/л; гематокрит — 23,7%; средний объем эритроцитов — 86,7 фл; среднее содержание гемоглобина в эритроците — 30,4 пг; средняя концентрация гемоглобина в эритроците — 351 г/л; ширина распределения эритроцитов по объему — 16,1%. Через 1 мес. признаки анемии сохранялись: эритроциты — 2,54×1012/л; гемоглобин — 80,2 г/л; гематокрит — 23%; средний объем эритроцитов — 82,3 фл; среднее содержание гемоглобина в эритроците — 27,4 пг; средняя концентрация гемоглобина в эритроците — 351 г/л; ширина распределения эритроцитов по объему — 17,1%. На фоне приема сульфата железа и аскорбиновой кислоты 200 мг/сут эффекта не наблюдалось.
Пациентку беспокоили одышка при минимальной физической нагрузке, в положении лежа, отеки, повышенная утомляемость. Через 6 мес. после операции в связи с сохранением жалоб, признаков анемии (гемоглобин — 70–80 г/л) находилась на лечении в терапевтическом отделении. У пациентки был повышен уровень непрямого билирубина (40,4 мкмоль/л), проба Кумбса отрицательная, отмечалось периодическое выделение мочи черного цвета. Эффекта от преднизолона не было. Была обследована у гематолога, диагностирована приобретенная гемолитическая анемия, обусловленная механическим повреждением эритроцитов протезированными клапанами сердца. Направлена в кардиохирургический стационар для решения вопроса о повторном оперативном вмешательстве.
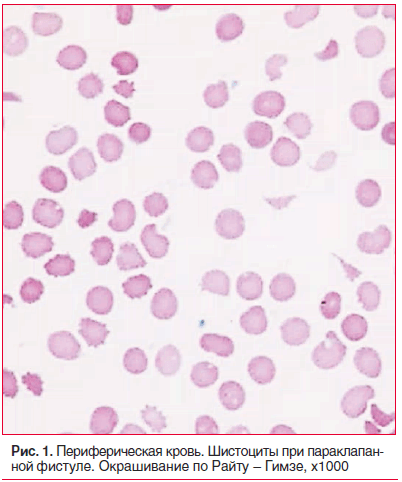
При поступлении в стационар состояние тяжелое. Кожные покровы бледные, желтушные. Живот увеличен за счет асцита. Пастозность стоп, лодыжек. Тоны сердца приглушены, аритмичные. Мелодия протеза четкая, систолический шум во всех точках. На эхокардиографии: в проекции аортального клапана протез без признаков дисфункции; в проекции митрального клапана диагностирована трансклапанная регургитация 1–2 степени, по задней части протеза — параклапанная фистула 2 степени. Показатели красной крови: эритроциты — 2,76×1012/л; гемоглобин — 90 г/л; гематокрит — 26,3%; средний объем эритроцитов — 95,6 фл; среднее содержание гемоглобина в эритроците — 32,2 пг; средняя концентрация гемоглобина в эритроците — 342 г/л; ширина распределения эритроцитов по объему — 24,3%, при микроскопии окрашенного мазка — полихромазия, шистоциты (2,0%) (рис. 1), ретикулоциты — 2,5%. Билирубин общий — 98,5 мкмоль/л, билирубин непрямой — 50,4 мкмоль/л, свободный гемоглобин — 0,6 г/л.
К сожалению, ввиду наличия у пациентки аортального протеза эндоваскулярное закрытие параклапанной фистулы митрального протеза было технически невыполнимо. В настоящее время пациентка наблюдается у кардиолога и гематолога по месту жительства. При снижении гемоглобина ниже 60 г/л ей проводятся трансфузии эритроцитосодержащих компонентов крови.
Пациентка, 60 лет. Диагноз: приобретенный порок митрального и трикуспидального клапанов. Проведены протезирование митрального (МедИнж 29) клапана, аннулопластика трикуспидального клапана по Де Вега.
Через 1 год после оперативного вмешательства у пациентки наблюдалось ухудшение состояния: одышка при минимальной физической нагрузке, отеки на ногах, последние 6 мес. — желтушность склер. В анализах, выполненных по месту жительства, — билирубин до 134 мкмоль/л. По данным чреспищеводной эхокардиографии в проекции митрального клапана — параклапанная фистула 1 степени.
Пациентка была госпитализирована в кардиохирургический стационар для устранения дефекта. При поступлении: билирубин — 110 мкмоль/л, непрямой билирубин — 22,7 мкмоль/л, свободный гемоглобин — 0,3 г/л. Наблюдалась гипохромная анемия: эритроциты — 4,6×1012/л; гемоглобин — 100 г/л; гематокрит — 36%; средний объем эритроцитов — 73,9 фл; среднее содержание гемоглобина в эритроците — 21,7 пг; средняя концентрация гемоглобина в эритроците — 291 г/л; ширина распределения эритроцитов по объему — 24,4%, шистоциты — 1,3%. Пациентке было проведено эндоваскулярное закрытие параклапанной фистулы окклюдером с положительной динамикой, с постепенным снижением уровня общего и непрямого билирубина, повышением уровня гемоглобина. При выписке гемоглобин — 128 г/л.
Таким образом, при подозрении на гемолиз у больных с ИКС всегда необходимо исключать механическую причину повреждения эритроцитов. Степень анемии в зависимости от степени и выраженности гемолиза может быть различной. Чаще всего анемия нормохромная, но при длительно протекающем гемолизе может носить гипохромный характер, с изменением морфологии красных клеток крови и присутствием шистоцитов либо только с присутствием шистоцитов как изолированным проявлением пойкилоцитоза. Рабочая группа Международного совета стандартизации в гематологии (МССГ (ICSH)) подготовила рекомендации для стандартизации, идентификации, подсчета и описания шистоцитов. Рекомендации определяют морфологическое описание шистоцитов, основанное на соответствующих критериях (в виде шлема; маленькие, неправильной треугольной формы, с наличием 2–3 углов; в форме полумесяца, с заостренными выступами, а также с отсутствием просветления в центре) [9–11]. В качестве полезного дополнения к микроскопу рекомендуется автоматизированный подсчет FRC. К сожалению, не все современные гематологические анализаторы демонстрируют сигналы тревоги («флаги»), сигнализирующие о наличии шистоцитов, а тем более проводят их подсчет. Да и специфичность автоматического метода очень низка (около 20%), требуется микроскопическое исследование для их подтверждения [9]. Поэтому общий анализ крови у пациентов с ИКС при подозрении на гемолиз необходимо дополнять микроскопией окрашенного мазка крови с описанием морфологии эритроцитов.
Выявленный шистоцитоз требует от врача-клинициста безотлагательных действий по установлению диагноза. При наличии клинической картины, лабораторных признаков гемолиза, нарастании в динамике процентного содержания шистоцитов диагноз механического разрушения эритроцитов становится очевидным. При подтверждении механической гемолитической анемии оправданным методом лечения является своевременное репротезирование клапанов сердца.
Источник
Представлено клиническое наблюдение за пациенткой, перенесшей трехклапанное протезирование, которое осложнилось развитием тяжелого внутрисосудистого гемолиза. Функция протезов была сохранной, признаки параклапанной регургитации отсутствовали, гемодинамический эффект операции расценивался как хороший. Репротезирование аортального и митрального клапанов каркасными биопротезами устранило проблему.
Субклинический внутрисосудистый гемолиз у пациентов, перенесших протезирование клапанов сердца, — достаточное частое явление, а основными факторами риска его развития являются имплантация механических протезов, многоклапанное протезирование и необходимость замены митрального клапана [1]. Однако развитие тяжелой гемолитической анемии, резистентной к консервативной терапии и обусловливающей необходимость повторной операции, — ситуация крайне редкая [2]. Мы приводим клинический случай такого осложнения после имплантации двух механических протезов в клапанные позиции левых отделов сердца у пациентки старшего возраста и ее успешного излечения после повторного кардиохирургического вмешательства.
Больная М., 62 года, поступила в клинику ФГБУ «НИИПК им. акад. Е.Н. Мешалкина» Минздрава РФ с жалобами на учащенное сердцебиение, одышку при прохождении менее 200 м. В детстве были частые ревматические атаки. В 1976 г. находилась на стационарном лечении по поводу инфекционного эндокардита, мерцательная аритмия с 1987 г., тогда же диагностирован митральный порок сердца. В 1990 г. больной выполнена операция — открытая митральная комиссуротомия, после которой в течение 15 лет отмечалось стабильное состояние. С 2005 г. отмечает постепенное снижение толерантности к нагрузкам, усиление одышки. Госпитализирована в клинику в июле 2008 г. с основным диагнозом: хроническая ревматическая болезнь сердца, выраженный митральный рестеноз, выраженный аортальный стеноз, выраженная трикуспидальная недостаточность, хроническая сердечная недостаточность III функционального класса.
По данным эхокардиографии (ЭхоКГ) при поступлении, конечный диастолический объем (КДО) левого желудочка (ЛЖ) 132 мл, фракция выброса (ФВ) ЛЖ 66%, площадь аортального отверстия 1,3 см2, пиковый трансаортальный градиент 55 мм рт. ст., площадь митрального отверстия 1,3 см2, площадь трикуспидального отверстия 3,4 см2, выраженная трикуспидальная регургитация.
Пациентке выполнена операция: протезирование митрального клапана механическим протезом «МИКС №25», аортального клапана механическим протезом «МИКС №21» и трикуспидального клапана механическим протезом «ЮниЛайн №30». Операционный этап прошел без осложнений. Ранний послеоперационный период протекал крайне тяжело — с развитием гемолитической анемии (стойкое снижение уровня общего гемоглобина крови до 70—75 г/л и увеличением свободного гемоглобина до 295—315 мг%), острой почечной недостаточности. После проведения курса гормональной терапии (преднизолон), гемотрансфузий, 5 сеансов гемодиализа удалось относительно стабилизировать состояние (свободный гемоглобин крови 78 мг%, общий — 74 г/л). Клинических и инструментальных данных, подтверждающих дисфункцию имплантированных протезов, не было. По данным контрольной ЭхоКГ, КДО ЛЖ 127 мл, ФВ ЛЖ 68%, в аортальной позиции механический протез (площадь отверстия 2,7 см2, пиковый транспротезный градиент давления 35 мм рт. ст., регургитации нет), в митральной позиции механический протез (площадь отверстия 3 см2, средний транспротезный градиент давления — СТГД 5 мм рт. ст., регургитация не зарегистрирована), в трикуспидальной позиции биологический протез (площадь отверстия 3,3 см2, СТГД 1,6 мм рт. ст., регургитации нет).
Больная выписана на дальнейшее лечение по месту жительства. В течение последующих 3 мес пациентка отмечала постепенное ухудшение состояния — тахикардия при подъеме на первый этаж, усиление одышки. Больной проводилось лечение в гематологическом отделении по месту жительства с незначительным эффектом. Там же была исключена аутоиммунная природа анемии, а гемолиз расценен как механический вследствие дефекта стенки эритроцитов. Пациентка повторно госпитализирована в клинику ФГБУ «НИИПК им. акад. Е.Н. Мешалкина». На момент поступления уровень общего гемоглобина крови 79 г/л, свободного — 96 мг%, анизоцитоз, шизоцитоз, сфероцитоз. По данным ЭхоКГ, имплантированные протезы работают без сбоев, дисфункции их не выявлено. С учетом рекомендаций гематолога и бесперспективности дальнейшего продолжения консервативной терапии было принято решение о выполнении репротезирования митрального и аортального клапанов биологическими протезами с целью уменьшения травматизации эритроцитов.
22 октября 2008 г. больной выполнена операция: репротезирование митрального клапана биологическим протезом «Carpentier-Edwards Lifesciences №25», репротезирование аортального клапана биологическим протезом «Sorin Pericarbon №21». При изучении эксплантированных механических протезов никаких признаков механических повреждений их структуры или иной дисфункции не наблюдали.
Послеоперационный период протекал с явлениями умеренной сердечной недостаточности, купированными к моменту выписки. В общем анализе крови отмечалось постепенное повышение уровня общего гемоглобина до 87 г/л и снижение уровня свободного гемоглобина до 4 мг%. По данным контрольной ЭхоКГ, КДО ЛЖ 104 мл, ФВ ЛЖ 70%, в аортальной позиции биологический протез (площадь отверстия 2,6 см2, пиковый транспротезный градиент давления 34 мм рт. ст., регургитации нет), в митральной позиции биологический протез (площадь отверстия 2,8 см2, СТГД 3 мм рт. ст., регургитация не зарегистрирована), в трикуспидальной позиции биологический протез (площадь отверстия 3 см2, СТГД 0,7 мм рт. ст., регургитации нет).
Пациентка выписана на 45-е сутки после операции после достижения стабилизации клинического состояния без необходимости проведения курсов гормональной или иной терапии, направленной на профилактику и лечение гемолитической анемии.
Данный клинический случай демонстрирует возможность успешного применения ксеноклапанов у больных с приобретенными пороками сердца с высоким риском механического гемолиза, обусловленным врожденной или приобретенной несостоятельностью стенки эритроцитов и их повреждением при контакте с элементами конструкции механических протезов.
1. Mecozzi G., Milano A., Carlo M. et al. Intravascular hemolysis in patients with new-generation prosthetic heart valves: A prospective study. J Thorac Cardiovasc Surg 2002;123:550—556.
2. Camishion R.C. Severe intravascular hemolysis after triple valve replacement: cure by replacement of aortic and mitral valves with porcine xenografts. Surgery 1979;85:246—248.
ФГБУ Новосибирский НИИ патологии кровообращения им. акад. Е.Н. Мешалкина Минздрава РФ
Кардиохирургическое отделение приобретенных пороков сердца
Астапов Д.А. – к.м.н., сердечно-сосудистый хирург.
Центр приобретенных пороков сердца и биотехнологий
Железнев С.И. – д.м.н., проф., руков. центра.
Семенова Е.И. – к.м.н., ст.н.с.
E-mail: dmast@rambler.ru
Источник
 Рекомендации пациентам с протезированным клапаном сердца 1.6 Мб
Рекомендации пациентам с протезированным клапаном сердца 1.6 Мб
Искусственный клапан сердца: 2 основных типа
При нарушении работы какого-либо из 4 клапанов сердца — их сужении (стеноз) или чрезмерном расширении (недостаточности) — существует возможность их замены или реконструкции при помощи искусственных аналогов. Искусственный клапан сердца — это протез, который обеспечивает требуемое направление тока крови за счет прерывистого перекрывания устьев венозных и артериальных сосудов. Основным показанием к протезированию служат грубые изменения створок клапана, приводящие к выраженному нарушению кровообращения.
Применяются два основных типа искусственных клапанов сердца: механические и биологические модели, каждая из которых имеют свои особенности, преимущества и недостатки1.
1.
Butchart EG et al. Recommendations for the management of patients after heart valve surgery. European Heart Journal. 2005: 26(22); 2465-2471.

Рисунок 1. Два основных типа искусственных клапанов
Механический клапан сердца или биологический протез?
Механический клапан сердца надежен, служит долго и не нуждается в замене, но требует постоянного приема специальных медикаментов, снижающих свертываемость крови.
2.
Bonow R.O., Carabello B.A., Kanu C. et al.; American College of Cardiology/American Heart Association Task Force on Practice Guidelines; Society of Cardiovascular Anesthesiologists; Society for Cardiovascular Angiography and Interventions; Society of Thoracic Surgeons. ACC/AHA 2006 guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (writing committee to revise the 1998 Guidelines for the Management of Patients With Valvular Heart Disease): developed in collaboration with the Society of Cardiovascular Anesthesiologists: endorsed by the Society for Cardiovascular Angiography and Interventions and the Society of Thoracic Surgeons. Circulation 2006; 114 (5): e84-231; J Am Coll Cardiol 2006; 48 (3): e1-148.
Биологические клапаны постепенно могут разрушаться. Срок их службы в значительной степени зависит от возраста больного и сопутствующих заболеваний. С возрастом процесс разрушения биологических клапанов существенно замедляется.
Решение о том, какой клапан наиболее оптимален, должно приниматься перед хирургическим вмешательством в ходе обязательной беседы между хирургом и пациентом2.
Жизнь с искусственным клапаном сердца
Люди с протезами сердечных клапанов относятся к категории пациентов с очень высоким риском тромбоэмболических осложнений. Борьба с тромбозами — основа стратегии ведения таких пациентов, и именно ее успешность во многом определяет прогноз для больного.
Риск тромбоэмболических осложнений уменьшается при использовании биологических протезов клапанов, но они имеют свои недостатки. Их имплантируют нечасто и преимущественно пожилым людям3.
Жизнь с искусственным клапаном сердца требует ряда ограничений. Большинство пациентов с протезированными клапанами — это лица с механическими протезами, которые принадлежат к группе высокого риска развития тромботических осложнений. Пациент вынужден постоянно принимать антитромботические препараты, в абсолютном большинстве случаев – непрямые антикоагулянты (варфарин). Их должны принимать практически все пациенты с механическими клапанами сердца. Выбор биопротеза также не исключает необходимость приема варфарина, особенно у больных с фибрилляцией предсердий. Во избежание опасных кровотечений, постоянно принимающим варфарин пациентам лучше отказаться от повседневной деятельности и развлечений, связанных с повышенным риском получения травм (контактные виды спорта, работа с режущими предметами или с высоким риском падений даже с высоты собственного роста).
К наиболее важным аспектам врачебного наблюдения за пациентом с искусственным клапаном сердца на сегодняшний день относятся4:
- контроль свертываемости крови;
- активная профилактика тромбоэмболических осложнений с помощью антикоагулянтов (чаще всего варфарина).
3.
Bonow R.O., Carabello B.A., Chatterjee K. et al.; American College of Cardiology/American Heart Association Task Force on Practice Guidelines. 2008 focused update incorporated into the ACC/AHA 2006 guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to revise the 1998 guidelines for the management of patients with valvular heart disease). Endorsed by the Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons. Circulation 2008;118 (15): e523-661; J Am Coll Cardiol 2008; 52 (13): e1-142.
Важно отметить, что в настоящее время европейские и американские эксперты считают слишком интенсивными те уровни антитромботической терапии, которые раньше рекомендовались для большинства пациентов. Современные подходы к оценке риска позволяют выделить подгруппы лиц с наиболее высоким риском тромбоэмболических осложнений и активной антитромботической терапией. Для других пациентов с протезированными сердечными клапанами достаточно эффективной будет менее агрессивная антитромботическая терапия4.
Профилактика тромбозов у пациентов с механическими клапанами сердца
Профилактика тромбоза у пациентов с механическим клапаном сердца требует пожизненной антитромботической терапии.
Интенсивность терапии варфарином зависит от локализации протеза и его типа. Например, в соответствии с рекомендациям ACC/AHA (2008) механический протез аортального клапана требует поддержания МНО в пределах 2,0-3,0 при использования двухлепестковых (двустворчатых) протезов, а также клапана Medtronic Hall (один из самых популярных в мире одностворчатых искусственных клапанов), или в дипазоне 2,5-3,5 для всех остальных дисковых клапанов, а также для шарового клапана Starr–Edwards.
4.
Salem D.N., O’Gara P.T., Madias C., Pauker S.G.; American College of Chest Physicians. Valvular and structural heart disease: American College of Chest Physicians Evidence
Механический протез митрального клапана требует удержания МНО в рамках 2,5-3,5 для всех типов клапанов3.
Таблица 1. Рекомендуемое значение МНО при механических клапанах сердца5
| Позиция клапана сердца | Факторы риска ТЭ-осложнений | |
| отсутствуют | присутствуют | |
| Аортальная | 2,0-3,0 | 2,5-3,5 |
| Митральная | 2,5-3,5 | 3,0-4,0 |
5.
Методические рекомендации рассмотрены и рекомендованы ученым советом ФГБУ “Научно-исследовательский институт комплексных проблем сердечно-сосудистых заболеваний” СО РАМН 01 июля 2011 г., обновлены 14 января 2014 г.
Однако даже на фоне рекомендованной антитромботической терапии риск тромбоэмболических осложнений у пациентов, перенесших протезирование клапанов сердца, остается на уровне 1-2 %. Результаты большинства клинических исследований свидетельствуют о том, что риск тромбоза выше у пациентов с протезами митральных клапанов (по сравнению с протезами аортальных). Если для пациентов с искусственными аортальными клапанами возможен менее интенсивный режим антикоагулянтной терапии (с целевым МНО 2,0-3,0), то в случае с механическим протезом митрального клапана режим антикоагулянтной терапии должен быть достаточно интенсивным (с целевым МНО 2,5-3,5)6.
6.
Vahanian A., Baumgartner H., Bax J. et al.; Task Force on the Management of Valvular Hearth Disease of the European Society of Cardiology; ESC Committee for Practice Guidelines. Guidelines on the management of valvular heart disease: The Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology. Eur Heart J 2007; 28 (2): 230-68.
Вне зависимости от типа используемого искусственного клапана риск тромбоза наиболее высок в первые несколько месяцев после операции – до завершения процессов эпителизации в месте имплантации протеза. Американские эксперты считают целесообразным удерживать МНО в рамках 2,5-3,5 в первые 3 мес. после операции даже для больных с искусственным аортальным клапаном3.
Кроме того, удержание МНО в более жестких рамках (2,5-3,5) рекомендуется ACC/AHA при наличии факторов высокого риска тромбоэмболизма вне зависимости от типа протеза и его локализации. К таким факторам относятся мерцательная аритмия, тромбоэмболия в анамнезе, дисфункция левого желудочка (ЛЖ), состояние гиперкоагуляции7.
В настоящее время существуют портативные аппараты для самостоятельного определения МНО (по типу систем для контроля уровня сахара у больных диабетом), которые помогают удерживать уровень МНО в необходимом диапазоне. Среди них зарекомендовал себя Coagucheck XS для самостоятельного проведения анализов и немедленного получения результатов ПТВ/МНО. Прибор позволяет получить точные результаты менее чем за минуту, используя при этом всего 8 мкл (одну каплю крови).
Тем не менее, независимо от выбранной стратегии антитромботического лечения после протезирования сердечных клапанов, принципиально важным остается регулярное наблюдение за пациентом, его обучение и тесное сотрудничество с лечащим врачом.
7.
Butchart E.G. Antithrombotic management in patients with prosthetic valves: a comparison of American and European guidelines. Heart 2009;95: 430 436.
Это позволяет своевременно корректировать дозы препаратов, а также изменения их тромболитической активности в зависимости от особенностей питания, состояния функции печени и почек пациента.
Профилактика тромбоза у пациентов с биопротезами клапанов
Пациентам с биопротезами клапанов показана менее агрессивная антикоагулянтная терапия, поскольку в большинстве исследований риск тромбоэмболических осложнений у таких больных даже при отсутствии терпи антикоагулянтами составлял в среднем всего 0,7 %.
По мнению американских экспертов добавление варфарина может быть полезным при повышенном риске тромбоэмболий, но не рекомендуется рутинно всем пациентам. При использовании варфарина следует удерживать МНО в рамках 2,0-3,0, если протезирован аортальный клапан, и 2,5-3,5 — если митральный3.
Применение варфарина с целевым МНО 2,0-3,0 также может быть целесообразно в первые 3 мес. после операции и у больных с протезом митрального или аортального клапана без факторов риска, учитывая повышенную склонность к тромбообразованию в ранние сроки после протезирования клапана. Особые преимущества от такой стратегии получают пациенты с протезом митрального клапана3.
Таблица 2. Рекомендуемое значение МНО при биологических клапанах сердца
| Позиция клапана сердца | Факторы риска ТЭ-осложнений | |
| отсутствуют | присутствуют | |
| Аортальная | 2,0-2,5 | 2,5-3,0 |
| Митральная | 2,5-3,0 | 3,0-3,5 |
| Трикуспидальная | 2,5-3,0 | 3,0-3,5 |
Однако европейские эксперты ESC полагают, что в настоящее время нет достаточно убедительных данных, подтверждающих необходимость длительной антитромботической терапии у пациентов с биопротезами сердечных клапанов, если у этих пациентов нет каких-либо дополнительных факторов риска7.
В европейском руководстве использовать варфарин у таких больных рекомендуется только на протяжении первых 3 мес. после операции (целевое МНО — 2,5).
Длительная (пожизненная) антикоагулянтная терапия у пациентов с биопротезами клапанов может быть целесообразной только при наличии факторов высокого риска (например, мерцательной аритмии; в меньшей мере таким фактором риска может выступать сердечная недостаточность с ФВ ЛЖ <30%), утверждается в руководстве ESC6.
Таким образом, и в отношении больных с биопротезами сердечных клапанов европейские эксперты рекомендуют более осторожную тактику антитромботической терапии, в то время как американские специалисты считают оправданным более агрессивный подход. В то же время в США более распространена тенденция минимизировать время нахождения пациента в стационаре и стоимость его лечения, поэтому американские врачи для профилактики тромбоэмболий предпочитают назначать пациентам с биопротезами препараты ацетилсалициловой кислоты. В Европе пока склонны удерживать пациента в стационаре дольше, если это требуется, и применять у данной категории больных варфарин, более требовательный к мониторингу показателей свертывания крови.
Одной из наиболее существенных проблем ведения таких пациентов в условиях отечественного здравоохранения является невозможность адекватного контроля показателей свертывания крови на фоне постоянного приема антикоагулянтов.
Именно показатель МНО рекомендован всеми международными руководствами как необходимый для обеспечения безопасности и эффективности терапии7.
 Рекомендации пациентам с протезированным клапаном сердца 1.6 Мб
Рекомендации пациентам с протезированным клапаном сердца 1.6 Мб
Источник
