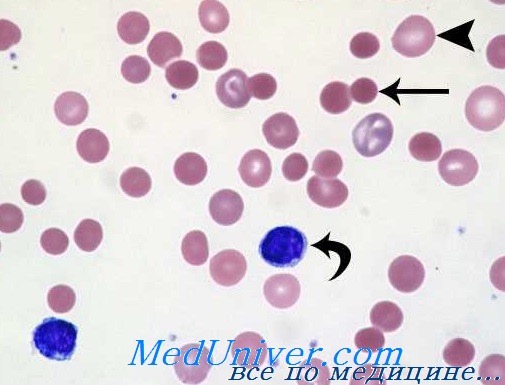
Рак и гемолитическая анемия характерны для


Анемия представляет собой патологическое состояние, для которого характерно снижение эритроцитов и/или концентрации гемоглобина в единице объема крови. Анемия не является самостоятельным заболеванием, это симптом, который характерен для самых разнообразных заболеваний, в том числе и для злокачественных опухолей.
Согласно статистике, данное состояние выявляется у каждого третьего онкологического пациента, а при прохождении химиотерапии — более чем в 90% случаев. Опасность анемии в онкологии заключается в том, что вместе с уменьшением уровня гемоглобина и эритроцитов, уменьшается и кислородная емкость крови. Этот фактор неблагоприятно сказывается на течении ракового процесса, снижает эффективность лечения и ухудшает дальнейший прогноз.
Основные причины развития анемии у онкологических пациентов
Снижение уровня эритроцитов и гемоглобина может развиваться вследствие снижения их образования, ускоренного разрушения или в результате потери. Каждой из этих причин способствуют собственные факторы, которые рассмотрим подробнее:
- Недостаточная выработка форменных элементов крови и гемоглобина может развиваться при поражении костного мозга, недостатке железа в организме или некоторых витаминов (фолиевая кислота, витамин В12). Данные состояния могут быть напрямую связаны с напрямую с онкологическим заболеванием. Например, потеря железа может развиваться в результате постоянной рвоты, отсутствия аппетита и нарушения его всасывания в кишечнике, который поражен опухолевым процессом. Некоторые виды препаратов, которые назначают при злокачественных опухолях, подавляют рост не только раковых клеток, но и клеток крови, которые активно делятся. Также анемия может развиваться при непосредственном поражении костного мозга опухолевым процессом.
- Ускоренное разрушение эритроцитов отмечается при воздействии различных лекарственных препаратов и при аномальной активности иммунной системы. Разрушение эритроцитов непосредственно в сосудах называется внутрисосудистым гемолизом. Этот процесс протекает в норме после завершения жизненного цикла эритроцитов, который составляет 120 дней. Однако при воздействии различных факторов (прием антибиотиков, цитостатиков, присоединение вторичной инфекции и др.), этот срок значительно уменьшается, что и приводит к развитию анемии.
- Кровопотеря у онкологических пациентов может быть как острой, так и хронической. Первый вариант встречается при проведении хирургического лечения рака, а также при развитии внутренних кровотечений, которые являются частым осложнением основного заболевания. Развитие анемии при хронической кровопотере отмечается в тех случаях, когда имеется скрытый источник незначительного кровотечения. Например, при колоректальном раке кровь может выделяться с калом незаметно для пациента.
Установление точной причины анемии играет решающее значение при выборе метода лечения. Кроме того, врач учитывает степень тяжести, тип анемии, общее состояние пациента и другие параметры. Получить эту информацию можно на диагностическом этапе.
Как выявить анемию
Обследование традиционно начинается с опроса пациента и сбора анамнеза. Врач должен помнить, что не всегда анемия развивается вследствие основного заболевания. Возможны наследственные или любые другие причины, которые не связаны с опухолевым процессом. Также необходимо установить вид предшествующего противоопухолевого лечения, продолжительность и количество курсов, наименование препаратов, которые применялись. На следующем этапе врач проводит общий осмотр. Анемия может проявляться бледностью кожных покровов, слабостью, потерей аппетита, головокружением и другими симптомами. Очень часто эти проявления отмечаются при различных видах рака, который протекает без анемии, поэтому поставить диагноз исходя только из жалоб пациента невозможно.
Объективную информацию можно получить только при помощи лабораторных исследований. Анемия диагностируется по следующим анализам:
- Количество ретикулоцитов.
- Уровень железа сыворотки крови.
- Уровень белка трансферрина и ферритина.
- Уровень витамина В12 и фолиевой кислоты.
Отдельное внимание уделяется общему анализу крови. В нем определяется уровень гемоглобина, количество эритроцитов и гематокрит (отношение форменных элементов к жидкой составляющей крови). Также определяют средний объем эритроцита, среднее содержание гемоглобина в эритроците и среднее содержание гемоглобина во всей эритроцитарной массе.
При необходимости в программу комплексного обследования при анемии могут включаться и другие лабораторные анализы или специальные методы.
Как классифицируется анемия
В зависимости от значения цветового показателя, степени тяжести и механизма развития, анемия разделяется на несколько категорий. Цветовой показатель крови отражает степень насыщения эритроцитов гемоглобином. Его значение в норме колеблется от 0,85 до 1,05 единиц. Снижение показателя отмечается при гипохромной анемии, а повышение — при гиперхромной. Если цветовой показатель в норме, но уровень гемоглобина все равно низкий, то говорят о нормохромной анемии.
По степени тяжести, анемия разделяется на три группы, в зависимости от концентрации гемоглобина:
- При легкой степени анемии уровень гемоглобина не опускается ниже отметки в 90 г/л.
- При средней степени анемии показатель колеблется в пределах 90-70 г/л.
- Тяжелая анемия характеризуется падением гемоглобина ниже 70 г/л.
Классификация анемии по механизму развития наиболее обширна. Среди распространенных форм отмечаются:
- Железодефицитная анемия. Развивается в результате нарушения всасывания, усиленной потери или недостаточного поступления железа в организм.
- Гемолитическая анемия. Характеризуется разрушением эритроцитов в сосудистом русле или за его пределами. Наиболее частые причины — недостаточность специфических ферментов, аутоиммунные заболевания, воздействие лекарственных препаратов.
- Постгеморрагическая анемия. Данное состояние характерно для острой или хронической кровопотери
- Апластическая анемия. Характеризуется снижением уровня клеток-предшественников эритроцитов в костном мозге. Обычно отмечается снижение и других форменных элементов — тромбоцитов и лейкоцитов.
- В12-дефицитная анемия. При недостатке витамина В12 нарушается процесс образования эритроцитов, снижается их продолжительность жизни. Дефицит витамина может быть связан как с нарушением его всасывания в кишечнике, так и с недостаточным поступлением в организм.
В большинстве случаев определить точный вид анемии можно после нескольких лабораторных тестов, но иногда приходится применять более сложные методы диагностики, например, генетическое исследование. Понимание механизма развития анемии и получение максимально полной информации об изменениях в показателях крови являются важным компонентом эффективной терапии данного симптома.
Методы лечения анемии
Устранить анемию у онкологических пациентов можно тремя способами: переливание эритроцитарной массы, введение эритропоэтина, назначение препаратов, содержащих железо. В отдельных случаях может применяться комбинация этих методов.
Переливание эритроцитарной массы при анемии
Переливание эритроцитарной массы является самым действенным методом, при помощи которого можно быстро восполнить дефицит эритроцитов, восстановить уровень гемоглобина и гематокрита. Однако без устранения причины анемии, этот способ даст лишь временный эффект. Поэтому переливание эритроцитарной массы не является альтернативой другим методикам и применяется только при наличии показаний. Одним из них является снижение уровня гемоглобина ниже 90 г/л. Переливание проводят при развитии у пациента характерных признаков анемии, среди которых отмечаются:
- Головокружение.
- Потеря сознания.
- Тахикардия.
- Быстрая утомляемость.
- Боль в груди.
- Одышка.
Данный метод лечения анемии также может применяться у пациентов, которые прошли курс химиотерапии или лучевой терапии и у которых отмечается быстрое снижение уровня гемоглобина или эритроцитов.
Применение стимуляторов эритропоэза
Стимуляторы эритропоэза при анемии увеличивают концентрацию гемоглобина и эритроцитов за счет усиления их образования в костном мозге. При сочетании с гемотрансфузиями, данный метод показывает очень хорошие результаты, но при этом имеет и ряд недостатков, которые касаются осложнений. В частности, применение стимуляторов эритропоэза для лечения анемии повышает риск развития тромботических осложнений, который и так является высоким у онкологических пациентов. По данным, полученным в ходе нескольких научных исследований, этот риск увеличивается в 1.4-1.7 раз.
В последнее время обсуждается вопрос о влиянии стимуляторов эритропоэза на выживаемость онкологических пациентов. В частности, специалисты установили, что применение препаратов данной группы при лечении анемии у пациентов с распространенным опухолевым процессом головы и шеи, шейки матки, молочной железы и других диагнозах снижает продолжительность жизни на 10-17%. В связи с этим специалисты предлагают придерживаться следующих правил:
- Если уровень гемоглобина составляет менее 100 г/л и пациент при этом проходит лечение химиопрепаратами, то стимуляторы эритропоэза могут назначаться с целью коррекции анемии и профилактики дальнейшего снижения показателей.
- Если уровень гемоглобина падает до 100 г/л и ниже, но химиотерапия при этом не проводится, то применять стимуляторы эритропоэза не рекомендуется ввиду повышенного риска развития осложнений и снижения продолжительности жизни.
- Во всех остальных случаях применять стимуляторы эритропоэза для лечения анемии у онкологических пациентов следует с осторожностью.
Также на протяжении всего времени лечения важно контролировать динамику лабораторных показателей и при увеличении уровня гемоглобина постепенно снижать дозировку стимуляторов эритропоэза.
Препараты железа при лечении анемии
Препараты железа применяются с целью лечения железодефицитных анемий, которые выявляются у 30-60% онкологический больных. При этом снижение уровня железа может быть связано как с самим опухолевым процессом или проводимым лечением, так и с другими факторами. Например, при назначении стимуляторов эритропоэза, существующего запаса железа в организме становится недостаточно для того, чтобы покрыть потребность, которая возникает в результате активного синтеза гемоглобина в костном мозге.

Для лечения анемии могут применяться как внутривенные, так и пероральные препараты. Второй вариант более удобен для пациента, так как таблетки проще принимать, но при этом данная форма действует медленнее и чаще приводит к осложнениям со стороны ЖКТ. Внутривенное введение позволяет добиться быстрого эффекта, что актуально при проведении химиотерапии.
Таким образом, для лечения анемии современная онкология может предложить различные методы, которые воздействуют на механизмы развития данного симптома. Точный план терапии подбирается индивидуально для каждого пациента, с учетом лабораторных показателей крови, особенностей лечения основного заболевания и других параметров.
Лечение анемии народными способами
Некоторые пациенты по разным причинам отказываются от приема описанных выше препаратов и обращаются к народной медицине. Безусловно, некоторые растения или продукты могут оказывать стимулирующее действие на систему кроветворения. Однако, учитывая основной диагноз и тяжесть анемии, этого действия крайне недостаточно для восстановления уровня гемоглобина и кислородной функции крови. В результате снижается эффективность противоопухолевого лечения, ухудшается прогноз и существенно повышается риск неблагоприятного исхода. Устранить выраженную анемию в домашних условиях при помощи народных методов невозможно. Этим должны заниматься врачи соответствующего профиля, в распоряжении которых имеются современные лекарственные препараты.
Токсическая гемолитическая анемия – причины, клиника, диагостика, лечениеТоксическая гемолитическая анемия (ТГА) относится к группе гемолитических анемий, обусловливаемых действием химических или медикаментозных агентов на эритроциты. С патологической точки зрения, равно как и в отношении клинических проявлений группа токсическая гемолитическая анемия не представляет собой обособленную нозологическую форму. Тем не менее практические соображения побуждают нас рассмотреть, в отдельной статье, ряд гемолитических анемий по критерию их этиологии за счет клеточных токсических факторов. Хотя токсическая гемолитическая анемия значительно реже иных видов гемолитических анемий (например АИГА) (Wintrobe и сотр.) в последнее время она приобретает все больший удельный вес в связи с увеличением профессиональных факторов отрицательного воздействия все растущего загрязнения среды и выпуска новых фармацевтических препаратов. Ниже приведены этиологические факторы, способствующие развитию токсической гемолитической анемии. Основные этиологические факторы, обусловливающие развитие токсической гемолитической анемии (ТГА): 2. Токсические вещества в отношении клеточных ферментов и/или гемоглобина: 3. Медикаменты «сенсибилизирующего» действия: В общих чертах воздействие токсических гемолитических (химических и медикаментозных) факторов на красные кроявные тельца осуществляется следующими тремя путями:
а) Непосредственное действие токсических веществ на составные элементы оболочки красных кровяных телец видимо последствие их адсорбции липопротеидами оболочки или комбинирования с последними. При этом нарушаются проницаемость и элластичность оболочки, происходит диффузия гемоглобина и прочих внутриклеточных составных, а в клетку проникают вода и натрий. Эритроциты приобретают «предшествующие расплавлению » формы, которые наблюдаются на мазках (сфероциты, зубчатые эритроциты). Сокращение элластичности оболочки приводит к понижению ее сопротивления непрерывным механическим воздействиям в потоке кровообращения. Процесс расплавления крови, вызываемый токсическими веществами оболочки прямо пропорционален дозе и длительности воздействия. Субстрат, на который действует гемолитический фактор, был уточнен в нескольких случаях (Douste-Blazy). Так, хлороформ, четыреххлористый углерод, бензол, толуол действуют на полюсные группы жировых цепей; анионовые детергенты (тетрадецилсульфат) закрепляются на цефалине; растительные вещества (дигитонин, сапонин) и отдельные катионовые мыла вступают в комбинацию с холестерином; змеиный яд (кобры) преобразовывает лецитин в лизолецитин. б) Группа веществ взаимодействует с отдельными клеточными ферментативными механизмами и/или подвергает их большой нагрузке. «Окисляющие » медикаментозные препараты действуют на эритроциты в норме, с большой нагрузкой на механизмы, сохраняющие гемоглобин в восстановленном виде, вплоть до их истощения. В результате образуется метгемоглобин и появляются тельца Гейнца. Влияние окислительных веществ слабее при наличии врожденного дефекта глютатионредуктазы или в условиях неустойчивого гемоглобина (гемоглобина Н или Цюрих). К гемоглобинизирующим веществам относятся: анилин, ацетанилид, нитриты, нитраты, хлораты, нитробензол, нитротолуол, фенацетин, сульфамиды. Отдельные вещества вызывают расплавление крови у лиц с врожденным недостатком Г-6-ФД (Wintrobe и сотр.), в том числе, примахин, памахин, хинакрин, хинин, сульфонамиды, сульфоны, нитрофурантоин, фуразолидон, ацетанилид, фенацетин, антипирин, пирамидон, пробенецид, синтетические заместители витамина К, фенилгидразин, изониазид, хлорамфеникол, хинидин, нафталин, тринитротолуол, метиленблау, растительные вещества (фасоль “Vicia faba”). Следует отметить, что некоторые медикаментозные препараты, вызывающие метгемоглобинизанию обусловливают расплавление крови и у лиц с недостатком Г-6-ФД. Объяснение этого явления следует искать в том, что Г-6-ФД действует в качестве донора восстановленного НАДФ для цепи реакций, нацеленных на борьбу с излишним образованием внутриклеточных окисленных соединений. Развивающаяся при сатурнизме анемия по комплексности и специфичности обусловливающего ее механизма занимает особое место. Свинец нарушает синтез гемоглобина на всех трех основных уровнях этого процесса — угнетает синтез гема, соединение железа с протопорфирином и синтез глобина. Влияя на синтез гема блокированием активности отдельных, богатых сульфгидрильными группами митохондриальных ферментов, таких как, дегидраза дельта-амино-левулиновой кислоты (ДДАЛК) и гемсинтетаза (Albahary) свинец обусловливает нарушение метаболизма порфиринов. Угнетение активности дегидразы ДАЛК препятствует синтезу содержащегося в последней порфобилиногена (ПБГ). Избыток ДДАЛК выделяется с мочой. Угнетение активности гемсинтетазы препятствует включению железа в протопорфирин. В таких условиях в эритроцитах скопляется значительное количество свободного протопорфирина (500—600 мкг/100 мл) (Кондаксе и сотр.), в то время как в митохондриях — нейтрализованного железа. Отравление свинцом обусловливает также выделение с мочой значительного количества копропорфирина III (1—2 мг в сутки) (Кондаксе и сотр.), видимо в связи с неиспользованием этого предшественника. Влияние свинца на глобин отражается в нарушениях, подобных наблюдаемым при легкой форме талассемии — примерно у 15% больных повышается процент гемоглобина А2 и F (Albahary). Отравление свинцом — болезнь не редкая. Ею заболевают наборщики, типографы, красильщики, шахтеры, потребители спиртных напитков, перегоняемых в самодельных установках и пр. К ведущим клиническим признакам относятся бледность, рези в желудке и неврологические проявления (полиневрит, нарушение поведения, энцефалопатия). Гематологические признаки определяет анемия, которая носит гипохромный и слегка микроцитный характер (Wintrobe и сотр.). Отмечается наличие точечно-базофильных эритроцитов. Показатель частоты последних не связан с интенсивностью воздействия токсического вещества. Число ретикулоцитов повышено, в частности при резко развившемся отравлении. На мазках периферической крови обнаруживаются также нормобласты, эритроциты с тельцами Жолли или кольцами Кабо. В костном мозге наблюдается эритроидная гиперплазия. В отдельных случаях отмечено наличие мнегоядерных эритробластов (Moore) или кольцевых сидеробластов (Wintrobe). Продолжительность жизни эритроцитов несколько меньше (Albahary). Интенсивность и скорость обмена железа плазмы занижены. Наблюдается рост показателя выделения желчных пигментов. Отмеченные аспекты могут подсказать мысль о неэффективности эритропоеза (Wintrobe). По мнению отдельных авторов анемию, вызываемую отравлением свинцом можно отнести к группе сидеробластических анемий (Moore). Уточнению диагноза способствуют обнаружение высокого показателя выделения АЛК и копропорфирина III с мочой (тест разборки) и нормальной концентрации свинца в крови и моче. При скрытом отравлении, когда наличие токсического вещества в крови и моче не выявимо постановке диагноза способствует исследование протопорфирина эритроцитов, при этом нормальный уровень исключает возможность отравления (Кондаксе и сотр.). Определение свинца в моче после введения стандартного количества ЭДТА—-еще один способ уточнения диагноза (Albahary). После введения комплексонов (БАЛ, ЭДТА) отмечается быстрая нормализация нарушенного метаболизма порфиринов, однако продолжительность жизни эритроцитов восстанавливается лишь после замены неполноценных эритроцитов нормальными (Wintrobe). Показатель гемоглобина нормализуется спустя несколько недель после назначения лечения. Изложенное приводит к следующему выводу большого практического значения: ряд химических веществ, оказывающих токсическое влияние на красную кровяную клетку обусловливают гемолитический эффект различными механизмами. Соединения бензола и толуола вызывают метгемоглобинемию и гемолиз, а иногда и аплазию, определяя развитие процесса относительной костномозговой недостаточности. В последнем случае анемия, хотя и представляется как результат гемолитического процесса, тем не менее не сопровождается численным ростом ретикулоцитоза. Ретикулоцитоз выявляется лишь после прекращения воздействия токсического вещества и восстановления костномозговой способности вырабатывать клетки, пропорционально интенсивности анемии. Подобно этому некоторые медикаменты, в том числе сульфонамиды, хинидин, фенацетин и пр., обусловливают расплавление крови либо посредством ферментного механизма, либо путем иммунологической агрессии. Выявление механизма, определяющего расплавление крови путем токсических веществ составляет решающий этап в процессе уточнения терапевтического подхода. Так, например, выявление телец Гейнца подсказывает мысль о возможной анемии под влиянием окисляющих метгемоглобинизирующих токсических веществ, или о наличии скрытого недостатжа Г-6-ФД и тем самым дает соответствующее направление исследованиям. – Также рекомендуем “Порфирии – история изучения, частота встречаемости, классификация” Оглавление темы “Порфирии”:
|