Распад гемоглобина в клетках
За сутки у человека распадается около 9 г гемопротеинов, в основном это гемоглобин эритроцитов.
Эритроциты в норме живут 90-120 дней, после чего лизируются в клетках ретикулоэндотелиальной системы – макрофагах селезенки (главным образом), купферовских клетках печени и макрофагах костного мозга. При разрушении эритроцитов в кровеносном русле высвобождаемый гемоглобин образует комплекс с белком-переносчиком гаптоглобином (фракция α2-глобулинов крови) и также переносится в клетки РЭС селезенки, печени и костного мозга.
Синтез билирубина
В клетках РЭС гем в составе гемоглобина окисляется молекулярным кислородом. В реакциях последовательно происходит разрыв метинового мостика между 1-м и 2-м пиррольными кольцами гема с их восстановлением, отщеплением железа и белковой части и образованием оранжевого пигмента билирубина. Высвобождаемое железо может либо запасаться в клетке в комплексе с ферритином, либо выделяться наружу и связываться с трансферрином.
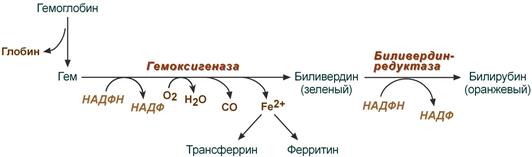
Реакции распада гемоглобина и образования билирубина
Билирубин – токсичное, жирорастворимое вещество, способное разобщать окислительное фосфорилирование в клетках. Особенно чувствительны к нему клетки нервной ткани.
Строение билирубина
Выведение билирубина
Из клеток ретикуло-эндотелиальной системы билирубин попадает в кровь. Здесь он находится в комплексе с альбумином плазмы, в гораздо меньшем количестве – в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами. Образование таких комплексов не позволяет выделяться билирубину с мочой. Билирубин в комплексе с альбумином называется свободный (неконъюгированный) или непрямой билирубин.
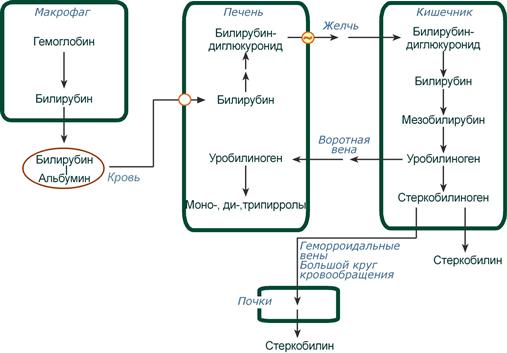
Этапы метаболизма билирубина в организме
Из сосудистого русла в гепатоциты билирубин попадает с помощью белка-переносчика (транспортный белок органических анионов) или по механизму флип-флоп. Далее при участии цитозольного связывающего белка лигандина (Y-протеин) билирубин транспортируется в ЭПР, где протекает реакция связывания билирубина с УДФ-глюкуроновой кислотой, при этом образуются моно- и диглюкурониды. Кроме глюкуроновой кислоты, в реакцию конъюгации могут вступать сульфаты, фосфаты, глюкозиды.
Билирубин-глюкуронид получил название связанный (конъюгированный) или прямой билирубин.
После образования билирубин-глюкурониды АТФ-зависимым переносчиком секретируются в желчные протоки и далее в кишечник, где при участии бактериальной β-глюкуронидазы превращаются в свободный билирубин. Одновременно, даже в норме (особенно у взрослых), некоторое количество билирубин-глюкуронидов может попадать из желчи в кровь по межклеточным щелям.
Таким образом, в плазме крови обычно присутствуют две формы билирубина: свободный (непрямой), попадающий сюда из клеток РЭС (80% и более всего количества), и связанный (прямой), попадающий из желчных протоков (в норме не более 20%).
Термины “связанный“, “конъюгированный“, “свободный“, “несвязанный” отражают взаимодействие билирубина и глюкуроновой кислоты (но не билирубина и альбумина!).
Термины “прямой” и “непрямой” введены, исходя из возможности химической реакции билирубина с диазореактивом Эрлиха. Связанный билирубин реагирует с реактивом напрямую, без добавления дополнительных реагентов, т.к. является водорастворимым. Несвязанный (жирорастворимый) билирубин требует добавочных реактивов, реагирует не прямо.
Превращение в кишечнике
В кишечнике билирубин подвергается восстановлению под действием микрофлоры до мезобилирубина и мезобилиногена (уробилиногена). Часть уробилиногена всасывается и с кровью портальной вены попадает в печень, где либо распадается до моно-, ди- и трипирролов, либо окисляется до билирубина и снова экскретируется. При этом при здоровой печени в общий круг кровообращения и в мочу мезобилирубин и уробилиноген не попадают, а полностью задерживаются гепатоцитами.
Оставшаяся в кишечнике часть пигментов ферментами бактериальной флоры толстого кишечника восстанавливается до стеркобилиногена. Далее
- малая часть стеркобилиногена может всасываться и катаболизировать в печени, подобно уробилиногену,
- незначительное количество стеркобилиногена через геморроидальные вены попадает в большой круг кровообращения, отсюда в почки и в мочу. После окисления на воздухе из стеркобилиногена образуется стеркобилин мочи,
- однако основное количество стеркобилиногена достигает нижних отделов толстого кишечника и выделяется. В прямой кишке и на воздухе стеркобилиноген окисляется в стеркобилин, окрашивая кал,
- аналогично уробилиноген, появляющийся в моче при патологии печени, окисляется в уробилин.
Очень часто стеркобилиноген, содержащийся в нормальной моче, называют уробилиногеном. И в клинической практике обычно не проводят различий между стеркобилиногеном и уробилиногеном мочи, их рассматривают как один пигмент – урохромы (уробилиноиды), что может создавать некоторую путаницу при оценке результатов анализа.
Источник
Продолжительность
жизни эритроцитов составляет 120 дней, затем они разрушаются и освобождается
гемоглобин. Главными органами, в которых происходят разрушение эритроцитов и
распад гемоглобина, являются печень, селезенка и костный мозг, хотя в принципе
оба процесса могут происходить и в клетках других органов. Распад гемоглобина в
печени начинается с разрыва α-метиновой связи между I и
II кольцами порфиринового кольца. Этот процесс катализируется НАДФ-содержащей
ок-сидазой и приводит к образованию зеленого пигмента вердоглобина
(холеглобина):
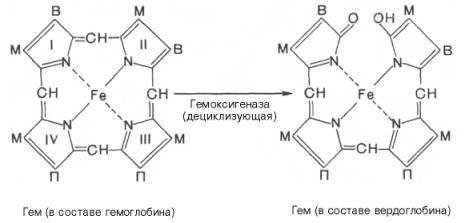
В приведенных
структурных формулах здесь и далее в желчных пигментах М – метильная СН3-группа,
В – (—СН=СН2) – винильная группа и П – (—СН2—СН2—СООН)
– остаток пропионовой кислоты.
Как видно из
приведенных формул, в молекуле вердоглобина еще сохраняются атом железа и
белковый компонент. Имеются экспериментальные доказательства, что в этом
окислительном превращении гемоглобина принимают участие витамин С, ионы Fe2+и другие кофакторы. Дальнейший распад вердоглобина, вероятнее всего, происходит
спонтанно с освобождением железа, белка-глобина и образованием одного из
желчных пигментов – биливердина. Спонтанный распад сопровождается
перераспределением двойных связей и атомов водорода в пиррольных кольцах и
метиновых мостиках. Образовавшийся биливердин ферментативным путем
восстанавливается в печени в билирубин, являющийся основным желчным пигментом у
человека и плотоядных животных:
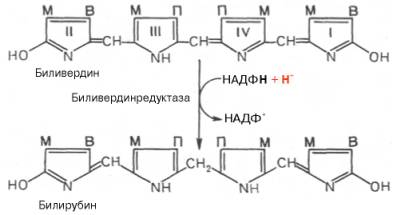
Основное
место образования билирубина – печень, селезенка и, по-видимому, эритроциты
(при распаде их иногда разрывается одна из метиновых связей в протопорфирине).
Образовавшийся во всех этих клетках билирубин поступает в печень, откуда вместе
с желчью попадает в желчный пузырь (см. главу 16). Билирубин, образовавшийся в
клетках системы макрофагов, называется свободным, или непрямым, билирубином,
поскольку вследствие плохой растворимости в воде он легко адсорбируется на
белках плазмы крови и для его определения в крови необходимо предварительное
осаждение белков спиртом. После этого билирубин вступает во взаимодействие с
диазореактивом Эрлиха.
В крови
взрослого здорового человека содержится относительно постоянное количество общего билирубина – от 4 до 26 мкмоль/л, в среднем 15 мкмоль/л.
Около 75% этого количества приходится на долю непрямого билирубина. Повышение
его концентрации в крови до 35 мкмоль/л приводит к желтухе. Более высокий
уровень билирубина в крови вызывает явления тяжелого отравления. Непрямой
билирубин, поступая с током крови в печень, подвергается обезвреживанию путем
связывания с глюку-роновой кислотой. В этом процессе принимают участие особый
фермент УДФ-глюкуронилтрансфераза и УДФ-глюкуроновая кислота, являющаяся
донором глюкуроновой кислоты. При этом к билирубину присоединяются 2 остатка
глюкуроновой кислоты с образованием сравнительно индифферентного комплекса –
билирубин-диглюкуронида, хорошо растворимого в воде и дающего прямую реакцию с
диазореактивом. В желчи всегда присутствует прямой билирубин. В крови
количество прямого и непрямого билирубина, а также соотношение между ними резко
меняются при поражениях печени, селезенки, костного мозга, болезнях крови и
т.д., поэтому определение содержания обеих форм билирубина в крови имеет
существенное значение при дифференциальной диагностике различных форм желтухи.
При желчнокаменной болезни в составе желчных камней наряду с основным их
компонентом – холестерином всегда обнаруживается непрямой билирубин. Вследствие
плохой растворимости в воде он выпадает в осадок в желчном пузыре в виде
билирубината кальция, участвующего в формировании камней.
Дальнейшая
судьба желчных пигментов, точнее билирубина, связана с их превращениями в
кишечнике под действием бактерий. Сначала глю-куроновая кислота отщепляется от
комплекса с билирубином и освободившийся билирубин подвергается восстановлению
в стеркобилиноген, который выводится из кишечника. В сутки человек выделяет
около 300 мг стеркобилиногена. Последний легко окисляется под действием света и
воздуха в стеркобилин. Механизм бактериальных превращений билирубина до
стеркобилина до конца еще не расшифрован. Имеются данные, что промежуточными
продуктами восстановления являются последовательно мезобилирубин и
мезобилиноген (уробилиноген). После всасывания небольшая часть мезобилиногена
поступает через воротную вену в печень, где подвергается разрушению с образованием
моно- и дипиррольных соединений. Кроме того, очень небольшая часть
стеркобилиногена после всасывания через систему геморроидальных вен попадает в
большой круг кровообращения, минуя печень, и в таком виде выводится с мочой.
Однако называть его уробилиногеном не совсем точно (см. главу 18). Суточное
содержание стеркобилиногена в моче составляет около 4 мг, и, пожалуй, именно
стеркобилиноген является нормальной органической составной частью мочи. Если с
мочой выделяется повышенное содержание уробилиногена (точнее, мезобилиногена),
то это является свидетельством недостаточности функции печени, например, при
печеночной или гемолитической желтухе, когда печень частично теряет способность
извлекать этот пигмент из крови воротной вены. Химически уробилиноген
(мезо-билиноген) неидентичен стеркобилиногену (уробилиногену) мочи.
Исчезновение стеркобилиногена (уробилиногена) из мочи при наличии билирубина и
биливердина является свидетельством полного прекращения поступления желчи в
кишечник. Такое состояние часто наблюдается при закупорке протока желчного
пузыря (желчнокаменная болезнь) или общего желчного протока (желчнокаменная
болезнь, раковые поражения поджелудочной железы и др.).
Таким
образом, количественный и качественный анализ желчных пигментов в моче может
представлять большой клинический интерес.
Источник
Разрушение гемоглобина. Разновидности анемий
При разрыве эритроцитов их гемоглобин почти сразу же фагоцитируется макрофагами во многих частях тела, но особенно клетками Купфера печени и макрофагами селезенки и костного мозга. В течение нескольких следующих часов или дней макрофаги освобождают железо из гемоглобина, и оно возвращается в кровь и переносится трансферрином либо в костный мозг для формирования новых красных клеток крови, либо в печень и другие ткани для хранения в форме ферритина.
Порфириновая часть молекулы гемоглобина превращается макрофагами через ряд стадий в желчный пигмент билирубин, который выделяется в кровь и позднее удаляется из организма путем секреции печенью в желчь.
Анемии
Анемия означает недостаток гемоглобина в крови, причиной может быть либо слишком малое число красных клеток крови, либо слишком малое количество гемоглобина в этих клетках. Далее представлены некоторые типы анемий и их физиологические причины.
а) Анемия, связанная с потерей крови. После острой кровопотери организм возмещает жидкую часть плазмы в течение 1-3 сут, но при этом концентрация красных клеток крови остается низкой. Концентрация эритроцитов обычно восстанавливается до нормы в течение 3-6 нед, если не происходит повторного кровотечения.
Часто при хронической кровопотере у человека железо из кишечника не может всасываться достаточно быстро, чтобы обеспечить адекватное возмещение теряемого с кровью гемоглобина. Формируемые в этом случае красные клетки крови гораздо мельче нормальных эритроцитов и содержат слишком мало гемоглобина, что характерно для микроцитарной гипохромной анемии; такие эритроциты показаны на рисунке.
б) Апластическая анемия. Аплазия костного мозга означает потерю функционирующего костного мозга. Например, у человека, подвергшегося облучению гамма-лучами при взрыве атомной бомбы, может произойти полное разрушение костного мозга с последующим развитием в течение нескольких недель летальной анемии. Тот же эффект могут вызвать избыточная рентгенотерапия, некоторые промышленные химикаты и даже лекарства, к которым у человека может быть повышенная чувствительность.
в) Мегалобластная анемия. На основании изложенного ранее обсуждения роли витамина B12, фолиевой кислоты и внутреннего фактора, секретируемого слизистой желудка, легко понять, что недостаток любого из этих веществ может привести к замедлению репродукции эритроцитов в костном мозге. В результате формируются слишком крупные красные клетки крови разнообразной формы, которые называют мегалобластами.
Следовательно, атрофия слизистой желудка, например при пернициозной анемии, или потеря всего желудка после хирургической тотальной гастрэктомии могут привести к мегалобластной анемии. Мегалобластная анемия часто развивается также у больных с кишечной спру, при которой плохо всасываются фолиевая кислота, витамин B12 и другие соединения витаминов группы В. Поскольку при этих состояниях эритробласты не могут пролиферировать достаточно быстро, чтобы формировать нормальное количество красных клеток крови, те эритроциты, которые формируются, по большей части увеличены в размерах, имеют неправильную форму и ломкие мембраны. Эти клетки легко рвутся, оставляя человека без необходимого количества красных клеток крови.
г) Гемолитическая анемия. Различные аномалии красных клеток крови, многие из которых — наследственные, делают клетки столь хрупкими, что они легко разрываются, проходя через капилляры, особенно в селезенке. Даже если количество формируемых красных клеток крови в норме или значительно ее превышает, как при некоторых гемолитических болезнях, срок жизни хрупкого эритроцита так короток, что клетки разрушаются быстрее, чем могут формироваться нормальные эритроциты; результатом этого является тяжелая анемия. Далее указаны некоторые из таких типов анемий.
При наследственном сфероцитозе красные клетки крови очень мелкие и сферические, а не двояковогнутые диски. Эти клетки не могут выдерживать сдавливания, поскольку не имеют нормальной свободной, мешкообразной клеточной мембраны, характерной для двояковогнутых дисков. При прохождении через пульпу селезенки и некоторые другие сосудистые ложа они легко ломаются даже при небольшом сдавливании.
При серповидно-клеточной анемии, которой болеют 0,3-1,0% коренных жителей Западной Африки, красные клетки крови содержат аномальный гемоглобин — гемоглобин S с поврежденными цепочками в его молекуле. Под действием низких концентраций кислорода такой гемоглобин осаждается в виде длинных кристаллов внутри эритроцита. Эти кристаллы удлиняют клетку и придают ей вид серпа, а не двояковогнутого диска.
Кроме того, осажденный гемоглобин повреждает клеточную мембрану, в результате клетка становится очень хрупкой, что сопровождается тяжелой анемией. Такие больные часто переживают порочный круг событий, называемый кризисом серповидно-клеточной болезни, при котором низкое напряжение кислорода в тканях вызывает образование серповидных форм эритроцитов, что ведет к разрушению красных клеток крови, а значит — к дальнейшему снижению напряжения кислорода, усилению образования серповидных форм и разрушению красных клеток крови. Сразу после начала процесс быстро прогрессирует, приводя в течение нескольких часов к резкому снижению числа красных клеток крови и часто — к смерти.
При гемолитической болезни новорожденных (эритробластозе) антитела от резус-отрицательной (Rh-) матери атакуют резус-положительные (Rh+) эритроциты плода. В результате резус-положительные клетки становятся ломкими, что ведет к их быстрому разрушению, способствуя развитию у новорожденного тяжелой анемии. Чрезвычайно быстрое формирование новых эритроцитов для возмещения разрушенных при гемолитической болезни новорожденных ведет к выделению в кровь из костного мозга большого количества молодых бластных форм красных клеток крови.
– Также рекомендуем “Влияние анемии на кровообращение. Полицитемия – эритремия”
Оглавление темы “Эритропоэз. Белые клетки крови”:
1. Влияние эритропоэтина на эритрогенез. Витамин В12 и фолиевая кислота в эритропоэзе
2. Пернициозная анемия. Образование гемоглобина
3. Связывание гемоглобина с кислородом. Обмен железа
4. Всасывание железа в кишечнике. Длительность жизни эритроцитов
5. Разрушение гемоглобина. Разновидности анемий
6. Влияние анемии на кровообращение. Полицитемия – эритремия
7. Влияние полицитемии на кровообращение. Лейкоциты – белые клетки крови
8. Типы белых клеток крови. Происхождение белых клеток крови
9. Длительность жизни белых клеток крови. Нейтрофилы и макрофаги
10. Фагоцитоз. Механизмы и значение фагоцитоза
Источник
В организме здорового человека с массой тела 70 кг каждый час разрушается около 1-2х108 эритроцитов, что, в перерасчете на массу гемоглобина, подвергающегося распаду, составляет, примерно, 6 г гемоглобина в сутки. Белковая часть гемоглобина разрушается до аминокислот, которые вновь используются клетками для синтеза белков. Катионы железа гема пополняют запасы железа в составе белка печени ферритина, а порфириновое кольцо гема разрушается до специальных продуктов – желчных пигментов (биливердин, билирубины и пигменты, образующиеся из билирубина в кишечнике).
Билирубин IXa
Билирубина диглюкуронид
Рис.19. Структура токсичного билирубина IXa и нетоксичного диглюкуронида билирубина.
Распад гемоглобина начинается, преимущественно, в клетках Купфера (печень) и клетках ретикулоэндотелиальной системы (РЭС) селезёнки (схема 3). Формирование промежуточных метаболитов распада гемоглобина (вердоглобин, биливердин, билирубин IXa) может происходить как в печени, так и в других органах, прежде всего в селезенке (схема 3), а конъюгация билирубина (образование диглюкуронида – только в гепатоцитах (схема 4)).
В качестве дополнительных источников билирубина выступают многочисленные гемопротеины, содержащиеся в значительных количествах во всех клетках тканей внутренних органов. Среди них особое место занимает белок скелетной мускулатуры и миокарда миоглобин, а также цитохромы.
Процесс превращения свободного (непрямого) билирубина, образующегося при разрушении эритроцитов и распаде гемоглобина в органах ретикулоэндотелиальной системы, в связанный, конъюгированный или прямой билирубин(билирубина диглюкуронид) в гепатоците (рис.20) осуществляется в три этапа (на рис.20 обозначены римскими цифрами):
I этап — захват билирубина (Б) печеночной клеткой после отщепления альбумина;
II этап — образование водорастворимого комплекса билирубин-диглюкуронида (Б-Г);
III этап— выделение образовавшегося связанного (прямого) билирубина (Б-Г) из печеночной клетки в желчные протоки.
Рис. 20. Функция гепатоцита в формировании и секреции прямого билирубина. Бн – свободный (непрямой) билирубин; Б-Г – билирубин-глюкуронид (связанный, или прямой билирубин); Мбг – мезобилиноген (уробилиноген).
Схема 3. Образование неконьюгированного (непрямого) билирубина.
Схема 4. Конъюгация билирубина в паренхиме печени.
В качестве источника глюкуроновой кислоты в этой реакции используется УДФ-глюкуроновая кислота:
Фермент УДФ-глюкуронилтрансфераза, подобно другим энзимам печени, подвергается индукции некоторыми ксенобиотиками. К таковым относятся в частности, широко используемые в клинической практике препараты барбитурового ряда (снотворные и седативные), некоторые противосудорожные препараты других фармакологических групп, транквилизаторы и пр.
В отличие от свободного билирубина, его конъюгированная форма хорошо растворима в воде. Конъюгаты билирубина, преимущественно в форме диглюкуронидов (до 75%), выделяются в желчь. При этом их транспорт направлен в сторону большей концентрации, т.е. против концентрационного градиента. Он обеспечивается специальной энергозависимой системой активного транспорта, встроенной в клеточную мембрану гепатоцитов. Дальнейший метаболизм билирубина связан с поступлением его в желчные пути и кишечник. В нижних отделах желчевыводящих путей и тонком кишечнике под воздействием микрофлоры происходит постепенное восстановление билирубина до мезобилиногена. Часть мезобилиногена. всасывается в кишечнике (уробилиноген) и по системе воротной вены вновь попадает в печень, где в норме происходит практически полное его разрушение до пирролов (схема 5).
Основное количество мезобилиногена из тонкой кишки поступает в толстую и здесь восстанавливается до стеркобилиногена при участии анаэробной микрофлоры (схема 5). Образовавшийся стеркобилиноген в нижних отделах толстой кишки (в основном в прямой кишке) окисляется до стеркобилина и выделяется с калом, определяя его окраску у здоровых людей. Лишь небольшая часть стеркобилиногена через геморроидальные вены попадает в систему нижней полой вены и в дальнейшем выводится с мочой (схема 5). Следовательно, в норме моча человека содержит лишь следы стеркобилиногена, не выявляющиеся клиническими лабораторными методами (за сутки его выделяется до 4 мг). К сожалению, до последнего времени в клинической практике стеркобилиноген, содержащийся в нормальной моче, продолжают называть уробилиногеном.
Схема 5. Превращение билирубина в кишечнике с образованием конечных продуктов в моче и кале.
При диагностике патологий пигментного обмена визуально оценивается интенсивность окраски мочи и кала больных, проводится количественное определение билирубинов (прямого, непрямого, общего) в плазме или сыворотке крови и уробилиногена в моче, иногда количественно определяется стеркобилин кала. При патологиях, сопровождающихся снижением концентрации эритроцитов (анемиях различной этиологии возникновения), обязятельным тестом является определение концентрации гемоглобина, и в качестве дополнительных, концентрация железа в крови человека.
Источник
