Распад гемоглобина в крови
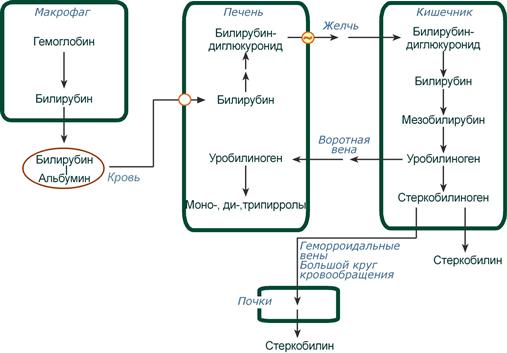
За сутки у человека распадается около 9 г гемопротеинов, в основном это гемоглобин эритроцитов.
Эритроциты в норме живут 90-120 дней, после чего лизируются в клетках ретикулоэндотелиальной системы – макрофагах селезенки (главным образом), купферовских клетках печени и макрофагах костного мозга. При разрушении эритроцитов в кровеносном русле высвобождаемый гемоглобин образует комплекс с белком-переносчиком гаптоглобином (фракция α2-глобулинов крови) и также переносится в клетки РЭС селезенки, печени и костного мозга.
Синтез билирубина
В клетках РЭС гем в составе гемоглобина окисляется молекулярным кислородом. В реакциях последовательно происходит разрыв метинового мостика между 1-м и 2-м пиррольными кольцами гема с их восстановлением, отщеплением железа и белковой части и образованием оранжевого пигмента билирубина. Высвобождаемое железо может либо запасаться в клетке в комплексе с ферритином, либо выделяться наружу и связываться с трансферрином.
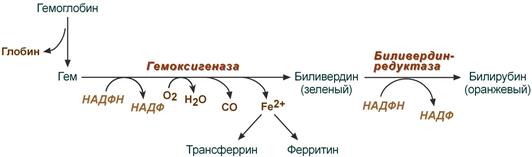
Реакции распада гемоглобина и образования билирубина
Билирубин – токсичное, жирорастворимое вещество, способное разобщать окислительное фосфорилирование в клетках. Особенно чувствительны к нему клетки нервной ткани.
Строение билирубина
Выведение билирубина
Из клеток ретикуло-эндотелиальной системы билирубин попадает в кровь. Здесь он находится в комплексе с альбумином плазмы, в гораздо меньшем количестве – в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами. Образование таких комплексов не позволяет выделяться билирубину с мочой. Билирубин в комплексе с альбумином называется свободный (неконъюгированный) или непрямой билирубин.

Этапы метаболизма билирубина в организме
Из сосудистого русла в гепатоциты билирубин попадает с помощью белка-переносчика (транспортный белок органических анионов) или по механизму флип-флоп. Далее при участии цитозольного связывающего белка лигандина (Y-протеин) билирубин транспортируется в ЭПР, где протекает реакция связывания билирубина с УДФ-глюкуроновой кислотой, при этом образуются моно- и диглюкурониды. Кроме глюкуроновой кислоты, в реакцию конъюгации могут вступать сульфаты, фосфаты, глюкозиды.
Билирубин-глюкуронид получил название связанный (конъюгированный) или прямой билирубин.
После образования билирубин-глюкурониды АТФ-зависимым переносчиком секретируются в желчные протоки и далее в кишечник, где при участии бактериальной β-глюкуронидазы превращаются в свободный билирубин. Одновременно, даже в норме (особенно у взрослых), некоторое количество билирубин-глюкуронидов может попадать из желчи в кровь по межклеточным щелям.
Таким образом, в плазме крови обычно присутствуют две формы билирубина: свободный (непрямой), попадающий сюда из клеток РЭС (80% и более всего количества), и связанный (прямой), попадающий из желчных протоков (в норме не более 20%).
Термины “связанный“, “конъюгированный“, “свободный“, “несвязанный” отражают взаимодействие билирубина и глюкуроновой кислоты (но не билирубина и альбумина!).
Термины “прямой” и “непрямой” введены, исходя из возможности химической реакции билирубина с диазореактивом Эрлиха. Связанный билирубин реагирует с реактивом напрямую, без добавления дополнительных реагентов, т.к. является водорастворимым. Несвязанный (жирорастворимый) билирубин требует добавочных реактивов, реагирует не прямо.
Превращение в кишечнике
В кишечнике билирубин подвергается восстановлению под действием микрофлоры до мезобилирубина и мезобилиногена (уробилиногена). Часть уробилиногена всасывается и с кровью портальной вены попадает в печень, где либо распадается до моно-, ди- и трипирролов, либо окисляется до билирубина и снова экскретируется. При этом при здоровой печени в общий круг кровообращения и в мочу мезобилирубин и уробилиноген не попадают, а полностью задерживаются гепатоцитами.
Оставшаяся в кишечнике часть пигментов ферментами бактериальной флоры толстого кишечника восстанавливается до стеркобилиногена. Далее
- малая часть стеркобилиногена может всасываться и катаболизировать в печени, подобно уробилиногену,
- незначительное количество стеркобилиногена через геморроидальные вены попадает в большой круг кровообращения, отсюда в почки и в мочу. После окисления на воздухе из стеркобилиногена образуется стеркобилин мочи,
- однако основное количество стеркобилиногена достигает нижних отделов толстого кишечника и выделяется. В прямой кишке и на воздухе стеркобилиноген окисляется в стеркобилин, окрашивая кал,
- аналогично уробилиноген, появляющийся в моче при патологии печени, окисляется в уробилин.
Очень часто стеркобилиноген, содержащийся в нормальной моче, называют уробилиногеном. И в клинической практике обычно не проводят различий между стеркобилиногеном и уробилиногеном мочи, их рассматривают как один пигмент – урохромы (уробилиноиды), что может создавать некоторую путаницу при оценке результатов анализа.
Распад гемоглобина может влиять на функционирование печени человека. В чем же тут может быть опасность для пациента?
Организм человека – сложная саморегулирующаяся система, которая для достижения оптимальных условий работы и существования сама себе помогает.
Вся работа тканей и органов держится на активных обменных процессах, проходящих в них. Основной связывающей средой между ними является кровь. С ее помощью происходит насыщение тканей кислородом, поступающим от легких. Взамен кровь транспортирует от клеток продукты их жизнедеятельности и образованный углекислый газ.
Молекулы в организме человека
В крови содержится довольно много молекул, обеспечивающих подобный транспорт. Главной из них является молекула гемоглобина, основная функция которой – доставка кислорода и удаление СО2.
Гемоглобин – сложная молекула, состоящая из двух больших, двух малых белковых субъединиц и находящегося между ними и связывающего их в единую молекулу атома железа.
В огромном количестве гемоглобин находится в эритроцитах – красных кровяных клетках, отвечающих за транспортную функцию. Чем эритроцитов больше, тем обычно больше гемоглобина.
Как и любая структура организма, эритроциты не вечны. После образования их в костном мозгу, они покидают его, некоторое время циркулируют по кровотоку и спустя определенное время (средняя продолжительность жизни эритроцита составляет около 120 дней) они попадают в селезенку, где проходит утилизация изношенных или поврежденных эритроцитов с их последующим распадом.
Частичный распад эритроцитов происходит и в кровяном русле.
Расшифровка схемы
В результате, чтобы не терять имеющееся в организме железо, старые эритроциты расщепляются на более простые структуры, которые впоследствии принимают участие в образовании новых эритроцитов. Процесс их образования довольно сложен. Он включает в себя достаточно большое количество стадий и для его протекания необходимо очень много вспомогательных веществ.
Соответственно, если разрушается эритроцит, то происходит и распад содержащегося в нем гемоглобина. Схема распада данного белка следующая:
- Под воздействием кислорода и молекулы, осуществляющей транспортировку протонов водорода, происходит превращение гемоглобина в вердоглобин (если изучать данный процесс под контролем зрения, можно заметить, что происходит смена цвета (гемоглобин дает красную окраску, в то время как вердоглобин окрашивает все в зеленый цвет)).
- В последующих реакциях происходит отщепление атома двухвалентного железа, которое после используется для синтеза нового гема, и белковых субъединиц, которые последовательно распадаются до аминокислот и в дальнейшем используются для синтеза новых белков. В результате от молекулы гемоглобина остается только одно вещество – биливердин. Гем при помощи белка-трансферрина переносится в печень, где находится депо железа. Оно используется в дальнейшем как для повторного синтеза молекулы гемоглобина, так и новых молекул.
- Воздействуя на биливердин специальным ферментом – редуктазой, происходит превращение его в новую молекулу – билирубин, который, в свою очередь, дает оранжевую окраску.
Данное вещество является достаточно токсичным и при большом количестве его в кровотоке приводит к развитию различных состояний, таких как желтуха. В тяжелых случаях может приводить к поражению нервной системы и развитию печеночной комы.
Оно используется в основном для синтеза желчных кислот в печени, поэтому после его образования дальнейшая схема утилизации гемоглобина может идти в двух направлениях.
Первое из них основывается на реакции конъюгации.
В крови билирубин может содержаться в трех формах – чистый билирубин, не связанный ни с одной молекулой, свободный, связанный преимущественно с альбуминами крови, и несвободный, или конъюгированный, составляющий комплекс билирубина с глюкуроновой кислотой.
Реакция конъюгации билирубина происходит преимущественно в печени.
Оттуда связанный с глюкуроновой кислотой билирубин попадает по системе желчных протоков в кишечник, где происходит дальнейшее превращение данной молекулы.
Некоторая часть уробилиногена всасывается в кровь и транспортируется с ее током в печень, где происходит образование сложных спиртов, необходимых для некоторых реакций метаболизма.
Большая же часть оставшегося в кишечнике уробилиногена под действием ферментов и пигментных молекул микроорганизмов окисляется до стеркобилиногена, придающего окраску калу и выводящегося с ним.
Малая часть стеркобилиногена по системе вен прямой кишки (кровоток от которой осуществляется по широко развитой системе геморроидальных вен) всасывается в кровь и транспортируется к почкам. В них происходит выделение стеркобилиногена с током мочи. Во внешней среде, за счет реакции с атомами кислорода, стеркобилиноген превращается в уробилин и стеркобилин, которые придают моче характерный цвет.
Таким образом выглядит схема реакции распада молекулы гемоглобина.
Искусственный метод распада гемоглобина
Все данные реакции протекают в крови под воздействием эндогенных ферментов. Подобную схему распада гемоглобина можно спроектировать и в лабораторных условиях, чтобы получить более наглядное представление о протекании данной реакции.
Как было сказано выше, эритроциты подвергаются разрушению с целью их повторного использования в дальнейшем. Данный механизм осуществляется по принципу физиологической смерти клеток, однако есть еще один механизм, вызывающий распад эритроцитов и образование желчных пигментов.
Данный механизм носит название апоптоза и активируется обычно в случае несостоятельности эритроцитов или ошибок во время их синтеза.
Схема распада эритроцита и гемоглобина, если имеет место нарушение синтеза, ничем не отличается от таковой как при физиологической утилизации. Единственным нюансом является то, что часть клеток распадается непосредственно в селезенке, а другая – в кровяном русле. Существенным изменениям молекула билирубина не подвергается, однако за счет наличия в крови огромного количества ионов, иных молекул и клеток системы крови реакция расщепления может пойти несколько непредсказуемо.
Если иммунная система организма в норме, подобный внутрисосудистый распад гемоглобина обычно никак не сказывается на состоянии здоровья человека. Если же имеются и какие-либо нарушения в работе системы иммунитета, то реакция может пойти несколько непредсказуемо, и сложно предугадать ее последствия.
Для чего же следует знать схему распада молекулы гемоглобина
Дело в том, что в норме в крови содержится определенное количество желчных пигментов. При развитии того или иного патологического процесса, который может проходить как в печени, так и селезенке, показатели билирубина могут значительно меняться и изменяться. При увеличении их количества судят о либо повышенной активности клеток крови и селезенки, либо же о значительных проблемах с печенью. Если такое поражение пустить на самотек и своевременно не обратиться к врачу, состояние может привести к летальному исходу или развитию печеночной комы.
Увеличение количества непрямого билирубина обычно является провоцирующим фактором развития желчнокаменной болезни, которая чаще всего приводит к нарушению работы пищеварительной системы, но может проявить себя и в виде ургентного состояния (печеночная колика).
Снижение же продуктов распада гемоглобина в крови говорит о нарушении работы транспортных систем организма или же о несостоятельности костного мозга, что может говорить за развитие онкологического процесса.
Любое увеличение количества билирубина чаще всего проявляется в виде желтухи, поэтому уже на стадии осмотра пациента можно заподозрить имеющиеся метаболические нарушения.
Именно поэтому крайне важно знать о возможных изменениях количества гемоглобина в крови и уметь правильно распознать имеющуюся патологию.
https://www.youtube.com/watch?v=Kr_vZTauVlc
Для определения количества данных веществ назначается специальный анализ – биохимия крови. Исследование количества гемоглобина и билирубина проводится в лабораториях специально обученным персоналом. На основании полученных ими данных удается сделать вывод об имеющихся нарушениях и предпринять соответствующие меры.
Разрушение гемоглобина. Разновидности анемий
При разрыве эритроцитов их гемоглобин почти сразу же фагоцитируется макрофагами во многих частях тела, но особенно клетками Купфера печени и макрофагами селезенки и костного мозга. В течение нескольких следующих часов или дней макрофаги освобождают железо из гемоглобина, и оно возвращается в кровь и переносится трансферрином либо в костный мозг для формирования новых красных клеток крови, либо в печень и другие ткани для хранения в форме ферритина.
Порфириновая часть молекулы гемоглобина превращается макрофагами через ряд стадий в желчный пигмент билирубин, который выделяется в кровь и позднее удаляется из организма путем секреции печенью в желчь.
Анемии
Анемия означает недостаток гемоглобина в крови, причиной может быть либо слишком малое число красных клеток крови, либо слишком малое количество гемоглобина в этих клетках. Далее представлены некоторые типы анемий и их физиологические причины.
а) Анемия, связанная с потерей крови. После острой кровопотери организм возмещает жидкую часть плазмы в течение 1-3 сут, но при этом концентрация красных клеток крови остается низкой. Концентрация эритроцитов обычно восстанавливается до нормы в течение 3-6 нед, если не происходит повторного кровотечения.
Часто при хронической кровопотере у человека железо из кишечника не может всасываться достаточно быстро, чтобы обеспечить адекватное возмещение теряемого с кровью гемоглобина. Формируемые в этом случае красные клетки крови гораздо мельче нормальных эритроцитов и содержат слишком мало гемоглобина, что характерно для микроцитарной гипохромной анемии; такие эритроциты показаны на рисунке.
б) Апластическая анемия. Аплазия костного мозга означает потерю функционирующего костного мозга. Например, у человека, подвергшегося облучению гамма-лучами при взрыве атомной бомбы, может произойти полное разрушение костного мозга с последующим развитием в течение нескольких недель летальной анемии. Тот же эффект могут вызвать избыточная рентгенотерапия, некоторые промышленные химикаты и даже лекарства, к которым у человека может быть повышенная чувствительность.
в) Мегалобластная анемия. На основании изложенного ранее обсуждения роли витамина B12, фолиевой кислоты и внутреннего фактора, секретируемого слизистой желудка, легко понять, что недостаток любого из этих веществ может привести к замедлению репродукции эритроцитов в костном мозге. В результате формируются слишком крупные красные клетки крови разнообразной формы, которые называют мегалобластами.
Следовательно, атрофия слизистой желудка, например при пернициозной анемии, или потеря всего желудка после хирургической тотальной гастрэктомии могут привести к мегалобластной анемии. Мегалобластная анемия часто развивается также у больных с кишечной спру, при которой плохо всасываются фолиевая кислота, витамин B12 и другие соединения витаминов группы В. Поскольку при этих состояниях эритробласты не могут пролиферировать достаточно быстро, чтобы формировать нормальное количество красных клеток крови, те эритроциты, которые формируются, по большей части увеличены в размерах, имеют неправильную форму и ломкие мембраны. Эти клетки легко рвутся, оставляя человека без необходимого количества красных клеток крови.
г) Гемолитическая анемия. Различные аномалии красных клеток крови, многие из которых — наследственные, делают клетки столь хрупкими, что они легко разрываются, проходя через капилляры, особенно в селезенке. Даже если количество формируемых красных клеток крови в норме или значительно ее превышает, как при некоторых гемолитических болезнях, срок жизни хрупкого эритроцита так короток, что клетки разрушаются быстрее, чем могут формироваться нормальные эритроциты; результатом этого является тяжелая анемия. Далее указаны некоторые из таких типов анемий.
При наследственном сфероцитозе красные клетки крови очень мелкие и сферические, а не двояковогнутые диски. Эти клетки не могут выдерживать сдавливания, поскольку не имеют нормальной свободной, мешкообразной клеточной мембраны, характерной для двояковогнутых дисков. При прохождении через пульпу селезенки и некоторые другие сосудистые ложа они легко ломаются даже при небольшом сдавливании.
При серповидно-клеточной анемии, которой болеют 0,3-1,0% коренных жителей Западной Африки, красные клетки крови содержат аномальный гемоглобин — гемоглобин S с поврежденными цепочками в его молекуле. Под действием низких концентраций кислорода такой гемоглобин осаждается в виде длинных кристаллов внутри эритроцита. Эти кристаллы удлиняют клетку и придают ей вид серпа, а не двояковогнутого диска.
Кроме того, осажденный гемоглобин повреждает клеточную мембрану, в результате клетка становится очень хрупкой, что сопровождается тяжелой анемией. Такие больные часто переживают порочный круг событий, называемый кризисом серповидно-клеточной болезни, при котором низкое напряжение кислорода в тканях вызывает образование серповидных форм эритроцитов, что ведет к разрушению красных клеток крови, а значит — к дальнейшему снижению напряжения кислорода, усилению образования серповидных форм и разрушению красных клеток крови. Сразу после начала процесс быстро прогрессирует, приводя в течение нескольких часов к резкому снижению числа красных клеток крови и часто — к смерти.
При гемолитической болезни новорожденных (эритробластозе) антитела от резус-отрицательной (Rh-) матери атакуют резус-положительные (Rh+) эритроциты плода. В результате резус-положительные клетки становятся ломкими, что ведет к их быстрому разрушению, способствуя развитию у новорожденного тяжелой анемии. Чрезвычайно быстрое формирование новых эритроцитов для возмещения разрушенных при гемолитической болезни новорожденных ведет к выделению в кровь из костного мозга большого количества молодых бластных форм красных клеток крови.
– Также рекомендуем “Влияние анемии на кровообращение. Полицитемия – эритремия”
Оглавление темы “Эритропоэз. Белые клетки крови”:
1. Влияние эритропоэтина на эритрогенез. Витамин В12 и фолиевая кислота в эритропоэзе
2. Пернициозная анемия. Образование гемоглобина
3. Связывание гемоглобина с кислородом. Обмен железа
4. Всасывание железа в кишечнике. Длительность жизни эритроцитов
5. Разрушение гемоглобина. Разновидности анемий
6. Влияние анемии на кровообращение. Полицитемия – эритремия
7. Влияние полицитемии на кровообращение. Лейкоциты – белые клетки крови
8. Типы белых клеток крови. Происхождение белых клеток крови
9. Длительность жизни белых клеток крови. Нейтрофилы и макрофаги
10. Фагоцитоз. Механизмы и значение фагоцитоза
