Рекомендации воз лечение анемии
Анемии — группа заболеваний, характеризующихся уменьшением гемоглобина и (или) количества циркулирующих эритроцитов в единице объема крови ниже нормального для данного возраста и пола.
Диагностика анемии основывается главным образом на данных лабораторных исследований, в первую очередь на результатах клинического исследования крови с определением концентрации гемоглобина.
Согласно рекомендациям ВОЗ, критерием анемии для детей является снижение концентрации гемоглобина до уровня менее 110 г/л, для женщин – менее 120 г/л (во время беременности – менее 110 г/л), для мужчин – менее 130 г/л.
По степени тяжести различают анемию легкую (уровень гемоглобина крови выше 90 г/л), средней тяжести (гемоглобин – 70–89 г/л) и тяжелую (гемоглобин менее 70 г/л).
Наиболее часто (80–95 % всех анемий) в терапевтической практике встречается хроническая железодефицитная анемия (ЖДА) — болезненное состояние, обусловленное нарушением синтеза гемоглобина вследствие дефицита железа.
По статистике ВОЗ, в мире около 2 млрд человек страдают в той или иной форме дефицитом железа, большинство из них женщины и дети. Частота ЖДА у беременных в мире колеблется от 25 до 50%, в развивающихся странах – от 35 до 75%, а в развитых составляет 18–20%. В МКБ-10 соответствует рубрике D50 — железодефицитная анемия.
Некоторые особенности обмена железа в организме
У мужчин с пищей поступает около 18 мг Fe в сутки, всасывается 1,0–1,5 мг, теряется Fe с мочой, калом, потом, эпителием кожи и кишечника. У женщин с пищей поступает 12–15 мг Fe в сутки, всасывается 1,0–1,3 мг, теряется Fe с мочой, калом, потом, эпителием кожи и кишечника, волосами, ногтями, во время менструального цикла, беременности и лактации. Во время менструального периода потери составляют 20–30 мг, при беременности, родах и лактации до 700–800 мг.
При повышении потребности организма в железе из пищи может всосаться не более 2,0–2,5 мг. Если потеря организмом Fe составляет более 2 мг/сут., после того как истощаются депо, развивается железодефицитная анемия.
К основным причинам развития ЖДА относят:
- Алиментарную недостаточность
Недостаточное поступление железа с пищей, в основном за счет нехватки мясных продуктов (например, при голодании, вегетарианстве), не позволяет восполнить его потери, возникающие вследствие разрушения эритроцитов.
- Нарушение всасывания железа
Развивается у пациентов с энтеритами различного генеза, синдромом мальабсорбции, послеоперационными состояниями (резекция желудка с выключением двенадцатиперстной кишки, резекция тонкой кишки), а также связано с приемом лекарственных препаратов, угнетающих всасывание железа.
- Повышенную потребность в железе
Как правило, обусловлена беременностью, лактацией, интенсивным ростом в пубертатный период, возникает в предклимактерический период и при лечении макроцитарной (В12-дефицитной) анемии витамином В12.
- Хронические кровопотери различной локализации
Хроническая кровопотеря обусловлена желудочно-кишечными (при рефлюкс-эзофагите, эрозивно-язвенных заболеваниях желудка, опухолях желудка и толстой кишки, болезни Крона, неспецифическом язвенном колите, дивертикулитах, кровоточащем геморрое), маточными (включая обильные менструации), носовыми, почечными (при гломерулонефрите, мочекаменной болезни, опухолях), десневыми, в замкнутые полости и ткани (изолированный легочный гемосидероз, внематочный эндометриоз) кровотечениями.
Наиболее распространена постгеморрагическая железодефицитная анемия при кровопотерях из ЖКТ. Эти кровопотери – самая частая причина дефицита железа у мужчин и вторая по частоте у женщин.
- Нарушение транспорта железа (гипопротеинемии различного генеза)
Основным патогенетическим механизмом развития ЖДА является недостаток в организме железа – основного строительного материала для построения молекул гемоглобина, в частности его железосодержащей части – гема.
Клинические проявления дефицита Fe манифестируют после длительного латентного периода, соответствующего истощению запасов Fe в организме. Выраженность симптомов может быть различна и зависит от причины, скорости кровопотери, пола и возраста пациента. Тяжесть состояния обусловлена снижением кислородсвязывающей емкости крови и тканевым дефицитом железа.
Анемический синдром обусловлен тканевой гипоксией, его проявления универсальны для всех видов анемий:
- слабость и/или быстрая утомляемость;
- бледность кожи и слизистых;
- головная боль и/или пульсация в висках;
- головокружение, обмороки;
- одышка и сердцебиение при привычной физической нагрузке;
- усиление ангинозных болей при ИБС;
- снижение толерантности к физической нагрузке;
- появление резистентности к проводимой терапии вазодилататорами при ИБС.
Сидеропенический синдром обусловлен тканевым дефицитом Fe и свойственен только ЖДА. Основные проявления:
- сухость кожи, трещины на поверхности кожи рук и ног, в углах рта (ангулярный стоматит);
- глоссит, сопровождающийся атрофией сосочков, болезненностью и покраснением языка;
- ломкость, истончение, расслоение ногтей, ногти ложкообразной формы (койлонихия);
- выпадение волос и раннее их поседение;
- извращение вкуса (pica chlorotica): пациенты едят мел, уголь, глину, песок и/или сырые продукты (крупы, фарш, тесто);
- пристрастие к необычным запахам (керосина, мазута, бензина, ацетона, гуталина, нафталина, выхлопных газов машин), которое полностью проходит на фоне приема препаратов Fe;
- дисфагия (затруднение глотания твердой и сухой пищи).
Синдром вторичного иммунодефицита — склонность к частым рецидивам и хронизации инфекционно-воспалительных заболеваний.
Висцеральный синдром включает:
- поражение желудочно-кишечного тракта (глоссит, дисфагия, снижение кислотообразующей функции желудка, суб- и атрофический гастрит, вздутие, запор, диарея);
- поражение гепатобилиарной системы (жировой гепатоз, дисфункциональные расстройства билиарного тракта);
- изменения сердечно-сосудистой системы (одышка, тахикардия, кардиалгия, отеки на ногах, ангинозные боли, гипотония, расширение границ сердца влево, наличие приглушенности тонов сердца и систолического шума на верхушке, возможно снижение зубца Т и депрессия сегмента ST на ЭКГ);
- поражение ЦНС (снижение памяти и способности концентрировать внимание);
- поражение мышечного каркаса и сфинктеров (мышечная слабость при обычной нагрузке, смешанное недержание мочи при отсутствии изменений в анализах мочи).
Кожа у пациентов с ЖДА бледная, не желтушная; печень, селезенка и периферические лимфатические узлы не увеличены. При ювенильном хлорозе склеры, а иногда и кожа приобретают голубоватый оттенок. Такие пациенты плохо загорают на солнце; девушки нередко инфантильны, у них часто наблюдаются расстройства менструального цикла – от аменореи до обильных менструаций.
Лабораторная диагностика
Основными лабораторными критериями ЖДА являются:
- низкий цветовой показатель;
- гипохромия эритроцитов, микроцитоз;
- снижение уровня сывороточного железа;
- повышение общей железосвязывающей способности сыворотки и снижение содержания ферритина в сыворотке.
После установления наличия анемии и степени ее выраженности необходимо выяснить причину и источник кровотечения.
Для этого необходимо провести целый ряд исследований. К основным исследованиям относятся:
- эндоскопическое исследование ЖКТ (ФГДС, колоноскопия, возможно, с биопсией);
- кал на скрытую кровь;
- гинекологическое мануальное и ультразвуковое исследование у женщин;
- исследование мочевыводящей системы (общий анализ мочи, УЗИ почек, цистоскопия);
- рентгенологическое исследование органов грудной полости;
- исследование мокроты и промывных вод бронхов на гемосидерин, атипичные клетки и микобактерии туберкулеза.
При отсутствии данных, свидетельствующих о явном эрозивно-язвенном процессе, следует провести онкологический поиск.
Лечение
Целями лечения ЖДА являются:
- устранение причины, ее вызвавшей (выявление источника кровотечения и его ликвидация, восстановление процесса усвоения Fe);
- восполнение дефицита Fe в организме;
- предотвращение развития дистрофических изменений внутренних органов и сохранение их функциональной способности в полном объеме.
Диета
Устранить ЖДА только с помощью диеты невозможно, поскольку всасывание Fe из продуктов питания составляет не более 2,5 мг/сутки, в то время как из лекарственных препаратов его всасывается в 15–20 раз больше. Тем не менее пациентам с ЖДА рекомендуются продукты, содержащие достаточное количество хорошо всасываемого белка и Fe. В мясных продуктах содержится Fe, входящее в состав гема (гемовое Fe), которое всасывается на 25–30 %. Входящее в состав гемосидерина и ферритина Fe (печень, яйца, рыба) всасывается на 10–15 %, а в состав продуктов растительного происхождения (бобовые, соя, шпинат, укроп, салат, абрикосы, чернослив, хлеб, рис) Fe – на 3–5 %.
Прием большого количества яблок, гранатов, моркови, свеклы, гречневой крупы не является оправданным с точки зрения ограниченного всасывания из них ионов Fe.
Люди, употребляющие в пищу мясо, получают больше железа гема (в составе миоглобина), чем вегетарианцы. У строгих вегетарианцев со временем может развиться дефицит железа, поскольку овощи и злаки содержат вещества, препятствующие всасыванию железа, в частности фосфаты.
Следует учитывать, что полноценная и сбалансированная по основным ингредиентам диета позволяет лишь «покрыть» физиологическую потребность организма в железе, но не устранить его дефицит, и должна рассматриваться как один из вспомогательных компонентов терапии.
Гемотрансфузии проводятся пациентам только по жизненным показаниям, причем показанием является не уровень Hb, а общее состояние пациента и гемодинамики. Чаще всего прибегают к гемотрансфузиям (трансфузиям эритроцитарной массы) при падении Hb ниже 40–50 г/л.
Медикаментозная терапия ЖДА
Проводится только препаратами Fe, в основном пероральными, реже парентеральными, длительно, под контролем развернутого анализа крови. Скорость восстановления показателей красной крови не зависит от пути введения.
К основным принципам лечения железодефицитной анемии препаратами Fe для перорального приема относятся:
- назначение препаратов Fe с достаточным содержанием в них двухвалентного Fe2+ (200–300 мг/сутки);
- при использовании новых форм следует ориентироваться на среднетерапевтическую дозу;
- назначение препаратов Fe совместно с веществами, усиливающими их всасывание (аскорбиновая и янтарная кислота);
- избегать одновременного приема веществ, уменьшающих всасывание Fe (антациды, танин, оксалаты);
- использовать препараты, не содержащие витаминные компоненты (особенно В6, В12);
- удобный режим дозирования (1–2 раза/сутки);
- хорошая биодоступность, всасываемость, переносимость препаратов Fe;
- достаточная продолжительность терапии не менее 6–8 недель до нормализации уровня гемоглобина;
- продолжить прием в половинной дозе еще в течение 4–6 недель после нормализации уровня гемоглобина;
- целесообразно назначать короткие ежемесячные курсы терапии (3–5 дней) в среднетерапевтической дозе женщинам с полименоррагиями.
Критерий эффективности лечения препаратами железа — прирост ретикулоцитов (ретикулоцитарный криз) в 3–5 раз на 7–10-й день от начала терапии (при однократном контроле регистрируют не всегда).
Препараты Fe классифицируют на: ионные ферропрепараты, представляющие собой солевые или полисахаридные соединения Fe2+, и неионные соединения, состоящие из гидроксидполимальтозного комплекса трехвалентного Fe3+.
Сульфат Fe, входящий в монокомпонентные и комбинированные ферропрепараты, хорошо всасывается (до 10%) и переносится больными. Хлоридные соединения Fe всасываются хуже (до 4%) и имеют больше нежелательных эффектов: металлический привкус во рту, потемнение зубов и десен, диспепсия.
В настоящее время предпочтение отдают препаратам, содержащим двухвалентное железо (лучше абсорбируются в кишечнике по сравнению с препаратами трехвалентного железа), суточная доза которого составляет 100–300 мг. Назначать более 300 мг Fe2+ в сутки не следует, т.к. его всасывание при этом не увеличивается.
Следует учитывать, что содержащийся в пищевых продуктах целый ряд веществ – фосфорная кислота, соли, кальций, фитин, танин (поэтому не рекомендуется запивать препараты железа чаем, кофе, кока-колой) – ингибирует всасывание железа. Такой же эффект отмечается при одновременном приеме двухвалентного железа некоторых лекарственных препаратов, таких как алмагель, соли магния.
Показания для парентерального введения препаратов Fe:
- нарушение кишечного всасывания (резекция кишечника, синдром мальабсорбции), обширные язвенные поверхности;
- абсолютная непереносимость пероральных препаратов Fe;
- необходимость быстрого насыщения железом (экстренное оперативное вмешательство);
- лечение эритропоэтином, когда резко, но на короткое время (2–3 часа после введения эритропоэтина) возрастает потребность в Fe в связи с его активным потреблением эритроцитами.
При парентеральном введении в случае неправильно установленного диагноза возможно развитие гемосидероза с полиорганной недостаточностью. Не следует вводить парентерально более 100 мг/сутки.
Профилактика ЖДА должна проводиться при наличии скрытых признаков дефицита Fe либо факторов риска для ее развития. Исследование Hb, сывороточного Fe должны выполняться не реже 1 раза в год, а при наличии клинических проявлений по мере необходимости у следующих категорий пациентов:
- доноры (особенно женщины), постоянно сдающие кровь;
- беременные женщины, особенно с частыми повторными беременностями на фоне ЖДА;
- женщины с длительными (более 5 дней) и обильными кровотечениями;
- недоношенные дети и дети, рожденные от многоплодной беременности;
- девушки в период полового созревания, при быстром росте, усиленных занятиях спортом (нарастающая мышечная масса поглощает много Fe), при ограничении мясных продуктов в питании;
- лица с постоянной и трудно устранимой кровопотерей (желудочные, кишечные, носовые, маточные и геморроидальные кровотечения);
- пациенты, длительно принимающие НПВП;
- лица с низким материальным достатком.
Железодефицитная анемия (ЖДА) представляет собой клинико–гематологический синдром, возникающий при развитии дефицита железа вследствие различных патологических (физиологических) процессов и характеризующийся снижением уровня гемоглобина (в меньшей степени эритроцитов) наряду с клиническими признаками анемии и сидеропении.
Клинические рекомендации ведения больных ЖДА включают: – выявление причины ЖДА и при необходимости – ее коррекция; – обучение больных ЖДА; – принятие решения о назначении лекарственных препаратов железа (ПЖ); – выбор лекарственного ПЖ; – путь введения ПЖ (внутрь или парентерально); – длительность лечения и необходимость поддерживающей терапии; – контроль переносимости ПЖ и коррекция при плохой переносимости; – оценку эффективности и выявление причин отсутствия или недостаточного эффекта; – коррекцию выявленных причин неэффективности.
Выявление причины ЖДА и возможности ее коррекции
После верификации железодефицитного характера анемии, т.е. синдрома ЖДА, необходимо выявление причины, лежащей в основе данного варианта анемического синдрома (нозологическая диагностика). Для клинициста этот этап является не менее важным и вместе с тем наиболее трудным и ответственным, поскольку в основе имеющейся ЖДА могут лежать потенциально курабельные заболевания. Наличие в МКБ–10 рубрики «Железодефицитная анемия неуточненная» оставляет для врача «лазейку» в случаях отсутствия явной причины анемии, «освобождая» его от тщательности и углубления диагностического поиска на этапе нозологической диагностики. Следует особо подчеркнуть роль врача–интерниста на этапах синдромной и нозологической диагностики, поскольку подавляющее большинство больных ЖДА (независимо от конкретной причины) обращаются прежде всего, как и многие другие пациенты, к терапевту, а не к гематологу или другому специалисту. При выявлении причины ЖДА лечение должно быть направлено на устранение этой причины (по возможности) или коррекцию имеющихся нарушений – лечение эрозивно–язвенных процессов в желудке, оперативные лечения при опухолях ЖКТ, миоме матки, лечение энтеритов, коррекция алиментарной недостаточностии т.д.
Обучение больных
Существенным компонентом ведения больных ЖДА является повышение их образовательного уровня в отношении данной патологии, создание мотивации к лечению, вовлечение пациентов в контроль за своим состоянием и лабораторными показателями. Необходимо разъяснение сущности ЖДА, причин ее возникновения, реальных возможностей коррекции дефицита железа и нормализации уровня гемоглобина. Особое значение имеют обучающие программы у беременных женщин с наличием ЖДА и пациенток, страдающих меноррагиями. У беременных должна создаваться мотивация необходимости коррекции дефицита железа с целью предотвращения недостатка железа у плода. Больные должны быть осведомлены о возможных побочных эффектах при лечении лекарственными препаратами железа, необходимости соблюдения врачебных назначений, в том числе и регулярности приема ПЖ. Следует обязательно указать на недопустимость попыток коррекции дефицита железа с помощью различных пищевых продуктов, а также на строгие показания к назначению инъекционных форм ПЖ.
Принятие решения о назначении лекарственных препаратов железа
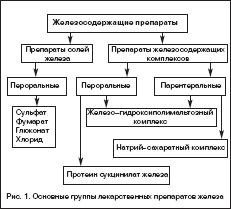
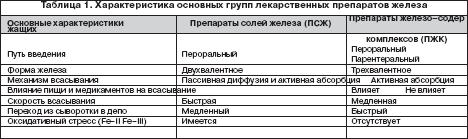
Всем больным ЖДА показана патогенетическая терапия препаратами железа. Следует подчеркнуть ошибочность мнения о возможности коррекции дефицита железа с помощью пищевых продуктов с высоким содержанием железа, что является одним из мифов в представлениях о ведении больных ЖДА. Об этом должны быть осведомлены больные, что следует считать важным образовательным компонентом ведения данной категории пациентов. Разумеется, пища должна быть богата продуктами, содержащими железо. Однако следует иметь в виду неодинаковую степень всасываемости железа из различных продуктов. Так например, железо, содержащееся в мясе в виде гема, всасывается на 40–50%, в то время как из растительных продуктов, овощей, фруктов всасывается всего 3–5% содержащегося в них железа. Поэтому средством выбора для коррекции дефицита железа и уровня гемоглобина у больных ЖДА являются лекарственные препараты железа. На фармацевтическом рынке России в настоящее время имеется большой арсенал ПЖ в различных лекарственных формах, с неодинаковым содержанием в них железа, наличием дополнительных компонентов, влияющих на биодоступность железа, различной стоимостью (рис. 1). Из ПСЖ железо всасывается в двухвалентной форме, в последующем превращается в трехвалетное, которое связывается с трансферрином и используется для построения молекулы гемоглобина. В ПЖК железо находится в трехвалентной форме и всасывается как бы в готовом виде. В ПЖК, в частности, в гидрооксиполимальтозном комплексе, связано как в физиологическом состоянии в молекуле ферритина. Существуют различия в механизмах всасывания железа из ПСЖ и ПЖК. Всасывание железа из ПСЖ происходит главным образом в виде пассивной диффузии согласно градиенту концентрации и в меньшей степени активно, в то время как абсорбция железа из ПЖК является активным процессом в виде конкурентного обмена. Это ведет к различному уровню железа в сыворотке, объему распределения, константам элиминации после абсорбции. Всасывание железа из ПЖК и нарастание его концентрации в сыворотке происходит медленно, но оно быстро поступает в запасы. При применении ПСЖ могут возникать нарушения окислительных процессов (оксидативные повреждения) вследствие превращения ионов двухвалентного железа в трехвалентное, которое соединяется с трансферрином и включается в молекулу гемоглобина. При окислении образуются свободные радикалы, которые вызывают клеточные повреждения, такие как перекисное окисление липидов, нарушение структуры мембранных и клеточных белков, повреждение клеточной ДНК и РНК. ПЖК в отличие от ПСЖ не вызывают «оксидативного стресса», поскольку ионы железа не меняют свою валентность в процессе всасывания (табл. 1). Для лучшей абсорбции ПСЖ рекомендуется принимать за час до еды т.е. на пустой желудок, что может вызывать нарушения со стороны желудка, кишечника и другие побочные эффекты. Современные технологии производства препаратов железа позволяют производить ПСЖ с замедленным высвобождением железа в тонком кишечнике, что уменьшает токсическое воздействие ионов железа на слизистую желудка. Частота побочных эффектов при лечении ПЖК меньше по сравнении с ПСЖ, что обеспечивает лучший комплайенс больных ЖДА. ПСЖ взаимодействуют с некоторыми пищевыми продуктами (танин, фитаты, соли кальция) и медикаментами (пленкообразующие препараты, тетрациклины, препараты кальция), снижающими биодоступность железа. В связи с этим ПСЖ не следует принимать одновременно с указанными пищевыми продуктами и лекарственными препаратами. В то же время пища и медикаменты не оказывают влияния на всасывание железа из ПЖК. Темпы прироста показателей гемоглобина при применении ПСЖ и ПЖК примерно одинаковые.
Путь введения препаратов железа
В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний ПЖ следует назначать внутрь. Путь введения ПЖ у больных ЖДА определяется конкретной клинической ситуацией, в частности, состоянием кишечного всасывания и переносимостью пероральных ПЖ.
Основными показаниями для парентерального введения ПЖ являются: – патологии кишечника с нарушением всасывания (различные энтериты, синдром недостаточности всасывания); – резекция тонкой кишки; – резекция желудка по Бильрот II с формированием «слепой петли»; – эрозивно–язвенные процессы в желудке (обострение язвенной болезни и др.); – непереносимость ПЖ для приема внутрь. Многие врачи обосновывают назначение парентеральных ПЖ выраженностью анемического синдрома в расчете на якобы больший их эффект, что также не имеет достаточных оснований и не подтверждается клинической практикой. Темпы прироста уровня гемоглобина при назначении ПЖ внутрь и парентерально оказались приблизительно одинаковыми, в связи с чем предпочтение ПЖ в инъекционных формах при необходимости более быстрой нормализации содержания гемоглобина (например, при подготовке к оперативному вмешательству) следует считать неоправданным. ПЖ для парентерального введения могут назначаться при плохой переносимости пероральных ПЖ, однако большинство современных ПСЖ и ПЖК переносятся сравнительно удовлетворительно. В связи с этим принятие решения о назначении парентерального ПЖ должно осуществляться только после ряда «врачебных маневров» (снижение дозы ПЖ, прием вместе с пищей, смена ПЖ для приема внутрь и т.д.).
Выбор лекарственного препарата железа
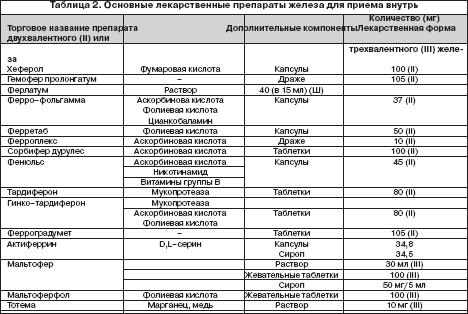
Выбор ПЖ и оптимального режима его дозирования должен определяться количеством и биодоступностью содержащегося в нем железа, переносимостью, стоимостью. При этом необходимо иметь в виду, что адекватный прирост показателей гемоглобина у больных ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг элементарного железа . Учитывая, что при развитии ЖДА всасывание железа увеличивается по сравнению с нормой и составляет 25–30% (при нормальных запасах железа – всего 3–7%), необходимо назначать от 100 до 300 мг элементарного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. С учетом этого при выборе ПЖ следует ориентироваться не на содержание в нем общего количества соединения железа, а на количество элементарного железа. Например, при назначении препаратов сульфата железа с низким содержанием элементарного железа (менее 100 мг) количество принимаемых таблеток должно быть от 3 и выше (в зависимости от содержания железа в каждой таблетке), в то время как препараты сульфата, фумарата или гидроксиполимальтозного комплекса железа с содержанием 100 мг элементарного железа можно принимать в количестве 1–2 таблеток в сутки. Основные ПСЖ представлены сульфатом железа, глюконатом, хлоридом, фумаратом, глицин сульфатом. Наибольшей степенью абсорбции обладают препараты сульфата железа, а наименьшей – глицин сульфата. Многие из ПСЖ содержат вещества, например, аскорбиновую кислоту, усиливающие всасывание железа и улучшающие биодоступность препарата, а также витамины (фолиевую кислоту, цианкобаламин). Среди ПЖК на отечественно рынке имеются гидроксиполимальтозный комплекс, железо–сорбитоловый комплекс, протеин сукцинилат железа, железо–сахарозный комплекс. К новым высокоэффективным и безопасным препаратам железа относятся препараты, представляющие собой неионные соединения железа на основе гидроксиполимальтозного комплекса (ГПК) трехвалентного железа. Структура комплекса состоит из многоядерных центров гидроксида Fe (III), окруженных нековалентно связанными молекулами полимальтозы. Комплекс имеет большой молекулярный вес, что затрудняет его диффузию через мембрану слизистой кишечника. Химическая структура комплекса максимально приближена к структуре естественных соединений железа с ферритином. Абсорбция железа в виде ГПК имеет принципиально иную схему по сравнению с его ионными соединениями и обеспечивается поступлением Fe (III) из кишечника в кровь путем активного всасывания. Неионная структура комплекса обеспечивает его стабильность и перенос железа с помощью транспортного белка, что предотвращает в организме свободную диффузию ионов железа, т.е. прооксидантные реакции. Данные по безопасности, полученные во время клинических исследований препарата железа на основе гидроксида Fe (III) с полимальтозой, свидетельствуют о более низкой частоте побочных эффектов по сравнению с солевыми препаратами железа. Для лучшей переносимости ПСЖ следует принимать во время еды, хотя следует иметь в виду, что всасывание железа лучше при приеме лекарственных препаратов перед едой. Всасываниежелеза может уменьшаться под влиянием содержащихся в некоторых пищевых продуктах веществ – фитинов (рис, соя), фосфатов (рыба, морепродукты), танина (чай, кофе). Многие больные склонны запивать лекарства чаем, что в случаях приема ПЖ в виде солей недопустимо, поскольку образуются плохо растворимые комплексы с низкой их абсорбцией в кишечнике. Кроме того, всасывание железа из ПЖ в виде солей ухудшается при одновременном приеме ряда медикаментов (тетрациклины, антациды, соли магния). С учетом этого следует рекомендовать прием препаратов солей железа в различное время с другими вышеуказанными медикаментами. Препараты ПЖК, в частности, гидроксиполимальтозный комплекс лишены подобных недостатков, поскольку пищевые продукты и медикаменты не оказывают влияние на всасываемость железа (в виде трехвалентной формы) из железосодержащих комплексов. В таблице 2 представлены основные зарегистрированные в России лекарственные ПСЖ и ПЖК для приема внутрь.
Оценка эффективности лечения
В случаях назначения ПЖ в достаточной дозе на 7–10–й день от начала лечения наблюдается повышение количества ретикулоцитов. Достоверное повышение уровня гемоглобина отмечается через 3–4 нед. от начала лечения. Нормализация показателей гемоглобина обычно происходит в сроки 4–9 нед. Иногда наблюдается резкое скачкообразное повышение гемоглобина. Эти индивидуальные колебания могут быть обусловлены, с одной стороны, выраженностью ЖДА, степенью истощения запасов железа, а с другой – эффективностью назначенного ПЖ (количество содержащегося железа, биодоступность и др.). Имеет также значение некомплаентность больных (нерегулярность приема ПЖ, побочные эффекты).
Длительность лечения и поддерживающая терапия
Оптимальная тактика ведения больных ЖДА предполагает насыщающую и поддерживающую терапию ПЖ. Длительность насыщающей терапии зависит от темпов прироста и сроков нормализации показателей гемоглобина, составляя в среднем 4–6 недель. Поддерживающая терапия показана в тех ситуациях, когда причина дефицита железа сохраняется (меноррагии, беременность) или в силу различных ситуаций является трудноустранимой (патология кишечника, носовые и другие кровотечения при геморрагических диатезах). Женщинам, страдающим ЖДА на фоне меноррагий, после нормализации показателей гемоглобина рекомендуется поддерживающая терапия ПЖ в течение 5–7 дней после очередной менструации. Больным надо разъяснять необходимость поддерживающего лечения в связи с продолжающимися избыточными потерями железа. Беременные с ЖДА должны получать ПЖ до конца беременности в целях обеспечения адекватной потребности плода в железе.
Переносимость препаратов железа
Среди побочных эффектов на фоне применения ПЖ внутрь наиболее часто возникают тошнота, анорексия, металлический вкус во рту, запоры, реже – поносы. Развитие запоров обусловлено, по всей вероятности, связыванием в кишечнике сероводорода, являющегося одним из стимулов кишечной перистальтики. В большинстве случаев современные ПЖ вызывают незначительные побочные явления, не требующие их отмены и перехода на парентеральный путь введения. Диспептические расстройства могут уменьшаться при приеме препаратов после еды или уменьшения суточной дозы препарата. Чаще побочные эффекты регистрируютсяпри приеме ПСЖ, в то время как препараты ПЖК (гидроксиполимальтозный комплекс) переносятся лучше и имеют в связи с этим определенные преимущества. В случаях сохраняющейся плохой переносимости пероральных ПЖ показано назначение ПЖ парентерально (внутримышечно или внутривенно). На фоне лечения парентеральными ПЖ, особенно для внутривенного введения, могут возникать аллергические реакции в виде крапивницы, лихорадка, флебиты, анафилактический шок. Кроме того, при внутримышечном введении ПЖ возможно потемнение кожи в местах инъекций, инфильтраты, абсцессы. Если ПЖ для парентерального введения назначают больным гипохромной анемией, не связанной с дефицитом железа, имеется повышенный риск возникновения тяжелых нарушений из–за «перегрузки» железом различных органов и тканей (печень, поджелудочная железа и др.) с развитием гемосидероза.
Причины неэффективности лечения препаратами железа
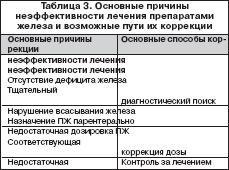
В случае отсутствия или недостаточного эффекта от лечения ПЖ следует выяснить причину с целью возможности ее коррекции. Возможные причины неэффективности лечения ПЖ и способы их коррекции представлены в таблице 3. Необходима убежденность в правильной трактовке всех клинико–лабораторных признаков и в достоверности синдрома ЖДА. Причиной отсутствия или недостаточной эффективности ПЖ может быть недостаточная суточная доза железа, что обычно связано с назначением ПЖ с низким содержанием в нем железа и малым количеством принимаемых таблеток. Так, например, при лечении препаратом, в котором содержится всего лишь 10 мг двухвалентного железа, число принимаемых таблеток должно быть не менее 10 в сутки. Такой режим дозирования неудобен для больных, чем и объясняется, вероятнее всего, невыполнение ими врачебного назначения. С учетом вышесказанного для обеспечения комплаентности следует назначать ПЖ с высоким содержанием железа (не менее 100 мг). Препараты с низким содержанием железа целесообразно использовать в педиатрической практике. Одной из причин неэффективности ПЖ при назначении внутрь может быть нарушение всасывания железа, в частности, у больных с невыявленной или недооцененной кишечной патологией. В этих случаях показано назначение парентеральных ПЖ. В ряде случаев вследствие улучшения самочувствия больные начинают нерегулярно принимать ПЖ или вообще прекращают лечение. В результате показатели гемоглобина не достигают нормальных значений и ЖДА при этом остается фактически недолеченной. С учетом этого длительность насыщающей терапии ПЖ должна определяться сроками достижения нормального уровня гемоглобина, что требует постоянного лабораторного мониторинга. Ряд больных не всегда выполняют назначение врача (регулярность приема ПЖ, достаточная продолжительность и т.д.). В некоторых случаях это может быть обусловлено развитиемпобочных эффектов от ПЖ и самостоятельным прекращением лечения. Поэтому необходим контроль за лечением, эффективностью, переносимостью ПЖ со стороны врача, среднего медперсонала, родственников больных. Отсутствие эффекта от ПЖ может быть связано с неустраненными причинами ЖДА, среди которых клинически наиболее значимыми являются скрытые кровопотери из желудочно–кишечного тракта, чаще из кишечника (невыявленная опухоль!). С учетом этого в подобных ситуациях при исключении других возможных причин неэффективности ПЖ необходимо тщательное эндоскопическое исследование кишечника (в ряде случаев – повторное). Таким образом, у больных ЖДА наряду с устранением причины обязательна патогенетическая терапия ПЖ (ПСЖ и ПЖК), которые должны назначаться преимущественно внутрь. Тактика лечения ПЖ предусматривает выбор пути введения ПЖ с учетом клинической ситуации, оптимального ПЖ с достаточным содержанием в нем железа, оценку эффективности и переносимости препарата, длительность насыщающей и обоснованность поддерживающей терапии. Своевременная верификация синдрома ЖДА и выявление ее причины, адекватная патогенетическая терапия с назначением ПЖ с оптимальными фармакокинетическими свойствами, клинической эффективностью, переносимостью позволяет корригировать анемический синдром и обеспечивать достаточный уровень качества жизни у данной категории пациентов.