Роль витамина с в образовании гемоглобина
Âèòàìèíû äëÿ ïîâûøåíèÿ ãåìîãëîáèíà â êðîâè ÿâëÿþòñÿ îäíèì èç ñàìûõ ýôôåêòèâíûõ ôàðìàêîëîãè÷åñêèõ ñðåäñòâ â áîðüáå õðîíè÷åñêèìè çàáîëåâàíèÿìè, â òîì ÷èñëå ñ àíåìèåé, ñâÿçàííîé ñ äåôèöèòîì æåëåçà. Ýòî îáúÿñíÿåòñÿ ôèçèîëîãè÷åñêîé ôóíêöèåé, êîòîðóþ îíè âûïîëíÿþò.
Ïîä âëèÿíèåì âèòàìèíîâ â îðãàíèçìå ïðîèñõîäèò ñëåäóþùåå:
-àêòèâèçèðóþòñÿ ýíåðãåòè÷åñêèå ïðîöåññû;
-íîðìàëèçóåòñÿ ìåòàáîëèçì â êëåòêàõ;
-óëó÷øàåòñÿ ïèòàíèå òêàíåé;
-òêàíè ðàñòóò è ðåãåíåðèðóþòñÿ;
-ïðîèñõîäèò ðåïðîäóêöèÿ íîâûõ êëåòîê;
-óêðåïëÿåòñÿ èììóíîëîãè÷åñêàÿ çàùèòà.
Çà ñ÷¸ò ÷åãî ýòî äåëàåòñÿ? Ïðîñòî ïîòîìó, ÷òî âèòàìèíû âõîäÿò â ñîñòàâ êîýíçèìîâ, àêòèâèçèðóþùèõ âñå áåëêîâûå ñòðóêòóðû è âûíóæäàþùèé èõ áåñïðåðûâíî âûïîëíÿòü ñâîè ôóíêöèè.
Ãåìîãëîáèí îòíîñèòñÿ èìåííî ê ýòèì áåëêàì. Ýòî ñâîåîáðàçíûé òðàíñïîðò¸ð, ïåðåäâèãàþùèéñÿ âíóòðè êðîâÿíîãî ðóñëà â âèäå ýðèòðîöèòîâ. Îí äîñòàâëÿåò íàøèì êëåòêàì, îáðàçóþùèì òêàíè è îðãàíû, ïîëó÷åííûé â ë¸ãêèõ êèñëîðîä, íåîáõîäèìûé äëÿ çàïóñêà è ïðîäîëæåíèÿ óêàçàííûõ âûøå ïðîöåññîâ íà ïðîòÿæåíèè âñåé æèçíè.
Óãëåêèñëûé ãàç â êà÷åñòâå ïîáî÷íîãî ïðîäóêòà îáíîâëåíèÿ îðãàíè÷åñêèõ ñîåäèíåíèé âûâîäèòñÿ èç îêèñëèòåëüíîãî öèêëà òåì æå ãåìîãëîáèíîì âîâíå ÷åðåç òå æå äûõàòåëüíûå ïóòè.
Íîðìîé ñ÷èòàåòñÿ, êîãäà óðîâåíü ãåìîãëîáèíà, ïðèñóòñòâóþùåãî â êðîâè, âïîëíå îáåñïå÷èâàåò æèçíåäåÿòåëüíîñòü.
Ó ìóæ÷èí ñðåäíåãî âîçðàñòà îí êîëåáëåòñÿ â ïðåäåëàõ îò 130 äî 170 ãðàììîâ íà ëèòð.
Ó æåíùèí 120 è 150.
Ó äåòåé 120 è 140.
 òîì ñëó÷àå, åñëè ýòè ïîêàçàòåëè îïóñêàþòñÿ íèæå ìèíèìàëüíîé ïëàíêè, â îðãàíèçìå âîçíèêàåò ñîñòîÿíèå, èçâåñòíîå êàê àíåìèÿ.  äèíàìèêå áîëåçíü ïðîÿâëÿåòñÿ ðÿäîì ñèìïòîìîâ:
-ñíà÷àëà áëåäíååò êîæà, ñòàíîâèòñÿ ñóõîé;
-çàòåì ïðè ìàëåéøåì íàïðÿæåíèè êðóæèòñÿ ãîëîâà, òåðÿåòñÿ îðèåíòàöèÿ â ïðîñòðàíñòâå;
-óõóäøàåòñÿ ñîí;
-ñíèæàåòñÿ àïïåòèò;
-óâåëè÷èâàåòñÿ âîñïðèèì÷èâîñòü ê èíôåêöèîííûì áîëåçíÿì;
-çàáîëåâøèé áûñòðî óòîìëÿåòñÿ,
-ñêëîíåí ê ïîñòîÿííûì ïåðåäûøêàì,
-âèä ó íåãî áîëåçíåííûé, îòñòðàí¸ííûé.
Ýòèîëîãèÿ àíåìèè
 îñíîâå çàáîëåâàíèÿ, êàê ïðàâèëî, äåôèöèò æåëåçîñîäåðæàùèõ âåùåñòâ, íåîáõîäèìûõ äëÿ îáðàçîâàíèÿ ãåìîãëîáèíà. Îí ìîæåò èìåòü êàê ïàòîëîãè÷åñêóþ, òàê è ôóíêöèîíàëüíóþ ïðèðîäó, ñâÿçàííóþ ñ âîçäåéñòâèåì âíåøíèõ ôàêòîðîâ.
Ê ñàìûì ðàñïðîñòðàí¸ííûì ïðè÷èíàì âîçíèêíîâåíèÿ æåëåçîäåôèöèòíîé àíåìèè âíåøíåãî òèïà ìîæíî îòíåñòè:
-ïîòåðþ áîëüøèõ îáú¸ìîâ êðîâè â ðåçóëüòàòå, òðàâì, õèðóðãè÷åñêèõ îïåðàöèé, äîíîðñòâà;
-êðîâîïîòåðè ó æåíùèí ïðè ìåíñòðóàöèÿõ è áåðåìåííîñòè;
-íåäîñòàòîê â ïèùåâîì ðàöèîíå æåëåçà è âèòàìèíîâ, ñòèìóëèðóþùèõ åãî óñâîÿåìîñòü.
Ñðåäè ïàòîëîãè÷åñêèõ èñòî÷íèêîâ, ñïîñîáíûõ ïîíèçèòü óñâîåíèå æåëåçîñîäåðæàùèõ ïðîäóêòîâ ñ âñïîìîãàòåëüíûìè âèòàìèíàìè, à ñ íèìè ãåìîãëîáèí ñëåäóåò âûäåëèòü:
-çàáîëåâàíèÿ æåëóäî÷íî-êèøå÷íîãî òðàêòà;
-çëîêà÷åñòâåííûå è äîáðîêà÷åñòâåííûå îïóõîëè, îñîáåííî â ñèñòåìå ïèùåâàðåíèÿ;
-èíôåêöèîííûé ãåïàòèò, ïíåâìîíèþ, òóáåðêóë¸ç;
-íàðóøåíèå ôóíêöèè ïî÷åê;
-âëèÿíèå ãåëüìèíòîâ, ñàëüìîíåë¸ç;
-àóòîèììóííûå ïàòîëîãèè: ïðåæäå âñåãî, ðåâìàòîèäíûé àðòðèò è «âîë÷àíêà»;
-îíêîëîãè÷åñêèå ïîðàæåíèÿ êðîâè (ëåéêîç)
-ïåðåõîä îñòðîé ôàçû æåëåçîäåôèöèòíîé àíåìèè â õðîíè÷åñêóþ.
Êàê íîðìàëèçîâàòü ãåìîãëîáèí
 ìåäèöèíñêîé ïðàêòèêå ïðè ïîíèæåííîì ãåìîãëîáèíå èñïîëüçóþòñÿ íåñêîëüêî ìåòîäîâ, ñïîñîáíûõ ñóùåñòâåííî ïîâûñèòü óðîâåíü ãåìîãëîáèíà â êðîâè. Íàçîâ¸ì òðè ñàìûõ ïðîñòûõ:
1) Âêëþ÷èòü â ïèùåâîé ðàöèîí ïðîäóêòû, èçîáèëóþùèå æåëåçîì, à òàêæå âèòàìèíàìè Â12 è Â9 (ôîëèåâàÿ êèñëîòà);
2) Ïðèíèìàòü ñïåöèàëüíûå ïðåïàðàòû, ïîâûøàþùèå ãåìîãëîáèí;
3) Êîìáèíèðîâàòü ïåðâûé ìåòîä ñî âòîðûì â ïðèåìëåìûõ ïðàïîðöèÿõ ïîä êîíòðîëåì âðà÷à.
Ðîëü âèòàìèíîâ â ïèòàíèè ïðè àíåìèè
Íåäîñòàòîê âèòàìèíà Â12 ñíèæàåò ýôôåêòèâíîñòü ïèòàíèÿ, íàïðàâëåííîãî íà óñòðàíåíèå æåëåçîäåôèöèòíîé àíåìèè.
Æåëåçîñîäåðæàùèå âèòàìèíû äëÿ ïîäíÿòèÿ ãåìîãëîáèíà ñîâåðøåííî íåîáõîäèìû äëÿ ëå÷åíèÿ è ïðîôèëàêòèêè çàáîëåâàíèé, õàðàêòåðèçóþùèõñÿ ïîíèæåííûì ñîäåðæàíèåì ãåìîãëîáèíà â êðîâÿíîì ðóñëå.
Îíè ïîìîãàþò èçáàâèòüñÿ:
-îò æåëåçîäåôèöèòíîé àíåìèè â õðîíè÷åñêîé ôîðìå;
-àíåìèè àëèìåíòàðíîãî ïðîèñõîæäåíèÿ, âûçâàííîé íåõâàòêîé â ïèùå æåëåçîñîäåðæàùèõ ïðîäóêòîâ;
-ôóíêöèîíàëüíîãî ãåìîãëîáèíîäåôèöèòà ó æåíùèí, òåðÿþùèõ êðîâü â ïåðèîä ìåíñòðóàöèé è áåðåìåííîñòè;
-ïîñòðàâìàòè÷åñêîé àíåìèè â ìèðíîå è â âîåííîå âðåìÿ;
-èíôåêöèîííûõ, òîêñè÷åñêèõ, îíêîëîãè÷åñêèõ àíåìèé.
Ïðîäóêòû, ñïîñîáíûå êîìïåíñèðîâàòü äåôèöèò æåëåçà è âèòàìèíîâ
Ïå÷åíü ãîâÿäèíû ýòî íàèáîëåå ïðåäïî÷òèòåëüíûé èç ìÿñíûõ ïðîäóêòîâ, ïîìîãàþùèõ ïðè àíåìèè ïîâûñèòü äî íîðìû íèçêèé ãåìîãëîáèí ó âçðîñëûõ.  òêàíè ïå÷åíè ñîäåðæèòñÿ áîëüøîå êîëè÷åñòâî æåëåçà è âèòàìèíîâ. Ïðè÷¸ì íå òîëüêî îòíîñÿùèõñÿ ê ãðóïïå Â, íî è âèòàìèíîâ À è Ñ, ïîääåðæèâàþùèõ èììóíèòåò è äûõàòåëüíóþ ôóíêöèþ.
Êðîìå òîãî, ýòî ìÿñî ëåãêî óñâàèâàåòñÿ, íå òåðÿÿ ñâîèõ ïîëåçíûõ ñâîéñòâ.  êà÷åñòâå äèåòè÷åñêîãî ïèòàíèÿ åãî íàçíà÷àþò æåíùèíàì â ïåðèîä áåðåìåííîñòè è äåòÿì, ñòðàäàþùèì àíåìèåé. Ïðè¸ì ýòîãî ïðîäóêòà â ïðåêëîííîì âîçðàñòå äîëæåí áûòü îãðàíè÷åí. Ýêñòðàêòèâíûå âåùåñòâà, òàêæå ñîäåðæàùèåñÿ â ïå÷åíè, ïîâûøàþò ñåêðåöèþ â ïèùåâàðèòåëüíîì òðàêòå è ìîãóò ñïîñîáñòâîâàòü ðàçâèòèþ ãàñòðèòà è ÿçâû æåëóäêà.
Ðåãóëÿðíîå âêëþ÷åíèå â ðàöèîí áëþä èç ïå÷åíè äîñòàòî÷íî áûñòðî äîâîäèò óðîâåíü ãåìîãëîáèíà äî ïðèåìëåìûõ ïîêàçàòåëåé.
Ãðå÷íåâàÿ êðóïà ïðè ïîíèæåííîì ãåìîãëîáèíå ýôôåêòèâíà ïðèìåðíî òàê æå, êàê ãîâÿæüÿ ïå÷åíü.  íåé òîæå ìíîãî æåëåçà, âèòàìèíîâ Â-ãðóïïû è ìèêðîýëåìåíòîâ, ñòèìóëèðóþùèõ óñâîÿåìîñòü ïðîäóêòà â êèøå÷íèêå.
×òîáû â ïðîöåññå âñàñûâàíèÿ ïîëó÷èëñÿ áîëåå âûñîêèé ãåìîãëîáèí, ñûðóþ êðóïó ïåðåä óïîòðåáëåíèåì ñëåäóåò ìåëêî èçìîëîòü â áëåíäåðå è íàñòîÿòü â êèïÿòêå èëè ñâàðèòü, ïîëó÷èâ êàøó. È â òîì è â äðóãîì âàðèàíòå ãðå÷êà îòñòàèâàåòñÿ íå ìåíåå ïîëóñóòîê. Ýòî äà¸ò âîçìîæíîñòü å¸ àêòèâíûì âåùåñòâàì íàáðàòü êîíöåíòðàöèþ, äàþùóþ íàèáîëüøèé òåðàïåâòè÷åñêèé ýôôåêò ïîñëå ïåðåâàðèâàíèÿ â æåëóäêå.
Ñîê ãðàíàòà, ïîìèìî æåëåçà è Â-âèòàìèíîâ, ñîäåðæèò ðåòèíîë (âèòàìèí À), íèêîòèíîâóþ êèñëîòó, ñòèìóëèðóþùóþ êðîâîîáðàùåíèå (âèòàìèí ÐÐ) è âèòàìèí Å, èíîãäà åù¸ íàçûâàåìûé «âèòàìèíîì ìîëîäîñòè».
Åäèíñòâåííûé íåäîñòàòîê ýòîãî ñîêà îí ïëîõî óñâàèâàåòñÿ, îñîáåííî â íåâûæàòîì âèäå. Íî äàæå è ÷èñòîãî ñîêà âïîëíå äîñòàòî÷íî íà ñóòêè 100 ãðàìì, è òî ëó÷øå, åñëè îí áóäåò ðàçáàâëåí ìîðêîâíûì ñîêîì èëè âîäîé.
Ñâåêëà òîæå èìååò â ñâî¸ì ñîñòàâå æåëåçî è âèòàìèíû Â9 è Â12. Îíà íå òåðÿåò ñâîèõ ñâîéñòâ íè â ñûðîì, íè â âàð¸íîì âèäå. Åñëè ñîäåðæàíèå ãåìîãëîáèíà â êðîâè ïîíèæåíî, âåñü àññîðòèìåíò áëþä èç ñâåêëû, íà÷èíàÿ îò ïðîñòîãî âèíåãðåòà è çàêàí÷èâàÿ ñåë¸äêîé ïîä øóáîé, ñãëàæèâàåò àíåìè÷åñêèé ñèíäðîì. Îñîáåííî ïîëåçåí ñâåæåâûæàòûé ñâåêîëüíûé ñîê. Òîëüêî ïåðåä óïîòðåáëåíèåì îí äîëæåí áûòü âûäåðæàí íå ìåíåå ÷àñà è îõëàæä¸í â õîëîäèëüíèêå.
Ïðîòèâîïîêàçàíèÿ ñâÿçàíû ñ åãî ïîëîæèòåëüíûì âîçäåéñòâèåì íà ñåêðåòîðíóþ ôóíêöèþ æåëóäêà è ïå÷åíè. Ëþäÿì, ñòðàäàþùèì ãàñòðèòîì è ÿçâîé æåëóäêà, à òàêæå õîëåöèñòèòîì, ðåêîìåíäóåòñÿ âîçäåðæèâàòüñÿ îò ýòîãî ñïîñîáà ëå÷åíèÿ àíåìèè.
ßáëîêè ïðè ïîíèæåííîì ãåìîãëîáèíå ïîëåçíû áåç âñÿêèõ îãðàíè÷åíèé â êîëè÷åñòâå è ñòåïåíè êèñëîòíîñòè. Íî ñîäåðæàíèå â íèõ æåëåçà íå òàê âåëèêî, êàê â ïðîäóêòàõ, óêàçàííûõ âûøå. Êðîìå òîãî, â ýòèõ ôðóêòàõ, åñëè îíè íå óïîòðåáëÿþòñÿ ñâåæèìè, ïîñëå äîëãîâðåìåííîãî õðàíåíèÿ, ñîâñåì íå îñòà¸òñÿ âèòàìèíîâ.
Ê ñàìûì ïîçèòèâíûì ðåçóëüòàòàì ïðè àíåìèè ïðèâîäèò óïîòðåáëåíèå â ïèùó ðàçëè÷íûõ ñî÷åòàíèé âñåõ ýòèõ ïðîäóêòîâ. Íàïðèìåð:
-áëþäî, ñîñòîÿùåå èç ñëåãêà îáæàðåííîé ãîâÿæüåé ïå÷åíè ñ ãàðíèðîì èç ãðå÷íåâîé êàøè;
-ñàëàò èç ñâåêëû,
-ñòàêàí ãðàíàòîâîãî ñîêà,
-ÿáëîêè íà äåñåðò.
Ôàðìàêîëîãè÷åñêèå ïðåïàðàòû, ïîâûøàþùèå ãåìîãëîáèí
Îáû÷íî äëÿ íîðìàëèçàöèè ïîêàçàòåëåé ãåìîãëîáèíà äîñòàòî÷íî íàñûùåííîãî äèåòè÷åñêîãî ïèòàíèÿ, âêëþ÷àþùåãî â ñåáÿ ñîîòâåòñòâóþùèå âèòàìèíû è æåëåçî. Ïðèìåíåíèå ëåêàðñòâåííîé òåðàïèè íåîáõîäèìî, êîãäà:
-óðîâåíü ãåìîãëîáèíà ñóùåñòâåííî íèæå íîðìû;
-ïîäáîð ïðîäóêòîâ äëÿ åãî ïîâûøåíèÿ çàòðóäí¸í èëè íåâîçìîæåí;
-äèåòè÷åñêîå ïèòàíèå ïî âîñïîëíåíèþ äåôèöèòà æåëåçà â êðîâè íå ïðèíåñëî ðåçóëüòàòîâ;
-êîëè÷åñòâî ãåìîãëîáèíà â ýðèòðîöèòàõ ïàäàåò ñëèøêîì áûñòðî;
-íàçíà÷åíà õèðóðãè÷åñêàÿ îïåðàöèÿ ïî óñòðàíåíèþ îäíîé èç ïðè÷èí àíåìèè.
Ñàìûìè äîñòóïíûìè è ýôôåêòèâíûìè äëÿ ïðîôèëàêòèêè è ëå÷åíèÿ àíåìèè â ýòèõ ñëó÷àÿõ ñ÷èòàþòñÿ ñëåäóþùèå ôàðìàêîëîãè÷åñêèå ñðåäñòâà:
-Ñîðáèôåð-äóðóëåñ (ïðîòèâîïîêàçàí ïðè ñòåíîçå ïèùåâîäà, íàëè÷èè âîñïàëèòåëüíûõ î÷àãîâ â êèøå÷íèêå, äåòÿì äî 12-òè ëåò).
-Òîòåìà (íå ïðèìåíÿåòñÿ ïðè ÿçâå æåëóäêà, ãåìîõðîìàòîçå, áîëåçíè Âèëüñîíà-Êîíîâàëîâà, àëëåðãèè ê ôðóêòîçå).
-Ôåíþëüñ æåëåçîñîäåðæàùèé ïðåïàðàò ñ ïîëíûì íàáîðîì âèòàìèíîâ À, Â, Ñ, Å, ÐÐ. Î÷åíü âûñîêàÿ óñâîÿåìîñòü. Ïðîòèâîïîêàçàí òîëüêî ïðè ãåìîñèäåðîçå, ãåìîõðîìàòîçå è èäèîñèíêðàçèè ê òîìó èëè èíîìó âèòàìèíó, âõîäÿùåìó â îáùèé êîìïëåêñ.
-Ôåððóì ëåê. Ïðîòèâîïîêàçàíèÿ: àíåìèè ãåìîëèòè÷åñêîãî òèïà, ãåìîñèäåðîç, òàëàññåìèÿ.
-Ôåððî-ôîëüãàììà. Ìåõàíèçì äåéñòâèÿ òîò æå: êîíöåíòðèðîâàííîå âîçäåéñòâèå æåëåçà, õîðîøàÿ óñâîÿåìîñòü â æåëóäî÷íî-êèøå÷íîì òðàêòå. Íå ïðèìåíÿåòñÿ ïðè ïå÷¸íî÷íîé íåäîñòàòî÷íîñòè è ãåìîõðîìàòîçå.
Íàçâàíèå êàæäîãî ïðåïàðàòà, êðîìå «Òîòåìà», îòðàæàåò íàëè÷èå â í¸ì æåëåçà (Ferrum). Îáû÷íî ìåòàëë òàì íàõîäèòñÿ â ñâÿçàííîì ñîñòîÿíèè â âèäå ñóëüôàòà.
 îáÿçàòåëüíîì ïîðÿäêå âî âñåõ ýòèõ ëåêàðñòâàõ ïðèñóòñòâóþò îñíîâíûå âèòàìèíû, óëó÷øàþùèå ïåðåõîä Fe2 (SO4)3 â ñîñòàâ ãåìîãëîáèíà.
Çàêëþ÷åíèå
Îêàçàâøèñü â ïëåíó ó òàêîãî îïàñíîãî âðàãà êàê àíåìèÿ, ïîñòîÿííî ñíèæàþùåãî âàøè æèçíåííûå âîçìîæíîñòè, íå ñòîèò âïàäàòü â îò÷àÿíüå. Íóæíî ïðîñòî ïðè ïåðâûõ æå ïðîÿâëåíèÿõ áîëåçíè îáðàòèòüñÿ ê âðà÷ó è íà÷àòü ëå÷åíèå.
×òî ýòîìó ìîæåò ïîìåøàòü? Òîëüêî íàèâíîñòü, ñêëîíÿþùàÿ ê òîìó, ÷òî âñ¸ îáîéä¸òñÿ. Íî ýòî íå ëó÷øèé ñîâåò÷èê äëÿ çäðàâîìûñëÿùåãî ÷åëîâåêà.
Источник
Источники
Свежие овощи и фрукты (по убыванию количества): шиповник, смородина, клюква, брусника, перец сладкий, укроп, капуста, земляника, клубника, апельсины, лимоны, малина.
При составлении рациона необходимо учитывать реальные условия. Например, несмотря на высочайшее содержание аскорбиновой кислоты в шиповнике (около 500 мг на 100 г свежей ягоды), на практике он несущественный источник, т.к. мало кто ест свежий шиповник как таковой, а при температурной обработке, длительном хранении и на свету большая часть витамина разрушается. Такая же ситуация с лимонами (400 мг на 100 г, один лимон среднего размера) и 1 долька в кружке горячего чая), различной зеленью, вареньем из ягод.
Суточная потребность
- младенцы – 30-35 мг,
- дети от 1 до 10 лет – 35-50 мг
- подростки и взрослые – 50-100 мг.
Строение
Витамин является производным глюкозы. Его синтез осуществляют все организмы, кроме приматов и морских свинок.
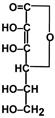
Строение
аскорбиновой кислоты
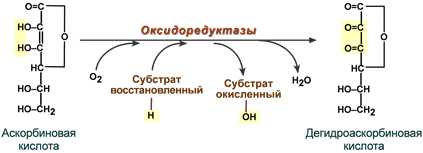
Биохимические функции
Витамин С не является коферментом в привычном понимании. Он используется как донор электронов, например, для восстановления ионов металлов (железо, медь), входящих в состав активного центра оксидоредуктаз, после осуществления ферментом своей реакции.

Окисление аскорбиновой кислоты в биохимической реакции
1. Реакции гидроксилирования:
- пролина и лизина в их гидроксиформы при “созревании” коллагена,
- при синтезе гиалуроновой кислоты и хондроитинсульфата, желчных кислот,
- при синтезе гормонов надпочечников (кортикостероидов и катехоламинов) и тиреоидных гормонов,
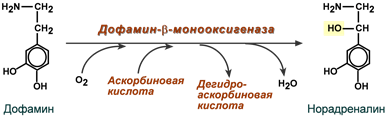
Пример реакции с участием аскорбиновой кислоты
- при синтезе биогенного амина нейромедиатора серотонина,
- при синтезе карнитина (витаминоподобное вещество Вт), необходимого для окисления жирных кислот.
2. Восстановление неорганического иона железа Fe3+ в ион Fe2+ в кишечнике для улучшения всасывания и в крови (высвобождение из связи с трансферрином).
3. Участие в иммунных реакциях:
- повышает продукцию защитных белков нейтрофилов,
- высокие дозы витамина стимулируют бактерицидную активность и миграцию нейтрофилов.
Видимо, именно данная функция повышает потребность организма в аскорбиновой кислоте при простудных и инфекционных заболеваниях до 1,0-1,5 г.
4. Антиоксидантная роль сводится к:
- восстановлению окисленного витамина Е,
- лимитирование свободнорадикальных реакций благодаря взаимодействию с супероксид-анион-радикалом, гидроксил-радикалом, синглетным кислородом,
- снижает окисление липопротеинов в плазме крови и, таким образом, оказывает антиатерогенный эффект.
Показано, что прием аскорбиновой кислоты в дозе 300 мг/сут понижает риск возникновения сердечно-сосудистых заболеваний на 30%.
Гиповитаминоз С
Причина
Пищевая недостаточность, тепловая обработка пищи (потери от 50 до 80%), длительное хранение продуктов (каждые 2-3 месяца количество витамина сокращается наполовину).
В весенне-зимний период дефицит витамина захватывает, в зависимости от региона, 25-75% населения России.
Клиническая картина
Так как особенно интенсивно аскорбиновая кислота накапливается в надпочечниках и тимусе, то ряд симптомов связана со сниженной функцией этих органов. Отмечается нарушение иммунитета, особенно легочного, развивается общая слабость, быстрая утомляемость, похудание, одышка, боли в сердце, отек нижних конечностей. У мужчин происходит слипание сперматозоидов и возникает бесплодие.
Снижается всасываемость железа в кишечнике, что вызывает снижение синтеза гема и гемоглобина и железодефицитную анемию. Уменьшается активность фолиевой кислоты – это приводит к мегалобластической анемии.
У детей дефицит аскорбиновой кислоты приводит к болезни Меллера-Барлоу, проявляющуюся в поражении костей: разрастание и минерализация хряща, торможение рассасывания хряща, корытовидное западение грудины, искривление длинных трубчатых костей ног, выступающие четкообразные концы ребер. Цинготные четки, в отличие от рахитических, болезненны.
Полное отсутствие витамина приводит к цинге – самому известному проявлению недостаточности аскорбиновой кислоты. При этом наблюдается нарушение синтеза коллагена, гиалуроновой кислоты и хондроитинсульфата, что приводит к поражению соединительной ткани, ломкости и проницаемости капилляров и к ухудшению заживления ран. Сопровождается дегенерацией одонтобластов и остеобластов, ухудшается состояние зубов.
Все животные способны синтезировать витамин С самостоятельно, только приматы и морские свинки утратили эту способность и должны получать аскорбиновую кислоту с пищей.
Лекарственные формы
Аскорбиновая кислота чистая или с глюкозой. Аскорутин (в комплексе с биофлавоноидом рутином).
Источник
Гемоглобин синтезируется во всех тканях, но с наибольшей скоростью в костном мозге и печени. В костном мозге гемоглобин необходим для синтеза гемоглобина в ретикулоцитах, в гепатоцитах – для образования цитохрома Р450ю Первая реакция синтеза гема – образование 5-аминолевулиновой кислоты из глицина и сукцинил-КоА идёт в матриксе митохондрий, где в ЦТК образуется один из субстратов этой реакции – сукцинил-КоА. Эту реакцию катализирует пиридоксальзависимый фермент аминолевулинатсинтаза.
Из митохондрий 5-аминолевулиновая кислота поступает в цитоплазму. В цитоплазме проходят промежуточные этапы синтеза гема: соединение 2 молекул 5-аминолевулиновой кислоты молекулу порфобилиногена, дезаминированиепорфобилиногена с образованием гидроксиметилбилана, ферментативное превращение гидроксиметилбилана в молекулу уропор-фобилиногена III, декарбоксилирование последнего с образованием копропорфириногена III. Гидроксиметилбилан может также неферментативно превращаться в уропорфириноген I, который декарбоксилируется в копропорфирино-ген I. Из цитоплазмы копропорфириноген III опять поступает в митохондрии, где проходят заключительные реакции синтеза гема. В результате двух последовательных окислительных реакций копропорфириноген III превращается в протопорфириногенIX, а протопорфириноген IX – в протопорфирин IX. Фермент феррохела-таза, присоединяя к протопорфирину IX двухвалентное железо, превращает его в гем. Источником железа для синтеза гема служит депонирующий железо белок ферритин. Синтезированный гем, соединяясь с б и в-полипепептидными цепями глобина, образует гемоглобин. Гемоглобин регулирует синтез глобина: при снижении скорости синтеза гема синтез глобина в ретикулоцитах тормозится.

Рис. 1. Синтез гемма
Цифрами на схеме указаны ферменты: 1 – аминолевулинатсинтаза; 2 – аминолевулинатдегидратаза; 3 – порфобилиногендезаминаза; 4 – уропорфириноген III косинтаза; 5 – уропорфириногендекарбоксилаза; 6 – копропорфи-риноген III оксидаза; 7 – протопорфириногеноксидаза; 8 – феррохелатаза.
Буквами обозначены заместители в пиррольных кольцах: М – метил, В – винил, П – остатки пропионовой кислоты, А – ацетил, ПФ – пиридоксальфосфат. Донором железа служит депонирующий железо в клетках белок ферритин.
Витамин В12 – биосинтез, биологическая роль. Значение витаминов группы К
Витамин В12 и родственные ему кобаламины играют важную роль в жизнедеятельности человека. Они участвуют в различных биохимических превращениях, предотвращают развитие злокачественной анемии крови, различных заболеваний печени, используются при лечении лучевой болезни. Кобаламины синтезируются различными микроорганизмами. В промышленности производство витамина В12 основано на использовании пропионовокислых бактерий.
Механизм образования витамина В12, наиболее сложного из известных тетрапиррольных пигментов, выяснен значительно лучше, чем, например, хлорофиллов и бактериохлорофиллов. По образному выражению известного английского ученого А. Баттерсби, внесшего большой вклад в раскрытие биосинтеза витамина В12.
Разветвление основного пути биосинтеза тетрапиррольных пигментов в сторону витамина В12 начинается с Урогена. Сначала под действием особых ферментов происходит введение метильной группы. Соединение, получившее название прекоррин-1, далее подвергается метилированию с образованием прекоррина-2. Третье метилирование проходит по мезо-углеродному мостику, и в результате возникает частично восстановленный макроцикл прекоррина-3.
Последующие превращения, каждое из которых контролируется своими ферментами, включает метилирование, сужение макроцикла с образованием корринового цикла, введение метильных групп и затем, два метилирования по мезо-мостикам и декарбоксилирование остатка уксусной кислоты. Заключает этот цикл превращений перегруппировка метильной группы с образованием важного промежуточного соединения – гидрогенобириновой кислоты.
На заключительном этапе биосинтеза кислота амидируется по остаткам уксусной кислоты и включает ионы двухвалентного кобальта, превращаясь в диамидкобириновой кислоты. Далее происходит восстановление Со2+ Со+, и эта активная форма превращается в диамидаденозилкобириновой кислоты. Наличие аденозильноголиганда, является необходимым условием для дальнейшего ступенчатого амидирования четырех карбоксильных групп. Оставшаяся карбоксильная группа кобировой кислоты участвует в образовании так называемой нуклеотидной петли.
Первоначально происходит присоединение 1-аминопропанола-2 с образованием соединения. Ферменты, контролирующие этот процесс, обладают высокой специфичностью к аденозилкобириновой кислоте. Фосфорилирование по гидроксильной группе аминопропанола дает фосфат. Последний превращается в коферментную форму витамина В12 аденозинкобаламина. Замена остатка аденозина на циано-группу приводит к цианкобаламину – лекарственной форме витамина В12. В организме происходит обратная замена [4].
Было установлено, что витамин В12 поступающий с пищевыми веществами, предохраняется от разрушения в кишечнике благодаря тому, что он соединяется с «внутренним» фактором Кастла, природа которого также была выявлена. Он оказался мукопротеином – белком, находящимся в желудочном соке здорового человека и содержащим в своём составе 11-12% гексозамина. Этот фактор был найден также в желтке яиц, в молоке и других пищевых продуктах.
Биохимическая роль витамина В12многогранна, роль витамина В12 заключается в синтезе нуклеиновых групп при превращении гомоцистеина в метионин, а оксиэтиламина в холин, являющихся липотропными факторами.
Витамин В12 принимает участие и в реакции ацетилиривакоэнзима А, ускоряя процесс биологического окисления уксусной и пировиноградной кислот.Введение витамина В12 приводит к уменьшению содержания сахара в крови вследствии усиления окисления глюкозы в тканях. В 1948 г. было доказано положительное действие этого витамина на синтез пуриновых пиримидиновых оснований, т.е. на синтез рибонуклеиновой дезоксирибонуклеиновой кислот.
Предполагают, что витамин В12 способствует превращению глюкозы в дезоксирибозу. Источником в этом случае служат некоторые аминокислоты – глицин, глютаминовая и метионин.
Витамин В12 способствует накоплению жира у животных, ускоряя превращение аминокислот в глюкозу, которая переходит в жир.
Витамин В12 участвует в превращении каротина в витамин А и отложении последнего в печени, он обезвреживает никотиновую кислоту путём её метилирования с образовниемметилникотина.
К витаминам группы К относятся природные вещества – витамин K1 (фнллохннон) и витамин К2 (менахинон). Из синтетических препаратов известны витамин Кз (метннон) и водорастворимый препарат викасол, обладающие высокой биологической активностью. Свое название витамин К получил от слова «коагуляция» (свертываемость).
Витамины группы К участвуют в процессах свертывания крови. Они оказывают влияние на биосинтез прокоагулянтов и являются стимуляторами биосинтеза в печени четырех белков ферментов, необходимых для свертывания крови и образования активных тромбопластина и тромбина.
У взрослого человека витамин К2 синтезируется кишечной микрофлорой (1,5мг в сутки). Синтез витаминов К кишечной микрофлорой исключает возможность возникновения у взрослого человека первичного К-авитамнноза. У взрослого человека возможны вторичные К-авитаминозы, развивающиеся в результате прекращения усвоения витаминов К в кишечнике или вследствие прекращения его эндогенного синтеза кишечной микрофлорой. Частой причиной вторичной недостаточности витамина К являются болезни печени. Вторичный К-авитаминоз может иметь место при обтурационной желтухе, когда вследствие прекращения поступления желчи s двенадцатиперстную кишку нарушается усвоение жирорастворимых веществ, в том числе витаминов группы К.
Вопрос 89.Гормоны передней доли гипофиза и их действие на организм животных
Передняя доля гипофиза вырабатывает группу гормонов белковой или полипептидной структуры, влияющих на организм через действие на щитовидную железу, надпочечники и половые железы.
Аденогипофиз продуцирует также гормоны, действующие на органы и ткани организма – соматотропный гормон или гормон роста, гормон, стимулирующий пигментные клетки -меланоцито-стимулирующий гормон (МСГ), экзофтальмический фактор.
Соматотропный гормон, полученный из гипофизов различных животных и человека, обладает специфичностью, отличаясь по своим физико-химическим и иммунологическим свойствам. Гормон роста, полученный из гипофизов домашних животных, не оказывает биологического действия на приматов. Соматотропный гормон домашних животных, молекулярный вес которого в два раза больше, чем молекулярный вес гормона роста приматов, состоит из биологически активного ядра, общего для соматотропинов всех видов, и аминокислотной оболочки.
Основной стороной биологического действия гормона роста является его способность стимулировать анаболические процессы.
Гормон роста повышает содержание белка в печени, мышцах и тканях, уменьшает выделение азота. Под влиянием гормона роста уменьшается выделение мочой калия, фосфора, магния, натрия и хлора; выделение кальция увеличивается. Увеличивается количество внеклеточной жидкости. Уровень мочевины в крови снижается. Для проявления анаболического действия гормона роста необходимо наличие в организме определенного уровня кортизола, инсулина и тироксина.
Гормон роста оказывает действие на углеводный обмен. При достаточно длительном применении он повышает уровень сахара в крови [3].
Этот гипергликемизирующий эффект осуществляется рядом механизмов. Гормон роста увеличивает поступление углеводов из печени в кровь. Гормон роста тормозит переход углеводов в жиры, повышает выделение инсулина. Это связано с непосредственным действием гормона на островки поджелудочной железы, либо является следствием повышенного поступления глюкозы в кровь. Одновременно гормон роста стимулирует выработку глюкагона клетками островков поджелудочной железы, активизирует инсулиназную активность печени, повышает выработку В-липопротеидного антагониста инсулина.
Гормон роста оказывает на углеводный обмен фазное действие. В первые часы после инъекции он вызывает снижение сахара крови, возможно, в связи с усилением выработки инсулина или вследствие высвобождения связанного инсулина. В дальнейшем проявляется гипергликемизирующее действие гормона роста. При длительном избытке гормона роста, наступает истощение инсулярного аппарата и может развиться сахарный диабет. У неполовозрелых животных, у которых способность инсулярного аппарата к регенерации велика, гормон роста не оказывает диабетогенного действия.
Гормон роста оказывает жиромобилизующее действие. После его введения повышается содержание неэстерофицированных жирных кислот в крови и имеет место увеличение количества жира в печени.
Гормон роста стимулирует окисление жира в печени, вызывая преходящуюгиперкетонемию. Выработка кетоновых тел в печени под влиянием гормона роста повышается. У животных с экспериментальным диабетом и у больных сахарным диабетом может развиться кетоацидоз. Этот эффект выражен у больных сахарным диабетом с удаленным гипофизом. Эффект гормона роста на жировой и белковый обмен проявляется на фоне «обусловливающего» пермессивного действия физиологического количества кортизола. Большие дозы гликокортикоидов тормозят жиромобилизующее действие гормона роста. Гормон роста усиливает функцию почек, повышает клиренс креатинина. Меланоцито-стимулирующий гормон (МСГ) вырабатывается у животных средней долей гипофиза, которая у человека является рудиментарным органом.
Источник
