Шабалов анемия у детей
Анемия – патологическое состояние, при котором снижается уровень эритроцитов и гемоглобина в единице крови. Анемии встречаются достаточно часто, способны утяжелять течение других заболеваний. В основе развития лежит нарушение эритропоэза, которое обеспечивает достаточное количество веществ для образования эритроцитов: медь, железо, кобальт, цинк, витамины группы В.
Нормы у детей: (доношенных)
? Эритроциты 5-7 *10 12/л
? Гемоглобин 180-240 г/л так как внутриутробная гипоксия
Преобладание фетального гемоглобина (70-80%), у 6-12 месячных детей и взрослых фетальный гемоглобин менее 12%. Первая неделя – анизоцитоз, полихроматофильный ретикулоцитоз 10-50 промилле, единичные нормобластные, т.е. усилена регенерация. Эритроциты и гемоглобин после рождения начинают снижаться, идет распад фетального гемоглобина, к концу 10 дня эритроциты составляют 5*10 12/л, а гемоглобин 180 г/л. В дальнейшем продолжают снижаться, но медленнее. Минимальный уровень в 4-6 месяцев: эритроциты равны 3,8*10 12/л гемоглобин 110 г/л. У доношенных физиологическая анемия, у недоношенных снижение эритроцитов и гемоглобина более выражены и равны 2,5 – 3*10 12/л и 80-100 эритроцитов и гемоглобина соответственно. Наступает раньше (1,5 месяца) – это ранняя анемия. Снижение эритроцитов и гемоглобина в первый месяц является результатом снижения продукции эритроцитов, увеличение скорости их разрушения, вслествии относительной гемодилюции. Через 4-6 месяцев эритроциты и гемоглобин увеличиваются ; эритроциты 4,2 – 4,5*10 12/л , а гемоглобин 130-150 г/л. Длительность жизни составляет 60-80 дней (120 в отличии от новорожденных).
Классификация (Мысягин):
- Дефицитная
? железодефицитная
? витаминодефицитная
? белководефицитная
- гипо- и апластическая
? врожденная
? приобретенная
- Геморрагическая
? острая кровопотеря
? хроническая кровопотеря
- Гемолитическая
? обусловленная наследственными аномалиями эритроцитов (микросфероцитарная, несфероцитарная, овалоклеточная)
? аномалии эритроцитов обусловленные химическими и лекарственными веществами (эритропатии, порфирии)
? приобретенные (ночная пароксизмальная гемоглобинурия)
? иммунные (аутоиммунные, …???)
? вызванные неиммунными агрессивными факторами (токсическая, ожоговая, внутри эритроцитарная инвазия)
- Анемия при других заболеваниях
? инфекционные
? злокачественные новообразования
? диффузные заболевания соединительной ткани и.т.д
- Анемия новорожденных (тур.???)
Каждая анемия по тяжести делится на легкую(Hb 110-83 г/л. эритроциты 3,5*10 12/л), среднюю(Hb 82-66 г/л, эритроциты 3,4-2,5 10 12/л), тяжелая (Hb менее 66 г/л, эритроциты менее 2,5*10 12/л).
Функциональные возможности оцениваются по ретикулоцитам:
? регенераторная (норморегенераторная) количество ретикулоцитов 5-50%
? гиперрегенераторная – количество ретикулоцитов более 50%
? гипорегенераторная — количество ретикулоцитов менее 5% или ретикулоцитоз не соответствует тяжести анемии. В норме у здорового человека 5-12%
По цветовому показателю:
? нормохромная ЦП = 0,8-1,0
? гипохромная ЦП менее 0,8
? гиперхромная ЦП более 1,0
При снижении эритроцитов уменьшается перенос кислорода к органам и тканям, развивается кислородное голодание. Наиболее чувствительными являются ЦНС и сердечно-сосудистая система: головная боль, головокружение, быстрая утомляемость, малоподвижность, снижение аппетита, тахикардия, одышка при физической нагрузке, приглушение сердечных тонов, систолический шум на верхушке и основании сердца. Ведущий симптом — бледность кожных покровов и слизистых, иногда желтушность.
Железодефицитная анемия (78% от всех анемий)
Наблюдается у 70% детей раннего возраста. В этом возрасте в организме около 4,5гр железа, 2/3 его в эритроцитах, остальное в костном мозге и клетках РЭС. Находится в двух формах: гем (гемоглобин, миоглобин, эритроциты), ферритин и гемосидерин (печень и селезенка). В физиологических условиях потребность растущего организма обусловлена:
- потерями железа
- увеличением массы тела, следовательно, и увеличение количества крови (у взрослых только 1е).
Потеря железа у мужчины 1,0-1,5 мг/сутки с калом, с мочой, с желчью, часть с эпителием кожи и потом, расход на ногти, волосы, явные и скрытые кровотечения, инвазии глистов. У доношенных новорожденных всего 250 мг железа в организме накопление железа у плода наиболее интенсивно в последние 3 месяца. У недоношенных детей железа меньше. К году 430 мг, ежедневный прирост 0,5 мг, следовательно, для компенсации потерь и обеспечения роста необходимо 1,0 мг/сутки. У ребенка теряется 0,5 мг/сутки. В период полового созревания потребность 1-2 мг/сутки. Всасывание железа происходит с пищей в 12-перстной и тощей кишке, гемовое железо всасывается лучше, негемовое ( трехвалентное) под действием желудочного сока превращается в закисное двухвалентное, часть трехвалентного связывается с аскорбиновой кислотой и образует растворимый комплекс. Гемовое железо всасывается независимо от желудочного сока. В слизистой кишечника распадается до двухвалентного железа (до этого без изменений). Далее железо попадает энтероциты, а оттуда в плазму крови где связывается с трансферрином, далее поступает в ткани и органы. При дефиците скорость перехода из плазмы в ткани увеличивается. Железо поступает в организм с пищей, содержится в растительных и животных продуктах: в печени, мясе, бобах, сои, петрушке, шпинате, яблоках, гранатах, черносливе, хлебе, рисе, гречке. Из растительной пищи всасывается ограниченно, из животной пищи всасывается полнее. Лучше всасывается в виде гема, следовательно, из печени (ферритин, гемосидерин) хуже, чем из мяса (90%). Отрицательно действуют на всасывание оксалаты, фосфаты, фитаты, тошен. Усиливает всасывание: витамин С, пировиноградная кислота, янтарная кислота, сорбит, фруктоза. При дефиците железа различают:
- железодефицитные состояния – отсутствие депо железа в организме (скрытый дефицит железа)
- железодефицитная анемия (неполноценные эритроциты).
Этиология
? В результате недостаточного поступления с пищей
? Нарушения всасывания
? Избыточное выведение (дисфункция кишечника)
? Повышенная потливость (препубертатный).
Чаще ращвивается от 6 месяцев до 1,5 лет – так как у ребенка неправильное питание (молочное), питание растительной пище приводит к дефициту железа из-за недостаточного всасывания, уязвимы недоношенные дети, с крупным весом, от многоплодной беременности, от женщин с анемией.
Зависит от тяжести.
- Общеанемические симптомы: головокружение, гепатоспленомегалия (увеличение на 10%), обморок, бледность кожи и слизистых оболочек.
- Сидеропеническая анемия: изменяются ЦНС, ЖКТ, ССС, кожа и слизистая, придатки кожи: ногти, волосы, извращение вкуса и обоняния, сухость кожи с трещинами, ангулярный стоматит, ногти сначала выпуклые затем становятся вогнутой формы, повышена ломкость ногтей и волос
? снижение общего гемоглобина и снижение содержания гемоглобина в эритроцитах
? гипохромная (цветной показатель до 0,4-0,6)
? микроцитоз (анизо- и пойкилоцитоз)
? количество ретикулоцитов обычно в норме ( на фоне лечения увеличивается)
? снижения железа в сыворотке
? увеличение общей и латентной железосвязывающей способности сыворотки крови
? снижение коэффициента насыщения железом трансферрина ( в норме 6-24%).
В костном мозге наблюдается эритроидная гиперплазия с уменьшением количества сидеробластов.
Клиника латентного периода: аналогична или отсутствует, в общем, анализе крови нет анемии, признаки только в биохимическом анализе. Течение скрытой анемии такое же как при железодефициной.
Устранение причин анемии, правильный режим (воздух, массаж, гимнастика) и питание (своевременные добавки и прикормы, увеличение количества мяса). Препараты железа назначаются только при убеждении в дефиците железа. Если передозировка железа, то можно отравить ребенка, а также может произойти поражение ЖКТ, гемосидероз, почечно-печеночная недостаточность. Препараты железа принимаются per os, внутримышечно и внутривенно.
Ионные препараты – на основе солей двухвалентного железа или полисахаридных комплексов с железом: сульфат железа, аскорбинат железа, ферроплекс, актиферрин, феррональ (44 мг), конферон (51мг железа+янтарная кислота).
Неионные препараты — с витамином С – полимальтозные содержащие компонент трехвалентного железа: мальтофер, феррум лек, ферлатум, эти препараты менее опасные. Суточная доза 4-6 мг/кг массы тела. Первые 2-3 дня вводят половинную дозу (чтобы избежать побочного действия –диспепсия), к 4-6 дню доводят до полной дозы, перед едой до 3 раз в сутки, в сочетании с витамином С если о не входит в состав препарата, не следует запивать, чаем и молоком т.к. они снижают всасывание железа в тонком кишечнике. В рационе следует снизить содержание злаковых, молока. Эффект развивается через 2 недели: повышается уровень гемоглобина, необходимо еще 6-8 недель для создания запасов, затем еще 8-12 недель принимают половинную дозу. Если отсутствует эффект через 2-3 недели то следовательно имеет место нарушение всасывания или нерегулярность приема. Внутримышечное и внутривенное введение проводят по показаниям:
? тяжелая анемия
? непереносимость перорального приема
Возможно развитие аллергических реакций и гемосидероза, исходя из этого, внутривенный и внутримышечный прием проводят только в стационаре.
Препараты трехвалентного железа: феррум лек, эктофер, фербитал.
Ферум лек: полиизомальтаза + железо назначают внутримышечно. 1 ампула – 100 мг железа.
Натрийсахаратный комплекс + железо назначают внутривенно. 1 ампула – 100 мг железа.
Расчет курсовой дозы:
- (120-Hb)*0,4* массу ребенка в килограммах = курсовая доза (мг)
- (масса ребенка*0,78 – 0,35)*Hb = курсовая доза (г/л)
вводят через день, первая инъекция меньше чем последующая. Эктофер и фербитол содержат сорбитовые компоненты их нельзя вводить внутривенно и внутримышечно вместе с преоральным приемом. Внутривенно и внутримышечно нельзя вводить при нарушении функции печени и почек – возможно развитие гемосидероза.
Дисферал – внутримышечно 60-80 мг/кг.
Тетацил натрия – 15-25 мг/кг, внутривенно, капельно. Дополнительно назначают витамины С, В1, В2. В6 и В12 не назначают (В6 способствует протопорфиринам).
Переливание эритроцитарной массы проводить не следует, так как эритроциты через 2-3 недели разрушаются (сенсибилизируют организм). Критерии эффективности лечения: появление ретикулоцитарного криза на 7-10 день от начала лечения (в 2 раза больше нормы), нарастание гемоглобина на 10 мг/л в неделю, клинико-лабораторная ремиссия в конце лечения.
У недоношенных анемия развивается в 60-90% случаях.
Классифицируют ее по срокам: ранняя ( первые 3 месяца), поздняя (после 3 месяцев). Раннюю анемию нельзя предупредить.
Патогенез: наличие усиленного гемолиза и функциональной незрелости костномозгового кроветворения. Гемолиз – недостаток фетального гемоглобина, недостаток витамина Е. Незрелость кроветворных органов – снижение эритропоэтических процессов в костном мозге. Ранняя анемия еще не железодефицитная (препараты железа не назначают).
Лечение: препараты железа назначать не надо, принимают витамин Е, аскорбиновая кислота, фолиевая кислота,витамины группы В. Через 3-4 месяца спонтанное повышение уровня эритроцитов, иногда впоследствие снова снижается. Поздняя анемия железодефицитная клиника ее соответствующая.
Лечение: препараты железа, витамин С, фолиевая кислота 1-5 мг/сутки, витамин Е 10-20 мг/сутки в течении 2-3 недель, далее поддерживающая терапия.
- Антенатальная: правильное питание беременных, своевременное лечение анемии беременных с препаратами железа.
- Постнатальная: своевременное введение соков, прикормов, массаж гимнастика, воздух, профилактика заболевания сопровождающих анемию (дистрофии, инфекции, рахит)
- Особенное внимание недоношенным, с крупной массой тела, от многоплодной беременности, от женщины с анемией. Недоношенным 2-12 месяцев – препараты железа 1-2 мг/кг/сутки. Детям от матерей с анемией: 1 месяц – 10 дней метаболитические комплексы, пантенат кальция, тиамин, липамид, токоферол, 2-3 месяц курс повторить 10 дней. 2 полугодие если гемоглобин снижен до 120 г/л назначают этот комплекс на 10 дней и в течении месяца необходимо принимать железо с фетином в разные часы.
Развивается при длительном белковом голодании, при вскармливании растительной, углеводной пищей, преимущественно у детей африки. Дефицт белка нарушает всасывание железа и витаминов следовательно развивается анемия.
Клиника: общеанемические симптомы сопровождаются отеками.
Лечение: препараты железа, достаточное количество белка и витаминов.
Витаминодефицитная анемия занимает второе место. В12 и фолиевая кислота нарушает созревание клеток в костном мозге и развивается мегалобластическое кроветворение страдает и тремоцитопоэз, и лейкопоэз, снижается продолжительностьжизни эритроцитов. Уровень железа в тканях и плазме увеличивается. Наиболее чувствительны дети младшего возраста. Могут быть обусловлены глитной инвазией6 развивается анемический синдром, поражается ЖКТ (глоссит, лакированный язык, неврологические симптомы, парастезии). Эритроциты уменьшаются в большей степени чем гемоглобин. В крови: макроцитоз, нормо или гиперхр, анизо и пойкилоцитоз, при тяжелой анемии – миелобласты в периферической крови. Лейкоцитопения, тромбоцитопения (геморрагический сиптом), в костном мозге мегалобластный эритропоэз.
Лечение: фолиевая кислота 10-30 мг/сутки в течении 2-3 недель, витамин В12 100-200 мк/гр в сутки, витамин С, препараты железа если оно снижено.
Гипо- и апластические анемии.
Снижение гемопоэза в костном мозге (все 3 ростка). Признаки: бледность , геморрагии на коже, слабость, в крови снижение эритроцитов,, особенно ретикулоцитов. Клиника и лабораторные изменения нарастают. При отсутствии лечения прогноз неблаагоприятный. Печень и селезенка не увеличиваются. Костный мозг беден ябросодержащими элементами, происходит замещение его жировой тканью.
Врожденная анемия.
Анемия Фанкони: снижение эритроцитов, лейкоцитов, эритропоэза, характеризуется врожденными уродствами (скелет, сердечно-сосудистая анемия). Наследственная патология, передается по рецессивному типу, прододжительность жизни 2 года.
Гипопластическая анемия Эстрена-Доминика: угнетает все 3 ростка кроветворения, но врожденных уродств нет.
Анемия Даймонда- Блэкфона: угнетается только эритропоэз, проявляется рано, живут до 10 и долее лет.
Лечение: премодическое переливание эритромассы, использование кортикостероидов и анаболических гормонов, витаминотерапия, спленэктомия. Оптимальное лечение – пересадка костного мозга.
Гемолитические анемии
Повышен распад эритроцитов в крови, наследственная микросфероцитарная, гемолитическая анемия, Минковского-Шоффара. Тип наследования доминантный. Дефект мембраны эритроцитов : мембрана эритроцитов проницаема для ионов натрия следовательно жидкость поступает в эритроциты и они превращаются в микроциты в селезенке происходит их изменения (микросфероциты) его устойчивость снижается, он проходит через селезенку 2-3 раза.
Клиника: волнообразное течение с кризами, основные симптомы: анемия желтуха спленомегалия. В кризе: 1,5-2*10 12 эритроцитов, ЦП в норме. Продукты распада не теряются, так как нет потери железа. Желтуха отчетлива в кризе из-за гемолиза эритроцитов и накапливается непрямой биллирубин. Селезенка увеличивается после первого года жизни. При длительном течении заболевание у детей башенный череп широкая переносица, отставание в психическом и нервно-психическом развитии. В крови признаки повышенной регенерации ( ретикулоцитоз, полихроматофиллия и.т.д.), диаметр эритроциты снижены до 5,4-6,0 микрон, характерно снижение максимальной осмотической устойчивости эритроцитов. Норма 0,44-0,48. При анемии минимальное снижение 0,6-0,7% во время криза увеличение соэ лейкоцитоз. В костном мозге интенсивная эритроидная реакция нормобластного типа. Криз может быть гипо или апластическим (при ошибочном диагнозе).
Леченпие кризов: эритромасса, гормоны, инфузионная терапия, если кризы частые спленэктомия желательно до 5 лет.
(Visited 704 times, 1 visits today)
Источник
В статье освещены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий у детей. Представлены основные принципы дифференциальной диагностики и лечения указанных дефицитных анемий у детей.
В настоящей публикации на основании данных литературы и анализа собственных наблюдений представлены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий, а также принципы их лечения у детей. Установлено, что основной формой дефицитных анемий (ДА) в педиатрической популяции является анемия, обусловленная недостаточным содержанием в организме железа. При этом особо подчеркивается, что железодефицитная анемия (ЖДА) не только наиболее распространенная ДА, но и самое частое гематологическое заболевание у детей [1–3]. С учетом того, что другие типы анемий (в т. ч. развивающиеся при дефиците таких витаминов, как фолиевая кислота и В12) хуже известны врачам-педиатрам, их верификация, как правило, запаздывает, т. к. они ошибочно принимаются за ЖДА. Поздняя диагностика и отсутствие адекватной терапии при этом приводят к прогрессированию патологических процессов. Это негативно сказывается на росте и развитии детского организма и ухудшает качество жизни ребенка. Принимая во внимание актуальность данной проблемы, авторы пришли к выводу о необходимости представить для практикующих врачей-педиатров ключевые положения дифференциальной диагностики и лечения анемий, обусловленных дефицитом железа, фолиевой кислоты и витамина В12 у детей.
Дифференциальная диагностика ДА у детей
Критерием анемии, независимо от этиологии, является снижение уровня гемоглобина (Hb) ниже возрастной нормы. Так, синдром анемии констатируют, если концентрация Hb в капиллярной крови ниже: 110 г/л — у детей в возрасте от 1 мес. до 5 лет, 115 г/л — у детей 6–12 лет, 120 г/л — у детей старше 12 лет и подростков. Кроме этого, зная уровень Hb, можно определить тяжесть анемического синдрома. Так, для детей, достигших месячного возраста и старше, снижение Нb до 90 г/л является признаком анемии легкой степени, уровень Нb в пределах 70–90 г/л характерен для анемии средней тяжести, а падение Нb ниже 70 г/л определяет тяжелую степень анемии [1–4].
Нозологическая верификация характера анемии проводится на основе анализа клинико-анамнестических данных, результатов лабораторного и, если необходимо, инструментального обследования пациента. Общими клиническими проявлениями анемии, независимо от этиологии, являются повышенная утомляемость, снижение работоспособности, склонность к инфекциям. Среди дополнительных симптомов, которые могут отмечаться при ЖДА, — извращение аппетита и пристрастие к необычным запахам, изменение ногтевых пластин, расслоение ногтей, выпадение волос, атрофия сосочков языка, дисфагия. В свою очередь, при витамин В12-дефицитной анемии имеют место неврологические нарушения (атаксия, парестезии, гипорефлексия и другие проявления фуникулярного миелоза), «лакированный» язык и желтуха. Непрямая гипербилирубинемия может также отмечаться и при фолиеводефицитной анемии (табл. 1).
Наличие желтухи и анемии при этом нередко становится причиной ошибочного заключения о гемолитическом характере анемии, если врач не обращает внимания на отсутствие ретикулоцитоза. Следует отметить, что иктеричность при анемиях, обусловленных дефицитом витамина В12 или фолиевой кислоты, связана с неэффективным эритропоэзом и повышенным разрушением предшественников эритроцитов в костном мозге [1–3, 5–7].
Несмотря на описанные выше симптомы, типичные для конкретных ДА, их клинические проявления могут быть слабо выражены при легкой степени анемии, особенно у детей раннего возраста. В связи с этим этиологическая верификация генеза анемического синдрома проводится на основании не только клинических проявлений и анамнестических данных. Обязательным условием установления диагноза является корректная трактовка результатов лабораторного обследования. При этом минимально достаточным уровнем лабораторного обследования является проведение клинического и биохимического анализов крови.
Хорошо известно, что показаниями к исследованию клинического анализа крови для исключения анемии у детей являются анамнестические (недоношенность, задержка внутриутробного развития, исключительно грудное вскармливание ребенка, если мать имеет хронические заболевания кишечника или является вегетарианкой и др.) и/или клинические факторы риска (геморрагический синдром, синдром мальабсорбции, инфекционно-воспалительные заболевания, желтуха, лимфаденопатия, гепато- или спленомегалия и другие патологические состояния). При оценке результатов клинического анализа крови нельзя ограничиваться только поиском лабораторных признаков анемии. Обязательно должны быть проанализированы все параметры гемограммы (эритроциты и их индексы, ретикулоциты, тромбоциты и их индексы, общее количество лейкоцитов, лейкоцитарная формула, а также абсолютное количество нейтрофилов, лимфоцитов, моноцитов и эозинофилов, СОЭ). Это позволяет уже при первичном обращении пациента очертить круг основных причин выявленной анемии и наметить основные диагностические мероприятия для расшифровки генеза заболевания [1–4].
Так, для ЖДА типичными признаками являются: гипохромия и микроцитоз эритроцитов при нормальном уровне ретикулоцитов, если недостаточное содержание железа в организме обусловлено алиментарными факторами или синдромом мальабсорбции. В тех же случаях, когда ЖДА имеет постгеморрагический генез, гипохромия и микроцитоз эритроцитов будут сопровождаться ретикулоцитозом [1–4]. В свою очередь для анемий, обусловленных недостатком в организме как фолиевой кислоты, так и витамина В12, характерны гиперхромия и макроцитоз эритроцитов, а также ретикулоцитопения (табл. 2).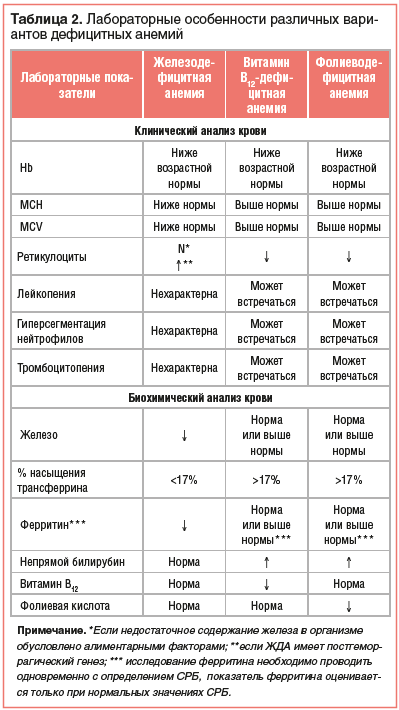
Кроме этого, при фолиево- и витамин В12-дефицитной анемиях могут встречаться лейко- и тромбоцитопения, гиперсегментация нейтрофилов. С учетом того, что в ряде случаев ДА имеет комбинированный генез, при котором дефицит железа сочетается с дефицитом фолиевой кислоты или витамина В12, типичные гематологические признаки могут не выявляться или быть разнонаправленными. Это определяет необходимость обязательного проведения биохимического анализа крови с определением, кроме общепринятых показателей, таких параметров, как железо, железосвязывающая способность, процент насыщения трансферрина, ферритин, фолиевая кислота и витамин В12 [6, 7]. Особо следует подчеркнуть, что ферритин должен определяться вместе с С-реактивным белком (СРБ). При этом оценивать уровень ферритина можно только в тех случаях, когда значения СРБ находятся в пределах нормативных. Это объясняется тем, что ферритин относится к протеинам воспаления и его уровень повышается при воспалительных процессах в организме. В связи с этим нормальный или высокий уровень ферритина при повышенных значениях СРБ может стать причиной ошибочного заключения об отсутствии железодефицитного состояния [2–4]. Особенности биохимического анализа крови при различных вариантах ДА представлены в таблице 2.
Лечение ДА у детей
Корректная трактовка клинико-анамнестических данных и результатов лабораторного обследования позволяет верифицировать причину ДА и своевременно назначить адекватную терапию. Принципиально важным при этом является положение о том, что компенсировать дефицитные состояния невозможно только за счет нормализации рациона питания. Основная роль в купировании дефицита железа, фолиевой кислоты и витамина В12 принадлежит заместительной фармакотерапии [1–7]. При этом для лечения ЖДА используются солевые препараты железа или препараты на основе железа гидроксид полимальтозата. Суточная доза препаратов зависит от массы тела и возраста ребенка, расчет при этом проводится по элементарному железу. Так, для солевых препаратов железа, назначаемых внутрь, используются следующие дозы (расчет по элементарному железу!): для детей до 3 лет — 3 мг/кг/сут, для детей старше 3 лет — 45–60 мг/сут, для подростков —
до 120 мг/сут. При использовании пероральных форм железа гидроксид полимальтозата рекомендованные дозы составляют 5 мг/кг/сут (расчет по элементарному железу!). Продолжительность терапии препаратами железа зависит от степени тяжести ЖДА. При легкой ЖДА курс лечения составляет 3 мес., при среднетяжелой форме — 4,5 мес., при тяжелой — до 6 мес. [3].
В случае диагностики фолиеводефицитной анемии заместительная терапия проводится препаратами фолиевой кислоты. Рекомендовано использовать следующие суточные дозы фолиевой кислоты: для детей до 1 года — 0,25–0,5 мг/сут, для детей старше 1 года — 1,0 мг/сут. При синдроме мальабсорбции доза может быть повышена до 5–15 мг фолиевой кислоты в сутки. Терапия проводится в указанных дозах ежедневно на протяжении 4–6 нед. Через 7 дней от начала лечения необходимо выполнить клинический анализ крови с обязательным подсчетом ретикулоцитов (рис. 1). Повышение уровня ретикулоцитов на фоне приема фолиевой кислоты указывает на правильно установленный диагноз и является обоснованием для продолжения терапии. Купирование анемии достигается через 4–6 нед. от начала лечения [6].
Для лечения витамин В12-дефицитной анемии используют препараты цианокобаламина для парентерального введения. При этом рекомендовано придерживаться следующего режима дозирования: для детей до 1 года — 5 мкг/кг/сут, для детей старше 1 года — 100 мкг/сут, для подростков — 200 мкг/сут. Препарат вводится внутримышечно 1 р./сут ежедневно. На 7–10-й день терапии проводят клинический анализ. Выявление ретикулоцитоза позволяет сделать вывод об эффективности проводимого лечения. Терапию следует продолжить в том же режиме дозирования еще в течение 3–4 нед. В дальнейшем, при достижении нормализации уровня гемоглобина, переходят на поддерживающее лечение: цианокобаламин вводят в терапевтической дозе 1 раз в 7 дней в течение 2 мес., а затем 1 раз в 14 дней в течение 6 мес. (рис. 2). Учитывая, что дефицит витамина В12, как правило, редко обусловлен алиментарными факторами, одновременно проводят поиск причин данного патологического состояния (болезнь Крона, целиакия, инвазия широким лентецом, наследственные нарушения всасывания и/или транспортировки витамина В12 и др.) [7]. В тех случаях, когда имеют место полидефицитные состояния с развитием анемического синдрома, оправданно комбинированное заместительное лечение. Чаще всего у детей встречается сочетанный дефицит железа и фолиевой кислоты, что требует одновременного назначения препаратов железа и фолиевой кислоты.
Заключение
Таким образом, выявление анемии у ребенка определяет необходимость обязательного уточнения причин указанного патологического состояния. Своевременная верификация этиологии анемии позволяет без промедления начать адекватную терапию, что определяет ее эффективность и улучшает качество жизни ребенка. Авторы выражают надежду, что информация, представленная в настоящей публикации, будет полезна практикующим врачам-педиатрам.
Источник
