Схема переноса кислорода гемоглобином
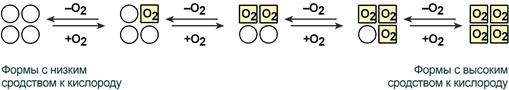
Кооперативное взаимодействие
Взаимовлияние протомеров олигомерного белка друг на друга называется кооперативное взаимодействие.
В легких такое взаимодействие субъединиц гемоглобина повышает его сродство к кислороду и ускоряет присоединение кислорода в 300 раз. В тканях идет обратный процесс, сродство снижается и ускорение отдачи кислорода также 300-кратное.

Схема кооперативного взаимодействия субъединиц гемоглобина
Объясняется такой феномен тем, что в легких при присоединении первой молекулы кислорода к железу (за счет 6-й координационной связи) атом железа втягивается в плоскость гема, кислород остается вне плоскости. Это вызывает перемещение участка белковой цепи и изменение конформации первого протомера. Такой измененный протомер влияет на другие субъединицы и облегчает связывание кислорода со второй субъединицей. Это меняет конформацию второй субъединицы, облегчая присоединение последующих молекул кислорода и изменение других протомеров.
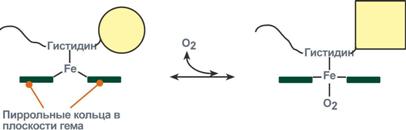
Изменение формы субъединиц гемоглобина
при присоединении и отщеплении кислорода
Дезоксиформа гемоглобина обозначается как Т-форма, напряженная (англ. tense), она обладает существенно более низким сродством к кислороду. Оксигенированная форма, или R-форма (англ. relaxed), обладает высоким сродством к кислороду.
Изменение рН среды
Влияние рН на сродство гемоглобина к кислороду носит название эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается.
При повышении концентрации протонов (закисление среды) в тканях возрастает освобождение кислорода из оксигемоглобина. В легких после удаления угольной кислоты (в виде СО2) из крови и одновременном увеличении концентрации кислорода высвобождаются ионы Н+ из гемоглобина.
Реакция взаимодействия кислорода с гемоглобином упрощенно имеет вид:

Изменение сродства гемоглобина к кислороду в тканях и в легких при изменении концентрации ионов H+ и О2 обусловлено конформационными перестройками глобиновой части молекулы. В тканях молекула О2 отрывается от железа и ионы водорода присоединяются к остаткам гистидина (глобиновой части), образуя восстановленный гемоглобин (H-Hb) с низким сродством к кислороду. В легких поступающий в больших количествах кислород “вытесняет” ион водорода из связи с остатком гистидина гемоглобиновой молекулы.
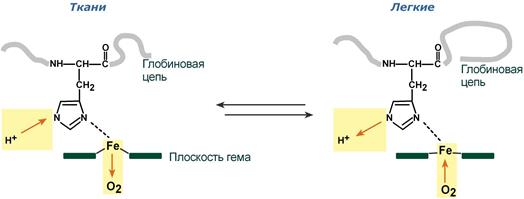
Механизм эффекта Бора
Роль 2,3-дифосфоглицерата
2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного метаболита гликолиза, в реакциях, получивших название шунт Раппопорта.
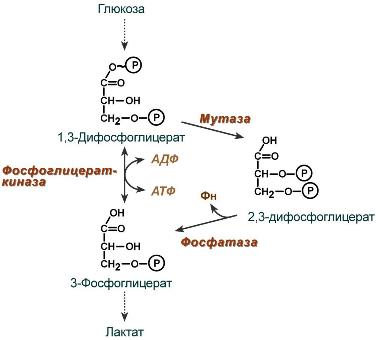
Реакции шунта Раппопорта
2,3-Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с β-цепями, образуя поперечный солевой мостик между атомами кислорода 2,3-дифосфоглицерата и аминогруппами концевого валина обеих β-цепей, также аминогруппами радикалов лизина и гистидина.
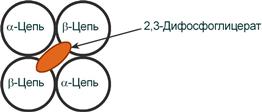
Расположение 2,3-дифосфоглицерата в гемоглобине
Функция 2,3-дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду, что имеет особенное значение при подъеме на высоту и при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в 2 раза.
ГБОУ ВПО.
<<Красноярский государственный
медицинский
Университет им. Проф. В.Ф. Войно-Ясенецкого>>
Министерства здравоохранения
и социального развития
Российской федерации.
Кафедра биологической
химии с курсом медицинской, фармацевтической
и токсикологической химии.
Зав.Кафедрой:Салмина Алла Борисовна
Преподаватель:Буйко Ольга Васильевна
Реферат по химии.
По
теме: Механизмы переноса кислорода
и углекислого газа с участием гемоглобина.
Выполнил: Студент 122-ой группы,
Факультета ФМО,
Специальности “Лечебное дело”
Арзамазов Леонид Александрович
Проверил(а):
2012
Содержание:
- Основные понятия по теме “Механизмы переноса кислорода и углекислого газа с участием гемоглобина” (стр.3)
Основные механизмы
переноса (стр.4-8)
- Механизм переноса кислорода путем диффузии кислорода и углекислого газа через аэрогематический барьер. (стр.4)
- Механизм транспорта кислорода кровью.(стр.5)
- Механизм транспорта углекислого газа кровью. (стр.6)
- Механизм транспорта газов в тканях.(стр.7-8)
- Регуляция дыхания. (стр.8-12)
- Заключение
Основные понятия:
Кровь- внутренняя среда организма,
образованная жидкой соединительной
тканью. Состоит из плазмы и форменных
элементов: клеток лейкоцитов и постклеточных
структур (эритроцитов и тромбоцитов).
Циркулирует по системе сосудов под действием
силы ритмически сокращающегося сердца
и не сообщается непосредственно с другими
тканями тела ввиду наличия гистогематических
барьеров. В среднем, массовая доля крови
к общей массе тела человека составляет
6,5-7%.
Плазма(крови)- жидкая часть крови,
в которой взвешены форменные элементы
— вторая часть крови. Процентное содержание
плазмы в крови составляет 52—61 %. Макроскопически
представляет собой однородную несколько
мутную (иногда почти прозрачную) желтоватую
жидкость, собирающуюся в верхней части
сосуда с кровью после осаждения форменных
элементов. Гистологически плазма является
межклеточным веществом жидкой ткани
крови.
Гемоглобин – сложный
железосодержащий белок кровосодержащих
животных, способный обратимо связываться
с кислородом, обеспечивая его перенос
в ткани. У позвоночных животных содержится
в эритроцитах.
Эритроцит- также известные под
названием кра́сные кровяны́е тельца́, — клетки
крови человека, позвоночных животных
и некоторых беспозвоночных главной функцией
которых, является перенос кислорода.
Диффузия – процесс взаимного проникновения
молекул одного вещества между молекулами
другого, приводящий к самопроизвольному
выравниванию их концентраций по всему
занимаемому объёму
Активный транспорт- перенос вещества
через клеточную или внутриклеточную
мембрану (трансмембранный А.т.) или через
слой клеток (трансцеллюлярный А.т.), протекающий
против градиента концентрации из области
низкой концентрации в область высокой,
т. е. с затратой свободной энергии организма.
В большинстве случаев, но не всегда, источником
энергии служит энергия макроэргических
связей АТФ.
Кислород(О2)– Химический элемент
главной подгруппы VI группы,
с атомным номером 8, при нормальных условиях —
газ без цвета, вкуса и запаха, молекула
которого состоит из двух атомов кислорода
(формула O2). Жидкий кислород имеет
светло-голубой цвет, а твёрдый представляет
собой кристаллы светло-синего цвета.
Углекислый газ(СО2)- бесцветный
газ (в нормальных условиях), без запаха,
со слегка кисловатым вкусом.
Сурфактант(легочный) – смесь поверхностно-активных
веществ, находящаяся на границе воздух-жидкость
в лёгочных альвеолах, то есть выстилающая
альвеолы изнутри. Препятствует спадению
(слипанию) альвеол за счёт снижения поверхностного
натяжения жидкости. Сурфактант секретируется
специальной разновидностью альвеолоцитов
II типа.
Аэрогематический барьер(аэро — воздух + гема – кровь)- барьер
между кровью и воздухом (в альвеолах)
Альвеола (лат. alveolus — ячейка, углубление, пузырёк)-
концевая часть дыхательного аппарата
в лёгком, имеющая форму пузырька, открытого
в просвет альвеолярного хода. Альвеолы
участвуют в акте дыхания, осуществляя
газообмен с лёгочными капиллярами.
Капилляр- (от лат. capillaris — волосяной)тонкие сосуды
в организме человека и
других животных. Средний их диаметр составляет
5-10 мкм.
Механизм переноса кислорода путем
диффузии кислорода и углекислого газа
через аэрогематический барьер
Схема аэрогематического
барьера –
Перенос О2 из альвеолярного газа в кровь
и СО2 из крови в альвеолярный газ
происходит исключительно путем диффузии.
Ее движущей силой служат разности (градиенты)
парциальных давлений (напряжений) О2
и СО2 по обе стороны аэрогематического
барьера, образованного альвеолокапиллярной
мембраной. Никакого механизма активного
транспорта газов здесь нет.
Кислород и углекислый газ диффундируют в растворенном
состоянии: все воздухоносные пути увлажнены
слоем слизи. Важное значение для облегчения
диффузии О2 имеет сурфактантная
выстилка альвеол, так как кислород растворяется
в фосфолипидах, входящих в состав сурфактантов,
гораздо лучше, чем в воде.
В ходе диффузии через аэрогематический
барьер молекулы растворенного газа
должны преодолеть: слой сурфактанта,
альвеолярный эпителий, две основные
мембраны, эндотелий кровеносного капилляра.
Ввиду того что в транспорте дыхательных
газов существенную роль играют эритроциты,
к этому списку добавляются слой плазмы
и мембрана эритроцита.
Диффузионная способность
легких для кислорода очень велика.
Это обусловлено огромным числом
(сотни миллионов) альвеол и большой
их газообменной поверхностью (у человека она составляет
около 100 м2), а также малой толщиной
(порядка 1 мкм) альвео-локапиллярной мембраны.
Диффузионная способность легких у человека
равна примерно 25 мл О2/мин в расчете
на 1 мм рт. ст. градиента парциальных давлений
кислорода. При учете того, что градиент
Ро2 между притекающей к легким венозной
кровью и альвеолярным газом обычно превышает
50 мм рт. ст., этого оказывается вполне
достаточно, чтобы за время прохождения
через легочный капилляр (около 0,8 с) напряжение
кислорода в ней успело уравновеситься
с альвеолярным – Ро2. Несколько
более низкое (на 3-6 мм рт. ст.) артериальное
–Ро2 по сравнению с альвеолярным
объясняется проникновением венозной
крови в артериальную через невентилируемые
альвеолы, а также артериовенозные шунты.
Лишь при ускорении легочного кровотока,
например при тяжелой мышечной работе,
когда время прохождения крови через капилляры
альвеол может сокращаться до 0,3 с, наблюдается
недонасыщение крови кислородом в легких,
что, однако, возмещается увеличением
минутного объема крови.
Что касается диффузии СО2 из венозной
крови в альвеолы, то даже сравнительно
небольшого градиента Рсо2 (6-10 мм
рт. ст.) здесь оказывается вполне достаточно,
так как растворимость углекислого газа
в 20-25 раз больше, чем у кислорода. Поэтому
после прохождения крови через легочные
капилляры –Рсо2 в ней оказывается
почти равным альвеолярному — обычно
около 40 мм рт. ст.
Механизм транспорта кислорода кровью.
Схема регуляции транспорта О2.
Лишь небольшая часть
О2 (около 2%), переносимого кровью,
растворена в плазме. Основная его часть
транспортируется в форме непрочного
соединения с гемоглобином, который у
позвоночных содержится в эритроцитах.
В молекулы этого дыхательного пигмента
входят видоспецифичный белок — глобин, и одинаково построенная
у всех животных простетическая группа
— гем, содержащая двухвалентное
железо.
Присоединение кислорода
к гемоглобину (оксигенация гемоглобина)
происходит без изменения валентности
железа, т. е. без переноса электронов,
характеризующего истинное окисление.
Тем не менее гемоглобин, связанный с кислородом,
принято называть окисленным (правильнее
— оксигемоглобин), а отдавший
кислород — восстановленным (правильнее
— дезоксигемоглобин).
1 г гемоглобина может
связать 1,36 мл газообразного О2 (при нормальном атмосферном давлении).
Учитывая, к примеру, что в крови человека
содержится примерно 150 г/л гемоглобина,
100 мл крови могут переносить около 21 мл О2.-Это так называемая кислородная емкость крови.
Оксигенация гемоглобина (иначе говоря,
процент, на который используется кислородная
емкость крови) зависит от парциального
давления О2 в среде, с которой контактирует
кровь. Такая зависимость описывается кривой диссоциации оксигемоглобина.
Сложная S-образная форма этой кривой объясняется
кооперативным эффектом четырех полипептидных
цепей гемоглобина, кислородсвязывающие
свойства (сродство к О2) которых
различны.
Благодаря такой особенности венозная кровь, проходя
легочные капилляры (альвеолярное Ро2
приходится на верхнюю часть кривой), оксигенируется
почти полностью, а артериальная кровь
в капиллярах тканей (где Ро2 соответствует
крутой части кривой) эффективно отдает
О2. Отдаче кислорода способствуетсодержащийся
в эритроцитах 2,3-дифосфоглицерат, синтез
которого усиливается при гипоксии и интенсификации
окислительного процесса в тканях.
Кривая диссоциации
оксигемоглобина сдвигается вправо
при повышении температуры и
при увеличении концентрации водородных ионов
в среде, которая, в свою очередь, зависит
от Рсо2 (эффект Вериго-Бора). Поэтому
создаются условия для более полной отдачи
кислорода оксигемоглобином в тканях,
особенно там, где выше интенсивность
метаболизма, например в работающих мышцах.
Однако и в венозной крови большая или
меньшая часть (от 40 до 70%) гемоглобина
остается в оксигенированной форме. Так,
у человека каждые 100 мл крови отдают тканям
5—6 мл О2 (так называемая артерио-венозная разница
по кислорду) и, естественно, на ту
же величину обогащаются кислородом в
легких.
Сродство гемоглобина
к кислороду измеряется величиной
парциального давления кислорода, при
которой гемоглобин насыщается на 50%
(Р50); У человека оно составляет в
норме 26,5 мм рт. ст. для артериальной крови.
Параметр р50 отражает способность
дыхательного пигмента связывать кислород.
Этот параметр выше для гемоглобина животных,
обитающих в бедной кислородом среде,
а также для так называемого фетального гемоглобина,
который содержится в крови плода, получающего
кислород из крови матери через плацентарный
барьер.
Механизм
транспорта углекислого газа кровью.
Хотя СО2 растворяется в жидкости гораздо
лучше, чем СО2, только 3-6% общего
количества продуцируемого тканями СО2
переносится плазмой крови в физически
растворенном состоянии. Остальная часть
вступает в химические связи.
Поступая в тканевые
капилляры, СО2 гидратируется, образуя нестойкую
угольную кислоту:
СО2 + Н20 = Н2СО3 à Н+ + НСО3-
Направление этой обратимой реакции зависит от
Рсо2 в среде. Она резко ускоряется
под действием фермента карбоангидразы,
находящегося в эритроцитах, куда СО2
быстро диффундирует из плазмы.
Около 4/5 углекислого
газа транспортируется в виде гидрокарбоната НСО2-. Связыванию СО2
способствует уменьшение кислотных свойств (протонного сродства)
гемоглобина в момент отдачи им кислорода
— дезоксигенирование (эффект
Холдейна). При этом гемоглобин высвобождает
связанный с ним ион калия, с которым, в
свою очередь, реагирует угольная кислота:
К+ + НbО2 + Н+
+ НСОз- àННЬ + КНСОз + О2
Часть ионов НСОз диффундирует в плазму, связывая
там ионы натрия, в эритроцит же поступают
в порядке сохранения ионного равновесия
ионы хлора.
Кроме того, также за счет уменьшения протонного сродства
дезоксигениро-ванный гемоглобин легче
образует карбаминовые соединения, связывая
при этом еще около 15% переносимого кровью
СО2.
В легочных капиллярах происходит
высвобождение части СО2, который диффундирует в альвеолярный
газ. Этому способствует более низкое,
чем в плазме, альвеолярное Рсо2,
а также усиление кислотных свойств гемоглобина
при его оксигенации. В ходе дегидратации
угольной кислоты в эритроцитах (эта реакция
тоже резко ускоряется карбоангидразой)
оксигемоглобин вытесняет ионы калия
из гидрокарбоната. Ионы НСОз-
поступают из плазмы в эритроцит,а ионы
С1-— в обратном направлении. Таким
путем каждые 100 мл крови отдают в легких
4—5 мл СО2 — то же количество, какое
кровь получает в тканях (артерио-венозная разница
по СО2).
Гемоглобин (в силу амфотерных
свойств) и гидрокарбонат являются
важными буферными системами крови. Гидрокарбонатная
система играет особую роль благодаря
тому, что в ее состав входит летучая угольная
кислота. Так, при поступлении в кровь кислых продуктов метаболизма гидрокарбонат
как соль слабой (угольной) кислоты отдает
свой анион, а избыток углекислого газа
выводится легкими, что способствует нормализации
рН крови. Поэтому гиповентиляция легких
сопровождается наряду с гиперкапнией
увеличением концентрации водородных
ионов в крови — дыхательным (респираторным)
ацидозом, а гипервентиляция наряду
с гипокапнией — сдвигом активной реакции
крови в щелочную сторону — дыхательным алкалозом.
Оглавление темы “Вентиляция легких. Перфузия легких кровью.”:
1. Вентиляция легких. Вентиляция кровью легких. Физиологическое мертвое пространство. Альвеолярная вентиляция.
2. Перфузия легких кровью. Влияние гравитации на вентиляцию легких. Влияние гравитации на перфузию легких кровью.
3. Коэффициент вентиляционно-перфузионных отношений в легких. Газообмен в легких.
4. Состав альвеолярного воздуха. Газовый состав альвеолярного воздуха.
5. Напряжение газов в крови капилляров легких. Скорость диффузии кислорода и углекислого газа в легких. Уравнение Фика.
6. Транспорт газов кровью. Транспорт кислорода. Кислородная емкость гемоглобина.
7. Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.
8. Углекислый газ. Транспорт углекислого газа.
9. Роль эритроцитов в транспорте углекислого газа. Эффект Холдена..
10. Регуляция дыхания. Регуляция вентиляции легких.
Транспорт газов кровью. Транспорт кислорода. Кислородная емкость гемоглобина.
Кровообращение выполняет одну из важнейших функций переноса кислорода от легких к тканям, а углекислого газа — от тканей к легким. Потребление кислорода клетками тканей может изменяться в значительных пределах, например при переходе от состояния покоя к физической нагрузке и наоборот. В связи с этим кровь должна обладать большими резервами, необходимыми для увеличения ее способности переносить кислород от легких к тканям, а углекислый газ в обратном направлении.
Транспорт кислорода.
При 37 С растворимость 02 в жидкости составляет 0,225 мл • л-1 • кПа-1 (0,03 мл/л/мм рт. ст.). В условиях нормального парциального давления кислорода в альвеолярном воздухе, т. е. 13,3 кПа или 100 мм рт.ст., 1 л плазмы крови может переносить только 3 мл 02, что недостаточно для жизнедеятельности организма в целом. В покое в организме человека за минуту потребляется примерно 250 мл кислорода. Чтобы тканям получить такое количество кислорода в физически растворенном состоянии, сердце должно перекачивать за минуту огромное количество крови. В эволюции живых существ проблема транспорта кислорода была более эффективно решена за счет обратимой химической реакции с гемоглобином эритроцитов. Кислород переносится кровью от легких к тканям организма молекулами гемоглобина, которые содержатся в эритроцитах.
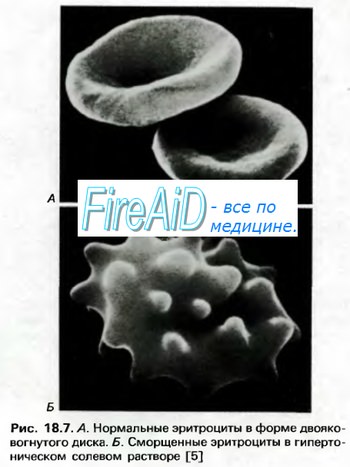
Гемоглобин способен захватывать кислород из альвеолярного воздуха (соединение называется ок-сигемоглобином) и освобождать необходимое количество кислорода в тканях. Особенностью химической реакции кислорода с гемоглобином является то, что количество связанного кислорода ограничено количеством молекул гемоглобина в эритроцитах крови. Молекула гемоглобина имеет 4 места связывания с кислородом, которые взаимодействуют таким образом, что зависимость между парциальным давлением кислорода и количеством переносимого кислорода с кровью имеет S-образную форму, которая носит название кривой насыщения или диссоциации оксигемоглобина (рис. 10.18). При парциальном давлении кислорода 10 мм рт. ст. насыщение гемоглобина кислородом составляет примерно 10 %, а при Р02 30 мм рт. ст. — 50—60 %. При дальнейшем увеличении парциального давления кислорода от 40 мм рт. ст. до 60 мм рт. ст. происходит уменьшение крутизны кривой диссоциации оксигемоглобина и процент его насыщения кислородом возрастает в диапазоне от 70—75 до 90 % соответственно. Затем кривая диссоциации оксигемоглобина начинает занимать практически горизонтальное положение, поскольку увеличение парциального давления кислорода с 60 до 80 мм рт. ст. вызывает прирост насыщения гемоглобина кислородом на 6 %. В диапазоне от 80 до 100 мм рт. ст. процент образования оксигемоглобина составляет порядка 2. В результате кривая диссоциации оксигемоглобина переходит в горизонтальную линию и процент насыщения гемоглобина кислородом достигает предела, т. е. 100. Насыщение гемоглобина кислородом под влиянием Р02 характеризует своеобразный молекулярный «аппетит» этого соединения к кислороду.
Значительная крутизна кривой насыщения гемоглобина кислородом в диапазоне парциального давления от 20 до 40 мм рт. ст. способствует тому, что в ткани организма значительное количество кислорода может диффундировать из крови в условиях фадиента его парциального давления между кровью и клетками тканей (не менее 20 мм рт. ст.). Незначительный процент насыщения гемоглобина кислородом в диапазоне его парциального давления от 80 до 100 мм рт. ст. способствует тому, что человек без риска снижения насыщения артериальной крови кислородом может перемещаться в диапазоне высот над уровнем моря до 2000 м.
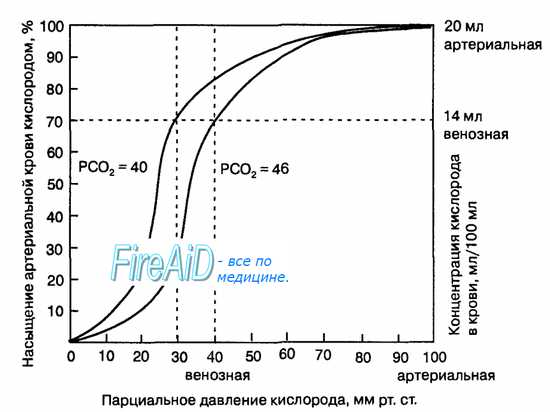
Рис. 10.18. Кривая диссоциации оксигемоглобина. Пределы колебания кривой при РС02 = 40 мм рт. ст. (артериальная кровь) и РС02 = 46 мм рт. ст. (венозная кровь) показывают изменение сродства гемоглобина к кислороду (эффект Ходена).
Общие запасы кислорода в организме обусловлены его количеством, находящимся в связанном состоянии с ионами Fe2+ в составе органических молекул гемоглобина эритроцитов и миоглобина мышечных клеток.
Один грамм гемоглобина связывает 1,34 мл 02. Поэтому в норме при концентрации гемоглобина 150 г/л каждые 100 мл крови могут переносить 20,0 мл 02.
Количество 02, которое может связаться с гемоглобином эритроцитов крови при насыщении 100 % его количества, называется кислородной емкостью гемоглобина. Другим показателем дыхательной функции крови является содержание 02 в крови (кислородная емкость крови), которое отражает его истинное количество, как связанного с гемоглобином, так и физически растворенного в плазме. Поскольку в норме артериальная кровь насыщена кислородом на 97 %, то в 100 мл артериальной крови содержится примерно 19,4 мл 02.
– Также рекомендуем “Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.”
