Синтез гема и гемоглобина
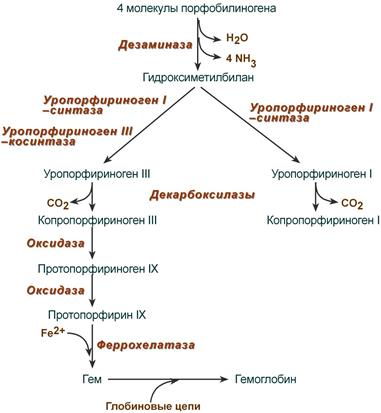
Гем является небелковой частью многих гемопротеинов:
- гемоглобин (до 85% общего количества гема организма), локализованный в эритроцитах и клетках костного мозга,
- миоглобин скелетных мышц и миокарда (до 17%),
- цитохромы дыхательной цепи,
- ферменты цитохромоксидаза, цитохром P450, гомогентизатоксидаза, миелопероксидаза, каталаза и глутатионпероксидаза, тиреопероксидаза и т.д. – менее 1%.
Строение и синтез гема
Гем – структура, включающая в себя порфириновое кольцо (состоящее из 4 пиррольных колец) и иона Fe2+. Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
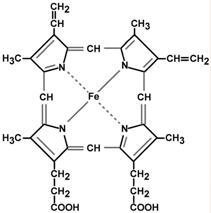
Строение гема
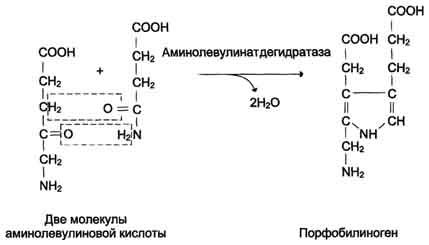
Синтез гема в основном идет в предшественниках эритроцитов, в клетках печени, почек, слизистой кишечника и в остальных тканях. Первая реакция синтеза с участием δ-аминолевулинат-синтазы (греч. δ – “дельта”) происходит в митохондриях. Следующая реакция при участии аминолевулинатдегидратазы (порфобилиноген-синтазы) протекает в цитозоле, здесь из двух молекул δ‑аминолевулиновой кислоты образуется циклический порфобилиноген (монопиррол).
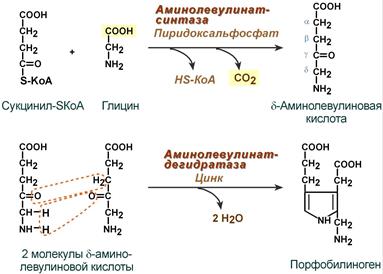
Синтез порфобилиногена
После синтеза порфобилиногена четыре его молекулы конденсируются в гидроксиметилбилан, который далее превращается в уропорфириноген типа I и уропорфириноген типа III. В синтезе обоих видов порфиринов принимает участие уропорфириноген I-синтаза, в образовании уропорфириногена III дополнительно принимает участие фермент уропорфириноген III-косинтаза.
Судьба обоих типов уропорфириногена двояка: они могут окисляться до уропорфирина (на рисунке не показано) или декарбоксилироваться до копропорфириногена соответствующего типа.

Синтез гема из порфобилиногена
Копропорфириноген III возвращается в митохондрии и окисляется в протопорфириноген IX и далее в протопорфирин IX. Последний после связывания с железом образует гем, реакцию катализирует феррохелатаза (гемсинтаза).
Скорость синтеза глобиновых цепей зависит от наличия гема, он ускоряет биосинтез “своих” белков.
Названия пигментов (уропорфирины и копропорфирины) были даны веществам по источнику их первоначального выделения, при этом восстановленные бесцветные формы называют порфириногенами. Для порфиринов характерно наличие изомерии вследствие различного расположения радикалов, что нашло отражение в порядковых номерах изомеров.
Регуляция синтеза гема
Основным регуляторным ферментом синтеза гема является аминолевулинатсинтаза.
1. Гем :
- напрямую оказывает отрицательный аллостерический эффект на фермент,
- влияет на транскрипцию фермента. После взаимодействия с молекулой белка-репрессора формирует активный репрессорный комплекс, связывается с ДНК и подавляет транскрипцию, мРНК для фермента не образуется и синтез фермента прекращается.
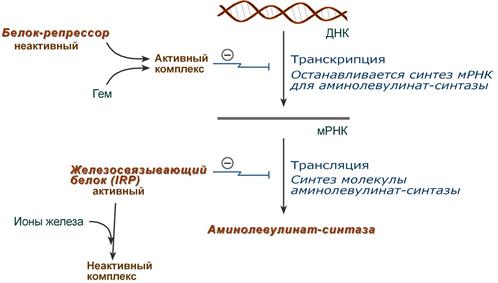
Регуляция синтеза аминолевулинатсинтазы
2. Ионы железа. Их достаточное количество оказывает положительный эффект при синтезе молекулы аминолевулинатсинтазы.
В клетке имеется железосвязывающий белок (англ. IRP, iron-responsive element-binding proteins – белок, связывающий железочувствительный элемент), который в отсутствии ионов железа обладает сродством к железочувствительному участку IRE (англ. iron-responsive element ) на матричной РНК фермента. Это связывание блокирует трансляцию мРНК в рибосоме, т.е. подавляет синтез белковой цепи.
При наличии ионов железа они связываются с железосвязывающим белком, образуя с ним неактивный комплекс, и это инициирует синтез фермента.
3. Положительным модулятором аминолевулинатсинтазы служит внутриклеточная гипоксия, которая в эритропоэтических тканях индуцирует синтез фермента.
4. В печени повышению активности аминолевулинатсинтазы способствуют различные соединения, усиливающие работу микросомальной системы окисления (жирорастворимые вещества, стероиды) – при этом возрастает потребление гема для образования цитохрома Р450, и снижается внутриклеточная концентрация свободного гема. В результате происходит усиление синтеза фермента.
Гем
синтезируется во всех тканях, но с
наибольшей скоростью в костном мозге
и печени (рис. 13-2). В костном мозге гем
необходим для синтеза гемоглобина в
ретикулоцитах, в гепатоцитах – для
образования цитохрома Р450.
Первая
реакция синтеза гема – образование
5-аминолевулиновой кислоты из глицина
и сук-цинил-КоА (рис. 13-3) идёт в матриксе
митохондрий, где в ЦТК образуется один
из субстратов этой реакции – сукцинил-КоА.
Эту реакцию катализирует пиридоксальзависимый
фермент аминолевулинатсинтаза.
Из
митохондрий 5-аминолевулиновая кислота
поступает в цитоплазму. В цитоплазме
проходят промежуточные этапы синтеза
гема: соединение 2 молекул 5-аминолевулиновой
кислоты молекулу порфобилиногена (рис.
13-4), дезаминированиепорфобилиногена с
образованием гидроксиметилбилана,
ферментативное превращение
гидроксиметилбилана в молекулу
уропор-фобилиногена III, декарбоксилирование
последнего с образованием копропорфириногена
III. Гидроксиметилбилан может также
нефермента-тивно превращаться в
уропорфириноген I, который декарбоксилируется
в копропорфирино-ген I. Из цитоплазмы
копропорфириноген III опять поступает
в митохондрии, где проходят заключительные
реакции синтеза гема. В результате двух
последовательных окислительных реакций
копропорфириноген III превращается в
протопорфириноген IX, а протопорфириноген
IX – в Протопорфирин IX. Фермент феррохела-таза,
присоединяя к протопорфирину IX
двухвалентноелентное железо, превращает
его в гем (рис. 13-2). Источником железа
для синтеза гема служит депонирующий
железо белок ферритин. Синтезированный
гем, соединяясь с α и β-полипепептидными
цепями глобина, образует гемоглобин.
Гем регулирует синтез глобина: при
снижении скорости синтеза гема синтез
глобина в ретикулоцитах тормозится.
Донором
железа служит депонирующий железо в
клетках белок ферритин.

Рис.
13-3. Реакция образования 5-аминолевулиновой
кислоты.
Регуляция
биосинтеза гема
Регуляторную
реакцию синтеза гема катализирует
пиридоксальзависимый фермент
аминолевулинатсинтаза. Скорость реакции
регулируется аллостерически и на уровне
трансляции фермента.
Аллостерическим
ингибитором и корепрессором синтеза
аминолевулинатсинтазы является гем
(рис. 13-5).
В
ретикулоцитах синтез этого фермента
на этапе трансляции регулирует железо.
На участке инициации мРНК, кодирующей
фермент, имеется последовательность
нуклеотидов, образующая шпилечную
петлю, которая называется железочувствительным
элементом (от англ, iron-responsiveelement, IRE)
(рис. 13-6).
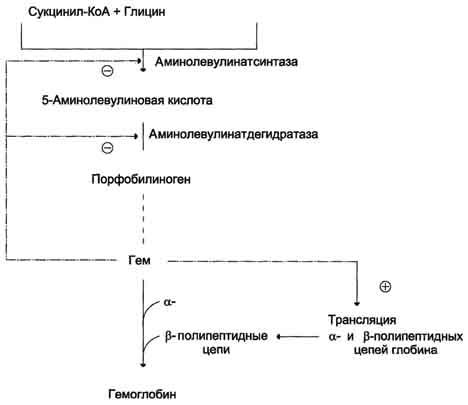
Рис.
13-5. Регуляция синтеза гема и гемоглобина. Гем
по принципу отрицательной обратной
связи ингибирует аминолевулинатсинтазу
и аминолевулинатдегидратазу и является
индуктором трансляции α- и β-цепей
гемоглобина.
При
высоких концентрациях железа в клетках
оно образует комплекс с остатками
цистеина регуляторного железосвязывающего
белка. Взаимодействие железа с регуляторным
железосвязывающим белком вызывает
снижение сродства этого белка к
IRE-элементу мРНК, кодирующей
аминолевулинатсинтазу, и продолжение
трансляции (рис. 13-6, А). При низких
концентрациях железа железосвязывающий
белок присоединяется к железо-чувствительному
элементу, находящемуся на 5′-нетранслируемом
конце мРНК, и трансляция аминолевулинатсинтазы
тормозится (рис. 13-6, Б).
Аминолевулинатдегидратаза
также аллостерически ингибируется
гемом, но так как активность этого
фермента почти в 80 раз превышает
активность аминолевулинатсинтазы, то
это не имеет большого физиологического
значения.
Дефицит
пиридоксальфосфата и лекарственные
препараты, которые являются его
структурными аналогами, снижают
активность аминолевулинатсинтазы.
Альфа-полипептидная
цепь заканчивается комбинацией
аминокислот валина-лейцина, а
бета-полипептидная цепь – комбинацией
валина-гистидина-лейцина. Альфа- и
бета-полипептидные цепи в гемоглобиновой
молекуле не размещены линейно, как это
выглядит на первый взгляд из данных,это
первичная структура .
Гемоглобинопатии
группа наследственных гемолитических
анемий, обусловленных нарушениями
первичной структуры гемоглобина
(качественные гемоглобинопатии) или
синтеза глобиновых цепей (количественные
гемоглобинопатии).
Соседние файлы в папке экз
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Тема 3 (вопрос 4 и 5).
Гем состоит из иона двухвалентного железа и порфирина. В основе структуры порфиринов находится порфин. Порфин представляет собой четыре пиррольных кольца, связанных между собой метеновыми мостиками. С наибольшей скоростью гем синтезируется в костном мозге (для синтеза гемоглобина ретикулоцитами) и в печени (для образования цитохрома Р-450).
Синтез гема происходит в несколько стадий:
1. На первой стадии в митохондриях сукцинил-КоА взаимодействует с глицином с образованием δ-аминолевулиновой кислоты. Эту реакцию катализирует специфический пиридоксальзависимый фермент δ-аминолевулинатсинтаза. Фермент активируется стероидами и ингибируется по типу обратной связи конечным продуктом – гемом. Продукт реакции из матрикса митохондрий переходит в цитозоль.
2. На второй стадии, в цитозоле, происходит конденсация 2-х молекул
δ-аминолевулиновой кислоты с образованием порфобилиногена. Фермент – порфобилиногенсинтаза – ингибируется конечным продуктом.
3. Из 4-х молекул порфобилиногена синтезируется протопорфирин IX, являющийся предшественником гема.
4. Протопорфирин IX присоединяет молекулу Fe при участии феррохелатазы (гемсинтаза) и образуется гем. Источником железа в этой реакции является белок ферритин, который депонирует железо.
Механизм регуляции синтеза тема в неэритроидных клетках имеет определенные отличия. Так, в клетках печени, где синтез гема происходит на высоком уровне, гем является отрицательным регулятором синтеза δ-аминолевулинатсинтазы по механизму репрессии-депрессии в процессе транскрипции. Главный регуляторный эффект гема состоит в том, что синтез фермента значительно ускоряется в отсутствии гема и замедляется в его присутствии.
Синтез белковой части гемоглобина происходит на рибосомах. Цепи α и β глобина синтезируются на полисомах, образованных, как правило, пятью рибосомами. Цепь α освобождается первой, присоединяется к β-цепи, еще связанной с рибосомой и отделяет ее, образуя димер αβ. Два димера соединяются в молекулу гемоглобина α2β2.
Соединение гема с глобином может происходить или в процессе синтеза полипептидных цепей, или после окончания синтеза глобина. Синтез полипептидных цепей происходит только в присутствии гема. При низкой концентрации гема синтез глобина замедляется. Отсюда следует, что синтез гема и глобина происходит координировано и ни один из этих компонентов не образуется в избыточном или недостаточном количестве.
Катаболизм гемоглобина
Эритроциты имеют короткое время жизни (примерно 120 дней). При физиологических условиях в организме взрослого человека разрушается около 1 – 2×1011 эритроцитов в сутки. Их катаболизм происходит, главным образом, в ретикулоэндотелиальных клетках селезёнки (РЭС), лимфатических узлов, костного мозга и печени. При распаде гемоглобина образуется билирубин. Билирубин является основным желчным пигментом у человека. При распаде 1 г гемоглобина образуется 35 мг билирубина, а в сутки у взрослого человека – примерно 250-350 мг. Дальнейший метаболизм билирубина происходит в печени.
Билирубин, образованный в клетках РЭС селезёнки и костного мозга, называется свободным (неконьюгированным)или непрямым, поскольку вследствие плохой растворимости в воде он легко адсорбируется на белках плазмы крови (альбуминах) и для его определения в крови необходимо предварительное осаждение белков спиртом. После этого билирубин определяют реакцией с диазореактивом Эрлиха. Свободный (непрямой) билирубин не проходит через почечный барьер и в мочу не попадает.
Каждая молекула альбумина связывает 2 (или 3) молекулы билирубина. При низком содержании альбумина в крови, а также при вытеснении билирубина из центров связывания на поверхности альбумина высокими концентрациями жирных кислот, лекарственных веществ (например, сульфаниламиды) увеличивается количество билирубина, не связанного с альбуминами. Он может проникать в клетки мозга и повреждать их.
Комплекс альбумин-билирубин с током крови попадает в печень, где происходит его превращение в прямой билирубин путем коньюгации с глюкуроновой кислотой. Реакцию катализирует УДФ-глюкуронилтрансфераза. Образующийся билирубиндиглюкуронид получил название прямого(коньюгированного) билирубина или связанного. Он растворим в воде и дает прямую реакцию с диазореактивом Эрлиха.
Прямой билирубин – это нормальный компонент желчи, попадающий в кровь в незначительном количестве. Он может проходить через почечный барьер, но в крови в норме его мало, поэтому в моче обычными лабораторными методами он не определяется.
Вместе с желчью прямой билирубин выводится в тонкий кишечник. В кишечнике билирубинглюкурониды гидролизуются специфическими бактериальными ферментами β-глюкуронидазами. Освободившийся билирубин под действием кишечной микрофлоры восстанавливается с образованием сначала мезобилирубина, а затем мезобилиногена(уробилиногена). Небольшая часть уробилиногенов, всасываясь в тонком кишечнике и верхнем отделе толстого, через систему воротной вены попадает в печень, где практически полностью разрушается до дипиррольных соединений. Уробилиноген при этом в общий кровоток не поступает и в моче не определяется.
Основная часть уробилиногена поступает в толстый кишечник, где под влиянием микрофлоры подвергается дальнейшему восстановлению с образованием стеркобилиногена. Образовавшийся стеркобилиноген почти полностью выделяется с калом. На воздухе он окисляется и превращается в стеркобилин, являющийся одним из пигментов кала. Небольшая часть стеркобилиногена попадает путем всасывания через слизистую толстого кишечника в систему нижней полой вены (через геморроидальные вены), доставляется в почки и выводится с мочой (4 мг/сутки).
Учитывая, что
белковая часть молекулы гемоглобина (глобин) синтезируется, как и все остальные
белки, далее подробно рассмотрен биосинтез его простетической группы, т.е.
синтез тетрапиррольного соединения – гема (см. главу 2).
К настоящему
времени почти полностью выяснены основные пути образования порфиринов и
протопорфиринов, являющихся непосредственными предшественниками гема и
хлорофилла. Благодаря исследованиям Д. Шемина и др. выяснены основные пути
синтеза гема. С помощью меченых предшественников было показано, что в синтезе
гема в бесклеточных экстрактах эритроцитов птиц специфическое участие принимают
глицин, уксусная и янтарная кислоты. Источником всех 4 атомов азота и 8 атомов
углерода тетрапиррольного кольца оказался глицин, а источником остальных 26 из
34 атомов углерода – янтарная кислота (сук-цинат), точнее ее производное
сукцинил-КоА. Последовательность химических реакций синтеза тетрапирролов в
организме животных можно условно разделить на несколько стадий.
На I стадии,
протекающей в 2 этапа, сукцинил-КоА взаимодействует с глицином и образованием
δ-аминолевулиновой кислоты (δ-АЛК).
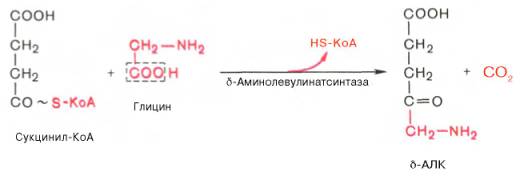
Эту стадию
катализирует специфический пиридоксальфосфатзависимый фермент
δ-аминолевулинатсинтаза – ключевой, аллостерический фермент синтеза тетрапирролов.
Впервые эта
синтаза была обнаружена в эндоплазматической сети клеток печени.
Фермент индуцируется стероидами и другими факторами и ингибируется по типу
обратной связи конечным продуктом биосинтеза – гемом.
На II стадии
происходит конденсация 2 молекул δ-аминолевулиновой кислоты с образованием
первого монопиррольного соединения – порфо-билиногена (ПБГ).
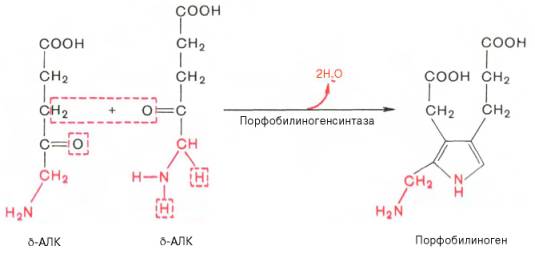
Фермент,
катализирующий эту стадию,– порфобилиногенсинтаза также является регуляторным
ферментом, подвергаясь ингибированию конечными продуктами синтеза. Предполагают,
что механизм этой сложной реакции дегидратации включает образование кетиминной
связи (шиффово основание) между кетогруппой одной молекулы
δ-аминолевулиновой кислоты и δ-аминогруппой лизина молекулы фермента.
В следующей многоступенчатой стадии, катализируемой соответствующими
ферментами, из 4 монопиррольных молекул порфобилиногена синтезируется
тетра-пиррольный комплекс протопорфирин IX, являющийся непосредственным
предшественником гема. Некоторые этапы сложного пути синтеза окончательно не установлены.
В
заключительной стадии протопорфирин IX присоединяет молекулу железа при участии
феррохелатазы (гемсинтазы), и образуется гем. Последний используется для
биосинтеза всех гемсодержащих хромопро-теинов.
Источником
железа для этой реакции является ферритин, который считается резервным
гемопротеином, откладывающимся в клетках костного мозга, печени и селезенки.
Имеются
указания, что, помимо железа, в синтезе гема участвуют некоторые кофакторы, в
частности витамин В12, ионы меди, хотя конкретная их роль не
раскрыта.
Таким
образом, весь путь синтеза гема может быть представлен в виде схемы, в которой
даны полные и сокращенные обозначения промежуточных метаболитов и ферментов.
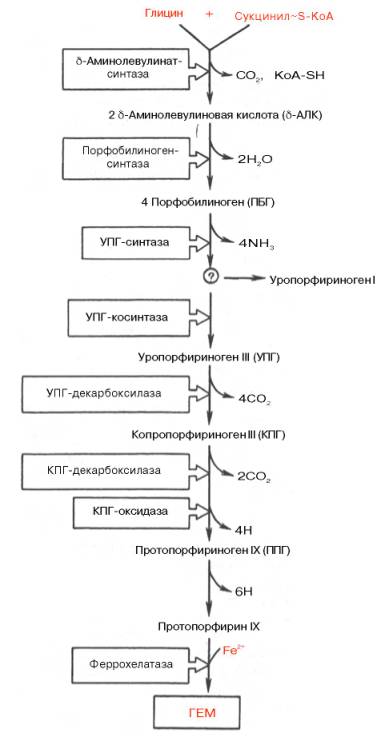
1. Гем является простетической группой гемоглобина, миоглобина, цитохромов, каталазы, пероксидазы.
2. Гем синтезируется во всех клетках, но наиболее активно синтез идет в печени и костном мозге. Эти ткани нуждаются в больших количествах гема, необходимого для образования гемоглобина и цитохромов. Субстратами синтеза гема являются глицин, сукцинил-КоА и Fe2+.В матриксе митохондрий из глицина и сукцинил-КоА под действием пиридоксальзависимого фермента 5-аминолевулинатсинтазыобразуется 5-аминолевулиновая кислота, которая поступает в цитоплазму. В цитоплазме фермент 5 -аминолевулинатдегидратазакатализирует реакцию конденсации двух молекул 5-аминолевулиновой кислоты с образованием порфобилиногена.Далее из четырех молекул порфобилиногена последовательно образуются промежуточные метаболиты – порфириногены,последний из которых поступает в митохондрии и превращается впротопорфирин ГХ.Фермент феррохелатазазавершает образование гема, присоединяя Fe2+ к протопорфирину IX (рис. 13.1).
Рис. 13.1. Синтез гема.
В митохондриях клеток пиридоксальзависимый фермент 5-аминолевулинатсинтаза катализирует первую реакцию синтеза гема. Затем 5-аминолевулиновая кислота поступает в цитоплазму, где 5-аминолевулинатдегидратаза катализирует превращение двух молекул 5-аминолевулината в порфобилиноген, имеющий циклическое строение. В результате последовательных реакций в цитоплазме образуется протопорфирин IX. Он поступает в митохондрии и под действием фермента феррохелатазы соединяется с Fe+2 с образованием гема
3. Две первые реакции синтеза гема катализируют ферменты, аллостерическим ингибитором которых является гем. Вместе с тем гем является индуктором синтеза α- и β-цепей гемоглобина. В ретикулоцитах Fe2+ индуцирует синтез 5-аминолевулинатсинтазы (рис. 13.2). Стероидные гормоны и некоторые лекарства (барбитураты, диклофенак, сульфаниламиды, эстрогены, прогестины) являются индукторами синтеза 5-аминолевулинатсинтазы.
4. В результате генетических дефектов или нарушений регуляции ферментов, участвующих в биосинтезе гема, развиваются порфирии.Первичные порфирии обусловлены генетическими дефектами в структуре генов,
Рис. 13.2. Регуляция синтеза гема и гемоглобина.
Гем по принципу отрицательной обратной связи ингибирует 5-аминолевулинатсин- тазу и 5-аминолевулинатдегидратазу, а также является индуктором трансляции α- и β-цепей гемоглобина. Ионы Fe2+ индуцируют синтез 5-аминолевулинатсинтазы
кодирующих ферменты синтеза гема, вторичные – связаны с нарушениями регуляции реакций синтеза гема. Порфирии может вызвать прием лекарственных препаратов, являющихся индукторами синтеза 5-аминолевулинат- синтазы. Эти заболевания сопровождаются накоплением в клетках промежуточных метаболитов синтеза гема порфириногенов, которые оказывают токсическое действие на нервную систему и вызывают нейропсихические симптомы. Порфириногены на свету превращаются в порфирины, которые при взаимодействии с кислородом образуют активные радикалы, повреждающие клетки кожи.
ТЕМА 13.2. ОБМЕН ЖЕЛЕЗА
Железо входит в состав гемсодержащих белков, а также металлофлавопротеинов, железосерных белков, трансферрина, ферритина.
1. Источником железа при биосинтезе белков, содержащих железо, являются пищевые продукты. Обычно всасывается не более 10% железа пищи. Железо, освобождающееся при постоянном распаде эритроцитов в клетках печени и селезенки, может повторно использоваться для синтеза железосодержащих белков.
Кислая среда желудка и присутствие в пище аскорбиновой кислоты,восстанавливающей Fe 3+, способствуют освобождению железа из солей органических кислот пищи (рис. 13.3).
2. Поступление железа из энтероцитов в кровь зависит от скорости синтеза в них белка апоферритина.Апоферритин улавливает железо в клетках слизистой кишечника и превращается в ферритин,который остается
Рис. 13.3. Обмен железа.
• Железо поступает с пищей, транспортируется кровью в форме трансферрина, запасается в виде ферритина и используется для синтеза цитохромов, железосодержащих ферментов, гемоглобина и миоглобина.
• Организм теряет железо с мочой, калом, потом и при кровотечениях.
• Гемосидерин аккумулирует избыток железа
в энтероцитах. Это снижает поступление железа в кровь из клеток кишечника. Когда потребности в железе невелики, скорость синтеза апоферритина повышается. Слущивание клеток слизистой оболочки кишечника освобождает организм от излишков железа. При недостатке железа в организме апоферритин в энтероцитах почти не синтезируется.
Фермент крови ферроксидаза (церулоплазмин)окисляет железо, оно связывается с гликопротеином крови трансферриноми транспортируется кровью (рис. 13.4).
3.Трансферрин взаимодействует со специфическими рецепторами и поступает в клетки. Количество рецепторов трансферрина зависит от содержания железа в клетках и регулируется на уровне транскрипции гена белкарецептора. При снижении содержания железа в клетках скорость синтеза рецепторов повышается, и наоборот.
Рис. 13.4. Поступление экзогенного железа в ткани.
В полости кишечника Fe3+ высвобождается из белков и солей органических кислот пищи. Усвоение Fe3+ улучшает аскорбиновая кислота, восстанавливающая его до Fe+2. Поступление Fe2+ из слизистой оболочки кишечника в кровь сопровождается окислением железа медьсодержащим ферментом плазмы крови ферроксидазой. Избыток поступившего в клетки слизистой оболочки кишечника железа соединяется с белком апоферритином, который окисляет железо и превращается в ферритин. В крови Fe3+ транспортирует белок плазмы крови трансферрин. В тканях Fe2+ используется для синтеза железосодержащих белков или депонируется в составе ферритина.
4.Белок ферритин играет роль депо железа в клетках печени, селезенки, костного мозга. Избыток железа аккумулируется в печени и других тканях в составе гранул гемосидерина. Если количество железа в клетках превышает объем ферритинового депо, то оно откладывается в белковой части молекулы ферритина. Таким образом ферритин превращается в гемосидерин, который плохо растворим в воде и может содержать до 37% железа. Накопление гранул гемосидерина в ретикулоэндотелиоцитах печени и селезенки может привести к повреждению органа – гемохроматозу.
При недостаточном поступлении или нарушении утилизации железа развивается железодефицитная анемия.
ТЕМА 13.3. КАТАБОЛИЗМ ГЕМА
1.Распад гема происходит в эндоплазматическом ретикулуме клеток эндотелиальной системы селезенки, костного мозга и печени при участии ферментов гемоксигеназной системы(рис. 13.5). В результате ряда превращений образуется непрямой (не дающий прямую реакцию с диазореактивом, так как связан с белком альбумином) – неконъюгированный билирубин.Билирубин плохо растворим в воде и транспортируется кровью в печень в комплексе с альбумином.
Рис. 13.5. Катаболизм гема
2.Билирубин поступает в гепатоциты по механизму облегченной диффузии с помощью белков-переносчиков лигандина и протеина Z. В печени билирубин конъюгирует с глюкуроновой кислотой под действием ферментов эндоплазматического ретикулума УДФ-глюкуронилтрансферазы I,катализирующей образование билирубинмоноглюкуронида и УДФ-глюкуронилтрансферазы II,образующей билирубиндиглюкуронид. В результате реакций конъюгации образуется прямойили конъюгированный, билирубин(рис. 13.6).
Рис. 13.6. Образование билирубинмоноглюкуронида и билирубиндиглюкуронида (прямого билирубина) в гепатоцитах
Синтез УДФ-глюкуронилтрансфераз индуцируют некоторые лекарственные препараты, например, фенобарбитал.
3. По механизму активного транспорта прямой билирубин в составе желчи поступает в двенадцатиперстную кишку. В кишечнике ферментами микрофлоры он гидролизуется с образованием билирубина и глюкуроновой кислоты. Билирубин в результате нескольких реакций восстановления превращается в бесцветные тетрапирролы – уробилиногены.В результате окисления они превращаются в уробилин, который выводится из организма, являясь пигментом кала уробилином (стеркобилином)(200-300 мг/сут). Небольшая часть уробилиногенов всасывается в кишечнике, с кровью воротной вены транспортируется в печень, оттуда поступает в кровь, затем в почки и, окисляясь в пигмент желтого цвета уробилин,удаляется с мочой(3-4 мг/ сут).
4. Концентрация общего билирубина в кровиздорового человека составляет 1,7-17 мкмоль/л (0,1-1 мг/дл).Повышение концентрации билирубина в крови – гипербилирубинемия– может быть обусловлено увеличением образования билирубина, превышающим способность гепатоцитов его конъюгировать и экскретировать в кишечник, закупоркой желчевыводящих протоков, генетическими дефектами ферментов и белков, участвующих в метаболизме билирубина в печени. Когда концентрация билирубина в крови превышает норму более чем в 2,5 раза, он поступает в ткани, окрашивая их в желтый цвет. Пожелтение склер глаз, кожи и слизистых оболочек из-за отложения в них билирубина называютжелтухой.
5.При дифференциальной диагностике желтух в крови определяют концентрацию прямого, непрямого и общего билирубина, в моче – содержание прямого билирубина и уробилина, в кале – содержание уробилина (стеркобилина). В зависимости от механизма возникновения различают несколько типов желтух.
• Гемолитическая (надпеченочная) желтухаявляется следствием ускоренного гемолиза эритроцитов при генетических дефектах глюкозо- 6-фосфат дегидрогеназы, пируваткиназы или белков плазматической мембраны эритроцитов, отравлении сильными окислителями, переливании несовместимых групп крови. При этом увеличивается по сравнению с нормой поступление билирубина в кровь и образование непрямого билирубина. Уровень непрямого билирубина в крови возрастает в 2-3 раза по сравнению с нормой, так как потенциальная способность гепатоцитов инактивировать билирубин ограничена. В моче и кале повышено содержание уробилина и стеркобилина, соответственно.
• Механическая (подпеченочная) желтухаявляется результатом нарушения секреции желчи, вызванным закупоркой желчных протоков камнями или послеоперационными рубцами. В крови повышается концентрация непрямого и прямого билирубина, который поступает в мочу, придавая ей коричневый цвет. В моче и кале отсутствуют уробилин и стеркобилин, поэтому кал больных ахолический (бесцветный).
• Печеночно-клеточная (печеночная) желтухасопровождает разные формы гепатита. В этом случае снижается способность гепатоцитов захватывать билирубин из крови и экскретировать его в кишечник, поэтому в крови повышается концентрация прямого и непрямого билирубина, а в моче и кале снижается содержание конечных продуктов распада гема. Поскольку концентрация прямого билирубина в крови превышает почечный порог, то он фильтруется в мочу, окрашивая ее в коричневый цвет. Из-за снижения содержания стеркобилина кал больных светлый.
• Желтуха новорожденных– это «физиологическая» желтуха. Она обусловлена большим по сравнению взрослым организмом количеством эритроцитов в расчете на массу тела. После рождения ребенка эритроциты разрушаются, так как HbF замещается HbA. Кроме того, у новорожденных может наблюдаться запаздывание «включения» гена глюкуронилтрансферазы, недостачная способность гепатоцитов улавливать билирубин из крови и экскретировать прямой билирубин в желчь. Неконъюгированный билирубин проходит через гематоэнцефалический барьер и, являясь разобщителем окислительного фосфорилирования, снижает синтез АТФ в клетках головного мозга и вызывает пирогенное действие. Дегенеративные изменения нервных клеток приводят к билирубиновой энцефалопатии. Новорожденным назначают барбитураты для индукции синтеза глюкуронилтрансферазы. Кроме того, для снижения уровня неконъюгированного билирубина используют фототерапию новорожденных сине-зеленым светом с длиной волны 620 нм. В результате такого облучения билирубин окисляется и превращается в гидрофильные фотоизомеры, которые поступают в почки и выводятся из организма с мочой.
• Наследственные желтухиобусловлены генетическими дефектами белков, участвующих в метаболизме билирубина в печени. Например,синдром Жильберасвязан с генетическими дефектами белков, захватывающих билирубин из крови, синдром Дубина-Джонса– с дефектом белков, участвующих в экскреции прямого билирубина в кишечник, а при синдроме Криглера-Найяранарушена первичная структура глюкуронилтрансферазы.
Рис. 13.7. Поступление, транпорт и использование железа в организме
МОДУЛЬ 14 БИОХИМИЯ КРОВИ
Темы_
14.1. Метаболизм эритроцитов
14.2. Особенности метаболизма фагоцитирующих клеток
14.3. Основные биохимические механизмы гемостаза
14.4. Основные свойства белковых фракций крови и значение их определения для диагностики заболеваний
